雪莲培养物高效液相色谱指纹图谱研究
2015-11-29贾康杰马昆鹏高丽华邵勇方均建董芳霆胡显文
贾康杰 ,马昆鹏,高丽华,邵勇,方均建,董芳霆,胡显文
1.山西康宝生物制品股份有限公司,山西 长治 046000;2.国家生物医学分析中心,北京 100850;3.军事医学科学院 生物工程研究所,北京 100071
雪莲属菊科凤毛菊属草本植物,主要分布于我国青藏高原及其毗邻地区,属于藏药中的名贵药材,八世纪藏族古代药物文献《月王药诊》中记载其具有散寒除湿、活血通络、抗癌、抗炎及抗疲劳等功效,可治疗妇女月经不调、风湿性关节炎、痈疮肿毒和高山不适应等多种疾病[1]。然而,由于野生雪莲独特的生长环境,人工栽培困难,加之近年采挖过度,导致该物种濒临灭绝。为解决珍稀濒危药用植物的资源问题,军事医学科学院生物工程研究所胡显文课题组经过多年探索,获得了稳定高产黄酮的水母雪莲细胞系,并建立了大规模植物细胞培养方法[2-3],目前该项目已成功进行工业化生产。我们采用高效液相色谱(HPLC)研究了10 个批次的雪莲培养物的指纹图谱,并利用相对保留值和相对面积研究雪莲培养物样品之间的异同,为雪莲培养物的质量控制提供依据。
1 材料和方法
1.1 材料
11 批雪莲培养物均由山西康宝生物制品股份有限公司提供;刺五加苷B(紫丁香苷)对照品(国家标准物质信息中心,批号:20110824);绿原酸对照品(国家标准物质信息中心,批号:20120314);乙腈、三氟乙酸(色谱纯,美国Fisher 公司);其余试剂均为分析纯。
HP1100高效液相色谱仪(美国安捷伦公司),包括HP Degasser(在线脱气机)、HP QUAT PUMP(四元梯度泵)、HP ALS(自动进样器)、HP COLCOMP(柱温箱)、HP DAD(二极管阵列检测器)。
1.2 色谱条件
色谱柱为CAPCELL PAK C18(4.6 mm×250 mm,5 μm),流动相A 为0.1% TFA/水,流动相B 为0.1% TFA/乙腈,梯度洗脱,流速1 mL/min,检测波长260 nm,柱温40℃,进样量20 μL。理论塔板数以紫丁香苷峰计,应不低于2500。紫丁香苷、绿原酸色谱峰的分离度应大于1.5。洗脱条件:0~1 min,0~0B%;1~16 min,0~10B%;16~41 min,10~25B%;41~56 min,25~60B%;56~65 min,60~100B%。
1.3 对照品溶液的制备
分别取紫丁香苷、绿原酸对照品适量,精密称定,加水溶解并稀释至20 μg/mL 的对照溶液,摇匀,备用。
1.4 供试品溶液的制备
取本品0.2 g,精密称定,置于10 mL 容量瓶中,加水约8 mL 超声波处理30 min,降至室温,加水稀释至刻度,摇匀,滤过,备用。
1.5 测定法及数据处理
分别精密吸取对照品溶液与供试品溶液各20 μL 注入液相色谱仪,记录60 min 的色谱图。数据处理采用中国药典委员会推荐的“中药指纹图谱计算机辅助相似度评价软件”(版本2004A),将10个批次的色谱图进行比较,得到可全面反映多个色谱图特征的雪莲培养物的对照指纹图谱,计算每个色谱图与之相比较的相似度。
2 结果
2.1 供试品提取条件
2.1.1 提取溶剂 称取雪莲培养物(批号20111121)样品5 份,每份0.2 g,分别置于10 mL 玻璃离心管中,分别加入100%甲醇、75%甲醇、50%甲醇、25%甲醇、水各8 mL,超声波提取20 min 后滤过,取滤液置于10 mL容量瓶中,加入各溶剂至刻度,分别取上述溶液各20 μL 注入液相色谱仪,记录色谱图。根据液相色谱图显示,水作为提取溶剂的色谱峰比例适中,信息丰富,所以选择纯水作为提取溶剂。
2.1.2 提取方式 称取雪莲培养物(批号20111121)样品3 份,每份0.2 g,分别置于10 mL 玻璃离心管中,加入水8 mL,分别采用室温浸提24 h、加热回流1 h、超声提取30 min等3种方式提取后,滤过,取滤液置于10 mL容量瓶中,加入水至刻度,分别取上述溶液各20 μL 注入液相色谱仪,记录色谱图。比较各色谱图,结果显示超声波提取效果最好,方法简单,重现性好,色谱峰较多。
2.1.3 提取时间 称取雪莲培养物(批号20111121)样品2 份,每份0.2 g,分别置于10 mL 玻璃离心管中,分别加入水8 mL,分别采用超声波提取30 和60 min 后,滤过,取滤液置于10 mL 容量瓶中,加入水至刻度,分别取上述溶液各20 μL 注入液相色谱仪,记录色谱图。比较各色谱图,结果显示提取30 min 和60 min 的色谱峰数量和强度差别不明显,所以选择提取时间为30 min。
2.2 色谱条件
2.2.1 检测波长 参照文献[5],比较了检测波长分别为220、260、280、320、360 nm 时的检测结果,发现提取液在220 nm波长有较好的色谱信息,但基线噪音较高,不利于分析。提取液在260 nm波长下各色谱峰均有较好的紫外吸收,色谱信息丰富、适中,特征峰之间分离良好,因此选择260 nm作为检测波长。
2.2.2 流动相 分别采用0.1%甲酸/水-0.1%甲酸/乙腈、0.1%乙酸/水-0.1%乙酸/乙腈、0.1%磷酸/水-0.1%磷酸/乙腈、0.1% TFA/水-0.1% TFA/乙腈等流动相进行梯度洗脱,记录色谱图。根据图谱对比,发现以0.1% TFA/水-0.1% TFA/乙腈为流动相时,在线性梯度下各组分得到较好的分离。
2.3 方法学考察
2.3.1 精密度试验 取同一批雪莲培养物样品(批号20111121)制备供试品溶液,连续进样6 次,以紫丁香苷的保留时间和峰面积为对照,计算各共有峰的相对保留时间和峰面积,结果相对保留时间相对标准偏差(RSD)均小于3%,占总峰面积百分比5%以上的共有峰的相对峰面积RSD均小于3%,表明仪器的精密度良好。
2.3.2 重复性试验 称取同一批雪莲培养物样品(批号20111121)5 份制备供试品溶液,分别进样测定。以紫丁香苷的保留时间和峰面积为对照,计算各共有峰的相对保留时间和相对峰面积,结果相对保留时间RSD均小于3%,占总峰面积百分比5%以上的共有峰的相对峰面积RSD均小于3%,表明本方法重复性良好。
2.3.3 稳定性试验 取同一批雪莲培养物样品(批号20111121)制备供试品溶液,分别于0、2、4、6、10 h 进样测定。以紫丁香苷的保留时间和峰面积为对照,计算各共有峰的相对保留时间和峰面积比值,结果相对保留时间RSD均小于3%,占总峰面积百分比5%以上的共有峰的峰面积比值RSD均小于5%,结果表明样品溶液在10 h内稳定。
2.4 雪莲培养物HPLC指纹图谱的建立
采用相对保留时间标定共有指纹峰,记录60 min 的色谱图,以图谱中紫丁香苷为参照物,各指纹峰保留时间与同一图谱中参照物峰的保留时间的比值为各指纹峰的相对保留时间,计算10 批雪莲培养物指纹图谱中各指纹峰的相对保留时间,以此确定共有指纹峰,各共有指纹峰的平均相对保留时间见表1,共标定出雪莲培养物的共有指纹峰9个。具有代表性的图谱见图1。采集对照品紫丁香苷和绿原酸的UV 光谱图及水母雪莲培养物7 号和8 号峰的UV 光谱图进行比较,确定其中7 号峰为紫丁香苷,8号峰为绿原酸(图2)。分别统计10批各共有峰面积与基准峰面积的比值,结果各共有峰的面积比值相对固定,单峰面积占总峰面积大于或等于10%,而小于20%的共有峰有4 个,分别为1、4、5、9 号,其差值小于±25%;单峰面积占总峰面积≥20%的共有峰有1个,为7 号峰,即紫丁香苷色谱峰。单峰面积占总峰面积<10%的共有峰,不作要求。10批共有指纹峰面积的比值均符合中药注射剂指纹图谱研究的技术要求(暂行)[4]。10 批雪莲培养物指纹图谱共有峰的峰面积比值结果见表2。
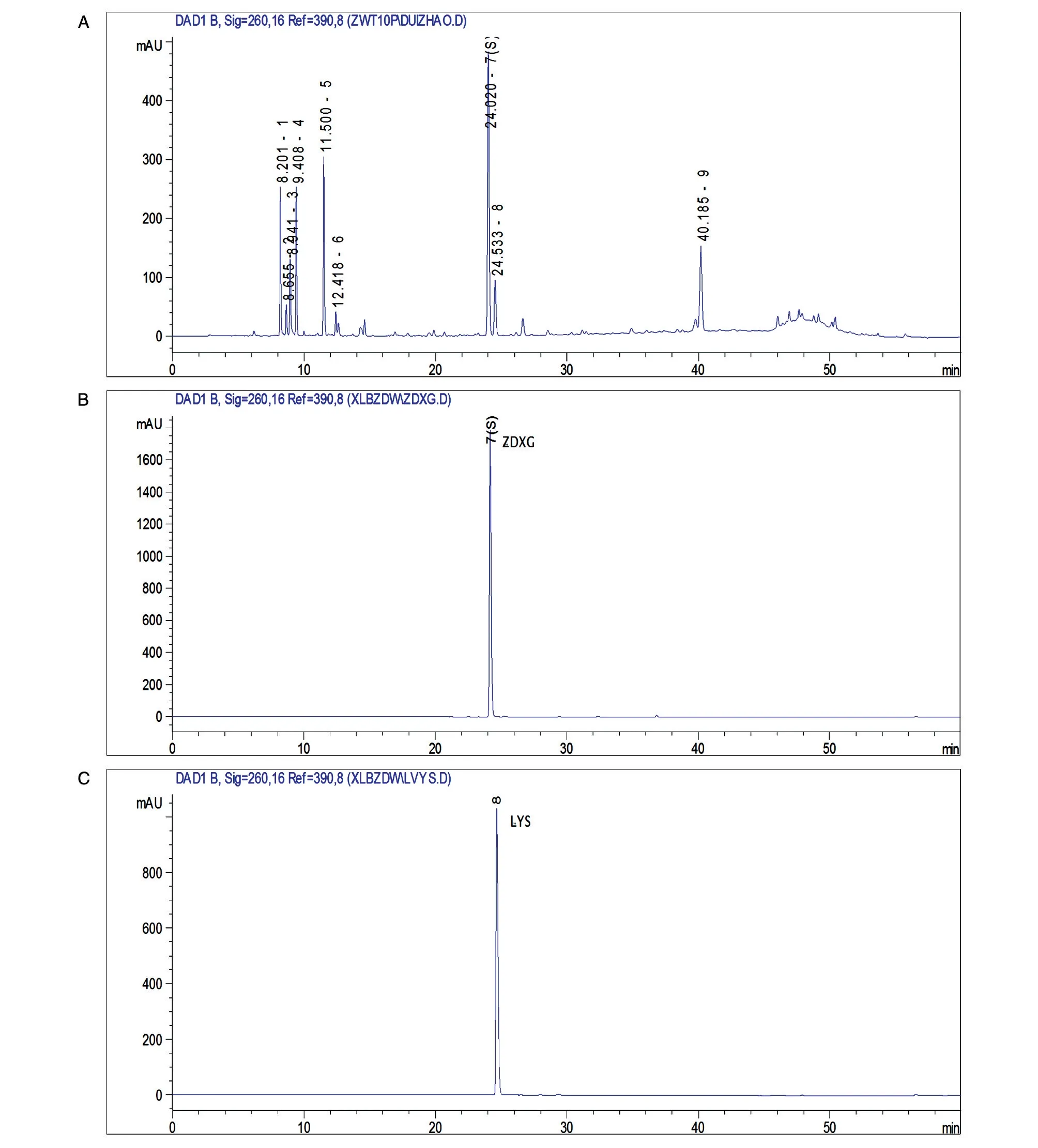
图1 雪莲培养物和对照品的HPLC图
2.5 样品相似度评价
按照建立的HPLC 方法,分别测定了10 批雪莲培养物的指纹图谱,利用“中药指纹图谱计算机辅助相似度评价软件”(版本2004A)对10 批样品图谱进行处理(图3),并进行共有谱峰拟合和相似度评价,以夹角余弦法(全图谱)计算的相似度评价结果为判断标准,10 批样品的相似度均大于0.9,相似度良好。表明样品的化学组成和含量基本一致,质量稳定。结果见表3。
3 讨论
色谱指纹图谱作为一种综合的、可量化的质量控制方法,可对中药产品的真实性、质量的一致性及稳定性进行有效检测和控制[6],也可作为植物细胞培养生产珍稀濒危野生中药材的有效质量控制方法。
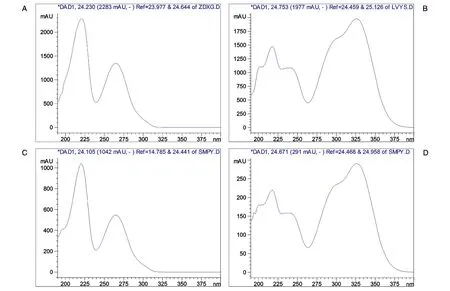
图2 雪莲培养物和对照品的UV图
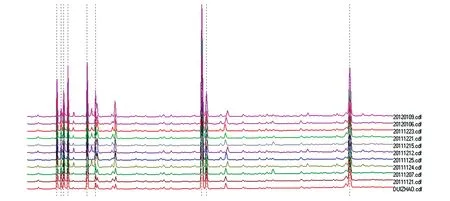
图3 10批雪莲培养物样品指纹图谱
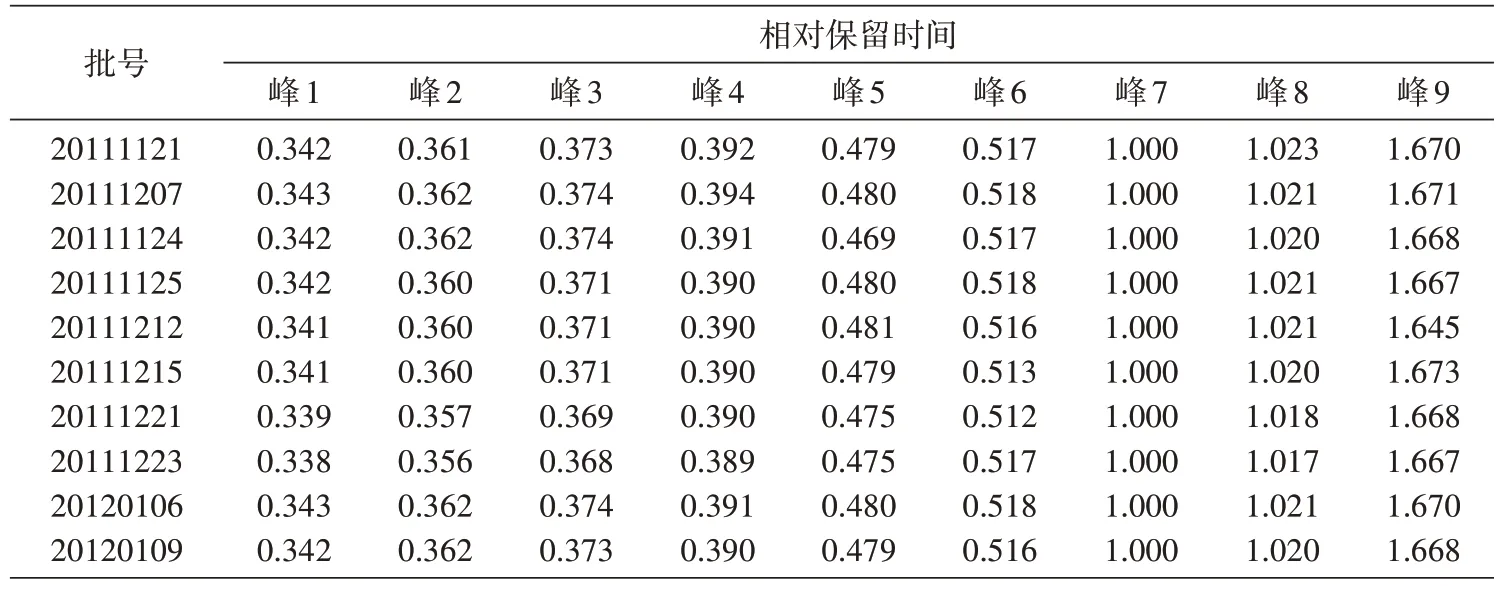
表1 10批雪莲培养物指纹图谱共有峰的相对保留时间
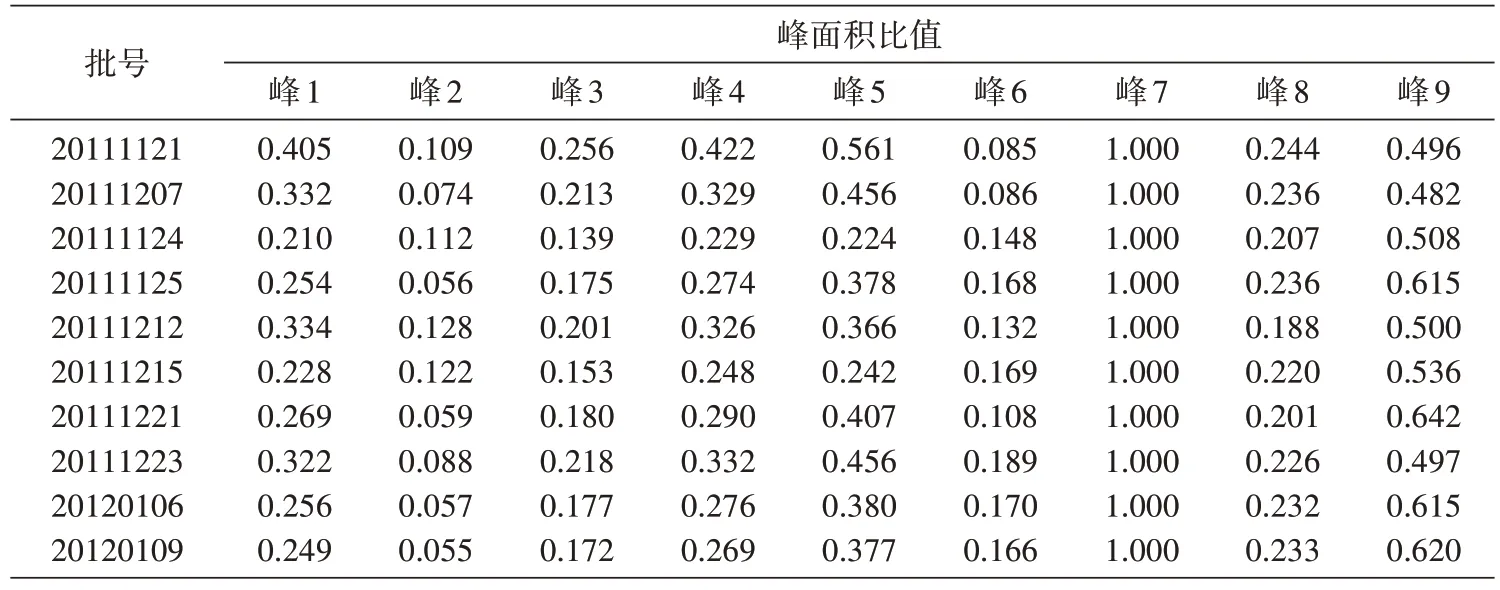
表2 10批雪莲培养物指纹图谱共有峰的峰面积比值
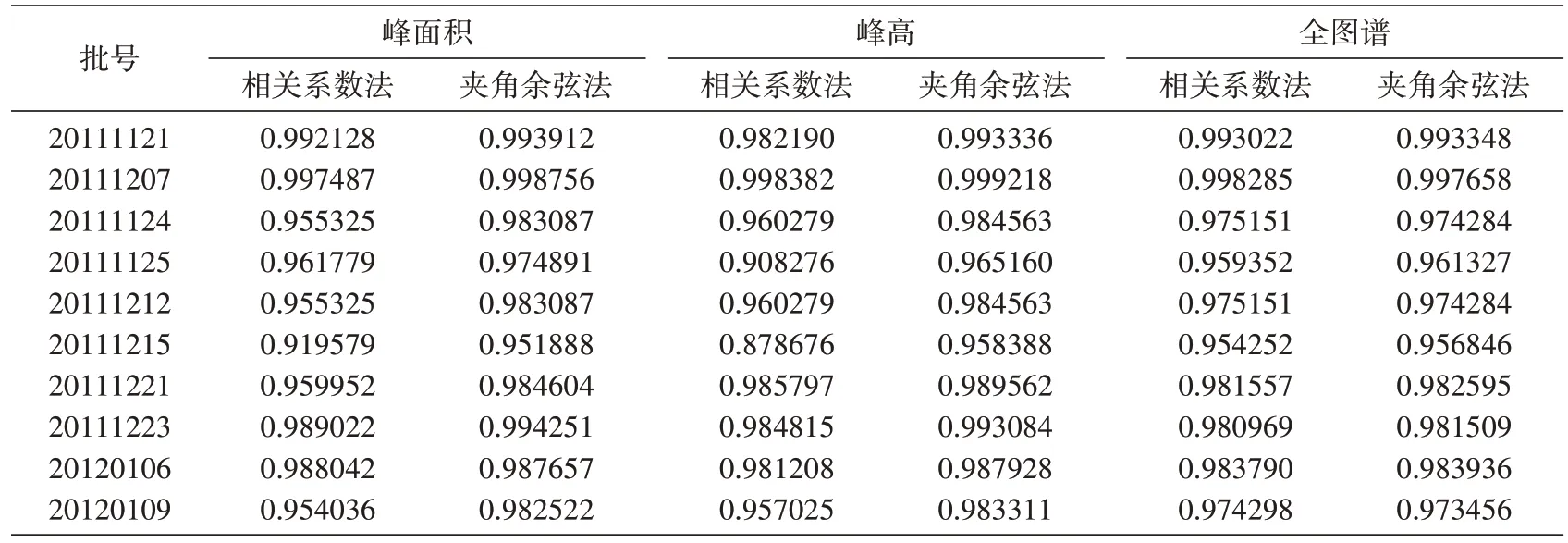
表3 10批雪莲培养物相似度评价结果
我们采用HPLC 法对雪莲培养物的特征成分进行了分析,考察了仪器的精密度,方法的重复性、精密度和样品的稳定性,同时对10 批雪莲培养物进行了指纹图谱检测。结果表明,本研究建立的雪莲培养物HPLC 指纹图谱检测方法稳定、可靠、专属性强、重现性好,采用相似度评价软件对指纹图谱结果进行评价,操作简便,不需大量复杂的计算,且数据的采集和处理更为全面和客观,可用于雪莲培养物产品的质量控制。
[1]杨永昌.藏药志[M].西宁:青海人民出版社,1992.
[2]胡显文,高丽华,赵德修,等.用于大规模植物细胞培养的稳定高产黄酮的雪莲细胞系及其建立方法[P].中国专利,CN1424395,2003-06-18.
[3]胡显文,高丽华,李佐虎,等.稳定高产黄酮的雪莲细胞系TUIP-8 的大规模高密度培养方法[P].中国专利,CN1556199,2004-12-22.
[4]国家药品监督管理局.中药注射剂指纹图谱研究的技术要求(暂行)[S].北京:国家药品监督管理局,2000.
[5]苗爱东,孙殿甲,彭燕,等.HPLC 法建立新疆雪莲指纹图谱研究[J].中成药,2003,(9):3-5.
[6]谢培山.色谱指纹图谱分析是中草药质量控制的可行策略[J].中药新药与临床药理,2001,(5):141-151.
