纳米Fe3O4-K2O·3Al2O3·6SiO2·2H2O 金色亮粉复合颗粒改性环氧涂层用于H68黄铜涂层的耐蚀性
2015-11-22裴国平周琼宇钟庆东顾帅帅
裴国平,周琼宇,钟庆东,顾帅帅,纪 丹
(上海大学 上海市现代冶金与材料制备重点实验室,上海 200072)
纳米Fe3O4-K2O·3Al2O3·6SiO2·2H2O 金色亮粉复合颗粒改性环氧涂层用于H68黄铜涂层的耐蚀性
裴国平,周琼宇,钟庆东,顾帅帅,纪 丹
(上海大学 上海市现代冶金与材料制备重点实验室,上海 200072)
利用机械混合的方法制备了纳米Fe3O4-K2O·3Al2O3·6SiO2·2H2O环氧复合涂层,并采用HV显微硬度试验,划格测试,电化学阻抗谱,极化曲线等方法研究了这种新型涂层的显微硬度、附着力和耐腐蚀性能。结果表明,这种具有黄铜色泽的新型复合环氧材料的显微硬度和附着力与环氧涂层相比略有增加,并在人工酸雨介质中具有良好的防腐蚀性能。因此,这种新型复合涂层材料是一种理想的黄铜保护材料。
防腐蚀;人工酸雨;环氧复合涂层;电化学阻抗谱;Fe3O4纳米颗粒
黄铜不仅具有优美的外观,而且耐蚀性好,具有良好的机械加工性和极强的抗生物污染能力,因此在工程应用及科学研究中得到了广泛关注。黄铜耐蚀性好的主要原因是其表面形成了一层保护性的氧化亚铜层,然而大气环境中存在酸雨的条件下,这种保护性的氧化层往往会因为局部梯度的pH变化而受到破坏[1-3]。在黄铜表面涂覆涂层能在黄铜和环境间提供一道有效的物理屏障,这被认为是一种有效的提高黄铜使用寿命及范围的方法。在已有的研究中,桐油,石蜡,油漆等都是常作为保护黄铜 (青铜)避免腐蚀的涂层材料。环氧树脂作为防腐蚀材料不但具有密实、抗水、抗渗漏好、强度高等特点,同时具有附着力强、常温操作、施工简便等良好的工艺性,而且价格适中,是金属表面涂层的理想材料。但是,现在所应用的保护涂层都不能保持黄铜的色泽,对其外观具有较大的影响,从而影响黄铜作为装饰性材料的应用。因此制备既能保持黄铜色泽又具有保护性作用的涂层具有重要的意义[4-7]。
近年来,关于用环氧涂层作为黄铜表面保护涂层的研究日益增多,对环氧涂层进行改性以进一步提高其耐蚀性能的研究具有重要的工程应用前景。Fe3O4作为一种不溶解的非惰性颜料,能够极大地提高底漆的防腐蚀性能。而K2O·3Al2O3·6SiO2·2H2O金色亮粉作为一种稳定的惰性颜料,是一种保持涂层性能的理想调色材料。本工作使用K2O·3Al2O3·6SiO2·2H2O金色亮粉配合Fe3O4调色,配制出一种具有黄铜色泽的颜料,并用其改性环氧材料,研究了纳米Fe3O4和K2O·3Al2O3·6SiO2·2H2O金色亮粉添加量对改性合环氧涂层的硬度,附着力及耐蚀性等性能的影响。
1 试验
1.1 纳米材料制备及表征
试验使用双酚-A型环氧树脂为E51型(上海树脂厂),固化剂为5784型(上海树脂厂),纳米改性材料为Fe3O4(上海圣纳米科技有限公司),纳米K2O·3Al2O3·6SiO2·2H2O 为CR112型金粉(杭州瑞彩化学科技公司) 。所有的纳米材料都严格控制控制其粒径及化学成分,如图1所示。硅烷偶联剂修饰后的纳米 Fe3O4的粒径分布均匀,约为80 nm。图2为K2O·3Al2O3·6SiO2·2H2O粉末的 TEM照片,粒径在200~300 nm。

图1 KH550 硅烷偶联剂修饰后纳米Fe3O4的TEM照片Fig. 1 TEM image of Fe3O4 particles modified by Silane coupling agent KH550

图2 纳米K2O·3Al2O3·6SiO2·2H2O的TEM照片Fig. 2TEM image of nano K2O·3Al2O3·6SiO2·2H2O particles
1.2 复合环氧涂层的制备
首先将金色亮粉 K2O·3Al2O3·6SiO2·2H2O粉末均匀分散到E51型环氧树脂,之后将 K2O·3Al2O3·6SiO2·2H2O-环氧树脂在50 ℃进行自脱气2 h。同时将20 g 纳米Fe3O4在120 ℃真空干燥12 h。将干燥后的粉体加入80 mL无水乙醇和去离子水的混合液体中(无水乙醇和去离子水的体积比为1∶1) ,机械搅拌均匀。将质量浓度为20%的硅烷偶联剂(4 g)滴入混合液体中后,将搅拌后混合液体在8 000 r/min的速率下进行离心分离,并用去离子水和无水乙醇反复清洗离心后的粉体。将Fe3O4纳米粉体在80 ℃真空干燥24 h,随后将一定量的Fe3O4纳米颗粒均匀分散在丙酮溶液中(金属氧化物粉末与丙酮的比重为1∶2,为了使涂层材料具有黄铜色泽)。最后将含Fe3O4纳米粉体的丙酮与K2O·3Al2O3·6SiO2·2H2O-环氧树脂混合并搅拌均匀后在50 ℃自脱气6 h。然后放置在真空环境中(-0.1 MPa,50 ℃、2 h)。
最后将5784型的固化剂加入所得的混合体 (质量比 E51∶5784=2∶1)降温至25 ℃,固化48 h。所得的产品就是环氧/K2O·3Al2O3·6SiO2·2H2O/Fe3O4纳米颗粒复合材料,试验中所制备的复合材料的名称及成分如表1所示。

表1 试验中所制备的复合环氧树脂中纳米粉体含量
纳米材料改性后的环氧树脂通过线棒涂布器涂覆在基体电极上。然后在温度为(25±2) ℃,相对湿度为50%的环境中固化48 h。涂层的厚度通过QF涂层测厚仪测得,保证涂层的厚度控制在(60±5) μm。试验中另外用H68黄铜电极及涂覆未改性过的纯E51环氧涂层进行对比试验。
1.3 电化学测试
电化学测试在CHI660C电化学工作站上完成。采用三电极体系,工作电极为涂覆复合环氧涂层的黄铜电极(面积为1 cm2),参比电极为饱和甘汞电极(SCE),辅助电极为铂电极。文中电位若无特指,均相对于SCE。极化曲线(Tafel)测试在开路电位±250 mV的电位范围内进行测试,扫描速率为0.01 V/s;电化学阻抗谱(EIS)测量在开路电位下进行,其频率范围为0.01 Hz ~100.0 kHz。以上电化学测试均在室温下进行。测试溶液为人工酸雨,具体成分见表2。试验中所用溶液均采用分析纯药品和去离子水配制。

表2 人工酸雨成分(pH=4.3)[8]
2 结果与讨论
2.1 涂层的密度
纳米Fe3O4-K2O·3Al2O3·6SiO2·2H2O-环氧树脂的密度(g/cm3)如下:E51 1.175,EFC1 1.186,EFC2 1.191。纳米填充物含量对密度的影响不大,计算出本工作所研究的两种环氧树脂1 000 g用量能制备厚度为60 μm的环氧涂层14 m2。2.2 涂层的显微硬度和附着力
涂层的显微硬度测试在ASTM E-384型维氏硬度仪上进行,测试载荷为1.96 N,保持压力5 s,硬度测试结果如下:E51 14.6 HV,EFC1 16.8HV,EFC2 18.5。可以看出用纳米Fe3O4-K2O·3Al2O3·6SiO2·2H2O改性过的环氧涂层的硬度大幅提升。
在环氧涂层中加入其他添加物不仅会改变涂层的耐蚀性,还会对涂层的机械性能产生很大的影响。根据文献报道,合适的添加颗粒及添加量能够大幅提高涂层的性能[9-11]。在这些性能中,良好的附着力是涂层具有良好耐腐蚀性能的基本要求。本工作中涂层的附着力采用GB/T 9286-1998 (相对于ISO 2409:1992)标准测试。结果表明,所有EFC样品的附着力都能达到“0”级,全面无一格脱落。但是对于E51样品,在切口交叉处有几点少许涂层脱落,样品的附着力能达到“1”级。所以,纳米Fe3O4-K2O·3Al2O3·6SiO2·2H2O 改性后环氧树脂能很好地涂覆在H68黄铜基体上。由显微硬度测试结果可见,加入纳米Fe3O4-K2O·3Al2O3·6SiO2·2H2O能够提高环氧涂层的显微硬度,Fe3O4加入量提高后(EFC2)能进一步提高其表面硬度。
2.3 涂层的耐蚀性
图3为H68黄铜,E51, EFC1,EFC2四种试样在人工酸雨中浸泡不同时间后的电化学阻抗谱。从图中可以看出,随着浸泡时间增加,阻抗值呈现下降的趋势,中频区的相角有向高频移动的趋势;H68黄铜表面涂覆涂层后表面的阻抗值显著增大,E51环氧涂层比基体增加2个数量级,而纳米Fe3O4-K2O·3Al2O3·6SiO2·2H2O改性后环氧树脂阻抗值增加有3个数量级。同时,基体阻抗相角图在中频区表现出一个时间常数,而涂层阻抗相角图在中频区均出现有两个时间常数。

图3 不同试样在人工酸雨中浸泡3 h和3 d后的阻抗Bode图Fig. 3 Bode plots of the samples immersied in ARW after 3 hours and 3 days
在电化学阻抗谱中,在低频区的阻抗模量(|Z|0.01 Hz)是表征涂层耐腐蚀性能的一个重要的参数[12-15],从图3中所得到的阻抗模量|Z|0.01 Hz列于表3中。由表3可见,在人工海水中浸泡3 h后,EFC2试样在频率为0.01 Hz 的时候表现出最高的|Z|0.01 Hz值(37.83 MΩ·cm2),其次是EFC1涂层(30.367 MΩ·cm2),而未改性的E51环氧涂层|Z|0.01 Hz较低,仅2.735 MΩ·cm2。而在浸泡3 d后,E51环氧涂层的|Z|0.01 Hz值大大降低(0.984 0 MΩ·cm2),表面人工酸雨已经侵蚀环氧涂层,涂层的保护性能大大减弱;而EFC1 及EFC2涂层则分别为10.59 MΩ·cm2和15.75 MΩ·cm2,阻抗值仍然保持在较高的数量级,表明纳米Fe3O4-K2O·3Al2O3·6SiO2·2H2O改性后环氧涂层具有更好的防腐蚀性能。而值得注意的是裸露的H68基体电极在浸泡后3 h和3 d后|Z|0.01 Hz值仅仅只有17.08 kΩ·cm2及10.89 kΩ·cm2。因此,采用EFC1及EFC2涂层涂覆在H68黄铜表面能大大提高黄铜的使用寿命。
图4为H68黄铜,E51, EFC1,EFC2 四种试样在人工酸雨中浸泡3 d后的极化曲线。表4为 其相关电化学参数拟合。可以看出,除了H68黄铜外,纯E51环氧树脂涂料腐蚀电流密度最高,EFC2涂层腐蚀电流密度最低,显示最好的保护作用,其次是复合涂层与EFC1混合,纯环氧树脂涂层提供了最大的保护作用。

表3 不同试样在人工酸雨中浸泡的阻抗模量|Z|0.01 Hz
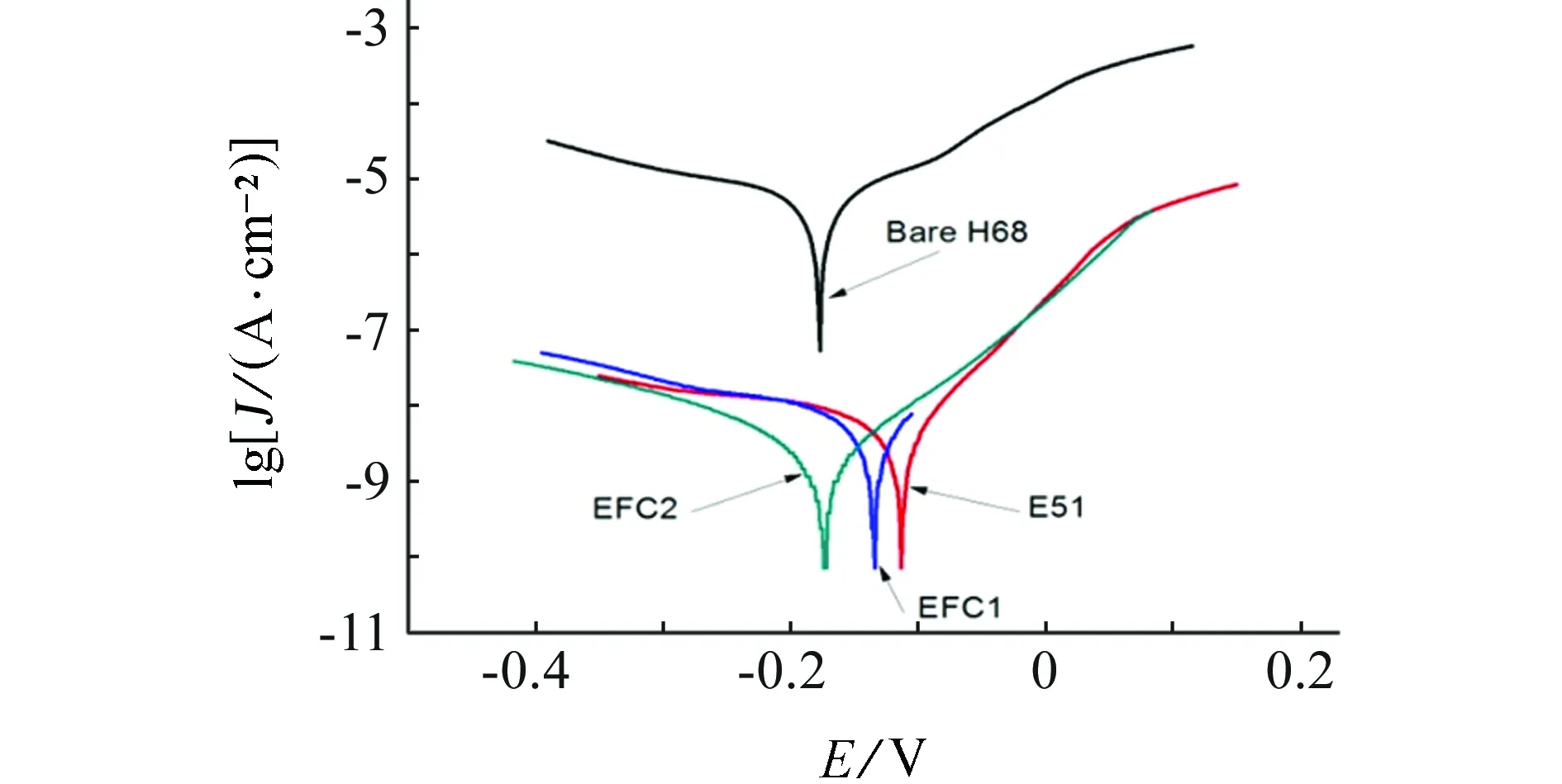
图4 浸泡3 d后的极化曲线Fig. 4 Tafel polarization curves of all samples after 3 days of immersion

试样Ecorr/VJcorr/(A·cm-2)BareH68-0.1745.333×10-6E51-0.0937.943×10-9EFC1-0.1335.321×10-9EFC2-0.1692.006×10-9
涂层对基体的保护作用主要是对离子腐蚀过程提供一个积极的屏障保护作用, EFC涂层不仅仅有高的阻抗模值,同时比未改性的E51型环氧涂层具有更好的附着力。对于E51型环氧涂层能够明显的观察到有高的孔隙度[14],而对于EFC涂层,因为纳米粒子具有良好的可分散性,分散在环氧中的纳米粒子能够减低孔隙度及增强交联作用,进而阻止或减少腐蚀离子渗透进入涂层/基体界面,从而提升其保护性能。因此,EFC涂层比E51涂层具有更好的保护作用,电解质更加难以扩散到基体表面,表现为更好的耐腐蚀性能。根据以前的研究表明[16],在涂层中纳米Fe3O4颗粒的存在将导致腐蚀电位Ecorr负移,纳米Fe3O4将对起到阴极反应抑制作用。从表4中极化曲线测试数据我们可以看出,加入纳米Fe3O4后,所测得阴极电位变负,腐蚀电流密度降低。这个现象充分说明纳米Fe3O4会降低涂层的腐蚀速率,提高其耐腐蚀性能。
2.4 样品的表面形貌
图5为4种试样浸泡前的照片。从图中可以看出,E51型环氧涂层为透明材料,试样显示为基体材料的淡黄色。而添加不同量纳米Fe3O4-K2O·3Al2O3·6SiO2·2H2O后,EFC1,EFC2均表现出与黄铜基体极其相似的颜色,因此,用纳米Fe3O4-K2O·3Al2O3·6SiO2·2H2O颗粒改性环氧树脂能够作为一种保护黄铜基体的理想材料。

(a) H68 (b) E51涂层

(c) EFC1涂层 (d) EFC2涂层图5 不同试样浸泡照片Fig. 5 Surface of samples before immersion
图6为不同试样浸泡3 d后的表面形貌。可以看出,在浸泡初期,侵蚀性的离子,比如Cl-,SO42-和NO3-腐蚀了H68黄铜表面,因此表面形成了一层腐蚀产物,颜色也变成深褐色。而对于E51环氧涂层试样,腐蚀性的离子逐渐渗透进入环氧/黄铜界面,并与黄铜发生反应,因此E51涂层颜色变深,并且出现深褐色的点。EFC涂层试样在浸泡3 d后只有少量的深褐色点出现在涂层/黄铜基体界面处,并且没有出现鼓泡现象。因此可以看出纳米Fe3O4-K2O·3Al2O3·6SiO2·2H2O颗粒均匀地掺杂在环氧树脂基质中,并减少了基质中的孔隙,极大地提环氧树脂基质中,并减少了基质中的孔隙,极大地提升环氧涂层的耐腐蚀性能。

(a) H68 (b) E51涂层

(c) EFC1涂层 (d) EFC2涂层图6 不同试样浸泡3 d后的表面光学照片Fig. 6 Samples surface of samples after 3 days of immersion
3 结论
加入1.5每百克份数K2O·3Al2O3·6SiO2·2H2O并添加1 和1.5每百克份数纳米Fe3O4能提高环氧的耐腐蚀性能及硬度,同时,K2O·3Al2O3·6SiO2·2H2O的加入能使涂层保持和黄铜及其相似的颜色。极化曲线测试表明,在浸泡3 d的试样中,EFC涂层得电流密度降低近3个数量级,电化学阻抗值也随着加入纳米Fe3O4-K2O·3Al2O3·6SiO2·2H2O颗粒而增大,加入1.5每百克份数Fe3O4纳米粉的涂层试样表现出最好的耐腐蚀性能。研究表明,这种新型的材料可以作为一种理想的黄铜表面保护涂层。
[1] ANDY M,RANI J,KANJIRAMPARAYIL P N,et al. Corrosion behavior of brass in the vembanad estuary,India[J]. Journal of Marine Science and Technology,2010,18(5):719-722.
[2] GUNILLA H,SARA G,INGER O W,et al. Corrosion induced release of Cu and Zn into rainwater from brass,bronze and their pure metals:A 2-year field study[J]. Environment Monitor Assess,2008,144:455-461.
[3] RODHE H,HERRERA R. Acidification in tropical countries. Chapter 6 the effect of acidification on corrosion of structures and cultural property[M]. London:John Wiley & Sons Ltd,1988.
[4] SUN X M,ZHOU Q,ZHOU Q Y,et al. Study on the deterioration process of bipolar coating using electrochemical impedance spectroscopy[J]. Applied Surface Science,2011,257:6095-6101.
[5] 刘成楼,隗功祥. 防腐耐磨抗砂石撞击配套涂料的研究[J]. 现代涂料与涂装,2011,14(5):17-20.
[6] WANDA D J,VIJAYA K R,TARIG A H,et al. Synthesis and characterization of (Fe3O4/MWCNTs)/epoxy nanocomposites[J]. Journal of Applied Polymer Science,2010,116:2783-2792.
[7] HONGBO G,SRUTHI T,YUDONG H,et al. Polyaniline stabilized magnetite nanoparticle reinforced epoxy nanocomposites[J]. ACS Application Materials and Interfaces,2012,4(10):5613-5624.
[8] PETER A,CHRISTINE M D,AILSA L D,et al. Column leaching and sorption experiments to assess the mobility of potentially toxic elements in industrially contaminated land[J]. Journal of Environment Monitor,2000,2:234-239.
[9] ANDREA K,IRINA S,JAROSLAV S,et al. Anticorrosion properties of polyaniline-coated pigments in organic coatings[J]. Corrosion Science,2008,50:3549-3560.
[10] SCHAUER T,JOOS A,DULOG L,et al. Protection of iron against corrosion with polyaniline primers[J]. Progress in Organic Coatings,1998,33:20-27.
[11] ARAUJO W S,MARGARIT I C P,FERREIRA M,et al. Undoped polyaniline anticorrosive properties[J]. Electrochimica Acta,2001,46:1307-1312.
[12] PARK J H,LEE G D,NISHIKATA A,et al. Anticorrosive behavior of hydroxyapatite as an environmentally friendly pigment[J]. Corrosion Science,2002,44:1087-1095.
[13] CHEN Y,WANG X H,LI J,et al. Long-term anticorrosion behaviour of polyaniline on mild steel[J]. Corrosion Science,2007,49:3052-3063.
[14] HOU W P,LIU Y,GE Z Y,et al. Comparison study on anticorrosion performances of the epoxy coatings with two different nano-polyanilines for Q235 steel[J]. Materials and Corrosion,2013,64:9999.
[15] SHI A,KOKA S,ULLETT J. Performance evaluation on the weathering resistance of two USAF coating systems (standard 85285 topcoat versus fiuorinated APC topcoat) via electrochemical impedance spectroscopy[J]. Progress in Organic Coatings,2005,52:196-209.[16] GAMAL A E M,AYMAN M A,HAMAD A A L. Synthesis and evaluation of poly (sodium 2-acrylamido-2-methylpropane sulfonate-co-styrene)/magnetite nanoparticle composites as corrosion inhibitors for steel[J]. Molecules,2014,19:1713-1731.
Anti-corrosion Performance of Glitter Gold Color Epoxy-based Composite Coating on H68 Brass Modified by Nano-Fe3O4-K2O·3Al2O3·6SiO2·2H2O
PEI Guo-ping, ZHOU Qiong-yu, ZHONG Qing-dong, GU Shuai-shuai, JI Dan
(Shanghai Key Laboratory of Modern Metallurgy and Material Processing, Shanghai University, Shanghai 200072, China)
An epoxy-based composite coating containing various combinations of magnetic iron oxide (Fe3O4) nanoparticles and glitter gold color powder (K2O·3Al2O3·6SiO2·2H2O) were prepared by mechanical mixing method. Microhardness, adhesion and corrosion resistance of the new composites were studied by Vickers′ hardness test (HV test), cross-cut test, electrochemical impedance spectroscopy (EIS) and polarization curves, respectively. The results showed that the microhardness and adhesion of the novel composites containing fillers slightly increased compared with those of epoxy. The results also pointed out that the new composites had good anti-corrosion properties in artificial acid rainwater (ARW). Hence, those new composites can be applied to protective coating on brass ideally.
anti-corrosion; artificial acid rainwater; epoxy-besed composite coating; EIS; Fe3O4nanoparticle
2014-04-27
国家自然科学基金(50571059,50615024); 教育部新世纪优秀人才支持计划(NCET-07-0536)
钟庆东(1969-),教授,博士,从事材料腐蚀相关研究,021-56338244,qdzhong@shu.edu.cn
TG174
A
1005-748X(2015)01-0006-05
