甲缩醛与三聚甲醛合成聚甲氧基二甲醚反应速率研究
2015-11-18张建强夏成良刘小兵刘显科房鼎业刘殿华
张建强,唐 斌,夏成良,刘小兵,刘显科,房鼎业,刘殿华
华东理工大学化工学院,上海 200237
近年来,随着石油消耗量的持续增加以及人们环境保护意识的不断加强,对以石油为主要原料的内燃机油耗和排放要求日益苛刻。为达到改善燃料品质、减少有害气体排放的目的,较为简单、经济、可行的一种方法是在燃料中添加含氧添加剂[1]。现阶段已经有不少化工企业以及化工研究所致力于开发合成较为合适的含氧化合物,其中包括:缩醛[2]、醚[3]、醇、脂、碳酸酯、甘油衍生物[4]等。聚甲氧基二甲醚[5](Polyoxymethylene Dimethyl Ethers,PODE)因十六烷值高、含氧量高等优点备受广大专家学者的关注。
聚甲氧基二甲醚具有良好的燃烧性能和环保性能,对于改善柴油品质具有重大意义。将它加入到柴油中可以提高燃油的十六烷值[6,7],有效抑制尾气黑烟的排放,本身固有的自供氧能力也在促进燃烧中起着明显的作用。聚甲氧基二甲醚结构通式为CH3O(CH2O)nCH3,PODE3-8十六烷值平均高达76,添加到柴油中品质好于超低硫柴油。在柴油中添加10%~15%(体积分数)的PODE 可降低50%以上的尾气污染[8-11],因此合成聚甲氧基二甲醚用作柴油添加组分具有战略意义和良好的经济价值[12-13]。
目前对PODE 的研究主要集中在合成上,虽然取得了一定的成效,但仍存在很多问题,其中催化剂、反应器和工艺设计都尚未达到工业化要求[14]。合成PODE 的原料包括提供两端CH3O-的甲醇、二甲醚、甲缩醛(DMM)和提供主链-CH2O-的甲醛(FA),甲醛的存在形式又分为甲醛溶液、三聚甲醛(TF)和多聚甲醛。催化剂的种类主要是具有强酸性的固体酸和液体酸,其中固体酸包括强酸性阳离子交换树脂[6,7]、强酸性硅铝分子筛[15]、氧化铝[16]、杂多酸[17]、对甲基苯磺酸、膨润土、蒙脱土等,液体酸包括离子液体[18,19]、硫酸、盐酸、甲酸、硝酸等[20-24]。
关于甲缩醛和三聚甲醛反应速率研究报道的文献很少,Burger 等[7]对甲缩醛和三聚甲醛间歇反应合成PODE 进行了反应速率方程的研究。对PODE 合成反应分别按照拟均相动力学模型和吸附动力学模型进行了模拟计算,结果表明吸附动力学模型计算结果与实验结果更为接近,吸附动力学模型能够很好地拟合PODE 间歇合成反应过程。对于连续固定床反应器中合成PODE 的反应速率研究尚未有报道。本实验采用甲缩醛和三聚甲醛为原料,以强酸性阳离子交换树脂和对甲基苯磺酸为复合催化剂,在连续固定床反应器中催化合成PODE。反应方程式如下:
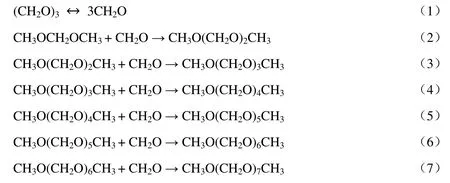
开展了在连续固定床反应器中合成PODE 反应速率研究,根据反应机理建立了反应速率方程,采用四阶龙格库塔法求解反应速率微分方程,使用粒子群法对反应速率方程参数进行了拟合回归。
1 实验部分
1.1 实验步骤
甲缩醛质量分数95%以上;甲醛溶液质量分数37%;多聚甲醛、三聚甲醛、无水甲醇和甲基苯磺酸均为分析纯;催化剂为阳离子交换树脂,化学纯。
PODE 合成反应在固定床管式反应器中进行。催化剂颗粒大小为0.180~0.425 mm,装填量0.5 g。催化剂装填完毕后,通入氮气置换、升压至反应所需压力;等反应压力稳定后,启动升温程序。待反应管温度达到设定值后,开始进料,反应一定时间(6 h)后进行取样。反应产物由气相色谱(PE GC580)分析,反应结果稳定后,停止进料,并降温、卸压。
1.2 分析方法
反应产物在色谱PE GC580上进行分析。Elite-wax毛细管柱,进样器和检测器的温度均为250 ℃,柱箱程序升温:45 ℃下保持3 min,以20 ℃/min 升温至220 ℃,保持3 min 后分析结束。
2 结果与讨论
2.1 实验结果
在进行反应速率实验之前考察了催化剂外扩散和催化剂寿命的影响,实验结果表明,当液体质量空速大于1.32 h-1时,外扩散影响消除;催化剂在反应条件70 ℃、2.0 MPa 下,运行300 h 过程中未发现有催化剂失活现象。因此,在本实验操作的反应条件下已经消除了外扩散和催化剂失活的影响。在反应温度为70 ℃下,反应速率实验采用单因素法考察了空速、压力、原料配比对反应活性的影响。实验数据见表1。
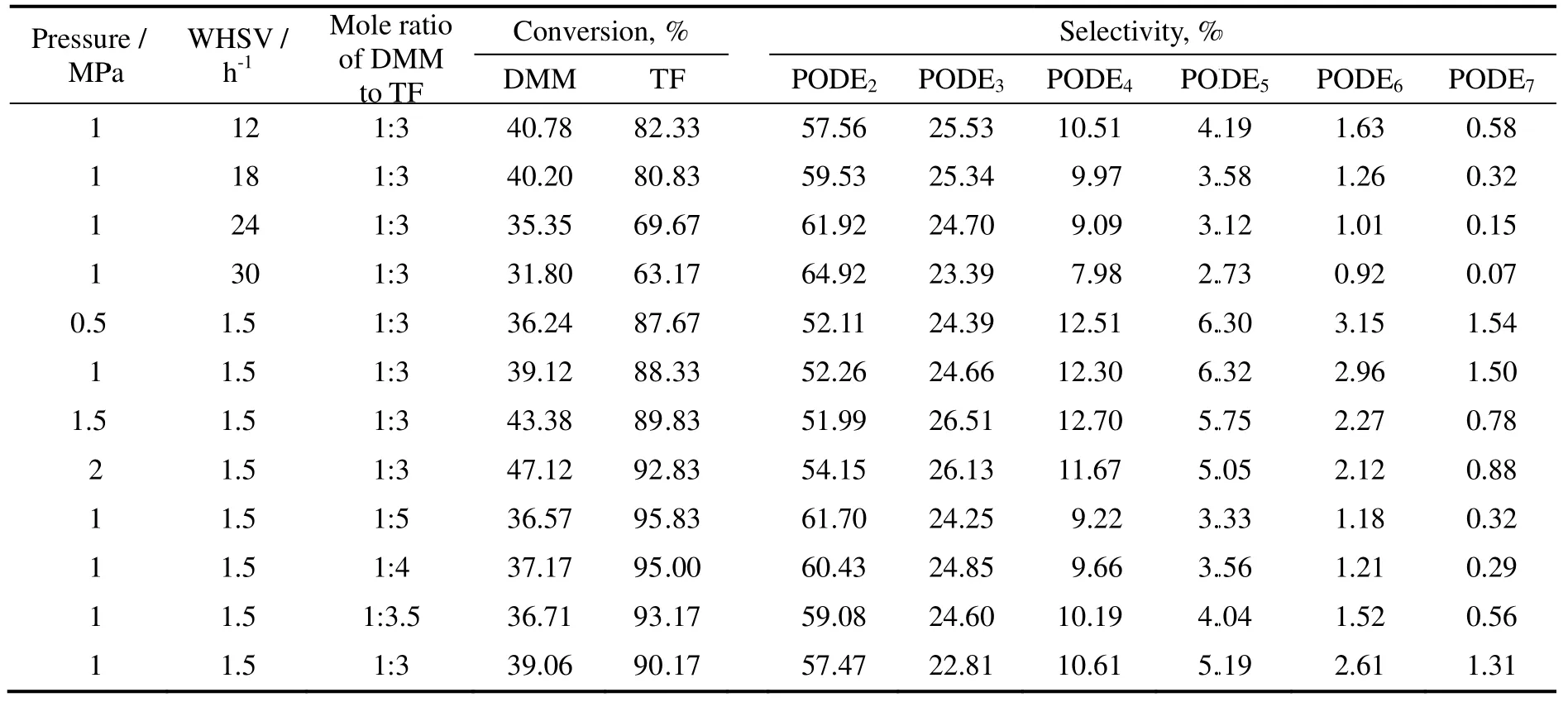
表1 反应速率实验数据Table 1 Experrimental data of the reaction rrate
2.2 反应速率方程
本实验在70 ℃下副反应较少,副产物物可以忽略不计。在反应方程组的基础上可得到如下反反应网络,如图1所示.
聚甲氧基二甲醚合成反体系中,三聚甲甲醛并不能直接参与反应,而是解聚成甲醛单体后参与PODE 的合成。三聚甲醛解聚为甲醛是一个可逆反应应而且反应速率较快,在短时间内可以达到反应平衡,假设反应(1)为一级反应,该反应速率方程可表示为:

图1 PODE合合成反应网络Fig.1 The completereacttion network for thePODE syntheesisfrom methyllal and trioxymethylene
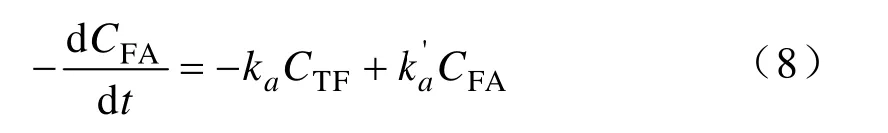
由于该反应速率较快,可以认为反应(1)在整个反应过程中均处处于平衡状态态,即:三聚甲醛与甲醛在达到反应平衡时的摩尔浓浓度关系为:实验验结果表明:当反应温度为70 ℃时,为3。
聚甲氧基二甲醚合成反应体系中各物质质的反应速率方程如下所示:
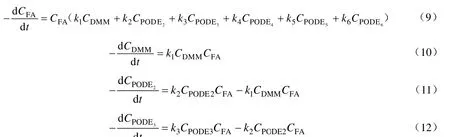

式中的Ci为i组分的摩尔浓度,kmol/m3;ki为速率常数;PODEn为聚合度为n的聚甲氧基二甲醚。
考虑到PODE 合成反应为液-固催化反应,因此在建立反应速率方程时需要考虑内扩散、吸附、反应以及脱附对反应造成的影响。反应过程中固体催化剂始终被包裹在液相中,因此,液体充满催化剂的各个孔道,造成孔道外流体中的反应物很难穿过孔中的液层向内扩散,而孔道内的反应生成物也难以向外扩散。对本反应所用催化剂而言,由于催化剂的活性很高,吸附-反应-脱附过程均能快速进行,因此可以近似认为甲缩醛和三聚甲醛催化制备聚甲氧基二甲醚的反应过程中内扩散为控速步骤。反应速率方程中涉及到甲醛、甲缩醛小分子物质浓度时,认为其一级反应级数不变。但对于PODE6和PODE7这两个大分子来讲,它们的组分浓度在催化剂孔内保持不变,反应级数视为0 级。PODE6和PODE7的反应速率方程表示为:

聚甲氧基二甲醚合成反应是总摩尔数不断减少的反应,所用固定床管式反应器又是平推流反应器,在之前的假设条件(恒温,恒压,恒体积的理想液态混合物)下,可认为任一催化剂床层截面微元的流体质量进料速率相同,为方便处理,以各组分的质量分数来代替摩尔浓度表示反应速率方程:
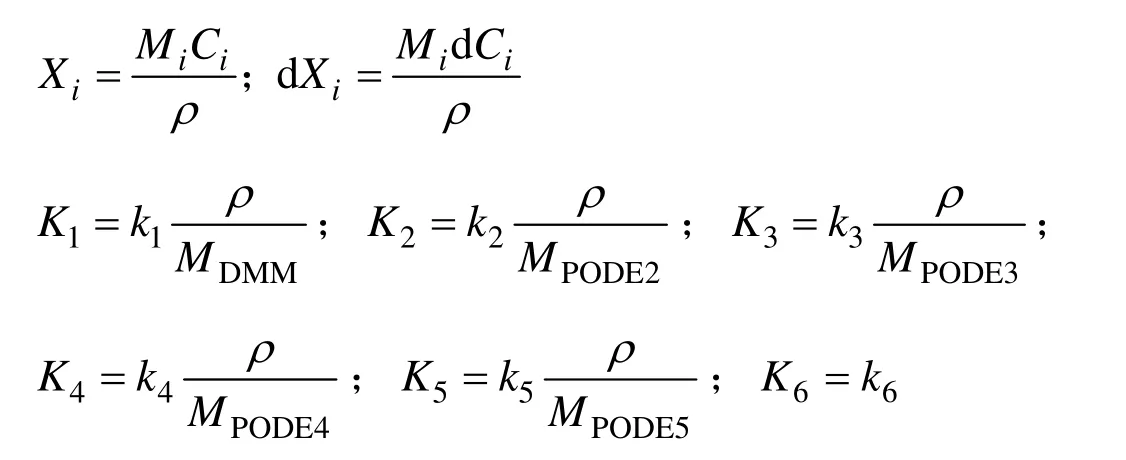
将上述表达式代入速率方程(9)~(14)、(17)、(18)整理得到:


在上述方程组中,Xi表示i组分的质量分数;Ki表示内扩散控制时表观反应速率常数;Mi为组分i的摩尔分子量g/mol;ρ为反应流体的密度,kg/m3。
为了求解反应速率方程参数,将上述方程组进行联立写成一个有约束条件的常微分方程组,用下式表示:

其中,t表示时间,s;表示因变量向量,表示初值向量。
目标函数为反应后各物质质量分数实验值和模型计算值的残差平方和最小:

其中Xi,j为通过反应速率计算得出的组分i的质量分数,xi,j为实验得到的组分i的质量分数。收敛判定标准为最小残差小于0.01。
模型参数的计算方法是将速率方程联立,对有约束条件的微分方程组(27)进行求解,得到催化剂床层出口处各组分浓度,通过对速率方程求解的各组分出口浓度和实测浓度进行优化,计算出被估参数的最优值。采用四阶龙格库塔方法对反应速率方程进行微分计算,使用粒子群法对反应速率方程参数进行了拟合回归,得到的结果见表2。

表2 反应速率常数Table 2 The rate constant Ki
根据计算结果分析所示,均方差、残差平方和、相关系数和F统计结果见表3。表3的统计结果表明该模型能够较好地拟合PODE 合成反应过程。

表3 反应速率方程模拟统计结果Table 3 The statistical results of reaction rate simulation
对不同质量空速下反应器出口各组分质量分数的实验值和反应速率方程的模拟计算值进行了比较,结果如图2所示。

图2 产物中各组分质量分数计算值和实验值的比较Fig.2 Comparison of calculated values with experimental data for compositions in products
图2对比了产物中甲缩醛、三聚甲醛、PODE2、PODE3、以及PODEn聚合度为4~7 的产物质量分数的计算值和实验值的比较,结果证明模型计算结果与实验值符合良好,该宏观反应速率方程推导及求解是合理的。
综上所述,建立的反应速率方程在实验的条件下能够很好的拟合甲缩醛和三聚甲醛合成PODE 反应的产物分布以及甲缩醛和三聚甲醛的转化率。
3 结 论
采用了对甲基苯磺酸改性的强酸性阳离子交换树脂催化剂催化甲缩醛和三聚甲醛合成聚甲氧基二甲醚,实验表明该催化剂具有较好的催化活性,三聚甲醛的转化率可达95%以上。根据连串反应机理,建立了幂函数反应速率方程,采用四阶龙格库塔法对反应速率方程进行微分计算,使用粒子群法对反应速率方程参数进行了拟合回归,计算结果表明,该模型能较好的拟合甲缩醛和三聚甲醛的转化率以及产物分布,为该反应进一步扩大生产提供了基础数据。
[1]冯伟樑, 李 丰, 高焕新, 等.聚甲醛二甲醚的制备方法:中国, 101768058A [P].2010-07-07.
[2]Celik F E, Kim T J, Bell A T.Effect of zeolite framework type and Si/Al ratio on dimethoxymethane carbonylation [J].Journal of Catalysis, 2010, 270(1):185-195.
[3]Liu D H, Yao C F, Zhang J Q, et al.Catalytic dehydration of methanol to dimethyl ether over modifiedγ-Al2O3catalyst [J].Fuel, 2011,90(5):1738-1742.
[4]Deshmukh S A R K, Annaland A V S, Kuipers J A M.Kinetics of the partial oxidation of methanol over a Fe-Mo catalyst [J].Applied Catalysis A-General, 2005, 289(2):240-255.
[5]Wiberg K B, Murcko M A.Rotational barriers 4 dimethoxymethane the anomeric effect revisited [J].Journal of the American Chemical Society, 1989, 111(13):4821-4828.
[6]Burger J, Siegert M, Strofer E, et al.Poly(oxymethylene) dimethyl ethers as components of tailored diesel fuel:Properties, synthesis and purification concepts [J].Fuel, 2010, 89 (11):3315-3319.
[7]Burger J, Strofer E, Hasse H.Chemical equilibrium and reaction kinetics of the heterogeneously catalyzed formation of poly(oxymethylene) dimethyl ethers from methylal and trioxane [J].Industrial &Engineering Chemistry Research, 2012,51(39):12751-12761.
[8]Hagen G P, Spangler M J.Preparation of polyoxymethylene dialkane ethers, by catalytic conversion of formaldehyde formed by dehydrogenation of methanol or dimethyl ether:US, 6350919 [P].2002-02-26.
[9]Hagen G P, Spangler M J.Preparation of polyoxymethylene dimethyl ethers by catalytic conversion of formaldehyde formed by oxidation of dimethyl ether:US, 6392102 [P].2002-05-21.
[10]Hagen G P, Spangler M J.Preparation of polyoxymethylene dimethyl ethers by catalytic conversion of formaldehyde formed by oxy-dehydrogenation of dimethyl ether:US, 0171534 [P].2003-09-11.
[11]Hagen G P, Spangler M J.Preparation of polyoxymethylene dimethyl ethers by acid-activated catalytic conversion of methanol with formadehyde formed by dehydrogenation of methanol:US, 0007089 [P].2002-01-17.
[12]Echhard S, Hans H, Sergej B.Method for producing polyoxymethylene dimethyl ethers from methanol and formaldehyde:US, 7671240 [P].2010-03-02.
[13]Hagen G P, Spangler M J.Preparation of polyoxymethylene dimethyl ethers by catalytic conversion of dimethyl ether with formaldehyde formed by dehydrogenation of dimethyl ether:US, 6160186 [P].2000-12-12.
[14]张建强, 唐 斌, 刘殿华, 等.聚甲氧基二甲醚合成研究现状 [J].煤化工, 2013, 164(1):41-43.Zhang J Q, Tang B, Liu D H, et al.Research process of polyoxymethylene dimethyl ethers synthesis [J].Coal Chemical Industry, 2013,164(1):41-43.
[15]李 丰, 冯伟樑, 高焕新, 等.分子筛催化合成聚甲醛二甲醚的方法:中国, 102040491A [P].2011-05-04.
[16]赵 光.改性γ-Al2O3催化合成聚甲氧基二甲醚 [D].上海:华东理工大学化工学院, 2012.
[17]冯杰荣.甲醇与甲醛合成聚甲氧基甲缩醛研究 [D].上海:华东理工大学化工学院, 2011.
[18]夏春谷, 宋河远, 陈 静, 等.甲醛与甲醇缩醛化反应制备聚甲氧基二甲醚的工艺过程:中国, 102249868A [P].2011-11-23.
[19]陈 静, 唐中华, 夏春谷, 等.聚甲氧基甲缩醛的制备方法:中国, 101182367 A [P].2008-05-21.
[20]李 丰, 蒋元力, 李伍成, 等.以甲醇与甲醛为原料合成聚甲醛二甲醚的方法:中国, 102320941A [P].2012-01-18.
[21]丁 鹏, 荣峻峰, 付 强, 等.一种氧化转化甲醇的催化剂:中国, 101940940A [P].2011-01-12.
[22]施特勒菲尔, 舍 林, 哈 塞, 等.由二氧杂环己烷和二烷基醚制备聚甲醛二烷基醚的方法:中国, 101198576 [P].2008-06-11.
[23]于 鹏, 荣俊峰, 付 强, 等.一种甲醇转化制备聚甲氧基二甲醚的方法:中国, 101817731A [P].2010-09-01.
[24]李晓云, 于海斌, 孙彦民, 等.一种以负载氧化铌催化剂制备聚甲醛二甲醚的方法:中国, 101972644A [P].2011-02-16.
