双纵坐标图像信息的解读思路与角度
2015-11-09夏时君
夏时君
摘要:以双纵坐标图像信息为研究对象,通过分析其研究范围和坐标关联,明确引入双纵坐标图像的必要性和重要性。从识图、析图和用图3个层面提出解读图像思路,并提出关注单线趋势、对比多线差异、分析多线联系等策略,完成图像信息解读从方法到操作的跨跃。
关键词:双纵坐标图像;图像信息;解读思路
文章编号:1005–6629(2015)9–0081–05 中图分类号:G633.8 文献标识码:B
双纵坐标图像作为图像表征的重要形式,是近年化学教学与考试的热点和亮点。相对于单纵坐标图,它涉及到影响因素增多、变量关系复杂、信息综合加强,这势必对图像信息的获取、处理和运用提出更高要求,使得图像信息的解读、描述、描绘难度增大。基于双纵坐标图像具有独特的知识、信息和工具等价值,笔者以近年各省市高考试题或模拟试题中典型素材为研究对象,剖析解读双纵坐标图像信息的思路和方法,以挖掘渗透其中的因素、关系和规律,达到更好的理解和运用图像的目的。
1 双纵坐标图像表征的适用性讨论
就认识化学反应而言,可从物质用途、物质结构、化学实验、物质转化、工业生产等10个角度进行理解[1]。就条件影响而言,同一条件可能引发多种影响。如温度除影响反应速率和化学平衡外,还可能导致物质状态、溶解性、稳定性、氧化性、水解性、酸性等性质变化,以及产品产量、外观、纯度等差异;又如溶液pH变化可能引发物质存在形式、浓度、含量、性质和反应等变化。
基于物质性质多样性、转化多向性、反应可逆性等原因,化学过程往往具有复杂性和动态性。在表征化学过程的因素关系、转化过程、数量比较上,单、双纵坐标具有各自独特的价值。相对于单纵坐标图像主要解决单一(或多个)自变量对单个因变量的影响;双纵坐标主要解决在一定实验条件下,一个自变量产生的两个或多个不同量纲、不同数量级的影响。借助双纵坐标图像可以巧妙地表达出变化的过程性和因素的关联性,从而揭示出图像背后的化学原理本质特征[2]。相对于借用多组单纵坐标图像反映一个自变量对多个因变量的影响,双纵坐标图像则显得简化一些,也更易于发现曲线间的逻辑顺序与因果关系。
2 双纵坐标图像坐标的关联性分析
所谓双纵坐标图像是指在同一坐标系中以左、右两个不同纵轴绘制的多条曲线。两个坐标可以具有不同量纲、不同数量级。双纵坐标的相关性有以下情况:(1)双纵坐标对应的化学意义具有同一性或相似性:如相同物理量,由于数值相差较大,为了图像呈现的简捷、直观、可读,采用不同数量级进行衡量;又如具体数值和百分比的数值差异太大,同一标准下无法显示信息的变化规律与特点,可采用不同的量纲。(2)双纵坐标对应的化学意义相关性弱:如物质制备中温度对物质产量和颗粒大小的影响;不同pH对物质存在含量和纯度的影响。(3)双纵坐标对应的化学意义具有相关性。如盐酸滴定氨水中(如图1),盐酸体积变化引起的溶液pH与温度间就存在相关性。当加入盐酸体积达到中和点时,溶液温度达到最大值,同时过程涉及中和点和中性点的区别与联系;溶液pH变化与水的电离、盐的水解、酸碱性判断、能量转化、浓度大小等化学意义多向联系。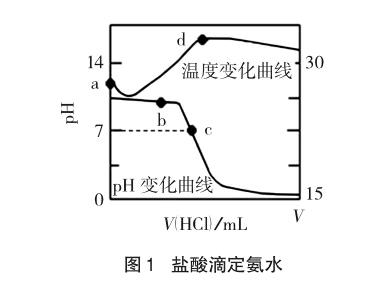
3 双纵坐标图像信息的解读思路
解读双纵坐标图像信息,可从识图、析图和用图三个层面进行。识图主要解决图像基本意义的理解,析图主要解决图像化学意义的解读,用图主要解决图像迁移运用。
识图时首先研究图像主题,它反映谁与谁的关系,重点理解坐标的表达含义、刻度和单位,有些坐标的量纲带有一定的数量级;其次弄清曲线的属性。双纵坐标图像对应两个纵坐标,曲线的属性常以图例方式区别。所谓图例就是集中于双纵坐标图一角或一侧的各种符号和颜色所代表内容与指标的说明,它是图像解读的阅读指南,常以线型、颜色和符号等形式予以区别。析图时关注曲线发展趋势和特殊变化,理解图像深层次的化学意义,即分析数形背后的化学规律、原因及关系等。用图时要善于提炼图像显性或隐性的原理及方法,通过对比情境、分析关系、把握规律,拓展研究角度和研究范围,灵活解决实际问题。
例1 钼酸钠晶体(Na2MoO4·2H2O)是无公害型冷却水系统的金属缓蚀剂,图2是碳钢在3种不同介质中的腐蚀速率实验结果。
解读:缓蚀技术是防止金属腐蚀的主要手段之一。以上图像以金属在不同条件下腐蚀效果为话题,探究缓蚀剂的作用与效果。所谓缓蚀剂是“一种以适当的浓度和形式存在于环境介质中,可以防止或减缓腐蚀的化学物质或几种化学物质的混合物”。它们通过在金属表面形成防护层,从而保持金属材料性能。从原理来看,钼酸盐是典型的无机缓蚀剂,它与金属离子作用,生成氧化物或氢氧化物覆盖在阳极上形成保护膜,抑制了金属向水中溶解,阳极被钝化,它是阳极型缓蚀剂和氧化膜型缓蚀剂。
从识图角度来看,图2反映在不同酸性条件下金属的腐蚀快慢和使用缓蚀剂的防腐效果,图例通过符号标记进行区分。
从用图角度来看,缓蚀剂从原理来看就是通过电化学的方法,在金属表面形成一层保护层,从而避免了金属的进一步腐蚀。基于以上考虑,在实际金属保护中,我们还可选择其他能在阳极形成氧化膜的物质,如铬酸盐、钨酸盐、钒酸盐、亚硝酸盐、硼酸盐等;同样也可选择阴极型缓蚀剂,如锌的碳酸盐、磷酸盐和氢氧化物,钙的碳酸盐和磷酸盐,它们在水中或在阴极区金属表面,反应产物在阴极沉积成膜,随着膜的增厚,阻挡阴极参与反应,同时能起缓蚀作用。同样使用混合型缓蚀剂因其分子有两种性质相反的极性基团,能吸附在清洁的金属表面形成单分子膜,在阳极和阴极都能成膜,拓展了使用范围和缓蚀效果[3]。
4 双纵坐标图像信息的解读角度
解读双纵坐标图像信息时,从数量上,可一条到多条曲线;从角度上,可从横向分析到纵向对比,从而完成图像表层认知到深层解读的升华。
4.1 关注单线趋势,关注特殊信息的解读
图像信息分析可从点、线、面入手,抓住点的解读和线的发展,关注一般趋势和特殊变化。具体分析过程如下:(1)关注特殊点:如起点、终点、拐点、平衡点。这些点呈现哪些数学信息?反映哪方面的化学含义?具有哪方面化学功能?(2)分析特殊曲线:如①增减性:它研究对象是什么?化学过程是如何发生的?②突变性和渐变性:产生的原因、影响和结果是什么?③斜率大小:反映的化学意义是什么?数据大小反映什么问题?④双曲线位置高低:是什么因素引起的?分析依据什么原理?转化方法是什么?总之,分析可从定性和定量分析;分析思想包括微粒观、平衡观、转化观、能量观、守恒观等。
例2 CuCl在氯的衍生物产品中占有较突出的位置,在有机合成工业中可作催化剂。以下是从含Cu2+、Fe3+的电镀废水中制备CuCl的工艺流程,见图3。
用滤液中Cu2+、Fe3+的含量对pH作图,可直观地反映出滤液中金属离子含量与pH之间的关系以及反应①系统pH与CuCl产率的关系,见图4。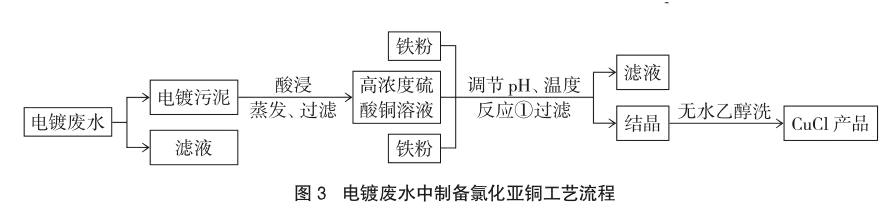
解读:左纵坐标反映pH对离子浓度大小的影响。从曲线的增减性来看,随着溶液pH的增加,Cu2+、Fe3+浓度不断减小。在pH=3.6,Fe3+完全沉淀,在pH=7.5时,Cu2+完全沉淀。在水解过程中,铁元素和铜元素的形态变化与数量分配遵循物料守恒和电荷守恒。右纵坐标反映pH对CuCl产率的影响。从曲线增减性来看,CuCl产率随pH的增加先增大后减小。在pH=3.5时,CuCl产率最大,原因是什么?从反应物来看,在Fe+2CuSO4+2NaCl= FeSO4+Na2SO4+2CuCl中,酸性条件下Fe转化为Fe2+,而碱性较强时Cu2+转化为Cu(OH)2,导致反应物的量下降,转化率下降;从产物来看,产物稳定性差,如易氧化、易分解、易挥发、易变质等也会导致产率下降。
4.2 对比多线差异,全面理解信息的异同
基于双纵坐标中一个自变量与两个因变量的对应关系,解读图像信息就可进行横向对比,对照和比较两方面的化学意义,以确定它们间的性质特征的异同,探寻事物间内在规律及联系,归纳它们的优缺点,扬长避短,找到最优化方案。
解读:(1)从曲线增减性来看,在其他条件不变下,随着氨碳比的增加,CO2的转化率不断增加, NH3的转化率不断减小,尿素的体积分数先增大后减小。(2)从曲线的斜率来看,在其他条件不变下,随着氨碳比的增加,CO2的转化率受氨碳比的影响越来越小,而NH3的转化率受氨碳比的影响几乎保持不变。(3)从曲线相对位置来看,当氨碳比<2时,转化率是NH3>CO2:当氨碳比>2时,转化率是NH3 4.3 分析多线联系,系统把握信息的逻辑关系 双纵坐标图像解读不仅要从横向对比,更要从纵向分析曲线间联系与关系。首先从逻辑入手分析曲线联系的可能性;从曲线转化中观察变量发展中的相关性和匹配性;从数量变化中分析曲线关系的主次性和量化性。常见双纵坐标图像间存在的关系有:(1)属种关系:一个物理量的全部外延与另一个物理量的部分外延重合;(2)交叉关系:一个物理量的部分外延与另一个物理量的部分外延重合;(3)矛盾关系:两个物理量外延一点也不重合,并且外延之和等于其共同属概念的外延;(4)反对关系:两个物理量的外延一点也不重合,并且外延之和小于其共同属概念外延。根据分析双纵坐标图像的相关程度,运用联系、发展和动态视角透视图像间在主次、因果、矛盾等方面的联系,更加立体系统地解读图像的化学意义。 解读:左纵坐标反映温度对催化剂催化效率的影响,右纵坐标反映温度对乙酸的生成速率的影响。从逻辑关系来看,显然催化剂催化效率也是影响反应速率的重要因素。在100~250℃时,反应速率增加与催化效率增加正相关,催化剂是主导因素;在250~300℃时,反应速率减小与催化效率降低相关,催化剂是主导因素;在300~400℃时,反应速率增加,温度是主导因素。 例5 “温室效应”是全球关注的环境问题之一。控制和治理CO2是解决温室效应的有效途径。某课题组利用CO2催化氢化制甲烷的研究过程如图7: H2参与反应Ⅰ和Ⅱ,总量逐渐减小;CH4是产物,总量逐渐增加。HCOOH是中间产物,若生成速率(反应Ⅰ)>消耗速率(反应Ⅱ),HCOOH的总量会大于CH4总量;若生成速率(反应Ⅰ)<消耗速率(反应Ⅱ),HCOOH的总量会小于CH4总量,HCOOH不断减少;若两者的速率相等,则HCOOH总量恒定。 左纵坐标反映反应物(H2)和产物(CH4)的物质的量变化;右纵坐标反映中间产物(HCOOH)的物质的量变化,两纵坐标的数量级不同。可以看出(1)增加适量镍粉后,H2和HCOOH的数量都有明显减少,说明Ni对反应Ⅰ起催化作用;(2)Ni的使用量由1mol到10mol增加中,CH4量增加,HCOOH减小;且HCOOH减小量远小于CH4的增加量,说明反应Ⅱ速率远大于反应Ⅰ;且两者间差值随着Ni的增加越来越大,说明Ni对反应Ⅱ起作用,且影响大于反应Ⅰ;(3)当Ni的使用量由10mol到20mol时,HCOOH变化量较小,CH4总量减小,而CH4与HCOOH两者总量差值在减小,H2的减小却未导致CH4的增加。究其原因是“镍粉吸附H2造成的。镍粉的催化作用是因为吸附在它活性中心一小部分的H2易与其他物质反应,大部分H2不在活性中心上,不能参与反应;且气相中H2浓度过小,难以得到有效补充,所以甲烷产量反而下降”[4]。 参考文献: [1]刘文兵.高考化学试题中图形的解读[J].化学教学,2012,(7):64~67. [2]郑学裕.在化学教学中让学生多角度理解化学反应[J].化学教育,2012,(7):35~38. [3] http://baike.baidu.com/link?url=RxNVMt86Bt-7Kc6-ON9UyeqpUuMQw-ctXnfKUqLb3s_Z_PdhGFHpDrLVZ0XTfyKe4Cz7-ZjOwiDgQ8ZlpLk9eaa. [4]崔邑诚.深入解读高考新图——双纵坐标图[J].化学教学,2009,(4):65~66.