超临界CO2微乳法制备盐酸小檗碱脂质体工艺的考察与优化
2015-11-08程泓波刘为为张少华
程泓波,刘为为,张少华,曹 婷,牟 晨,礼 彤
(沈阳药科大学制药工程学院,辽宁沈阳 110016)
盐酸小檗碱[1](Berberine Hydrochloride B.H)又称黄连素,属于异喹啉类生物碱,作为抗菌药,广泛用于治疗胃肠炎、细菌性痢疾等。随着研究的深入,人们发现它还可以治疗心律失常、高血压、高脂血症、糖尿病、肿瘤等疾病,然而研究也发现盐酸小檗碱体内抑瘤作用没有体外明显,可能因其肠道吸收较差,在体内很难达到对肿瘤细胞直接作用的较高血药浓度。而且盐酸小檗碱静脉给药可能引起药疹、过敏反应、血红蛋白及血红细胞减少、药敏性休克等副作用,1982年以来我国已明令禁止使用盐酸小檗碱静脉给药。因此,如何发挥盐酸小檗碱在癌症治疗上的效果,抑制其副作用是我们面临的一大问题。脂质体[2]是一种新的给药系统,静脉注射脂质体后,脂质体很快被网状内皮系统(RES)摄取,增加药物局部浓度,提高药物疗效,降低或减少药物的不良反应。
目前制备盐酸小檗碱脂质体有薄膜分散法[3]和pH梯度法[4]等,但此法制备工艺复杂,有机溶剂使用量大,限制了盐酸小檗碱脂质体的工业化生产。笔者采用超临界CO2流体技术[5]制备盐酸小檗碱脂质体旨在探索一条环保、无污染、工艺简单的新方法路线,为其工业化生产提供可能性。
1 仪器与材料
CLJ-B-120-35-1超临界流体设备(沈阳东宇药物技术研究院超临界制造分公司),TU-1810紫外可见分光光度计(北京普析通用仪器有限责任公司),WJL激光粒度仪(苏州江东精密仪器有限公司),AR2130电子分析天平(美国 Ohaus公司),PHS-3C酸度计(中国 LIDA instrument公司),透析袋(截留分子质量8 000~14 000 U,美国Scientific Research-Special公司),恒温磁力搅拌器(南汇电讯器材厂),台式离心机80-2(常州国华电器有限公司)。
盐酸小檗碱原料药(质量分数≥98%,四川什邡华安药物原料有限公司);盐酸小檗碱标准品(中国药品生物制品检定所,批号110713-200609);CO2(食品级,沈阳景泉气体厂);LipoidS100天然大豆磷脂(SPC,质量分数≥94%,德国Lipoid公司);无水乙醇、胆固醇、磷酸氢二钠、磷酸二氢钠(天津大茂化学试剂厂);蒸馏水(沈阳药科大学自产)。
2 方法与结果
2.1 磷酸盐缓冲液的配置 精密称取Na2HPO4·12H2O 0.37 g,NaH2PO4·2H2O 2.0 g,溶于适量蒸馏水中,定容至1 000 mL,并用NaHCO3溶液调节pH=7.0,得磷酸盐缓冲液(PBS)。
2.2 超临界CO2微乳法制备盐酸小檗碱脂质体用适量无水乙醇溶解一定配比(3∶1)的大豆磷脂(SPC,磷脂浓度30 g·L-1)和胆固醇(Chol),得溶液A,将盐酸小檗碱(药脂比1∶4)加至PBS中,进行充分搅拌得溶液B。将A,B混合液超声混匀得乳黄色悬浊液,将此悬浊液置于超临界设备中,在相应条件下进行制备,反应结束后,恒速泄压得澄清半透明黄色盐酸小檗碱脂质体。
2.3 盐酸小檗碱含量测定方法
2.3.1 检测波长的确定 分别称取适量的盐酸小檗碱和空白脂质体溶于磷酸盐缓冲液(pH=7)—无水乙醇(体积比2∶3)的混合溶剂A中,并以混合溶剂A为空白,在波长200~400 nm内进行紫外扫描,如图1和图2所示,盐酸小檗碱共有242、268、345 nm三个吸收峰,而空白脂质体在近紫外端243 nm处有吸收,远紫外端345 nm处没有紫外吸收,故空白脂质体在345 nm处无紫外干扰,最终确定345 nm为紫外分光光度法测定盐酸小檗碱含量的检测波长。
2.3.2 标准曲线的制作 精密称取盐酸小檗碱标准品20 mg,加入pH=7.0磷酸缓冲液使其完全溶解,稀释并定容至100 mL后,再将该溶液用pH=7.0磷酸缓冲液稀释成 0.25、0.5、1.0、2.0、4.0、8.0 mg·L-1的标准溶液,于345 nm波长处测定其各自的吸光度。结果表明,在0.25~8.0 mg·L-1浓度范围内,盐酸小檗碱的吸光度A与其浓度C呈线性关系,回归方程为 A=5.361×10-2C+1.840×10-3,r=0.999 0。
2.3.3 精密度与稳定性实验 取高、中、低3种浓度(8.0、2.0、0.25 mg·L-1)盐酸小檗碱标准溶液,连续测定5次,得日内精密度RSD(n=5)分别为1.32%、1.02%和1.36%。连续测5 d,得到日间精密度RSD(n=5)分别为1.10%、1.35%和1.38%。结果表明,用紫外分光光度法测定盐酸小檗碱含量精密度,稳定性均良好。
2.3.4 回收率实验 精密量取0.5 mL空白脂质体溶液,分别加入高、中、低浓度(8.0、2.0、0.25 mg·L-1)盐酸小檗碱标准溶液,用溶剂A定容至25 mL,并在波长345 nm处测定吸光度,计算回收率。所得平均回收率分别为100.30%、99.89%和100.04%,RSD分别为0.16%、0.18%和1.74%,符合规定。
2.4 盐酸小檗碱脂质体包封率的测定 超临界CO2微乳法制备盐酸小檗碱脂质体,目的在于提高盐酸小檗碱脂质体被动载药的包封率,并增加其载药量,使得盐酸小檗碱脂质体有可能达到抑瘤所需要的血药浓度,同时降低给药体积,增加生物安全性。因此本文以脂质体包封率为实验指标。
选择无盐酸小檗碱的脂质体透析溶液为参比,采用紫外可见分光光度计在波长345 nm处测量透析[6]后游离的盐酸小檗碱的含量,通过下式计算出脂质体的包封率(EE%):
式中 m1——脂质体中盐酸小檗碱的总质量
m2——游离盐酸小檗碱质量
2.5 超临界CO2流体制备盐酸小檗碱脂质体的工艺考察
2.5.1 压力对盐酸小檗碱脂质体包封率的影响由图3可见,随着制备压力的增加,包封率呈先增后减的趋势。分析认为当系统处于亚临界状态时,随着体系CO2含量的增加,CO2气体小分子进入脂质体双分子层内部溶胀形成球形胶质结构,当处于超临界CO2状态时,加压过程有利于形成胶束,此过程包封率增加显著。脂质体胶束属于溶液体系,压力对系统影响不如对亚临界的气体系统影响大,但是过高的压力,会使胶束破裂,造成脂质体泄漏致使包封率减少。
2.5.2 温度对盐酸小檗碱脂质体包封率的影响由图4可见,随着制备温度的升高,脂质体包封率呈先增后减的趋势,而变化趋势尤其在相变温度的附近增减较为明显,分析认为膜分子运动随着温度的增加而加快,相变温度是脂质体膜由“凝胶态”转变为“液晶态”,其磷脂分子疏水链由“全反式”向“扭曲态”过渡,其紊乱度及活动度增加,疏水链纵向长度减少,膜分子间距增加;膜通透性增大,包封率增大,相变时脂质体会发生相分离(phase separation),即凝胶相和液晶态会同时存在,当凝胶相和液态相同时存在时,磷脂结构域间距最大,此时膜通透性最大,但是超过玻璃转换温度,即磷脂全部以液态相存在时,膜的流动性更高,包封药物的释放速度也增大,包封率下降。
2.5.3 孵化时间对盐酸小檗碱脂质体包封率的影响 由图5可见,当系统刚进入超临界状态时,随着体系CO2含量的增加,脂质体双分子层形成球形胶质结构—溶液胶束过渡形态,随着孵化时间的延长,脂质体胶束溶液形成,此时是一种相对稳定的体系,包封率最高,过长的平衡时间使脂质体表面张力下降,内部分子交联,不利于胶束的稳定性,包封率下降。

表1 Box Behnken法因素水平表
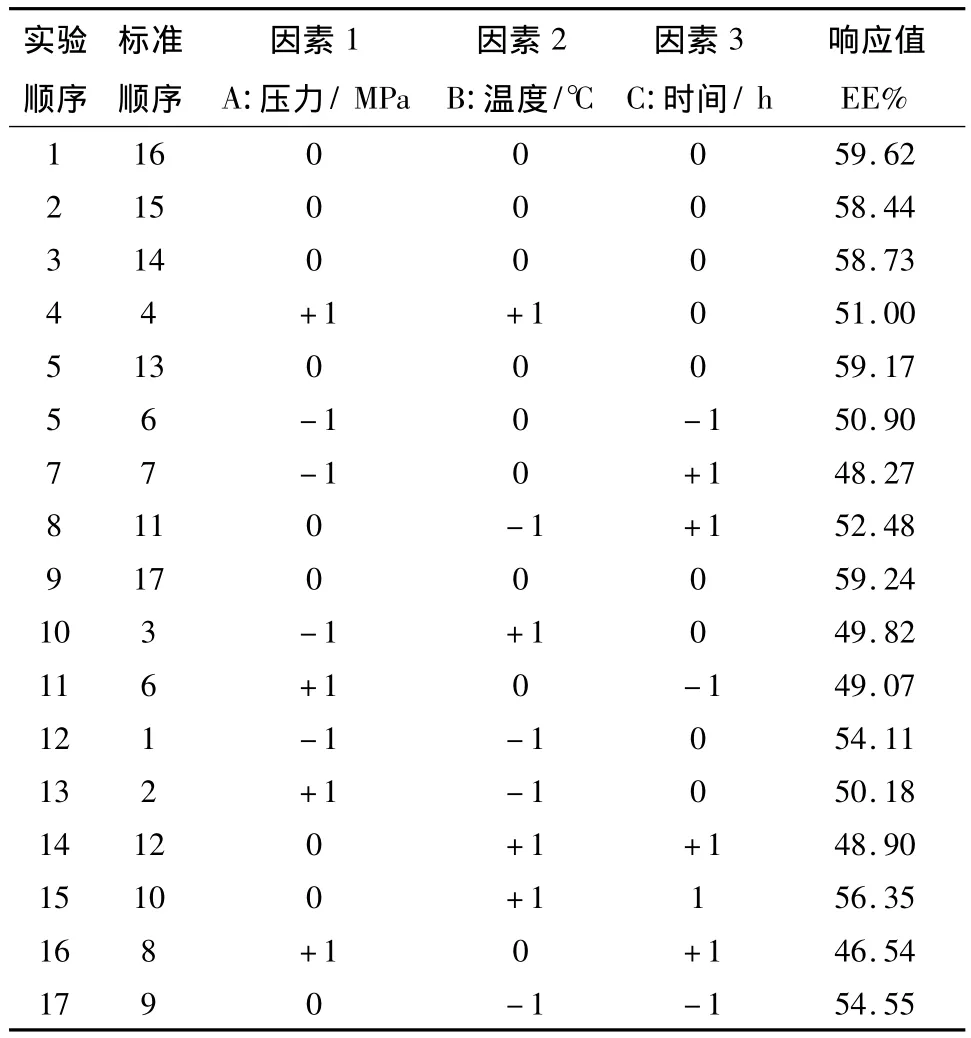
表2 Box Behnken法实验方案与结果
2.6 Box Behnken优化盐酸小檗碱脂质体制备工艺 根据单因素研究,筛选出压力、温度、孵化时间为优化对象,采用Box Behnken法优化盐酸小檗碱脂质体的超临界制备工艺,以包封率为响应值,标准顺序中1~12号为析因实验,13~17为5个中心实验,用于估计实验误差,实验设计见表1,方案与结果见表2。
采用design expert8.0响应面对实验数据进行回归分析,其中二次多项式回归拟合度最高,并且更好地表征了不同因素之间的交互作用,采用二次多项式回归拟合,建立二次多元回归方程,对该方程的回归分析和方差分析结果见表3。
由表3可知,EE%和自变量之间的线性关系极明显,该模型回归极显著(P<0.000 1),失拟项不显著,并且该模型R2=0.988 5,说明该模型与实验拟合良好,其中自变量A、B、C、AB、BC、B2与响应值之间线性关系显著,自变量A2,C2与响应值之间线性关系极显著,可以用于该模型的理论推测,由F检验可以得到因子贡献率为:A2>C2>>C>B2>BC>AB>A>B,推断超临界操作条件对包封率的影响:压力>时间>温度。AB,BC交互作用显著;AC之间交互作用不显著,详见图6~8。

表3 包封率响应结果回归分析与方差分析表
Box Behnken设计优化超临界操作最佳条件为压力19.59 MPa,温度52.78℃,孵化时间1.81 h,实验预测值该操作条件下最佳包封率为59.29%。在该压力下进行验证试验,得到最佳包封率为59.35%,平均包封率为59.26%,实验值与预测值吻合,见表4。
2.7 盐酸小檗碱脂质体粒径的测定 粒径及分布是影响脂质体在体内行为、物理稳定性和临床应用安全性的重要指标。粒径大小及其分布是影响脂质体在体内靶向性,物理稳定性的重要指标,是脂质体质量控制的关键之一。本文采用了激光粒度仪对盐酸小檗碱脂质体的粒径及分布进行了测定,结果如图9。由图9所示,盐酸小檗碱脂质体分布均匀且集中,平均粒径1.304 μm,粒径分布0.3 ~3 μm。
3 讨论
尽管早在20世纪60年代初,国外就开始了脂质体的研究,但目前真正上市的脂质体并不多。脂质体剂型对制备条件的变化很敏感,为了保证最终顺利过渡到大生产,打好坚实的研究基础是很有必要的。对于关键的工艺条件和工艺步骤应进行验证,说明工艺的合理性和重现性。在脂质体的制备过程中,常使用有一定毒性的氯仿,甲醇等有机溶剂来溶解磷脂,这些均限制了其在工业化中的生产。
虽然薄膜分散法等方法[7]制备的脂质体包封率较高,但工艺复杂和有机溶剂的大量使用均限制了其工业化生产。目前静态的超临界CO2技术在制备固体分散体中应用较广泛[8],而在有关制备脂质体的研究较少,本实验制备的盐酸小檗碱脂质体仅使用少量乙醇最大程度降低了有机溶剂的使用,无环境污染和溶剂残留,且工艺简单,传质速率高,有利于孵化过程中药物分子从膜外向膜内扩散[9],同时超临界CO2在一定温度下经高压作用形成,体系中的高压同样有利于药物进入脂质体内水相,进而提高脂质体的包封率,增大载药量。张志丽等[6]用超临界法制备盐酸小檗碱脂质体时,考察了药脂比和磷脂浓度对脂质体包封率和载药量的影响,得到了包封率为73.1%,载药量为16.15%的脂质体,这为盐酸小檗碱脂质体的工业化生产提供了更大的可能性。
4 结论
在超临界条件下,分别考察了制备压力、温度、时间对盐酸小檗碱脂质体包封率的影响,并采用Box Behnken设计优化超临界CO2制备盐酸小檗碱的最佳条件:压力19.59 MPa,温度52.78℃,孵化时间1.81 h,预测包封率为59.29%,而实验包封率为59.35%,平均包封率为59.26%,实验值与预测值吻合。并初步考察了脂质体的粒径大小和分布:平均粒径1.304 μm,粒径分布 0.3 ~3 μm。
采用超临界CO2流体技术制备盐酸小檗碱脂质体,旨在探索一种条件温和、工艺简单、绿色环保的新方法,提高盐酸小檗碱脂质体被动载药的包封率,增加载药量从而使其有可能达到治疗所需的较高血药浓度,同时降低副作用。实验表明,超临界流体制备盐酸小檗碱脂质体是可行的,操作简单,无溶剂残留,且在操作条件可以控制脂质体的粒径大小,提高脂质体稳定性[10-11],为其实现工业化生产提供了可能,若要提高其包封率和载药量,还需进一步考察研究。
[1] 王雪超,杜美容.盐酸小檗碱溶解度与相分配系数研究[J].河北北方学院学报(自然科学版),2011,27(1):26-29.
[2] 崔福德主编.药剂学[M].7版.北京:人民卫生出版社,2011:402-410.
[3] 金 青,赵文英,张国雨,等.注射用盐酸小檗碱脂质体的制备[J].医药导报,2011,30(3):353-355.
[4] 牟琳琳,徐 洋,蒋宫平,等.改良pH梯度法制备盐酸小檗碱脂质体[J].中国药学杂志,2013,48(1):49-53.
[5] 徐少洪,赵 斌,闫志强,等.超临界流体技术在脂质体制备中的应用[J].材料导报,2014,28(5):98-102.
[6] 张志丽,张少华,张志云,等.响应面设计优化超临界CO2法制备盐酸小檗碱脂质体的处方工艺[J].沈阳药科大学学报,2012,29(10):747-752,811.
[7] 王兴慧,李俊生,吕佳佳,等.盐酸小檗碱脂质体的制备工艺优选及体外释放性质考察[J].中国实验方剂学杂志,2013,19(18):39-42.
[8] 张 维,张志云,张志丽,等.超临界流体技术制备固体分散体的研究进展[J].安徽医药,2013,17(6):903-905.
[9] Lesoin L,Boutin O,Crampon C,et al.CO2/water/surfactant ternary systems and liposome formation using supercritical CO2:A review[J].Colloids and Surfaces A:Physicochemical and Engineering Aspects,2011,377(1/3):1-14.
[10]安学勤,裘 丹,沈伟国,等.超临界二氧化碳法制备纳米盐酸小檗碱脂质体的方法:中国,101683322A[P].2010-03-31.
[11] Meure LA,Foster NR,Dehghani F.Conventional and dense gas techniques for the production of liposomes:a review[J].AAPS PharmSciTech,2008,9(3):798-809.
