蚕沙低甲氧基果胶的提取工艺研究
2015-11-04张睿姣江南大学食品学院江苏无锡214122
张睿姣,周 雯,吕 兵(江南大学食品学院,江苏无锡214122)
蚕沙低甲氧基果胶的提取工艺研究
张睿姣,周雯,吕兵*
(江南大学食品学院,江苏无锡214122)
采用酸萃取-铁盐沉淀法提取蚕沙低甲氧基果胶,通过单因素和正交实验确定最佳提取条件:用0.25%草酸水解,水解条件为:料液比1∶20(g/mL)、pH1.5、85℃、60 min,沉淀条件为:pH3.5、铁盐浓度0.5%。采用该优化工艺处理蚕沙,得到的果胶得率为5.21%。产品理化性质分析结果表明,该优化工艺提取的蚕沙果胶,其甲氧基含量5.62%,酯化度34.46%,半乳糖醛酸含量69.58%,品质达到国标要求。
蚕沙,果胶,铁盐沉淀,提取
果胶是一种线性植物多糖,主要由D-半乳糖醛酸构成,分子量约5~30万。按其酯化度(degree of esterification,DE)高低,可分为高甲氧基果胶(high methoxyl pectin,HMP,DE>50%)和低甲氧基果胶(low methoxyl pectin,LMP,DE<50%)。果胶作为稳定剂、胶凝剂及增稠剂,广泛应用于食品、医药和化工等行业中。全球果胶的年需求量约4万吨,并以5%~10%的速度逐年增长,国内年需求量约为3000吨,其中进口果胶约占八成[1]。目前,商品果胶多为HMP,通常来源于植物组织,如柑橘皮、苹果皮、甜菜渣等,而LMP主要由HMP脱酯所得,脱酯方法主要包括酶法、酸化乙醇法、碱化法和酰胺化法[2-4]。
蚕沙即蚕粪,家蚕不能吸收利用桑叶中的果胶,而由粪便中排出,因此蚕沙中含有一定量的果胶。蚕沙果胶是天然的低甲氧基果胶,其抗菌性好、实用性强,还可作为重金属中毒的解毒剂[5-6]。我国干蚕沙年产量超过60万吨,其成本低廉、来源丰富,是一种很好的潜在果胶来源[6-7]。目前,蚕沙果胶的提取多采用乙醇沉淀法,其工业化生产刚刚起步,生产中仍存在许多问题,如乙醇用量较大、产品灰分高、脱色难等[8]。因此,对蚕沙果胶提取工艺的优化及其基本性质的系统研究显得尤为重要。本文采用酸萃取-铁盐沉淀法,尝试从酸解、脱色和沉淀等环节入手,优化蚕沙果胶提取工艺,以提高产品得率和品质、降低成本。
1 材料与方法
1.1材料与仪器
蚕沙江苏南通海安大公镇提供;盐酸、草酸、硫酸、颗粒活性炭、氨水、氯化铁、95%乙醇、无水乙醇、粒状氢氧化钠均为分析纯。
DK-8D电热恒温水槽上海精宏设备有限公司;DUG-9203A电热恒温鼓风干燥箱上海精宏设备有限公司;RJ-TGL-16G-Ⅱ台式高速离心机无锡市瑞江分析仪器有限公司;EL20pH计梅特勒-托利多仪器(上海)有限公司。
1.2实验方法
1.2.1工艺流程原料磨碎→灭酶→漂洗→脱色I→软化→水洗压干→酸解萃取→脱色II→沉淀→洗涤→干燥
1.2.2操作要点灭酶:蚕沙中加入去离子水,加热并保持微沸3~5 min,防止原果胶在天然果胶酶的作用下变为水溶性果胶,降低果胶得率。
漂洗:洗去灰尘、枝叶,初步除去色素和糖分等可溶性成分;可溶性果胶在漂洗过程中的损失可以忽略。
脱色I:加入85%~90%乙醇,用量为蚕沙∶乙醇= 1∶2(g/mL),40℃恒温水浴3 h,重复3次。除去蚕沙中叶绿素、蛋白质和脂肪等,滤渣用乙醇冲洗,少量多次,至滤液无色。
软化:浸泡提取过叶绿素的蚕沙,过滤后静置6 h以上,使之松软。
水洗压干:水洗,用纱布过滤至滤液无色后,将水分压干,压干后蚕沙质量约为处理前的3倍。
酸解萃取:用18%盐酸调节酸解液pH,恒温水浴并间歇搅拌。
脱色II:加入活性炭并不断搅拌,60℃恒温水浴1 h,3000 r/min离心5 min,抽滤,滤液待用。
铁盐沉淀:用氨水调节滤液pH,细线状加入FeCl3溶液(预先配制成20%的浓度)并缓慢搅拌,有大量絮状沉淀产生,静置时间>6 h,抽滤。
洗涤干燥:将10%HCl缓慢加入至抽滤所得的果胶酸铁沉淀中,用尽量少的盐酸使沉淀完全溶解;加入95%乙醇并缓慢搅拌,使乙醇最终浓度>70%,溶液中产生米黄色絮状沉淀,静置,待沉淀完全后抽滤;用95%乙醇及无水乙醇洗涤沉淀至滤液无色;55~60℃烘箱中干燥5 h,粉碎。
1.2.3单因素实验针对蚕沙果胶提取中的关键步骤:酸解萃取和铁盐沉淀,选取8个因素:酸的种类、料液比、酸解pH、酸解温度、酸解时间、活性炭用量、沉淀pH、铁盐终浓度进行单因素实验。
1.2.3.1酸种类的确定精密称取蚕沙20.00 g,在酸解料液比1∶20(g/mL)、pH2.0、温度85℃、时间60 min,脱色活性炭用量1 g/200 mL萃取液,沉淀条件为pH3.5、铁盐终浓度0.5%,考察不同酸的种类(0.25%盐酸、0.25%草酸、0.25%硫酸)对果胶得率的影响;
1.2.3.2料液比的确定用0.25%草酸水解,在pH1.5、温度85℃、时间60 min,脱色活性炭用量1 g/200 mL萃取液,沉淀条件为:pH3.5、铁盐终浓度0.5%的条件下,考察不同料液比(1∶10、1∶15、1∶20、1∶25 g/mL)对果胶得率的影响;
1.2.3.3酸解pH的确定在酸解料液比1∶20(g/mL)、pH1.5、温度85℃、时间60 min,脱色活性炭用量1 g/200 mL萃取液,沉淀条件为:pH3.5、铁盐终浓度0.5%的条件下,考察不同酸解pH(1.0、1.5、2.0、2.5)对果胶得率的影响;
1.2.3.4酸解温度的确定在酸解料液比1∶20(g/mL)、pH1.5、时间60 min,脱色活性炭用量1 g/200 mL萃取液,沉淀条件为:pH3.5、铁盐终浓度0.5%的条件下,考察不同酸解温度(65、75、85、95℃)对果胶得率的影响;
1.2.3.5酸解时间的确定在酸解料液比1∶20(g/mL)、pH1.5,温度85℃、脱色活性炭用量1 g/200 mL萃取液,沉淀条件为:pH3.5、铁盐终浓度0.5%的条件下,考察不同酸解时间(30、60、90、120 min)对果胶得率的影响;
1.2.3.6活性炭用量的确定在酸解料液比1∶20(g/mL)、pH1.5、温度85℃、时间60 min,沉淀条件为:pH3.5、铁盐终浓度0.5%的条件下,考察不同活性炭用量(0、0.5、1.0、1.5 g/200 mL萃取液)对果胶脱色的影响;
1.2.3.7沉淀pH的确定在酸解料液比1∶20(g/mL)、pH1.5、时间60 min、温度85℃,铁盐终浓度0.5%的条件下,考察不同沉淀pH(3.0、3.5、4.0、4.5、5.0)对果胶得率的影响;
1.2.3.8铁盐终浓度的确定在酸解料液比1∶20(g/mL)、pH1.5、时间60 min、温度85℃,沉淀pH3.5的条件下,考察不同铁盐终浓度(0.25%、0.50%、0.75%、1.00%)对果胶得率的影响。
上述每组实验均重复3次,以确定各因素的适宜范围。
1.2.4正交实验在上述单因素实验基础上,进一步进行正交实验。采用L9(34)正交表,对酸解液pH、酸解温度、沉淀pH及铁盐终浓度四个因素进行探讨,以果胶得率为指标优化果胶提取条件。
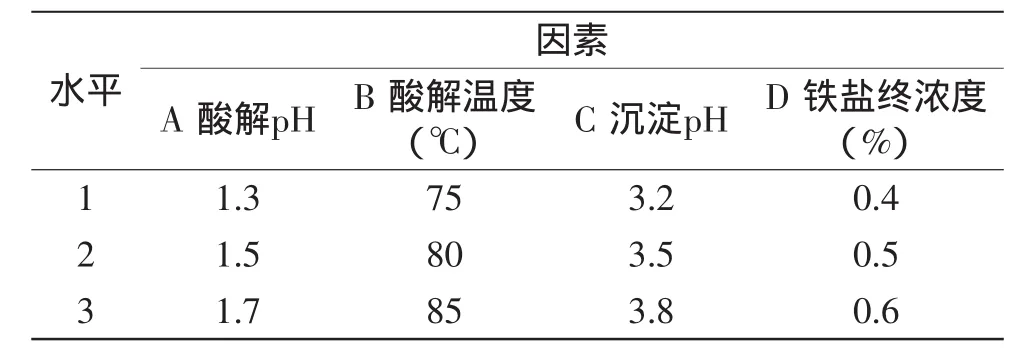
表1 正交实验因素水平表Table 1 Orthogonal factors and levels table
1.2.5果胶得率测定果胶得率(%)=(提取的蚕沙果胶干重/蚕沙原料干重)×100。
1.2.6产品鉴别实验[9]
1.2.6.1取1 g样品,加40 mL水,不断搅拌,经加热后冷却。
1.2.6.2取5 mL样品溶液(1%),加入1 mL NaOH溶液(2 mol/L),静置15 min。
1.2.6.3在1.2.6.2基础上加入1 mL盐酸溶液(1+1)。
1.2.7产品理化指标依据GB25533-2010[9]和QB 2484-2000[10]中所述方法进行测定。
1.2.8数据处理使用Excel进行数据处理并作图,使用SPSS 18.0进行数据统计分析。
2 结果与分析
2.1单因素影响及结果分析
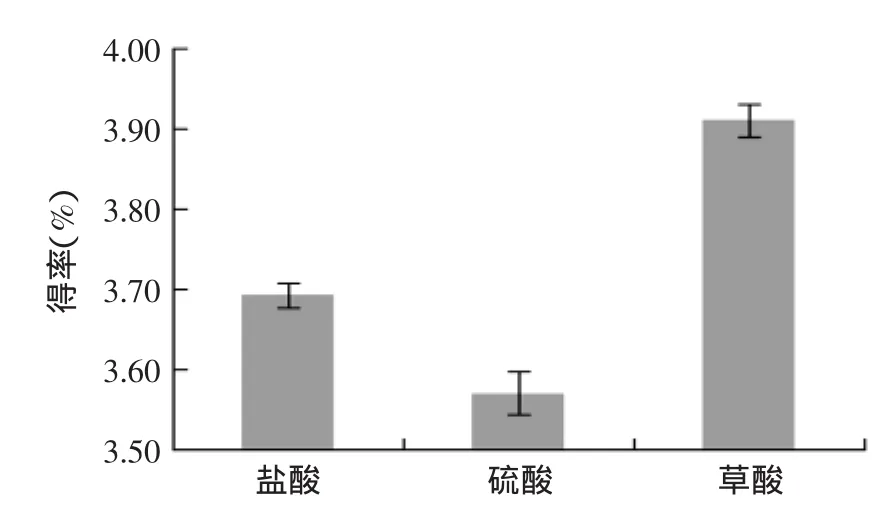
图1 酸的种类对果胶得率的影响Fig.1 Effect of type of acid on pectin yield
2.1.1酸的种类对果胶得率的影响由图1可知,采用草酸酸解的得率高于盐酸和硫酸。这可能是因为盐酸和硫酸酸解太过剧烈,果胶分子降解,得率下降,也可能是因为草酸会螯合钙离子,释放钙结合型果胶,果胶得率相对较高,故选用草酸水解较为合适。
2.1.2料液比对果胶得率的影响由图2可知,酸解过程中,若料液比过小,萃取不完全,并且萃取液黏度较大,增加过滤操作的难度,得率较低;若料液比过大,萃取液中果胶浓度过低,沉淀难度较大,得率下降,且酸和铁盐用量增多,能耗和成本相应增加。因此,选择料液比1∶20 g/mL较为合适。
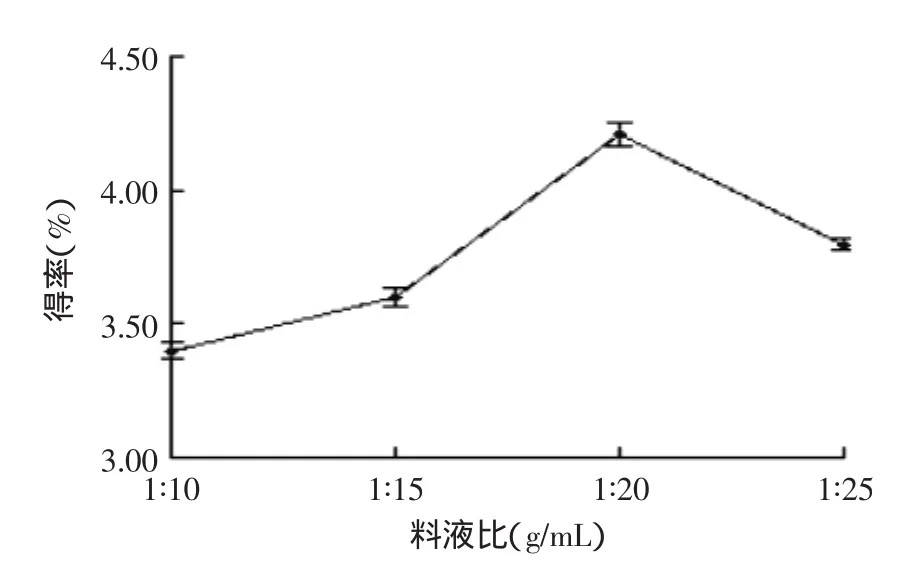
图2 料液比对果胶得率的影响Fig.2 Effect of solid-liquid on pectin yield
2.1.3酸解液pH对果胶得率的影响由图3可知,酸解的目的是尽可能地促使原果胶向可溶性果胶转化,同时减少果胶分子的降解。若酸解液pH过大,果胶水解较慢,导致生产周期延长、成本增加;若酸解液pH过小,果胶分子脱酸裂解,果胶酯化度及凝胶强度下降,得率降低。因此,选择酸解pH1.5左右为宜。
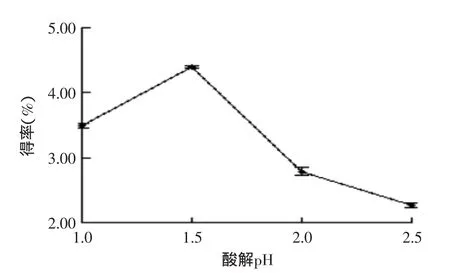
图3 酸解液pH值对果胶得率的影响Fig.3 Effect of pH on pectin yield
2.1.4酸解时间对果胶得率的影响由图4可知,酸解时间过短时,果胶未完全水解,得率较低;适当延长酸解时间,能使果胶充分水解,但过长时间的酸萃取处理容易导致果胶水解过度,影响果胶品质和得率。因此,酸解时间选择60 min较为合适。
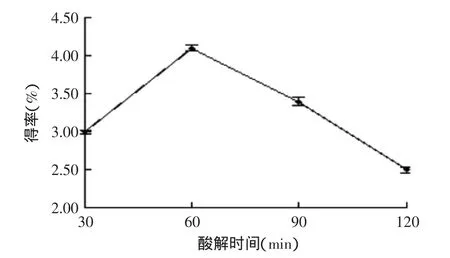
图4 酸解时间对果胶得率的影响Fig.4 Effect of time on pectin yield
2.1.5酸解温度对果胶得率的影响由图5可知,萃取温度过低会影响果胶水解速度,且过长时间的酸解处理会使果胶过度脱酯,得率较低;适当地升高温度可以促进果胶的水解,但果胶耐热性差,过高的温度会破坏其结构,因此,酸解温度选择85℃为宜。

图5 酸解温度对果胶得率的影响Fig.5 Effect of temperature on pectin yield
2.1.6活性炭用量对果胶脱色的影响由表2可知,不同添加量的活性炭脱色处理后,果胶的色泽并无明显差别,而残留的活性炭颗粒又会增加果胶的灰分含量。因为本实验中活性炭脱色前的果胶的浅米灰色已可以接受,综合考虑生产工艺的简化及最终品质,确定略去活性炭脱色步骤。

表2 活性炭用量对脱色结果的影响Table 2 Effect of activated carbon concentration on pectin extraction rate
2.1.7沉淀pH对果胶得率的影响由图6可知,蚕沙中的果胶酸钙在酸性条件下能够转变为可溶性的果胶酸,其羧基能被NH3+中和,因此,先加入氨水使其形成铵盐,再加入铁盐溶液,使之生成果胶酸铁沉淀。果胶在其等电点pH3.5时,溶解度最小。当沉淀pH<3.5时,果胶酸铁沉淀溶解,得率下降;当沉淀pH>3.5时,Fe3+水解,生成氢氧化铁沉淀,阻碍果胶酸铁的形成,降低果胶得率,影响产品颜色。因此,选择沉淀pH3.5较为合适。

图6 沉淀pH对果胶得率的影响Fig.6 Effect of precipitation pH on pectin yield
2.1.8铁盐用量对果胶得率的影响由图7可知,沉淀液中铁盐终浓度为0.5%时,果胶得率最高。若铁盐用量过少,果胶酸铁无法完全沉淀,影响最终得率;若用量过多,产品中Fe3+含量增大,后期除铁时的盐酸用量增加,可能也会造成果胶的损失,使其得率下降。因此,铁盐用量以终浓度0.5%左右为宜。
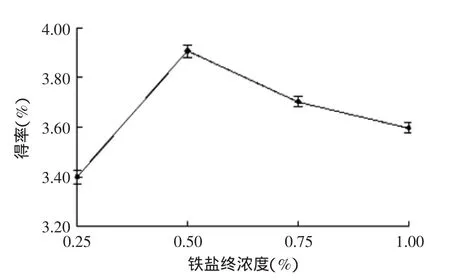
图7 铁盐用量对果胶得率的影响Fig.7 Effect of molysite concentration on pectin yield
2.2正交实验及结果分析
正交实验结果见表3。由表3可知,各因素对蚕沙果胶得率的影响顺序为A>B>C>D,蚕沙果胶提取工艺的最佳组合为A2B3C2D2,即酸解pH为1.5,酸解温度85℃,沉淀pH3.5,铁盐终浓度0.5%,验证实验表明,果胶得率可达5.21%±0.05%。由正交实验的方差分析(见表4)可知,酸解pH、酸解温度、沉淀pH、铁盐终浓度四个因素对果胶得率的影响均十分显著(p<0.01)。
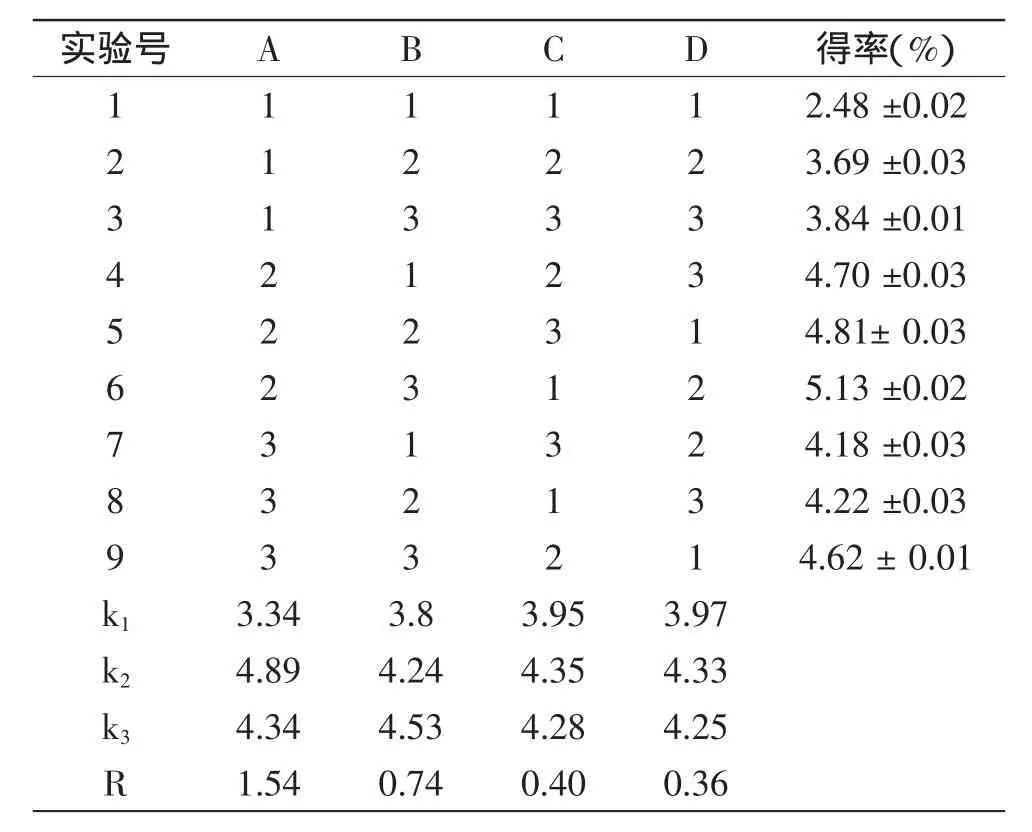
表3 正交实验结果分析Table 3 Analysis of orthogonal test results
2.3产品性质分析
2.3.1定性鉴别按1.2.6.1的方法处理,形成黏稠状液体;按1.2.6.2的方法处理,形成不透明凝胶;按1.2.6.3的方法处理,形成无色凝胶,煮沸后生成絮状沉淀。上述结果表明,本实验提取得到的产品为果胶。
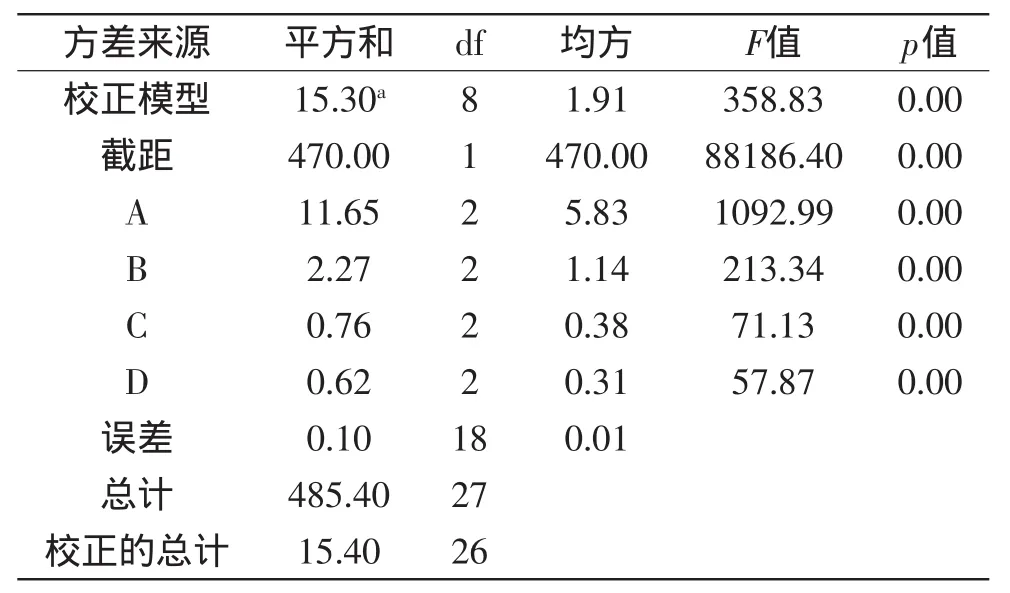
表4 正交实验结果方差分析Table 4 Variance analysis of orthogonal test results
2.3.2理化指标结果表明,本实验得到的低甲氧基果胶品质达到国标要求。

表5 理化指标Table 5 Physicochemical indexes
3 结论
在单因素实验和正交实验的基础上综合得出,蚕沙果胶提取工艺的优化条件为:用0.25%草酸酸解,水解条件为:料液比1∶20 g/mL、pH1.5、酸解时间60 min、酸解温度85℃;沉淀pH3.5、铁盐用量约0.5%,在此条件下,蚕沙果胶得率为5.21%±0.05%。果胶样品的理化指标分析结果表明,由蚕沙果胶制备的低甲氧基果胶品质达到国标要求。由此可见,蚕沙是一种极具潜力的天然低甲氧基果胶来源。
[1]黄山三生缘生物技术有限公司.2013年中国果胶行业分析报告[R/EB].http://www.doc88.com/p-1068775107281.html,2013-3-29.
[2]Liu L,Cao J,Huang J.Extraction of pectins with different degrees of esterification from mulberry branch bark[J].Bioresource Technology,2010,101:3268-3273.
[3]刘忆冬,张磊,陈国刚,等.低甲氧基果胶生产工艺现状及其发展前景[J].农产品加工,2008,1(1):57-58.
[4]邓红,宋纪蓉.盐析法从苹果渣中提取果胶的工艺条件研究[J].食品科学,2002,23(3):57-60.
[5]唐翠娥,杨海霞,朱祥瑞,等.蚕沙的开发利用研究进展[J].[6]杨海霞,朱祥瑞,房泽民,等.蚕沙的开发利用研究进展[J].桑蚕通报,2002,33(3):9-12.
饮料工业,2011,14(11):8-12.
[7]万里平.从蚕沙中提取果胶的研究[J].重庆三峡学院学报,2001,6(17):83-85.
[8]徐要学.蚕沙中果胶的提取[J].化学世界,1989,5:230-232.
[9]GB25533-2010.食品安全国家标准食品添加剂果胶[S].
[10]QB2484-2000.食品添加剂果胶[S].
Study on extraction of low methoxyl pectin from silkworm excrement
ZHANG Rui-jiao,ZHOU Wen,LV Bing*
(School of Food Science and Technology,Jiangnan University,Wuxi 214122,China)
Pectins were extracted from silkworm excrement by means of acid extraction and then molysite precipitation.A single-factor experiment and an orthogonal test were used to optimize the production conditions.The optimal conditions for pectin production were determined to include extraction at pH1.7 and a solid-liquid ratio of 1∶20(g/mL)in oxalic acid solution for 60 min at 85℃,and precipitation with 0.5%molysite solution at pH3.5.Under optimal conditions,the extraction rate of the pectin was 5.21%,the methoxy content and the degree of esterification(DE)was 5.62%and 34.46%,respectively,and the total galacturonic acid content of the pectin was 69.58%.Thus,the quality of the pectin was absolutely acceptable.
silkworm excrement;pectin;molysite precipitation;extraction
TS202.3
B
1002-0306(2015)18-0267-05
10.13386/j.issn1002-0306.2015.18.015
2014-12-22
张睿姣(1992-),女,本科,研究方向:食品科学与工程,E-mail:1045839225@qq.com。
吕兵(1967-),女,博士,副教授,研究方向:食品加工,E-mail:lubing6709@163.com。
