低温等离子体促进煤层甲烷活化转化
2015-11-03朱丽华
徐 锋,李 创,朱丽华
(黑龙江科技大学 安全工程学院,哈尔滨 150022)
低温等离子体促进煤层甲烷活化转化
徐 锋,李 创,朱丽华
(黑龙江科技大学 安全工程学院,哈尔滨 150022)
为探究低温等离子体促进煤层甲烷活化转化的电源参数和工艺参数,以自制实验系统对CH4、O2和N2的混合气体进行介质阻挡放电,考察输入电压、放电频率、气体总流量、气体组分、放电间隙对CH4转化率及主要产物产率的影响。结果表明:若以CH4转化率和CO产率为评价指标,输入电压90 V、放电频率7 kHz、气体总流量65 mL/min较适宜;若以CH3OH和CO2产率为评价指标,输入电压65 V、放电频率9 kHz、气体总流量195 mL/min较为适宜;若以CH4转化率及CO、CO2产率为评价指标,反应气体中CH4体积分数不宜高、而O2与N2的量比不宜低,放电间隙2 mm为宜;若以CH3OH的产率为评价指标,反应气体中CH4体积分数为40%、O2与N2的量比为0.25,放电间隙1 mm为宜。电源输入电压65 V、放电频率9 kHz、气体总流量195 mL/min、反应气体中CH4体积分数及O2与N2的量比分别为40%和0.25、放电间隙1 mm时,CH4转化率及主要产物产率较高。
甲烷;活化;转化;等离子体;介质阻挡放电
0 引言
瓦斯(主要成分是甲烷)不仅是煤矿重大灾害源和大气污染源,也是一种宝贵的资源[1-2]。加强煤层甲烷回收利用可以在保障煤矿安全生产、减少温室气体排放等方面获得显著的安全和环境效益[3]。随着石化资源的日益短缺,煤层甲烷的化工利用倍受关注。煤层甲烷的化工利用以甲烷分子的活化为基础和前提。甲烷堪称结构最稳定的有机分子,其活化和转化通常需要极为苛刻的反应条件。因此,甲烷的活化和转化一直是科研工作者研究的热点和难点。
低温等离子体技术可突破热力学平衡限制,实现甲烷温和条件下的“非平衡”直接转化。低温等离子体可以通过电晕放电、辉光放电、介质阻挡放电、射频放电及微波放电等多种方式产生[4-5]。由于介质阻挡放电可在常压下完成,且反应器结构简单,因此,被研究者们广泛采用。Wang Qi和白敏冬等[6-7]利用介质阻挡反应器对CH4制合成气的反应进行研究,发现采用低温等离子体方法可获得较高的CO和H2选择性。同时指出,向反应体系中添加CO2或N2可明显提高CH4的转化率。Gesser H D等[8]利用串联介质阻挡反应器以CH4、CO2、N2混合气体为反应物制合成气,得到CH4转化率45.12%,H2、CO产率分别为22.30%和17.02%的实验结果。Spiess F J等[9]指出电极的材质对CH4转化有较大影响。Yu Wang等[10]在常压、100℃条件下,研究CH4和CH3OCH3的等离子体反应,结果表明,CH3OCH3可有效促进CH4的转化。王皓等[11]利用介质阻挡放电反应器进行CH4部分氧化重整制氢实验,探讨放电参数和放电区域的填充物对CH4转化率及产氢效果的影响。在此基础上,笔者利用介质阻挡放电反应器对低温等离子体促进煤层甲烷活化转化进行实验研究,以期为煤层甲烷的回收利用提供借鉴。
1 实 验
1.1实验系统
实验系统为自制的等离子体活化煤层甲烷实验系统,主要由配气系统、反应系统、产物收集系统及数据采集与分析系统组成,如图1所示。配气系统主要包括高压钢瓶、压力调节器、质量流量控制器(D07-19B)和气体混合器。反应系统由高压交流电源(CTP-2000 K)、接触式调压器、同轴式介质阻挡反应器、温控电炉组成,其中,同轴式介质阻挡反应器以刚玉管为介质(内径20 mm、外径25 mm、长615 mm),管内的高压电极为不锈钢螺纹棒,管外低压电极为不锈钢网。产物收集系统主要由采样管和气囊构成。数据采集与分析系统主要由数字示波器(DS1102E)、气相色谱仪(FULI9790、FULI9790Ⅱ)等组成。
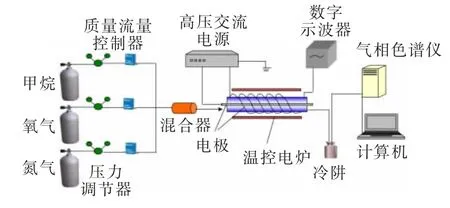
图1 实验系统示意Fig.1 Schematic diagram of experimental system
1.2实验及分析测试方法
CH4、O2、N2经质量流量控制器精确控制流量和配比,充分混合后引入同轴式介质阻挡反应器进行等离子体反应。反应后尾气中的CH3OH经蒸馏水冷凝吸收后,用GC9790型气相色谱仪进行检测,填充柱为GDX-102型,FID检测器,外标法计算;不凝气经干燥、气囊收集后,用GC9790Ⅱ型气相色谱仪检测,填充柱为TDX-01型,FID检测器,外标法计算。
2 结果与分析
2.1输入电压的影响
以CH4、O2、N2体积分数分别为40%、12%、48%的混合气体为反应物,在放电频率7.5 kHz、放电间隙1 mm、实验温度150℃、混合气体总流量195 mL/ min的条件下,对混合气体进行介质阻挡放电。经色谱分析,产物中主要有CH3OH、CO和CO2。图2为介质阻挡放电过程中输入电压U对CH4转化率α及主要产物产率η的作用规律。由图2可见,随着输入电压的增大,CH4转化率明显增加,当输入电压从50 V变到90 V时,CH4转化率从6.36%快速增至44.70%,说明加大输入电压利于甲烷活化;CO产率与输入电压之间也表现出正相关关系,但当输入电压超过65 V后,CO产率增加趋势明显放缓;CH3OH和CO2的产率随着输入电压的增大先增加后降低,在输入电压为65 V时取得最大值。在其他条件保持不变的情况下,增大输入电压,相当于增加了系统的输入能量,在反应系统中可产生更多的高能活性粒子,活化CH4的能力增强。因此,CH4的转化率随着输入电压的增大而增加。当输入电压超过65 V,CO产率增加趋势放缓及CH3OH和CO2的产率降低,可能是由于系统能量达到一定值后,部分活化的CH4转化为C2H4、C2H2等其他烃类化合物所致。
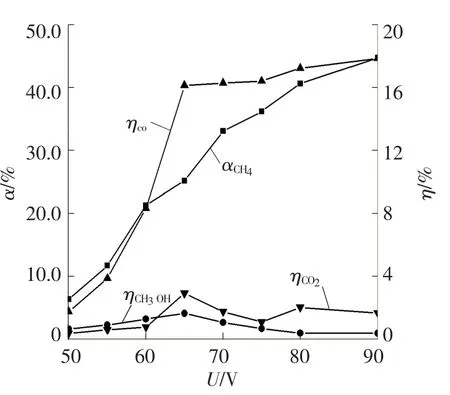
图2 输入电压对CH4转化率、主要产物产率的影响Fig.2 Effect of input voltage on conversion of CH4andyields of CO,CO2and CH3OH
2.2放电频率的影响
在输入电压65 V、放电间隙1 mm、实验温度150℃、气体总流量195 mL/min的条件下,对CH4、O2、N2体积分数分别为40%、12%和48%的混合气体进行介质阻挡放电,考察了放电频率对CH4转化率及主要产物产率的影响,实验结果如图3所示。图3显示,在实验考察的放电频率范围内,CH4转化率和CO产率随着放电频率的增大而降低;CH3OH产率随着放电频率的增大先增加后降低;当放电频率小于9 kHz时,CO2产率基本保持不变,当放电频率大于9 kHz时,CO2产率降低。
介质阻挡放电过程中,反应体系中高能活性粒子的密度正比于放电功率,而放电功率与放电频率有密切的关系。当放电频率与放电电极的固有谐振频率相匹配时,放电功率最大,放电频率越偏离放电电极的固有谐振频率,放电功率越小[12]。采用QV Lissajous图形法[13]对放电功率进行计算。结果表明,当放电频率从7 kHz增大至12 kHz时,放电功率从108 W迅速降至9 W,这说明实验所用放电电极的固有频率小于或等于7 kHz。由于实验所用高压交流电源的放电频率最小可调至7 kHz,所以将7 kHz作为放电频率考察的起点。在实验考察放电频率为7~12 kHz时,放电频率越大越偏离所用放电电极的固有谐振频率,放电功率越小,反应体系中高能活性粒子的密度越小,活化CH4的能力越弱。因此,随着放电频率的增大,CH4转化率和CO产率反而降低。CH3OH是CH4活化转化的活性中间产物,当放电频率从7 kHz增大至9 kHz时,虽然因相应的放电功率减小而导致CH4转化率有所降低,但CH3OH的过氧化反应也随之减弱;当放电频率大于9 kHz时,因反应体系中高能活性粒子的密度大幅减小,而导致CH3OH产率降低。CO和CH3OH产率的综合变化,致使CO2产率表现出先不变后降低的趋势。
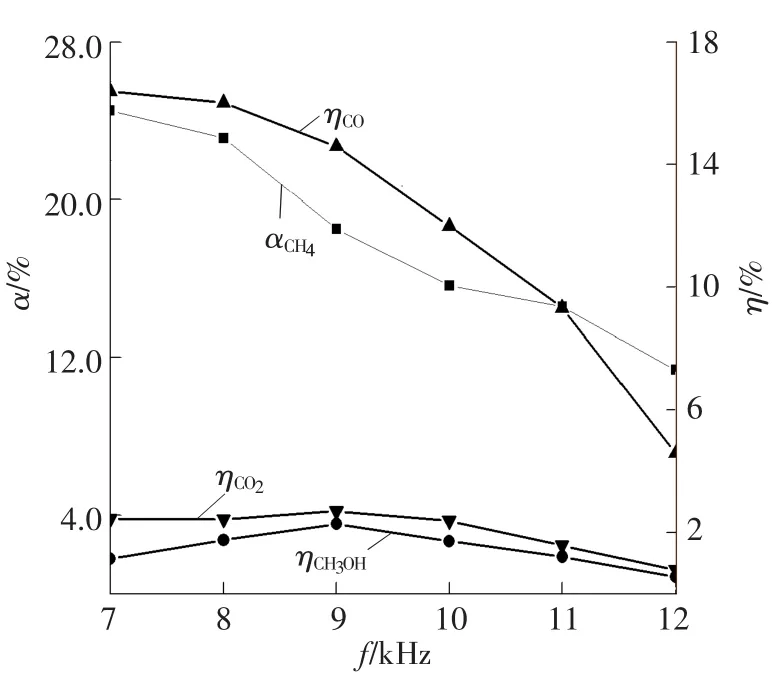
图3 放电频率对CH4转化率、主要产物产率的影响Fig.3 Effect of discharge frequency on conversion of CH4and yields of CO,CO2and CH3OH
2.3气体总流量的影响
以 CH4、O2、N2体积分数分别为40%、12%和48%的混合气体为反应气体,在输入电压65 V、放电频率9 kHz、放电间隙1 mm、实验温度150℃的条件下,考察了气体总流量对CH4转化率及主要产物产率的影响,实验结果如图4所示。由图4可见,气体总流量qV对CO2产率的影响不明显,但对CH4转化率及CO和CH3OH的产率影响较显著。随着气体总流量的增加,CH4转化率及CO产率降低,而CH3OH的产率逐渐升高。这主要是因为,气体总流量增加,相当于减少了气体在放电区域的停留时间,反应气体与高能活性粒子撞击的机会减少,CH4被活化解离的几率降低。当气体总流量从65 mL/min增加到195 mL/min时,CH4转化率由48.35%减小至18.49%,而CH3OH选择性却从1.4%增加至12.3%。在CH4转化率及CH3OH选择性的综合作用下,CH3OH的产率逐渐升高。在CH4转化率降低的情况下,CH3OH选择性却逐渐升高,说明增加气体总流量可以防止化学活性较高的中间产物CH3OH被进一步解离。
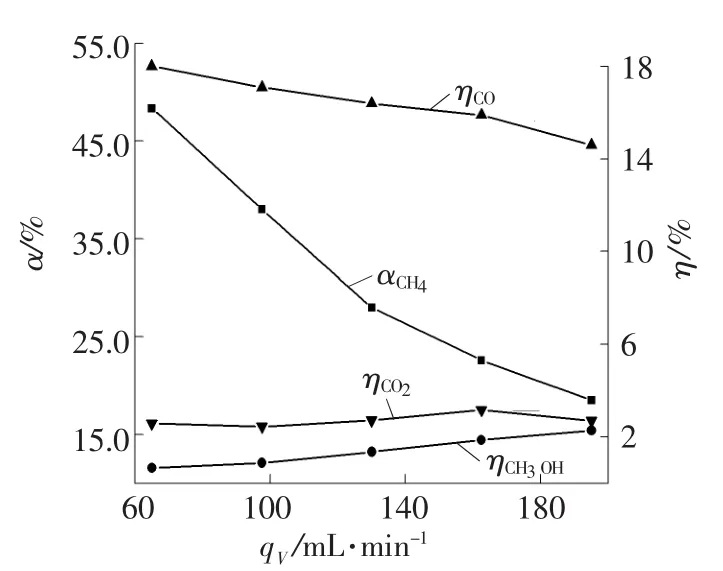
图4 总流量对CH4转化率、主要产物产率的影响Fig.4 Effect of feed flow rate of gas on conversion of CH4and yields of CO,CO2and CH3OH
2.4气体组分的影响
在输入电压65 V、放电频率9 kHz、放电间隙1 mm、实验温度150℃、气体总流量195 mL/min的条件下,考察CH4、O2、N2混合气体中CH4的体积分数对CH4转化率及主要产物产率的影响,实验结果如图5所示。由图5可见,混合气体中CH4的体积分数是该反应的重要影响因素。CH4转化率及CO、CO2产率均随着反应气体中CH4的体积分数的升高快速降低。这是因为,反应过程中O2和N2的量比值保持0.25不变,升高CH4体积分数,势必会降低体系中O2的量,致使体系中没有足够的O2与CH4充分反应,因而CH4转化率及CO、CO2产率均降低。从图5还可明显看出,当混合气中CH4的体积分数为40%时,CH3OH的产率取得最大值。这是由于体系中CH4量过低时,O2的量相对过剩,容易发生过氧化反应,致使CH3OH的产率不高;当体系中CH4量过高时,O2的量相对匮乏,反应不充分,CH3OH的产率仍然保持在较低的水平。
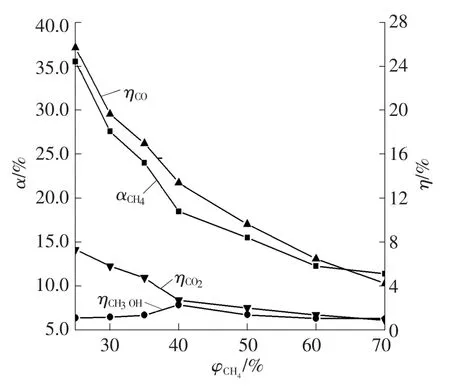
图5 CH4体积分数对CH4转化率、主要产物产率的影响Fig.5 Effect of volume fraction of CH4on conversion of CH4and yields of CO,CO2and CH3OH
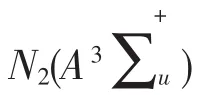
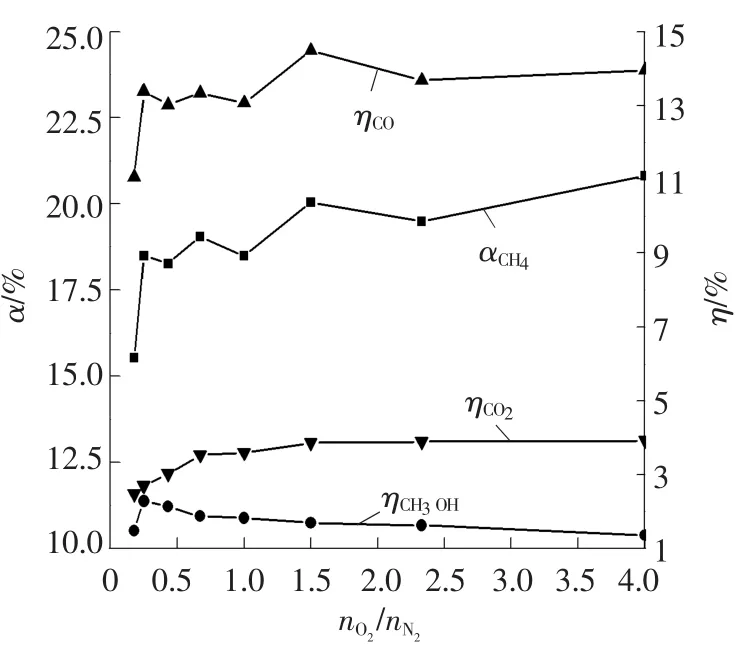
图6 O2与N2的量比值对CH4转化率、主要产物产率的影响Fig.6 Effect of O2/N2molar ratio on conversion of CH4and yields of CO,CO2and CH3OH
2.5放电间隙的影响
以CH4的体积分数为40%的CH4和空气混合物为反应气体,在输入电压65 V、放电频率9 kHz、实验温度150℃、气体总流量195 mL/min的条件下,考察了放电间隙lg对CH4转化率及主要产物产率的影响。由图7可见,当放电间隙从1 mm增至3 mm时,CH4转化率及CO、CO2的产率先增大后降低,而CH3OH产率则逐渐降低。这一实验结果揭示,较小的放电间隙利于CH3OH的生成,而放电间隙过小或过大都不利于CH4转化及CO、CO2生成。
因气体总流量保持不变,增大放电间隙相当于延长了气体停留时间,利于CH4转化。而实验结果表明,CH4转化率及CO、CO2产率与放电间隙之间不存在简单的递增或递减关系,这是由于改变放电间隙也会使放电间隙电场强度发生变化。对于介质阻挡放电反应器而言,放电间隙电场强度由式(1)计算[14]:

式中:E——电场强度,kV/mm;
U——输入电压,kV;
εg、εd——放电气体和介质的相对介电常数,无量纲;
ld、lg——放电介质的厚度和放电间隙,mm。
从式(1)可看出,在保持输入电压不变的情况下,放电间隙从1 mm增加到3 mm时,电场强度减小,赋予反应气体的能量降低,不利于甲烷的活化转化。在停留时间和电场强度两个因素的综合作用下,CH4转化率及CO、CO2产率在放电间隙2 mm时达最佳。CH3OH产率随着放电间隙增大单调递减有两方面的原因。其一,放电间隙增大,气体停留时间延长,CH3OH发生过氧化的可能性加大;其二,放电间隙增大,电场强度减小,活化CH4的能力减弱,主要产物产率随之降低。在放电频率一定的情况下,改变电极的放电间隙,电极的固有频率和放电功率也随之发生变化,但固有频率和放电功率改变都源于放电间隙的改变,因此,研究中未考虑三者的交互作用。

图7 放电间隙对CH4转化率、主要产物产率的影响Fig.7 Effect of discharge gap distance on conversion of CH4and yields of CO,CO2and CH3OH
3 结论
(1)CH4转化率和CO产率随着输入电压的增大而增大,而CH3OH和CO2的产率随着输入电压的增大先增加后降低,当输入电压为 65 V时,CH3OH和CO2的产率取得最大值。
(2)CH4转化率和CO产率随着放电频率的增大而降低,而CH3OH产率随着放电频率的增大先增加后降低。当放电频率小于9 kHz时,CO2产率基本保持不变;当放电频率大于9 kHz时,CO2产率降低。
(3)气体总流量对CO2产率的影响不明显,但对CH4转化率及CO和CH3OH的产率影响较显著。随着气体总流量的增加,CH4转化率及CO产率降低,而CH3OH的产率逐渐升高。
(4)CH4转化率及CO、CO2产率均随着反应气体中CH4体积分数的升高快速降低。当混合气体中CH4的体积分数为40%时,CH3OH的产率取得最大值。
(5)当反应气体中O2与N2的量比值升高时,CH4转化率及CO、CO2产率总体保持增大的趋势,而CH3OH产率的变化趋势则是先升高后降低,在O2与N2的量比为0.25时取得最大值。
(6)较小的放电间隙利于CH3OH的生成,而放电间隙过小或过大都不利于CH4转化及CO、CO2的生成。
[1]谢和平,周宏伟,薛东杰,等.我国煤与瓦斯共采:理论、技术与工程[J].煤炭学报,2014,39(8):1391-1397.
[2]董春游,张斌斌.云模型和D-S理论的煤与瓦斯共采综合评价[J].黑龙江科技大学学报,2015,25(4):450-456.
[3]朱红威,邵菊芳,陶秀祥.煤矿甲烷生物转化生产高附加值产物的研究[J].洁净煤技术,2013,19(2):47-54.
[4]BOGAERTS A,NEYTS E,GIJBELS R,et al.Gas discharge plasmas and their applications[J].Spectrochimica Acta Part B,2002,57(4):609-658.
[5]陈琳.低温等离子体催化氧化甲烷合成甲醇的应用基础研究[D].杭州:浙江大学,2010.
[6]WANG QI,YANG BIMHANG,JIN YONG,et al.Investigation of dry reforming of methane in a dielectric barrier discharge reactor[J].Plasma Chemistry and Plasma Processing,2009,29(3):217-228.
[7]白敏冬,朱晓峰,白敏菂,等.大气压DBD甲烷二氧化碳转化方法研究[J].北京理工大学学报,2005,25(S1):217-221.
[8]GESSER H D,HUNTER N R,PROBAWONO D.The CO2reforming of natural gas in a silent discharge reactor[J].Plasma Chemistry and Plasma Processing,1998,18(2):241-245.
[9]SPIESS F J,SUIB S L,IRIE K,et al.Metal effect and flow rate effect in the hydrogen production from methane[J].Catalysis Today,2004,89(1/2):35-45.
[10]WANG Y,LIU C J,ZHANG Y P.Plasma methane conversion in the presence of dimethyl ether using dielectric-barrierdischarge[J].Energy&Fuels,2005,19(3):877-881.
[11]王皓,宋凌珺,李兴虎,等.介质阻挡放电等离子体甲烷部分氧化重整制氢[J].物理化学学报,2015,31(7):1406-1412.
[12]叶振鑫,刘海涛,陈志刚,等.介质阻挡放电功率相关因素分析[J].机电技术,2011,34(1):41-43.
[13]刘钟阳,吴彦,王宁会.DBD等离子体反应器放电功率测量的研究[J].仪器仪表学报,2001,22(3):78-83.
[14]徐学基,诸定昌.气体放电物理[M].上海:复旦大学出版社,1996.
(编缉王冬)
Study on activation and conversion of methane using non-thermal plasma
XU Feng,LI Chuang,ZHU Lihua
(School of Safety Engineering,Heilongjiang University of Science&Technology,Harbin 150022,China)
This paper is dev oted to investigating power parameters and process parameters of non-thermal plasma promoting coalbed methane activation.The investigation is realized by the dielectric barrier discharge of gas mixture of CH4,O2and N2in a self-made experimental system;the exploration of the effect of input voltage,discharge frequency,total flow rate,gas composition,discharge gap distance on CH4conversion and yield of other main products.The experiment results show that taking CH4conversion and yield of CO as an evaluation index justifies the application of input voltage of 90 V,discharge frequency of 7 kHz and total flow rate of 65 mL/min;choosing yield of CH3OH and CO2as an evaluation index involves input voltage of 65 V,discharge frequency of 9 kHz and total flow rate of 195 mL/min;choosing CH4conversion and yield of CO,CO2as an evaluation index means the application of neither a high volume fraction of CH4in reactive gas nor a low molar ratio of O2to N2and of discharge gap distance of 2 mm;taking yield of CH3OH as an evaluation index dictates the prescribed reaction conditions:volume fraction of CH440%,molar ratio of O2to N20.25,and discharge gap distance 1 mm. The comprehensive comparison shows that a higher CH4conversion and yield of other main products come from the proposed reaction conditions:input voltage 90 V,discharge frequency 9 kHz,total flow rate 195 mL/min,volume fraction of CH440%,molar ratio of O2to N20.25,and discharge gap distance 1 mm.
methane;activation;conversion;plasma;dielectric barrier discharge
10.3969/j.issn.2095-7262.2015.06.005
TD712
2095-7262(2015)06-0597-05
A
2015-09-23
国家自然科学基金项目(51504087,51374098);黑龙江省教育厅科学技术研究项目(12543056)
徐锋(1979-),男,黑龙江省巴彦人,副教授,博士,研究方向:瓦斯防治及利用,E-mail:xufeng79_79@163.com。
