榄香烯联合吉西他滨+顺铂综合治疗晚期非小细胞肺癌临床效果观察
2015-10-27刘君温福刚李彬
刘君 温福刚 李彬
辽宁省鞍山市肿瘤医院八病区,辽宁鞍山114036
榄香烯联合吉西他滨+顺铂综合治疗晚期非小细胞肺癌临床效果观察
刘君温福刚李彬
辽宁省鞍山市肿瘤医院八病区,辽宁鞍山114036
目的探讨榄香烯联合吉西他滨+顺铂(GP方案)综合治疗晚期非小细胞肺癌的临床效果。方法选取2012年4月~2014年7月鞍山市肿瘤医院收治的72例晚期非小细胞肺癌患者为研究对象,随机分成A、B两组,每组36例。B组采用单一GP方案,A组在B组治疗的基础上辅以榄香烯联合治疗。记录两组患者治疗前后健康状况调查问卷(SF-36)评分结果,对比其疗效及不良反发生应率。结果A组治疗有效率为58.33%,明显高于B组的27.78%,差异有统计学意义(P<0.05);治疗后A组SF-36量表各项评分均高于B组,差异均有统计学意义(P<0.05);两组患者脱发、恶心呕吐、胸痛、气短等不良反应发生率比较差异无统计学意义(P>0.05)。结论对晚期非小细胞肺癌患者采用榄香烯联合GP疗法,抗肿瘤效果显著,对提高患者生活质量具有积极意义。
榄香烯;吉西他滨+顺铂方案;晚期非小细胞肺癌
临床研究表明[1],榄香烯作为国家二类抗肿瘤新药,将其与吉西他滨+顺铂(GP方案)联用,可有效改善化疗毒副作用、提高患者耐受性[1-2]。本研究选取72例晚期非小细胞肺癌(non-small cell lung cancer,NSCLC)患者为研究对象,以探讨榄香烯联合GP方案综合治疗晚期NSCLC的临床效果,现整理报道如下:
1 资料与方法
1.1一般资料
选取2012年4月~2014年7月辽宁省鞍山市肿瘤医院(以下简称“我院”)收治的72例患者为研究对象,所有患者均通过病理学确诊为晚期NSCLC。排除严重心、肝、肾功能障碍者,排除白细胞水平低于4.0× 109/L者[3]。本次受试患者中男41例,女31例;年龄58~70岁,平均(61.3±4.3)岁;腺癌42例,肺鳞癌21例,大细胞未分化癌9例。所有患者均采用双数字法随机分成A、B两组,每组各36例。两组患者性别、年龄、疾病分别等一般资料比较差异无统计学意义(P>0.05),具有可比性。本研究均经患者知情并同意,研究项目经我院医学伦理委员会批准。
1.2治疗方法
B组患者采用GP方案:吉西他滨(江苏奥赛康药业股份有限公司;国药准字H20093698)1000 mg/m2,静脉滴注30 min,第1天、第8天各1次;顺铂(云南生物谷药业股份有限公司;国药准字H20043888)75 mg/m2,30 min,第1天静脉滴注。21 d为1个疗程,均持续3个疗程。A组患者在上述治疗基础上辅以榄香烯联合治疗:榄香烯(大连华立金港药业有限公司;国药准字H10960114)0.6 g/d,连用14 d,21 d为1个疗程,持续3个疗程。
1.3评估标准
1.3.1疗效判断标准显效(CR):病灶完全消失时间≥28 d;有效(PR):病灶持续4周以上缩小≥50%;一般(SD):病灶缩小<50%;无效(PD):病灶增加25%或出现新病灶。有效率(RR)=(CR+PR)/总例数×100%[3]。
1.3.2健康状况调查问卷(SF-36)[4]从活力(VT)、生理功能(PF)、社会功能(SF)、总体健康(GH)4个方面反映患者生活质量,分值越高,生活质量越高。
1.4统计学方法
采用SPSS 12.0统计学软件进行数据分析,计量资料数据用均数±标准差表示,两组间比较采用t检验;计数资料用率表示,组间比较采用χ2检验,以P<0.05为差异有统计学意义。
2 结果
2.1疗效对比分析
A组治疗有效率明显高于B组,两组比较差异有统计学意义(P<0.05)。见表1。
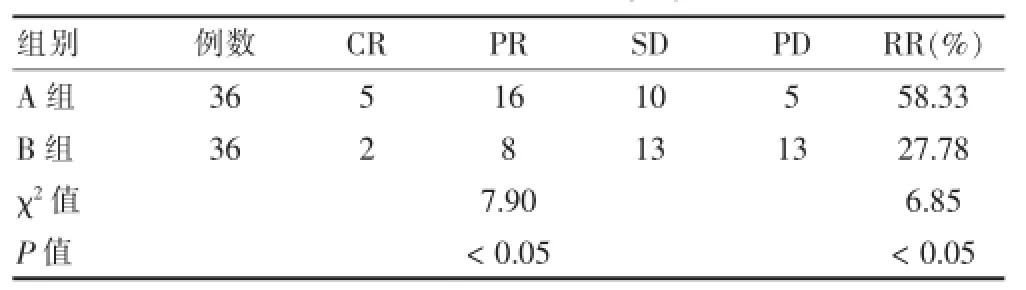
表1 两组疗效比较(例)
2.2治疗后生活质量评分情况分析
治疗后A组SF-36问卷各项评分均高于B组,两组比较差异均有统计学意义(P<0.05)。见表2。
2.3治疗后不良反应发生情况分析
两组患者脱发、恶心呕吐、胸痛、气短等不良反应发生率比较,差异无统计学意义(χ2=0.83,P>0.05),但A组患者个别用药后出现轻微发热症状,于服药前半小时口服强的松可有效缓解该症状。
表2 治疗后两组SF-36评分比较
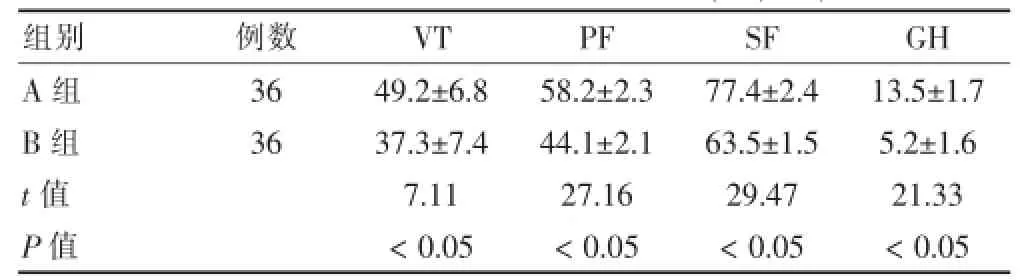
表2 治疗后两组SF-36评分比较
注:VT:活力;PF:生理功能;SF:社会功能;GH:总体健康
组别例数VTPFSFGH A组B组36 36 t值P值49.2±6.8 37.3±7.4 7.11<0.05 58.2±2.3 44.1±2.1 27.16<0.05 77.4±2.4 63.5±1.5 29.47<0.05 13.5±1.7 5.2±1.6 21.33<0.05
3 讨论
据不完全资料统计,NSCLC是当前国内外肺癌发病率最高、患病群体最大的恶性肿瘤疾病,占总肺癌患者的80%以上[5]。患此病症的大部分患者因缺乏体检观念,在确诊时病情已经发展到晚期,即便在此时采用最有效的化疗干预治疗,也有部分患者因对化疗耐受性差而丧失治疗机会,导致癌细胞进一步扩散或转移,为NSCLC患者临床治疗增加了难度[6]。
一般来说,小细胞肺癌通常是很早就开始蔓延,而放疗和化疗的敏感性较高,从而使小细胞肺癌化疗和手术治疗成功率较高,但因为它很容易治疗后复发,患者往往长期使用抗癌中医,确保抑制肿瘤的同时,增强免疫力[7]。NSCLC占肺癌总数的80%,是最常见的肺癌[8],主要包括腺癌、鳞状细胞癌和大细胞未分化癌3种,其对传统的放疗和化疗敏感性差。胸部X线片对肺癌早期诊断具有一定的临床价值,除常规的血液常规检查外,还可在病理检查中发现有助于诊断的病理细胞。一系列深入的检查还包括纤维支气管镜肺活检、纵隔镜、胸腔镜等,目前肺癌手术的主要治疗方法为放疗和化疗和中医药治疗[9]。一般来说,疾病分期取决于肿瘤患者的类型和参考因素,如年龄,选择一个或多个方案组合疗法[10]。对于NSCLC的患者,中医药疗法和化疗是首选治疗方法,例如服用抗癌中药,延缓肺癌相关症状如咳嗽、呼吸困难、疼痛加重[11]。当今,晚期NSCLC患者诊断时部分已经错过了手术时机,且多数有临床或潜在转移,以化疗为主的临床疗效并不理想。
近年来,EK作为代表的受体酪氨酸激酶家族中的表皮生长因子受体的靶向药物和NSCLC治疗中的临床应用研究带来新的曙光[12-13]。表皮生长因子受体为原癌基因产物,具有酪氨酸激酶活性。相关文献显示[14],表皮生长因子受体可以和细胞外配体结合的形式二聚体,通过刺激酪氨酸激酶活性,让二聚体出现磷酸化本身,使信号转移到触发级联在细胞。一旦表皮生长因子受体基因突变,直接参与肿瘤细胞的增殖、血管生成、肿瘤浸润、转移和凋亡抑制的过程。表皮生长因子受体酪氨酸激酶抑制剂对肿瘤细胞的表皮生长因子受体特异性结合阻断细胞信号转导通路,抑制肿瘤细胞增殖,促进其凋亡[15]。顺铂是一种小分子化合物,可抑制人表皮生长因子受体(表皮生长因子受体)信号通路,通过抑制酪氨酸激酶活性抑制肿瘤的形成和生长,抑制肿瘤细胞的特异性,降低肿瘤细胞的黏附力,促进肿瘤细胞的凋亡,提高患者对化疗的敏感性[16-18]。顺铂最常见的不良反应是腹泻和皮疹,少数患者可出现间质性肺疾病和肝损伤[19]。有研究对66例晚期NSCLC顺铂治疗的患者的不良反应进行了观察,发现所有患者均未出现严重白细胞减少、转氨酶升高,在常规化的基础上,大剂量顺铂(150 mg/d)治疗的副作用是可以控制的[20]。
本次研究为探究榄香烯联合GP方案对晚期NSCLC患者临床治疗效果,对72例受试患者分别给予单一疗法与联合用药疗法进行治疗干预,发现联合疗法的A组患者治疗后有效率为58.33%,明显高于单一GP方案的B组患者(27.78%),这一结果提示了榄香烯对无手术指征的晚期NSCLC患者抗癌效果显著,具有较好抑制肿瘤细胞生长及转移效果,可通过直接作用细胞膜,加快肿瘤细胞破裂速度,以此改变其免疫原性,促进免疫反应生成[21-22]。与既往的研究[23-24]结论基本一致。此外,本次研究还发现,A组患者治疗后生活质量评分高于B组,且A组不良反应发生率略低于B组,说明榄香烯对降低化疗毒副作用效果明显,将其与GP方案联合治疗,可缓解患者恶心、脱发、胸痛等化疗不良反应,利于提高患者生活质量及耐受性,增加其治疗舒适度,加强治疗依从性[25-26]。但少数注入榄香烯患者治疗后出现低热症状,笔者认为此为药物正常反应,若无明显改善,可于后续治疗中提前口服解热镇痛类药物以缓和该症状[27-29]。
综上所述,对晚期NSCLC患者采用榄香烯联合GP疗法,可有效提升其抗肿瘤效果,减少不良反应发生,对提高患者生活质量、减轻其痛苦等具有积极意义,值得临床推广使用。
[1]王丽华,沈芳.榄香烯乳剂联合GP方案治疗晚期非小细胞肺癌的疗效观察[J].中国癌症杂志,2010,20(7):547-550.
[2]陆忠华,徐珍,汤华,等.姑息放疗联合榄香烯治疗晚期NSCLC的临床疗效观察[J].实用肿瘤杂志,2012,27(6):617-619.
[3]陈燕平,庄文斌,刘云聪,等.榄香烯联合DC方案治疗晚期非小细胞肺癌疗效观察[J].山东医药,2008,48(30):54-55.
[4]杨国旺,韩冬,于洁,等.榄香烯在晚期非小细胞肺癌二线治疗中的疗效观察[C]//第三届国际中医、中西医结合肿瘤学术交流大会暨第十二届全国中西医结合肿瘤学术大会论文集,2010:915-918.
[5]杨国旺,韩冬,于洁,等.榄香烯在晚期非小细胞肺癌二线治疗中的疗效观察[J].实用肿瘤杂志,2010,25(2):200-202.
[6]Orlandi RR,Kennedy DW.Revision endoscopic frontal sinus surgery[J].Otolaryngol Clin North Am,2013,34(1):77-90.
[7]樊佳奇,田锋.小细胞肺癌综合治疗的新进展[J].中国医药,2013,8(2):275-277.
[8]陈南江,李杭,谭诗生.周剂量多西紫杉醇联合榄香烯乳治疗高龄晚期非小细胞肺癌68例观察[J].中国肿瘤临床,2012,32(15):896-897.
[9]鳍浩斌,黄冬生.多西紫杉醇联合卡铂治疗晚期非小细胞肺癌的疗效观察[J].临床肺科杂志,2013,15(1):3-4.
[10]马军,秦书逵.中国临床肿瘤学教育专辑[M].北京:中国协和医科大学出版社,2009:11-18.
[11]杨波,高建飞,饶智国.DP与GP方案治疗国人晚期非小细胞肺癌疗效Meta分析[J].现代肿瘤医学,2014,19(10):1976-1979.
[12]赵学红.长春瑞滨(NVB)配合放疗治疗晚期非小细胞肺癌的临床研究[J].临床肿瘤学杂志,2012,17(6):472-473.
[13]洪丹,张泝平.培美曲塞的实验和临床研究进展[J].中国癌症杂志,2014,18(1):73.
[14]李树婷,马飞,孙燕.抗肿瘤代谢新药-培美曲塞[J].癌症进展,2015,3(5):471.
[15]吉浩明,张燕.周剂量紫杉醇同步放疗治疗26例晚期非小细胞肺癌的临床观察[J].临床肿瘤学杂志,2012,13(11):1025.
[16]郝学志,张湘茹,孙燕.国产多西他赛治疗乳腺癌和非小细胞肺癌的临床观察[J].中国肿瘤临床,2013,32(18):1064.
[17]刘尧,汪华.吉西他滨联合铂类治疗晚期非小细胞肺癌的临床分析[J].临床内科杂志,2014,26(7):456-459.
[18]裴保香,单文治,王玮,等.培美曲塞和多西他赛分别与顺铂联用治疗非小细胞肺癌的效果观察[J].中国医药,2013,8(11):1566-1567.
[19]Kew J,Rees GL,Close D.Multiplanar reconstructed computed tomography images improves depiction and understanding of the anatomy of the frontal sinus and recess[J]. Am J Rhinol,2014,16(2):19-23.
[20]Shelbourne KD,Brueckmann FR.Rush-pin fixation of supracondylar and intercondylar fractures of the femur[J]. J Bone Joint Surg Am,2014,64(2):161-169.[21]Stammberger HR,Kennedy DW.Paranasal sinuses:anatomicterminologyandnomenclature[J].AnnOtolRhinolLaryngol,1995,167(10):7-16.
[22]Zhang Y,Li W,Yan T.Early detection of lesions of dorsal artery of foot in patients with type 2 diabetes mellitus by high-frequency ultrasonography[J].Huazhong Univ Sci Technolog Med Sci,2015,29(3):387-390.
[23]Nicolls MR,Haskins K,Flores SC.Oxidant stress,immune dysregulation,and vascular function in type I diabetes[J].Antioxid Redox Signal,2007,9(7):879-889.
[24]孙玺媛,梁隽婷,李松,等.中医辨证联合第三代细胞毒单药治疗老年晚期非小细胞肺癌22例[J].中国老年学杂志,2013,33(18):4526-4527.
[25]祝利民,张晖,周浩,等.抗瘤增效方减轻晚期非小细胞肺癌化疗不良反应的时效研究[J].上海交通大学学报:医学版,2011,31(6):797-801.
[26]何敏,周浴,邝军,等.扶正抗癌方联合化疗治疗非小细胞肺癌疗效研究[J].环球中医药,2014,11(4):278-281.
[27]Hoegh A,Lindholt JS.Basic science review.Vascular distensibility as a predictive tool in the management of small asymptomatic abdominal aortic aneurysms[J].Vasc Endovascular Surg,2009,43(4):333-338.
[28]Shingu Y,Shiiya N,Ooka T.Augmentation index is elevated in aortic aneurysm and dissection[J].Ann Thorac Surg,2009,87(5):1373-1377.
[29]Várady E,Feher E,Levai A,et al.Estimation of vessel age and early diagnose of atherosclerosis in progeria syndrome by using echo-tracking[J].Clin Hemorheol Microcirc,2010,44(4):297-301.
Clinical effect of comprehensive treatment of Elemene combined with Gemcitabine and Cisplatin in the treatment of advanced non-small cell lung cancer
LIU JunWEN FugangLI Bin
Ward 8,Anshan Cancer Hospital,Liaoning Province,Anshan114036,China
Objective To explore the clinical effect of comprehensive treatment of Elemene combined with Gemcitabine and Cisplatin(GP schemes)in the treatment of advanced non-small cell lung cancer.Methods 72 patients with advanced non-small cell carcinoma from April 2012 to July 2014 in Anshan Cancer Hospital were selected as the research object,and they were randomly divided into group A and group B,36 cases in each group.Group B was given chemotherapy of GP schemes,Group A was given the Elemene based on the treatment of group A.SF-36 scale of patients in the two groups before and after treatment was recorded;the curative effect and adverse reaction rate of two groups were compared.Results Effective rate of treatment in group A was 58.33%,significantly higher than that of the group B(27.78%),the difference was statistically significant(P<0.05);SF-36 scores of the group A after treatment were higher than those of the group B,the differences were statistically significant(P<0.05);incidence of adverse drug reactions of patients in the two groups,such as the hair loss,nausea,chest pain,shortness of breath,had no statistically significant differences(P>0.05).Conclusion Elemene combined with GP schemes has significant effect of anti-tumor in the treatment of advanced non-small cell lung cancer,plays a positive role in improvement of the patients quality of life.
Elemene;GP schemes;Advanced non-small cell lung cancer
R734.2
A
1673-7210(2015)12(b)-0080-04
2015-08-27本文编辑:任念)
辽宁省鞍山市科学技术项目(鞍科鉴字[2013]22号)。
