原位构造超顺磁性纳米氧化铁/甲壳素复合凝胶
2015-10-24桑秋章王雯静李国祥
邵 宇,桑秋章,王雯静,李国祥
(湖北民族学院化学与环境工程学院,湖北 恩施 445000)
原位构造超顺磁性纳米氧化铁/甲壳素复合凝胶
邵 宇,桑秋章,王雯静,李国祥*
(湖北民族学院化学与环境工程学院,湖北恩施445000)
以氯化铁为前驱体溶液、甲壳素凝胶为基质,成功制备了含有大量氧化铁纳米粒子的甲壳素复合凝胶.通过扫描电镜(SEM)、红外(FT-IR)、X-衍射(XRD)、热重分析和磁强计分析(VSM),考察了复合材料的结构和性能.结果显示:粒径为22.5~33.7nm的球形氧化铁纳米粒子均匀的分散和固载在甲壳素基体中,且随着前驱体溶液浓度从0.05mol/L增至0.5mol/L,氧化铁纳米粒子的量从9wt.%逐渐增加至45 wt.%;复合纳米材料有非常小的磁滞回线和较低的矫顽力.提供了一种制备高含量磁性纳米离子复合凝胶的绿色方法.
甲壳素凝胶;氧化铁;磁性纳米材料
近年来,将功能无机纳米粒子包嵌在凝胶网络中的新型凝胶引起了人们极大地研究兴趣,这主要是归因于它们独特的功能特性.在大多数设想的应用中,多糖基磁性纳米复合凝胶由于具有良好的生物相容性、可生物降解性和生态安全性而显示出了独特的魅力[1-2].通常,构造这种功能复合材料的关键步骤是在加工成型之前须将无机纳米粒子和高分子溶液的均匀混合.然而共混过程中,疏水的高分子和亲水的无机纳米粒子往往容易导致纳米粒子的团聚,引起复合材料结构的不连续性和不均匀性,从而导致材料的功能缺陷[3].因此,如何采用一种简单方法来制备磁性纳米复合材料对纳米科技意义重大.
甲壳素是一种丰富的可再生资源,它是由N-乙酰-2-氨基-2-脱氧-D-吡喃葡萄糖单元通过β-(1→4)糖苷键连接而成的线型多糖,其分子内及分子间存在强烈的氢键作用,使其难溶于一般溶剂,这极大的限制了甲壳素资源的广泛应用.在前期工作中,用8 wt.%NaOH/4 wt.%尿素-水溶液在低温下直接溶解了甲壳素.有趣的是,当温度变化到40℃时,这种高分子溶液容易形成凝胶[4-5].而且近来,在室温下通过离子交联的方法成功的构造了磁性甲壳素复合凝胶微球.因此,本工作中,尝试在甲壳素基体中原位合成氧化铁纳米粒子来构造甲壳素磁性纳米复合凝胶,并考察它们的结构和性能.本研究试图建立一种制备甲壳素磁性凝胶的新的有效途径.
1 实验部分
1.1仪器与试剂
甲壳素样品(蟹壳,α-甲壳素)由山东金湖甲壳素有限公司提供.将甲壳素烘干、粉碎,并过40目筛.粘均分子量(Mη)通过乌氏黏度计在25±0.1℃下于NaOH/尿素水溶液中测定,并依Mark-Houwink方程[6]∶[η]=0.26Mw0.56±0.02(mL·g-1)计算为2.1×106.同时,根据文献报道的方法[7]测得甲壳素乙酰度为0.97.氯化铁购于国药集团化学试剂有限公司,其它试剂均为国产分析纯.
1.2磁性甲壳素凝胶的制备
依据文献报道的方法[8],在8 wt.%NaOH/4 wt.%尿素水溶液中,2 wt.%甲壳素溶液制备:4g的甲壳素溶解于200g的8 wt.%NaOH/4 wt.%尿素水溶液得到清亮的甲壳素溶液.将所得溶液用10 mL烧杯分装,40℃保存一定时间得到甲壳素凝胶.将凝胶经水洗干净,然后分别浸入不同浓度的FeCl3溶液中12h,经去离子水洗,以除去吸附凝胶表面的Fe3+离子,随后经2mol·L-1NaOH处理30min,室温下用去离子水漂洗几次除去多余的碱.未经FeCl3处理的甲壳素凝胶记为G0,分别经0.05、0.2mol·L-1和0.5mol·L-1FeCl3处理的甲壳素复合凝胶记为G1、G2、G3.

图1 复合凝胶G0和G1照片Fig.1 The optical photographs of G0(a)and G1(b),respectively
1.3表征及性能测试
湿态凝胶先用液氮冷冻,然后冷冻干燥(CHRIST AlpHa 1-2,Germany).将干燥的珠粒喷Pt后,用场发射扫描电镜(SEM,SIRION TMP,FEI)观察微观结构,加速电压为20kV;将干燥的凝胶研磨成粉状,60℃真空干燥48h备用.红外光谱测试用170SX傅立叶光谱仪(American Niolet Company),粉末样品用KBr压片,扫描范围4000~400cm-1;X-ray衍射分析在D8 Advance diffractometer(Bruker,U.S.A.)上进行,连续记谱扫描,CuKɑ辐射(λ=0.15406nm),管电压40kV,电流50mA,扫描范围分别为8°~50°,扫描速度4°/min;用磁强计(VSM,Lake Shore,7304,USA)对复合凝胶粉末进行磁性能测试,25℃下记录磁场在-1.7至+1.7 T范围的磁滞回线.
2 结果与讨论
2.1磁性甲壳素复合凝胶的构造与结构
包含氧化铁的纳米复合凝胶通过一种简便有效的方式制备.图1(a,b)显示了G0和G1的形态.凝胶均呈圆柱形;在溶胀状态下,G0和G1平均直径分别约为21mm和23 mm.但它们的粒径之间有些微区别,G1略大于G0,这主要是在甲壳素基体内合成了氧化铁,氧化铁纳米粒子占据了高分子基体的部分空间.而且很明显,氧化铁纳米粒子的形成使得无色的甲壳素高分子凝胶转变为红棕色.此外,有趣的是复合凝胶的颜色会随着组分中无机纳米粒子含量的增加从浅黄到棕色变化.这主要是因为甲壳素凝胶基体中氧化铁纳米粒子会随着前驱体溶液中Fe3+浓度的增大相应增加.
图2(a,b,c,d)分别是凝胶G0和复合凝胶(G1,G2,G3)的表面扫描电镜图片.图2显示,甲壳素凝胶G0的表面存在微孔结构,微孔的形成主要是在溶胶-凝胶过程中水诱导相分离的结果,溶剂多的地方有助于形成微孔.而且和G0相比,复合凝胶的表面更加致密,这主要是无机纳米粒子的贡献.当甲壳素凝胶浸在FeCl3溶液中时,Fe3+很容易通过微孔进入到甲壳素凝胶网络,由于甲壳素分子内羟基中富电子氧与过渡金属离子的相互作用,Fe3+被限制在甲壳素大分子上.这是值得注意的,当凝胶经NaOH溶液处理、水洗、干燥过程中,分解和氧化反应会发生.因此,在甲壳素基体内原位合成了氧化铁纳米粒子,从而得到含有氧化铁的复合凝胶.且球形氧化铁粒子均匀分散在甲壳素基体中,粒径约50nm.随着FeCl3溶液浓度从0.05mol/L增加至0.5 mol/L,纳米粒子的平均粒径稍有增加,如图2(c,d)所示.甲壳素复合凝胶氧化铁纳米粒子的量能通过Fe3+离子的扩散平衡加以控制.图3是G1的扫描电镜能谱图(EDS).EDS显示复合凝胶仅存在C、O和Fe元素,这进一步证明在甲壳素复合凝胶中合成了无机纳米粒子.因此,本工作建立了一种原位合成甲壳素复合纳米凝胶的简单有效方法;甲壳素凝胶的羟基官能团和微孔结构对改善氧化铁纳米粒子的分散和稳定扮演着重要的角色,而且甲壳素凝胶的微孔能作为模板有效防止氧化铁纳米粒子的团聚.

图2 复合凝胶G0(a),G1(b),G2(c),G3(d)表层电镜照片Fig.2 The SEM of the surface of G0(a),G1(b),G2(c),G3(d),respectively

图3 复合凝胶G1的电镜EDS能谱图Fig.3 EDS spectrum from SEM of G1
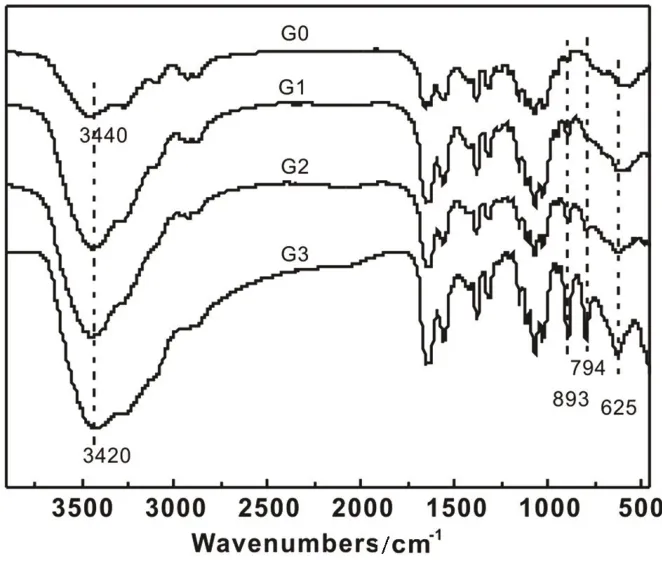
图4 凝胶的红外光谱图Fig.4 FT-IR spectra of the gels

图5 凝胶的X衍射图谱Fig.5 X-ray diffraction patterns of the gels
凝胶的红外光谱如图4所示.图4显示,3400 cm-1处有一个明显的单峰,这是甲壳素羟基的伸缩振动峰,对比G0,复合凝胶的羟基峰明显变宽,且向低波数移动,这表明甲壳素分子中的基团和氧化铁纳米粒子之间有较强的相互作用,而且在600~800cm-1的低波数区有新的吸收峰出现,这是“金属-氧”键(M-O)的特征吸收峰,表明了Fe-O键的存在.因此,无机纳米粒子在多糖分子基体内的固载,并不仅仅是物理作用,而主要是化学作用.由于氧化铁在胶中的高稳定性,氧化铁纳米粒子在凝胶基体原位沉淀下来,并成为凝胶的染色成分.氧化铁纳米粒子的稳定性对甲壳素复合凝胶的性能非常重要.
图5为甲壳素凝胶和复合凝胶的XRD衍射图.甲壳素凝胶在2θ= 9.3°、19.4°和25.7°有三个结晶峰,分别对应着(110)、(100)和(200)晶面,这是α-甲壳素的衍射特征峰.在复合凝胶中甲壳素的结晶度明显低于G0,且随着氧化铁纳米粒子含量的增加而降低.这表明纳米复合凝胶中甲壳素的结晶度由于纳米粒子的形成而被部分破坏.显示了氧化铁和甲壳素分子之间较强的相互作用.此外,复合凝胶在35.57°、40.9°、43.24°、54.2°出现了新的吸收峰,这是氧化铁的特征峰.根据Scherrer方程,得到在G1、G2和G3中的磁性纳米粒子的平均粒径分别约为22.5、28.6和33.7 nm,这和扫描电镜分析的结果基本一致.因此,通过甲壳素凝胶微孔成功合成了氧化铁磁性纳米粒子.且随着前驱体浓度的增大,磁性纳米粒子相对衍射峰的强度相应增加,表明甲壳素基体中无机纳米相的量也增大.
复合凝胶在氮气氛围下的热重(TG)和差热分析(DTG)的曲线如图6所示.样品在40~80℃有一个失重率为8%~11%的失重峰,这主要是样品中吸潮水份的挥发.随着温度的变化,甲壳素膜的热分解曲线有两个明显的台阶.280~380℃为甲壳素凝胶最大失重范围,这主要归因于甲壳素开始分解,包括糖环的脱水、聚合以及乙酰基的分解、甲壳素重复单元的脱乙酰化.450~600℃范围的失重主要是样品的氧化和碳化.和G0相比,甲壳素复合凝胶的热稳定性明显降低,这可能是复合凝胶中甲壳素结晶度的降低以及氧化铁纳米粒子催化作用引起的协同效应的结果.且随着FeCl3浓度在0.05~0.5 mol·L-1范围的变化,纳米粒子的含量相应的从9 wt.%增加至45 wt.%.
2.2磁性能
磁性能是复合凝胶的最重要的特征之一.图7显示了室温下复合凝胶的磁化曲线磁场.复合凝胶的磁化强度随磁场的增加而增强.所有复合凝胶的磁化强度都较弱,且缺乏饱和性,但它们表现了极小的磁化圈和较低的矫顽力.这是单畴粒子的典型特征[9].众所周知,对于磁性粒子,当它们的粒径低于临界尺寸的时候,被称为单畴,此时磁性粒子会表现出超顺磁行为.一方面每个单畴粒子被磁化后会按同一方向排列.由于没有畴壁移动,磁化强度将会反自旋扭转;另一方面,在一种小粒子体系中形状的各向异性是矫顽力的另一个来源.单畴粒子偏离球形,对矫顽力有明显影响.因此,能观察到纳米复合凝胶有较低的矫顽力.这对它们的进一步应用有重要的意义.因而,在这里提供了一种简便易行的绿色方法来构造磁性纳米复合凝胶材料.
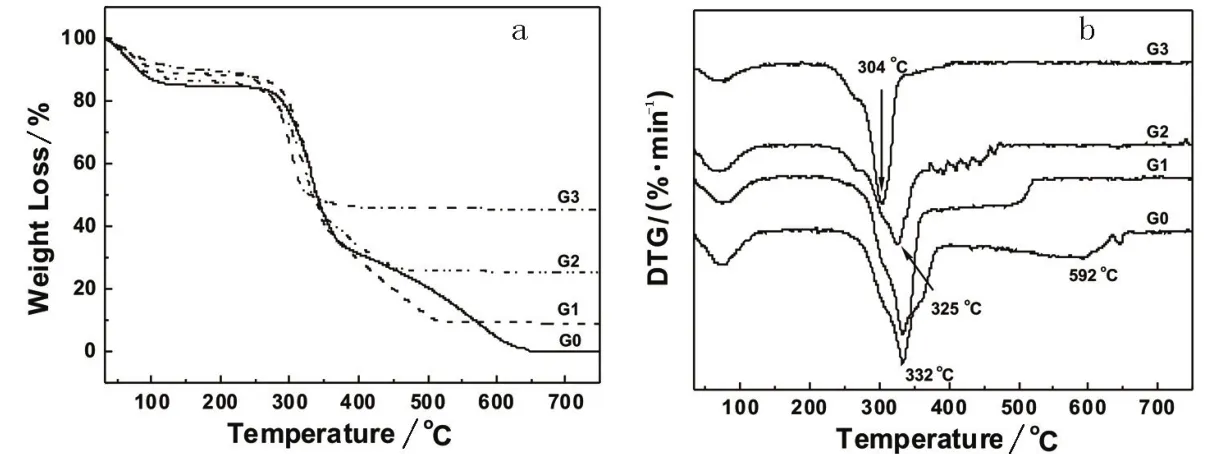
图6 氮气保护下凝胶的热重分析(a)和差热分析(b)曲线Fig.6 The thermogravimetry(a)and differential thermogravimetry(b)curves of the gels under nitrogen atmosphere

图7 室温下复合凝胶G1(▲)、G2(●)和G3(■)磁滞回线Fig.7 The magnetic hysteresis loops of the composite gels G1(▲),G2(●)and G3(■)at 298 K
3 结论
通过一种简单方法成功的原位构造了氧化铁纳米磁性凝胶.氧化铁纳米粒子独特的分散在甲壳素基体中,粒径约50nm.且随着Fe3+离子浓度从0.05mol·L-1增加到0.5mol·L-1,氧化铁纳米粒子的含量相应的从9 wt.%增大到45 wt.%.甲壳素基体和无机纳米粒子之间存在较强的相互作用.甲壳素复合凝胶体现了超顺磁性能,渴望在介电材料、催化及生物医学领域有潜在的应用.
[1]WU J,ZHENG Y,WEN X,et al.Silver nanoparticle/bacterial cellulose gel membranes for antibacterial wound dressing:investigation in vitro and in vivo[J].Biomed Mater,2014,9(3):035005.
[2]KANMANI P,RHIMJ W.Physicochemical properties of gelatin/silver nanoparticle antimicrobial composite films[J].Food Chem,2014,148(2):162 -169.
[3]HU X W,TANG Y F,WANG Q,et al.Rheological behaviour of chitin in NaOH/urea aqueous solution[J].Carbohyd Polym,2011,83(3):1128-1133.
[4]LI G X,DU Y M,TAO Y Z,et al.Dilute solution properties of four natural chitin in NaOH/urea aqueous system[J].Carbohyd Polym,2010,80(3):970-976.
[5]LI G X,LI W Z,DENG H B,et al.Structure and properties of chitin/alginate blend membranes from NaOH/urea aqueous solution[J].Int J Biol Macromol,2012,51(5):1121-1126.
[6]LI G X,LU D C,S X D,et al.Highly selective removal of organic dyes from aqueous solutions using chitin beads entrapping rectorite[J].J Appl Polym Sci,2014,131:40905.
[7]ZHENG H,ZHOU J P,DU Y M,et al.Cellulose/chitin films blended in NaOH/urea aqueous solution[J].J Appl Polym Sci,2002,86(7):1679-1683.
[8]LI G X,DU Y M,TAO Y Z,et al.Iron(II)cross-linked chitin-based gel beads:Preparation,magnetic property and adsorption of methyl orange[J].Carbohyd Polym,2010,82(3):706-713.
[9]LIU S,ZHANG L,ZHOU J,et al.Structure and properties of cellulose/Fe2O3nanocomposite fibers spun via aneffective pathway[J].J Phys Chem C,2008,112(12):4538-4544.
责任编辑:高 山
In-situ Formation of Iron Oxide/chitin Nanocomposite Gels with Super Paramagnetic Properties
SHAO Yu,SANG Qiuzhang,WANG Wenjing,LI Guoxiang*
(School of Chemical and Environmental Engineering,Hubei University for Nationalities,Enshi 445000,China)
Chitin nanocomposite gels containing high contents of Fe2O3nanoparticles were successfully prepared with chitin gels as a matrix and FeCl3as precursors.The structure and properties of the nanocomposites were investigated using scanning electron microscopy(SEM),fourier-transform infrared(FT -IR),X-ray diffraction(XRD),thermogravimetric analysis,and vibrating sample magnetometry(VSM).The results indicated that the spherical magnetic Fe2O3nanoparticles were homogeneously dispersed and immobilized in the chitin matrix.With an increase in the concentration of precursors from 0.05 to 0.5 mol/L,the content of Fe2O3nanoparticles in the dried nanocomposites increased from 9 to 45 wt %,and the particle diameter increased from 22.5 to 33.7 nm.The magnetometric measurements revealed that superparamagnetic behavior of the nanocomposites,and they had extremely small hysteresis loop and low coercivity.This study provided a simple and“green”process for the preparation of biobased magnetic nanocomposite gels with high nanophase content.
Chitin gels;ferric oxide;magnetic nanocomposite
TB324
A
1008-8423(2015)04-0449-04DOI:10.13501/j.cnki.42-1569/n.2015.12.023
2015-10-23.
湖北省教育厅中青年项目(Q20122907).
邵宇(1976-),男,硕士,讲师,主要从事有机高分子材料的研究;*
李国祥(1975-),男,博士,副教授,主要从事再生资源化学生物学的研究.
