小檗碱衍生物的活性研究进展
2015-10-21京聂晶姚其正
张 磊* 王 京聂 晶姚其正
(1 遵义医学院药学院,贵州 遵义 563003;2 中国药科大学药学院,江苏 南京 210009)
小檗碱衍生物的活性研究进展
张 磊1* 王 京1聂 晶1姚其正2
(1 遵义医学院药学院,贵州 遵义 563003;2 中国药科大学药学院,江苏 南京 210009)
小檗碱是一种来源于植物的天然药物,其在医药领域内具有广泛的应用价值。本文综述了近年来小檗碱衍生物的活性研究进展,旨在能为以天然产物小檗碱为核心的结构改造上提供一些有益的帮助。
小檗碱;衍生物;活性;研究进展
1 概 述
小檗碱[1]又称黄连素,是从中草药黄连等植物中提取分离得到的一类异喹啉类生物碱。小檗碱在临床上主要用于治疗细菌性胃肠道疾病。近年来,小檗碱成了国内外天然药物化学领域的研究热点之一,大量的小檗碱结构衍生物被合成出来。研究结果表明,这些小檗碱的结构衍生物具有多种药理活性,如治疗阿尔兹海默综合征、抗微生物、抗肿瘤和抗病毒等[2]。因此,本文综述了近年来小檗碱衍生物的活性研究进展。小檗碱结构式见图1。
2 小檗碱衍生物的药理活性
2.1治疗阿尔兹海默综合征:阿尔茨海默病(alzheimer disease,AD)是一种中枢神经系统变性病,起病隐袭,病程呈慢性进行性。AD的病因及发病机制尚未阐明,特征性病理改变为β淀粉样蛋白沉积形成的细胞外老年斑和tau蛋白过度磷酸化形成的神经细胞内神经原纤维缠结,以及神经元丢失伴胶质细胞增生还包括氧化应激、乙酰胆碱酯酶(AChE)、丁酰胆碱酯酶(BuChE)等有关。
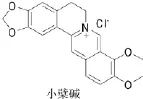
图1 小檗碱结构式
研究表明,天然产物小檗碱对阿尔兹海默综合征有一定的疗效[3]。Shi等[4]利用点击化学,将叠氮基和炔基环合得到了一系列含有三氮唑的小檗碱衍生物,并在体外将所合成的小檗碱衍生物测定了对乙酰胆碱酯酶(AChE)和丁酰胆碱酯酶(BuChE)的抑制活性,实验结果表明,该系列化合物对这两种酶都有一定的抑制活性,其中,化合物1(图2)对AChE的抑制活性最强,IC50值为(0.044±0.001)μmol,对BuChE的IC50为(6.21±0.127)μmol,对AChE的选择性为141,而阳性药加兰它敏对AChE的IC50为(0.623±0.099)μmol,对BuChE的IC50为(15.7±0.787)μmol,对AChE的选择性为25.3。化合物1对β淀粉样蛋白的聚合也有较强的抑制活性,在20 μmol浓度下,其抑制率为77.9%。进一步的分子对接模型显示,其可以通过与AChE蛋白结构中的Trp84形成π-π形式的相互作用而起到抑制活性。
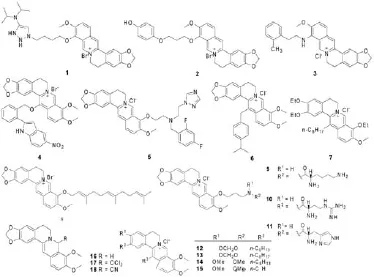
图2 小檗碱类衍生物(1~18)
Jiang等[5]合成了一系列小檗碱与苯酚、褪黑素、阿魏酸杂合的小分子衍生物,并对阿尔兹海默综合征进行了相关研究,实验结果表明,杂合分子的抗氧化性和Aβ蛋白聚合抑制性均强于小檗碱,但是其中一些化合物的AChE的抑制活性有所降低。化合物2(图2)对Aβ蛋白聚合抑制性达到92%(20 μmol),对AChE,BuChE也有较强的抑制活性。该类型的杂合小檗碱衍生物是一类有前途的,具有多重作用机制的AD药物。
Shande等[6]合成了9-N-取代的小檗碱类化合物,并研究了这些化合物的多种生物活性,实验结果显示,该系列化合物均有较好的抗氧化活性及抗AChE,BuChE,Aβ蛋白聚合的活性。其中,化合物3(图2)的活性最好:抗氧化活性相当于4.05 μmol Trolox;对AChE和 BuChE 的IC50值分别为(0.027±0.002)μmol,(0.713±0.016)μmol;对Aβ蛋白聚合抑制的IC50为2.73 μmol。
2.2抗微生物:小檗碱抗菌谱广泛,对金黄色葡萄球菌、链球菌等有较强抗菌作用;对枯草杆菌、肺炎杆菌、结核杆菌也有抗菌作用,其作用机制在于抑制微生物的DNA和蛋白质的合成。
根据药物分子药效团杂合的原理,Samosorn等[7]将NorA抑制剂与小檗碱通过亚甲基醚连接成一个小分子,合成了13位取代的小檗碱衍生物,通过体外一系列生物测试表明,化合物4(图2)对金色葡萄球菌具有强烈的抑菌活性,MIC为1.7 μmoL,是小檗碱的382倍;该化合物对NorA泵也具有一定的阻止活性。构效关系研究显示,杂合分子中的吲哚结构对抑制NorA泵的活性没有贡献,但是其是保持杂合分子具有较好抗菌活性的必要基团。
Zhang等[8]设计并合成了一系列9位取代的小檗碱衍生物,并考察其对革兰阳性菌、革兰阴性菌及两种真菌的抑制活性。实验结果表明,合成的小檗碱衍生物的抗细菌及真菌的活性与小檗碱相当或优于小檗碱,化合物5(图2)对MRSA、S.aureus、B.subtilis、M.luteus、E.coli和P.vulgaris的MIC值在2~8 μg/mL,优于氯新霉素和小檗碱,与诺氟沙星相当;抗真菌方面,其对C.albicans、C.mycoderma的MIC分别为4 μg/mL和2 μg/mL。
Park等[9]在小檗碱和小檗红碱的13位引入了苯甲基取代基,并对所合成的化合物进行了体外抗病原性真菌的实验。实验数据表明,取代小檗碱衍生物的抗真菌活性较小檗碱和小檗红碱有明显的提高,化合物6(图2)对C.albicans、C.tropicalis和C.krusei的MIC分别4 μg/mL、1 μg/mL和8 μg/mL,均优于小檗碱和小檗红碱。
Liu等[10]合成了28个13-正辛基小檗碱盐,对多药耐药性结核分枝杆菌H37RV的抑制实验表明,化合物均对H37Rv具有抑制活性,其中化合物7(图2)的活性最强,其MIC值为0.125 μg/mL,并且该化合物对耐利福平和异烟肼的结核分枝杆菌具有较好的活性,该化合物还在进一步的研究中。
2.3抗肿瘤:近年来的研究结果表明,小檗碱具有较强的抗肿瘤活性。主要的机制:①影响肿瘤细胞生长周期;②抑制拓朴异构酶;③调节凋亡相关基因;④抑制肿瘤血管生成等。
Lo等[11]报道了9-O-烷基修饰的小檗碱类衍生物,体外抗肿瘤实验表明,随着烷基链的增持,化合物的ClogP值也在不断的变大,对HepG2和HT-29肿瘤细胞的抑制活性也提高,当R=Farnesyl时,化合物8(图2)对两种肿瘤细胞的抑制活性都较强,对HepG2和HT-29的IC50(48 h)值分别为(0.08±0.02)μmol,(0.27±0.07)μmol,强于小檗碱(8.32±2.11)μmol,(8.45±0.35)μmol和顺铂(36.00± 3.10)μmol,(24.10±0.10)μmol;荧光实验证明该化合物能够明显的减少肿瘤细胞的数量,并导致肿瘤细胞的形态发生明显的变化,如皱缩,核酸裂解等;进一步的annexin V-FITC实验还证明,其能够诱导HepG2肿瘤细胞的凋亡。
Ma等[12]设计合成了3个多胺取代的小檗碱衍生物9~11(图2),并利用圆二色光谱(CD)、荧光共振能量转移(FRET)熔点实验、荧光光谱和聚合酶链反应(PCR)终止实验等手段研究了小檗碱衍生物与端粒DNA 的相互作用。小檗碱衍生物可以诱导端粒DNA序列形成反平行结构G-四链体,显著地提高了端粒G-四链体的稳定性,有效地抑制了端粒的扩增;而与双链DNA 的相互作用则很小,是高选择性的端粒G-四链体配体。构型关系表明:侧链长越长,侧链与四链体表面的作用越强;侧链的碱性基团更容易与磷酸基团发生静电作用;侧链上容易质子化的氨基个数越多,对于稳定作用的贡献越大。这些化合物可作为开发端粒酶抑制剂抗癌药物的先导化合物。
Zhang[13]等将小檗碱及结构类似物巴马汀分子结构的C-13位引入长的烷烃链12~15(图2),并研究不同长度烷烃链对化合物抗肿瘤活性的影响。实验结果表明,小檗碱及巴马汀衍生物对多种肿瘤细胞(如7701QGY、SMMC7721、HepG2等)的IC50值在(0.02±0.01)~(13.58 ±2.84)μmoL,并能够显著抑制小鼠S180移植瘤的生长。构效关系研究显示:13-烷基取代小檗碱和13-烷基取代巴马汀抑制肿瘤细胞生长活性均分别高于小檗碱和巴马汀它们相应的同系物,同时还显示出随着13-位取代的直链烷基的碳链增长,相应的抗肿瘤活性也随之增加。
2.4抗病毒:病毒是一种主要是由蛋白质和核酸组成的微生物,其结构非常简单,只有几个到十几个基因,如HIV病毒等。病毒的特点是在宿主细胞的细胞内寄生,利用宿主细胞的成分来为它自己复制,并危害宿主。
Yang[14]等报道了巴马汀及小檗碱的抗HIV-1研究,它们的EC50为44.5 mg/L和63.1 mg/L;而在13-正己基小檗碱盐酸盐(12)和13-正己基巴马汀盐酸盐(14)对HIV-1没有抑制活性。但是12和14抑制对HIV-1感染的C8166细胞抑制作用都较好,EC50为0.16 mg/L,0.08 mg/L,明显优于小檗碱和巴马汀。
研究显示[15],通过对小檗碱类似物16~18(图2)的抗人巨细胞病毒(HCMV)及细胞毒性研究,盐酸小檗碱与更昔洛韦的抑制HCMV活性相当,IC50=0.68 μmol、0.91 μmol。化合物17和18具有与更昔洛韦相当的抗HCMV活性,但是它们的细胞毒性较大。
3 结束语
综上所述,天然药物小檗碱的结构修饰产物具有多种较强的药理活性,如治疗阿尔兹海默综合征、抗微生物、抗肿瘤和抗病毒等,部分衍生物的活性强于小檗碱或毒性低于小檗碱。因此,小檗碱衍生物是一类具有较大研究价值的先导化合物。
[1]Singh IP,Mahajan S.Berberine and its derivatives: a patent review(2009-2012)[J].Expert Opin Ther Patents,2013,23(2): 215-231.
[2]Huang ZJ,Zeng Y,Lan P,et al.Advances in structural modifications and biological activities of berberine: an active compound in traditional Chinese medicine[J].Mini-Rev Med Chem,2011,11(13):1122-1129.
[3]Ji HF,Shen L.Berberine: A Potential Multipotent Natural Product to Combat Alzheimer’s Disease[J].Molecules,2011,16(8): 6732-6740.
[4]Shi A,Huang L,Lu C,et al.Synthesis,biological evaluation and molecular modeling of novel triazole-containing berberine derivatives as acetylcholine-esterase and β-amyloid aggregation inhibitors[J].Bioorg Med Chem,2011,19(7): 2298-2305.
[5]Jiang H,Wang X,Huang L,et al.Benzenediol-berberine hybrids: Multifunctional agents for Alzheimer's disease[J].Bioorg Med Chem,2011,19(23): 7228-7235.
[6]Shan W J,Huang L,Zhou Q,et al.Synthesis,biological evaluation of 9-N-substituted berberine derivatives as multi-functional agents of antioxidant,inhibitors of acetylcholinesterase,butyrylcholineste rase and amyloid-b aggregation[J].Eur J Med Chem,2011,46(12):5885-5893.
[7]Samosorn S,Tanwirat B,Muhamad N,et al.Antibacterial activity of berberine-NorA pump inhibitor hybrids with a methylene ether linking group[J].Bioorg Med Chem,2009,17(11):3866-3872.
[8]Zhang SL,Chang JJ,Damua GLV,et al.Novel berberine triazoles:Synthesis,antimicrobial evaluation and competitive interactions with metal ions to Human Serum Albumin[J].Bioorg Med Chem Lett,2013,23(4): 1008-1012.
[9]Park KD,Lee JH,Kim SH,et al.Synthesis of 13-(substituted benzyl)berberine and berberrubine derivatives as antifungal agents[J]. Bioorg Med Chem Lett,2006,16(15): 3913-3916.
[10]Liu YX,Xiao CL,Wang YX,et al.Synthesis,structureeactivity relationship and in vitro anti-mycobacterial evaluation of 13-n-octylberberine derivatives[J].Eur J Med Chem,2012,71(52):151-158.
[11]Lo CY,Hsu YC,Chen MS,et al.Synthesis and anticancer activity of a novel series of 9-O-substituted berberine derivatives: A lipophilic substitute role[J].Bioorg Med Chem Lett,2013,23(1):305-309.
[12]马彦,黄志纾.高选择性端粒G-四链体稳定性配体: 9-O-多胺取代小檗碱衍生物的合成及活性评价[J].高等学校化学学报,2012,33(10): 2217-2222.
[13]Zhang L,Li J,Ma F,et al.Synthesis and Cytotoxicity Evaluation of 13-n-Alkyl Berberine and Palmatine Analogues as Anticancer Agents[J].Molecules,2012,17(10): 11294-11302.
[14]杨柳萌,王睿睿,李晶晶.四个小檗碱类化合物的体外抗HIV-1活性[J].中国天然药物,2007,3(5): 225-228.
[15]Hayashi K,Minod K,Nagaok Y,et al.Antiviral activity of berberine and related compounds against human cytomegalovirus[J].Bioorg Med Chem Lett,2007,17(6): 1562-1564.
Advances in Research on Activities of Berberine Derivatives
ZHANG Lei1, WANG Jing1, NIE Jing1, YAO Qi-zheng2
(1 School of Pharmacy, Zunyi Medical College, Zunyi 563003, China;2 School of Pharmacy, China Pharmaceutical University, Nanjing 210009, China)
Berberine was a natural drug derived from plants, and it played important roles in the medicine. The advances in research on activities of berberine derivatives were reviewed in this paper for the structural modifications of berberine.
Berberine; Derivatives; Activities; Recent advance
R282.71
A
1671-8194(2015)012-0032-03
E-mail:lei_chang@yeah.net
