小牛血清去蛋白注射液与6种输液配伍的稳定性考察
2015-10-19邹立芳梁晓美邹慧龙
邹立芳 梁晓美 邹慧龙
小牛血清去蛋白注射液与6种输液配伍的稳定性考察
邹立芳梁晓美邹慧龙
目的 考察小牛血清去蛋白注射液与6种临床常用输液配伍的稳定性,为临床使用提供参考。方法 模拟临床用药浓度,将小牛血清去蛋白注射液20mL分别加入250ml 0.9%氯化钠注射液(0.9%NS)、5%葡萄糖注射液(5%GS)、10%葡萄糖注射液(10%GS)、5%葡萄糖氯化钠注射液(5%GNS)、果糖注射液和转化糖注射液中,依次在0、1、2、4、6h时间点,采用外观观察法、pH检测法、不溶性微粒检查法、紫外-可见分光光度法、无菌检查法,比较小牛血清去蛋白注射液与6种输液配伍后的外观、pH、不溶性微粒、紫外吸收光谱的变化,以及无菌检查是否合格。结果 6种配伍液在各时间点,外观、pH值、紫外吸收光谱均无显著变化,且无菌检查合格,但不溶性微粒明显增多。结论 小牛血清去蛋白注射液可以与上述6种输液配伍,在6h内较稳定,但配伍后不溶性微粒明显增多。因此,在临床应用中应重视加强配伍后不溶性微粒的监测,尽量避免不良反应发生,确保临床用药安全。
小牛血清去蛋白注射液 稳定性 配伍 不溶性微粒
小牛血清去蛋白注射液为小牛血清去蛋白提取、精制而得,内含多种游离氨基酸和肽,能改善氧和葡萄糖的吸收及利用,从而提高ATP的周转,为细胞提供较高的能量[1]。目前临床上主要应用于改善脑部血液循环和营养障碍性疾病所引起的神经功能缺损;末梢动脉、静脉循环障碍及其引起的动脉血管病,腿部溃疡等[2]。作者自2014年1月至3月观察小牛血清去蛋白注射液与不同输液配伍的变化及其稳定性,为临床用药提供参考。报道如下。
1 仪器与试药
1.1仪器 雷磁pHSJ-4A实验室pH计(上海精密科学仪器有限公司),GWF-8JA微粒分析仪(天津天河医疗仪器有限公司),UV-1601紫外可见分光光度计(北京瑞利分析仪器公司),HTY-2000A集菌仪(杭州泰林生物技术设备有限公司),SW-CJ-1B标准型净化工作台(苏州净化设备总厂),SA-1800-1水平净化工作台(上海上净净化设备有限公司),一次性使用无菌注射器(浙江灵洋医疗器械有限公司)。
1.2试药 小牛血清去蛋白注射液(锦州奥鸿药业有限责任公司,20ml:0.8g),0.9%氯化钠注射液(浙江国镜药业有限公司,250ml:2.25g),5%葡萄糖注射液(浙江国镜药业有限公司,250ml:12.5g),10%葡萄糖注射液(浙江国镜药业有限公司,250ml:25g),5%葡萄糖氯化钠注射液(浙江国镜药业有限公司,250ml:葡萄糖12.5g与氯化钠2.25g),果糖注射液(安徽丰原药业股份有限公司,250ml:25g),转化糖注射液(四川美大康佳乐药业有限公司,250ml:果糖:12.5g与葡萄糖12.5g)。
1.3方法 在本院静脉用药配置中心的净化环境下,按临床常用浓度,将小牛血清去蛋白注射液20ml分别加入到0.9%NS、5%GS、10%GS、5%GNS、果糖注射液和转化糖注射液中,作为供试品溶液。
1.4稳定性观察 将供试品溶液置于室温下观察,分别在0、1、2、4、6h进行外观、pH、不溶性微粒、紫外吸收光谱及无菌检查,观察其稳定性。
2 结果
2.1外观检查 配伍后各混合溶液随静置时间增加溶液颜色无明显变化,且溶液澄清,无可见异物,即配伍液在各时间点外观上无明显不稳定现象。
2.2pH值测定 在各时间点依次测定pH值,观察并比较6种输液配伍前、后pH的变化(pH计以磷酸盐标准缓冲液和苯二甲酸盐标准缓冲液校准),见表1。
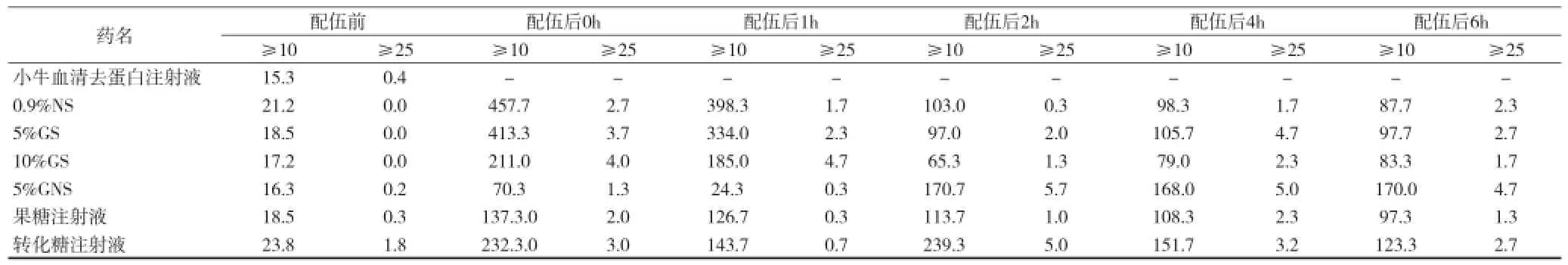
表2 小牛血清去蛋白注射液与6种输液配伍后的微粒数(个/ml)(μm)
2.3不溶性微粒测定 在净化工作台上,用纯净水反复冲洗测定杯,分别取小牛血清去蛋白注射液、0.9%NS、5%GS、10%GS、5%GNS、果糖注射液、转化糖注射液40ml,用微粒检测仪按照不溶性微粒检查法(《中国药典》2010年版二部附录IXC)[3]检查,测定4次,取后3次的结果计算,取平均值,测出每毫升微粒直径≥10μm、≥25μm的微粒数,作为空白对照。同法,取供试品溶液依次在各时间点,测定配伍后的微粒数,见表2。
2.4紫外吸收光谱测定 取供试品溶液,以蒸馏水作空白对照,在200~400nm波长范围内,在各时间点依次扫描配伍后混合液的紫外吸收最大吸收波长。结果显示,小牛血清去蛋白注射液与6种输液配伍后的紫外吸收光谱无显著变化,见表3。
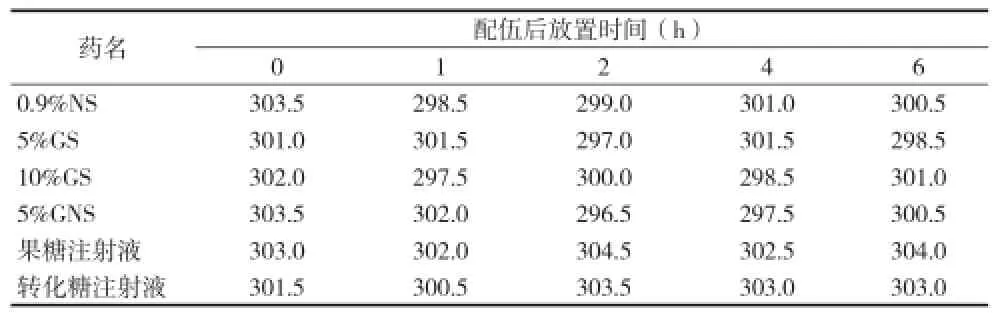
表3 小牛血清去蛋白注射液与6种输液配伍后的紫外吸收光谱
2.5无菌检查 用薄膜过滤法处理后,依法检查(中国药典2010 年版二部附录Ⅺ H)[3]。具体操作步骤:取适量供试品,在无菌操作下将该供试品分别接种于需氧菌、厌氧菌培养基(硫乙醇酸盐流体培养基)6管,其中1管接种金黄色葡萄球菌对照用菌液1ml,作为阳性对照,另接种于真菌培养基(改良马丁培养基)5管。轻轻摇动,使供试品与培养基混合。硫乙醇酸盐流体培养基管置30~35℃、改良马丁培养基管置20~25℃、培养7d。在培养期间应逐日观察并记录是否有菌生长。阳性对照管在24h内应有菌生长,如在加入供试品后,培养基出现浑浊,培养7d后,不能从外观上判断有无微生物生长,可取该培养液适量转种至同种新鲜培养基中或斜面培养基上继续培养,细菌培养2d,真菌培养3d,观察是否再出现浑浊或斜面有无菌生长,或用接种环取培养液涂片,染色,用显微镜观察是否有菌。小牛血清去蛋白注射液与6种输液配伍后以及放置6h后进行无菌检查,结果全部合格。
3 讨论
在脑功能降低和能量需求增加等情况下,小牛血清去蛋白注射液可增进与能量有关的功能代谢,保持细胞功能,促使供血量增加。在外周组织中亦可起到改善微循环,提高组织细胞再生修复能力,增强受损组织细胞对能量的利用,因而可以使胶原纤维重组,减少或避免瘢痕形成[4]。
本资料结果表明,配伍前,小牛血清去蛋白注射液与6种输液的pH及微粒测定结果均符合规定,配伍后,6种混合溶液置于室温条件下0、1、2、4、6h后,其外观未见明显变化,pH值无显著变化,紫外吸收光谱无明显变化,配伍后不同直径的不溶性微粒明显增加,可能与气泡有关,因微粒检测仪不能分辨气泡和微粒。所以输液配制完毕后,应静置以后输注较好。
本文采用光阻法测定不溶性微粒,光阻法操作简便、快速,《中国药典》将光阻法作为不溶性微粒的首选方法,且关于注射液不溶性微粒数的限度如下:标示量为100ml或>100ml的静脉用注射液,每1ml中含≥10μm微粒<25粒,含≥25μm微粒<3粒[5]。虽对复配以后的输液未作要求。且尚无具体的限量规定,但微粒对人体的危害,仍应引起重视。从本试验可看出,在复配后的输液中微粒数大幅增加,甚至明显超出药典标准,当然有部分是因为气泡的干扰。药物复配过程的各个环节均可能影响不溶性微粒,临床配药操作及药物之间的理化变化及使用的输液器不合理等多方面引起[6]。因此,控制不溶性微粒现已成为保证输液安全的重要环节,为确保静脉用药的安全,减少不溶性微粒对人体的危害,临床配药、使用、医疗护理及医疗器械等部门均应高度重视,加强监控和管理力度,以提高临床静脉给药的质量,确保临床用药安全。
1 赵宗阁,王尊文,徐康森.国内小牛血、小牛血清去蛋白提取物注射液质量分析及其抗缺氧作用研究.药物分析杂志,Chin J pHarm Anal,2008, 28(10):1637~1640.
2 吕媛,权菊香.小牛血清去蛋白注射液.中国临床药理学杂志,2006,22(2):141~144.
3 国家药典委员会.中华人民共和国药典(二部).2010年版.北京:中国医药科技出版社,2010.附录IX R,XI H.
4 陈新谦,金有豫,汤光.新编药物学.第17版.北京:人民卫生出版社,2011.323.
5 严叶霞,疏血通注射液与源种溶媒配伍稳定性考察.中国药师,2013,16(7):1085.
6 梁晓美,康艾注射液与5种输液配伍的稳定性.医药导报,2013, 32(6):805~806.
Objective To observe the stability of infusion compatibility between the deproteinized calf blood serum injection and six kinds of infusion solutions,and to provide the clinical reference of using drug. Methods By simulating the clinical concentration,deproteinized calf blood serum injection was respectively added to 0.9% sodium chloride injection,5% glucose injection,10% glucose injection,5% glucose and sodium chloride injection,fructose injection and invert sugar injection,the appearance,pH,insoluble particules,UV absorption spectrum and sterility test at different time intervals were observed. Results The appearance,pH and UV absorption spectrum were all stable in 6 infusion solutions,and sterility test is qualifi ed,but the numbers of insoluble particules of different diameters were obviously increased. Conclusion Deproteinized calf blood serum injection can be mixed in these six infusion solutions,and was stable within 6 hours,but the increase of insoluble particules in infusion solutions may be focused and monitored during clinical use,so the adverse reactions can avoid as far as possible,and the drug of clinical use can be safe.
Deproteinized calf blood serum injection Mixing Stability Mixing Insoluble particules
323000 浙江省丽水市人民医院
