双波长双指示剂催化动力学光度法测定痕量Fe(Ⅲ)
2015-10-16侯法菊陈玉静苗延虹
侯法菊, 陈玉静, 苗延虹, 徐 慧
(1.鲁东大学化学与材料科学学院,山东烟台 264025;2.山东农业大学化学与材料科学学院,山东泰安 271000)
铁是人体所必需的最重要的微量元素之一。铁参与血红蛋白、肌红蛋白、细胞色素及许多酶的合成,是身体内制造血红蛋白的主要原料,在氧的运输及呼吸等许多代谢中起重要作用,因此,研究测定食品中铁的新方法有重要的现实意义。目前,测定痕量Fe(Ⅲ)的方法主要有原子吸收光谱法[1]、荧光法[2]、示波极谱法[3]和催化动力学光度法[4 - 6]等。利用双波长和双指示剂光度法测定痕量组分可进一步提高灵敏度。
本实验研究了在HCl介质中,利用邻菲罗啉活化Fe(Ⅲ)催化H2O2氧化甲基橙和亚甲基蓝混合指示剂的褪色反应,通过510和660 nm波长处吸光度差值的加和与Fe(Ⅲ)浓度的线性关系,建立了双波长双指示剂催化动力学光度法测定痕量Fe(Ⅲ)的新方法。该方法简单、快捷,可用于食品中痕量铁的测定。
1 实验部分
1.1 仪器与试剂
7200型可见分光光度计(尤尼柯(上海)仪器有限公司);电子天平(奥豪斯仪器(上海)有限公司制造);电热蒸馏水器(上海生银医疗仪器仪表有限公司)。
Fe(Ⅲ)标准溶液:1.0 mg/mL,准确称取0.8638 g硫酸铁铵,用6 mL 3.0 mol/L H2SO4将其溶解并转入100 mL容量瓶中,加水定容,摇匀,使用时再逐级稀释为0.1 μg/mL工作溶液;甲基橙溶液:1.0 g/L,准确称取0.2500 g甲基橙定容至250 mL容量瓶;亚甲基蓝溶液:1.0×10-3mol/L,准确称取0.0935 g亚甲基蓝定容至250 mL容量瓶;3%H2O2:取33.6 mL 30%的H2O2定容至250 mL容量瓶,现用现配;HCl:0.10 mol/L;邻菲罗啉溶液:1.0×10-3mol/L,准确称取0.0496 g邻菲罗啉定容至250 mL容量瓶;上述试剂均为分析纯。实验用水为二次蒸馏水。
1.2 实验方法
在两支25 mL比色管中,分别加入0.7 mL HCl,3.0 mL亚甲基蓝溶液,1.0 mL甲基橙溶液,3.0 mL邻菲罗啉溶液,1.0 mL H2O2,其中一支加入3.0 mL Fe(Ⅲ)标准工作溶液(催化反应,吸光度为A),另一支不加Fe(Ⅲ)标准工作溶液(非催化反应,吸光度为A0),用水稀释至刻度,摇匀。置于沸水浴中,加热18 min后,迅速取出,用自来水冷却,停止反应。最后,以水作为参比,用1 cm的比色皿,在波长510和660 nm处,分别测定非催化和催化体系的吸光度A510 0、A660 0、A510、A660,并计算△A510=A510 0-A510,△A660=A660 0-A660,△A=△A510+△A660。
2 结果与讨论
2.1 吸收光谱

图1 吸收光谱Fig.1 Absorption spectra1.system of non-catalytic reaction;2.system of catalytic reaction.
按实验方法,分别测量催化反应和非催化反应体系的吸收光谱曲线,结果见图1。实验表明,在双指示剂体系中,催化反应体系和非催化反应体系在波长510和660 nm出现两个吸收峰,故本实验分别选用510和660 nm作为测量波长。
2.2 反应介质及其用量的选择
按实验方法,试验了不同介质对催化反应速度的影响。结果表明,在相同酸度条件下的H2SO4、HCl、HNO3介质中Fe(Ⅲ)对反应均有催化作用,但催化反应速度不同。在稀HCl介质中,催化作用最强,△A最大,故选用HCl控制体系的酸度。另外0.10 mol/L HCl为0.5~1.0 mL时,△A较大且稳定,选择HCl的最佳用量为0.7 mL。
2.3 试剂用量的选择
2.3.1亚甲基蓝用量的影响按实验方法试验了亚甲基蓝溶液的用量对实验的影响。结果表明,当1.0×10-3mol/L亚甲基蓝溶液用量为3.0 mL时,△A达到最大且稳定。实验选用亚甲基蓝溶液的用量为3.0 mL。
2.3.2甲基橙用量的影响按实验方法试验了甲基橙溶液的用量对实验的影响。结果表明,当1.0 g/L甲基橙溶液用量为1.0 mL时,△A达到最大且稳定。实验选用甲基橙溶液的用量为1.0 mL。
2.3.3过氧化氢用量的影响按实验方法试验了H2O2的用量对实验的影响。当3%H2O2用量为1.0 mL时,△A达到最大且稳定。实验选用H2O2的用量为1.0 mL。
2.3.4邻菲罗啉用量的影响按实验方法试验了邻菲罗啉溶液的用量对实验的影响。当1.0×10-3mol/L邻菲罗啉溶液用量为3.0 mL时,△A达到最大且稳定。实验选择的用量为3.0 mL。
2.4 反应时间的影响
当反应温度为100 ℃时,实验了反应时间对体系△A的影响。结果表明,当反应时间为18 min时△A值最大且稳定。实验选用反应时间为18 min。
2.5 分析应用
2.5.1线性范围和检出限在最佳实验条件下,以本方法测得Fe(Ⅲ)的浓度与体系△A呈现良好的线性关系,相关系数r=0.9978。方法线性范围为0.008~0.24 μg/mL,检出限为0.003 μg/mL。
2.5.2样品处理及测定实验选取菠菜、紫菜和熟蛋黄作为样品。将一定量样品先用自来水洗净,再用蒸馏水漂洗2~3次,晾干表面水分后,切碎,置于恒温鼓风干燥箱中于105 ℃烘干,冷却后准确称取干基样品,置于蒸发皿中于电热套内加热,至样品炭化并灰化后,转入马弗炉中,于600 ℃灼烧2~3 h,冷却后加入15~20 mL HCl溶解,用小火加热至近干,冷却后加入少量蒸馏水溶解,过滤,滤液转入100 mL容量瓶中,用蒸馏水洗涤蒸发皿,洗液合并于容量瓶中,定容,摇匀,分别贴上标签作为样品溶液待用(菠菜:样品①;紫菜:样品②;蛋黄:样品③)。按实验方法在最佳实验条件下测定样品中Fe(Ⅲ)的含量,结果如表1所示。
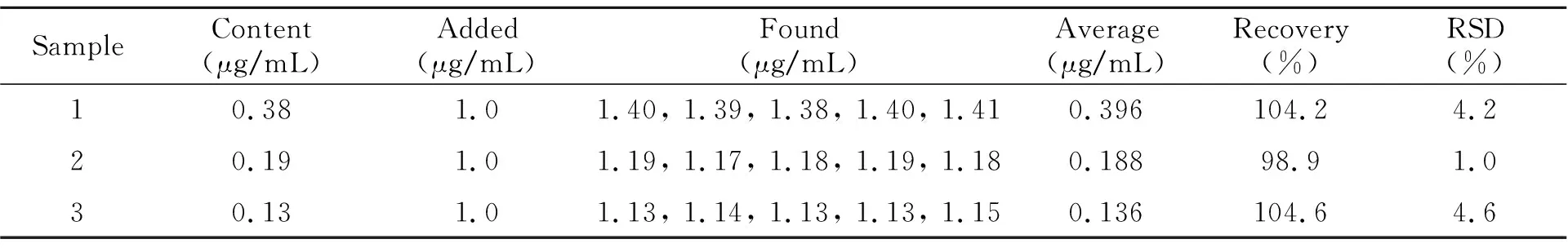
表1 样品中铁的测定结果
实验结果表明,该法的回收率在98.9%~104.6%范围。
3 结论
本实验研究了双波长双指示剂催化动力学光度法测定痕量Fe(Ⅲ)的方法。该方法操作简单、快速准确。
