替吉奥联合介入治疗晚期胰腺癌的近期效果观察
2015-09-25于洪波李拥军张卫华
于洪波,李拥军,张卫华
(南通市肿瘤医院介入科,江苏226361)
替吉奥联合介入治疗晚期胰腺癌的近期效果观察
于洪波,李拥军,张卫华*
(南通市肿瘤医院介入科,江苏226361)
目的:探讨替吉奥(S-1)胶囊联合介入治疗晚期胰腺癌的近期效果。方法:对46例晚期胰腺癌患者的临床资料进行回顾性分析,其中24例采用替吉奥胶囊联合介入方案治疗(观察组);22例采用单纯介入治疗(对照组)。采用Kaplan Meier法分析患者的生存时间,并比较两组患者的客观有效率、疾病控制率、临床受益率和不良反应。结果:观察组客观有效率(ORR)明显高于对照组(45.8%vs 18.2%),差异有统计学意义(P=0.046)。观察组疾病控制率(DCR)高于对照组(75.0%vs 40.9%),差异有统计学意义(P=0.019)。与对照组相比,观察组的临床受益率(70.8%vs 45.5%)、6个月生存率(70.8%vs 59.1%)均较高,但差异无统计学意义。中位生存时间观察组明显高于对照组,且差异有统计学意义(P=0.013)。两组不良反应的发生率差异无统计学意义(P>0.05)。结论:对于晚期胰腺癌,替吉奥胶囊联合介入治疗与单纯介入治疗相比较,在临床疗效方面表现出一定优势,患者受益明显,且不良反应可耐受,是晚期胰腺癌的一种有效治疗方案。
晚期胰腺癌;替吉奥;介入治疗
胰腺癌是临床常见且恶性程度极高的恶性肿瘤之一,预后差,病死率高,胰腺癌死亡人数已占肿瘤死亡第4位,居消化道癌症死因的第2位[1]。胰腺癌起病隐匿,患者早期症状不明显,确诊时多数已属中晚期[2],手术根治率低。通常诊断时只有20%患者有手术机会,手术切除后5年生存率也仅为1%~3%。介入治疗胰腺癌是除手术、化疗外的一种安全有效的方法,在延长生存时间和提高患者生活质量方面有一定的作用[3],但因接受治疗者多为晚期病例,总体临床获益不高。有研究表明,替吉奥胶囊可以明显改善晚期胰腺癌患者的预后[4]。我科2011年1月—2014年1月采用替吉奥胶囊联合介入治疗晚期胰腺癌24例,取得了一定的效果,并与采用单纯介入治疗的22例进行对照比较,现报告如下。
1 资料与方法
1.1一般资料晚期胰腺癌46例均为经B超、CT、MR及病理学(活检或细胞学)等检查确诊为进展期或已有转移的晚期胰腺癌。预计生存期大于3个月,心肺功能基本正常,肝肾功能于正常高值2倍以内,血常规及凝血功能基本正常。其中男31例,女15例,年龄36~74岁,中位年龄56岁。其中胰头癌29例、胰体癌8例、胰尾癌9例。既往未接受化疗及放疗,均无介入治疗的禁忌证。每例患者治疗前后均有完整的病例资料,并获得了患者家属的同意并签署知情同意书。临床分期按照国际抗癌联盟(UICC)分期法,所有入组患者均为Ⅲ期或Ⅳ期。其中采用替吉奥胶囊联合介入的治疗方案的24例设为观察组,22例采用单纯介入治疗的作为对照组,在一般临床资料上两组之间差异无统计学意义,具有可比性。
1.2方法两组患者均常规行介入治疗。根据患者的病灶有无转移等情况选择不同的介入方式:病灶仅位于胰腺,无肝脏转移,行动脉灌注化疗(TAI)术;若存在肝转移,则在灌注化疗的基础上行肝动脉栓塞化疗(TACE)术。在局部麻醉下采用Seldinger技术穿刺右侧股动脉,至腹腔动脉及肠系膜上动脉行DSA造影,胰体尾部肿瘤需同时行脾动脉造影,明确肿瘤位置、数目及供血情况。化疗药物稀释后经上述供血血管灌注,如造影后能明确供应肿瘤的分支血管者,可选用3F微导管进一步超选择肿瘤分支血管内灌注化疗药物。灌注化疗药物方案:吉西他滨1 000mg/m2,奥沙利铂100mg/m2。有肝转移患者,则在胰腺灌注化疗的基础上再行肝动脉造影,根据血管造影情况,用吉西他滨与超液化碘化油5~10mL混合制成混悬液,超选择插管至肝动脉肿瘤供血动脉行栓塞化疗。每4周为一个介入治疗周期。观察组:于介入治疗的同时开始口服替吉奥胶囊,起始剂量:体表面积<1.25m2,80mg/日;1.25m2≤体表面积<1.5m2,100mg/日;体表面积≥1.5m2,120mg/日,2次/日,d1-21,28天为1个周期。对照组:单纯行介入治疗,不口服替吉奥胶囊。两组均在2个周期治疗结束后评价疗效。
1.3疗效评价标准根据CT或MR结果评价治疗前后肿瘤大小变化,按照世界卫生组织(WHO)制定的实体瘤疗效评价标准,分为完全缓解(CR),部分缓解(PR),疾病稳定(SD),疾病进展(PD)。客观有效率(ORR)为CR+PR,疾病控制率(DCR)为CR+PR+ SD。临床受益率(CBR)的评定标准如下:(1)体力状况改善,KPS评分增加至少20分;(2)肿瘤引起的疼痛强度减轻≥50%;(3)镇痛药物的使用剂量减少≥50%;(4)排除体液潴留等因素,体重增加≥7。以上指标有一项符合改善标准,持续4周以上,且无1项指标恶化,则视为临床受益病例。不良反应分级标准采用WHO的抗癌药物的急性与亚急性不良反应分级标准。
1.4统计学处理所有统计数据资料使用SPSS 19.0统计学软件进行分析。计数资料使用χ2检验,计量资料使用t检验,以Kaplan-Meier分析方法进行生存分析,假设检验均为双侧检验,以P<0.05为差异有统计学意义。
2 结 果
2.1疗效比较所有患者均在2个周期结束后评价客观疗效(表1)。观察组的客观有效率(ORR)为45.8%,明显高于对照组(18.2%),差异有统计学意义(P=0.046)。观察组的疾病控制率(DCR)为75.0%,明显高于对照组的40.9%,差异具有统计学意义(P= 0.019)。

表1 两组患者临床疗效比较
2.2临床受益比较从体力状况改善、疼痛缓解情况及体重增加三个方面评价临床受益率,观察组患者临床受益率为70.8%,高于对照组(45.5%),但两组差异无统计学意义(P>0.05),见表2。

表2 两组患者临床受益及生存时间比较
2.3生存时间比较两组患者的生存情况见表2。观察组的中位生存时间(mOS)为10.1个月(95%可信区间:8.2~12.0个月),显著高于对照组的7.2个月(95%可信区间:4.9~9.5个月),差异有统计学意义(P=0.013),见图1;观察组的6个月生存率为70.8%,也高于对照组(59.1%),但差异无统计学意义(P>0.05)。
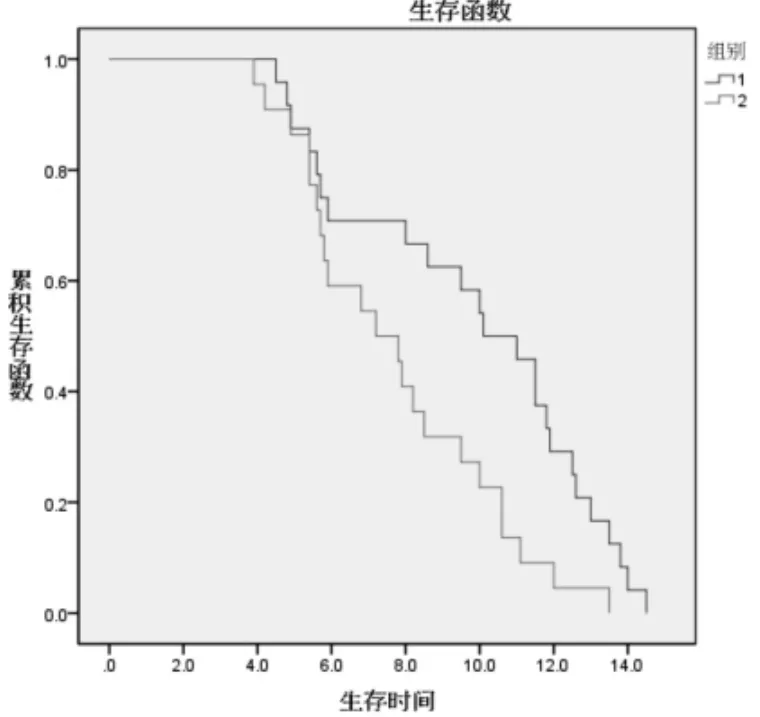
图1 两组生存曲线
2.4不良反应比较按WHO分级标准评价分级,治疗中的主要不良反应为血液学毒性、肝功能受损、恶心呕吐及腹泻。所有患者均未因严重不良反应终止治疗,未出现治疗相关性死亡。两组患者不良反应发生情况见表3。两组间差异均无统计学意义(P>0.05)。
3 讨 论
介入治疗是胰腺癌的一种重要的姑息治疗手段,因其全身不良反应小、局部药物浓度高等特点,尤其适用于不能手术切除的晚期胰腺癌以及年老体弱者。经动脉的介入治疗包括TAI和TACE,胰腺癌原发部位的病灶采取TAI的治疗方案,存在肝转移或者有明确的胰腺肿瘤血管选择TACE[5-6]。胰腺癌是对化疗药有很高耐药性的肿瘤,原因主要为胰腺癌瘤体外部包裹有致密的、化疗药物难以透过的纤维膜;此外,胰腺癌还能够表达多药耐药基因,透入的化疗药物还可被多重耐药机制清除[7]。而动脉局部灌注化疗大大提高了肿瘤组织局部的药物浓度。而且,经腹腔动脉和肠系膜上动脉等灌注入的化疗药物,随后可经门静脉系统回流肝脏,形成对肝脏的再灌注,进一步杀灭门脉系统内和肝内的转移病灶。有报道,对于中晚期胰腺癌,介入动脉灌注化疗较传统全身静脉化疗明显提高临床受益率和1年生存率[8]。另外,关于胰腺癌介入灌注化疗药物的选择,目前尚无统一标准,文献报道使用较多的为吉西他滨联合奥沙利铂的方案。替吉奥胶囊是口服的复方化疗药物,主要包含氟尿嘧啶类药物,有报道称,对于晚期胰腺癌,替吉奥胶囊与吉西他滨联合应用与单用吉西他滨比较,临床获益明显,不良反应无明显增加[9]。
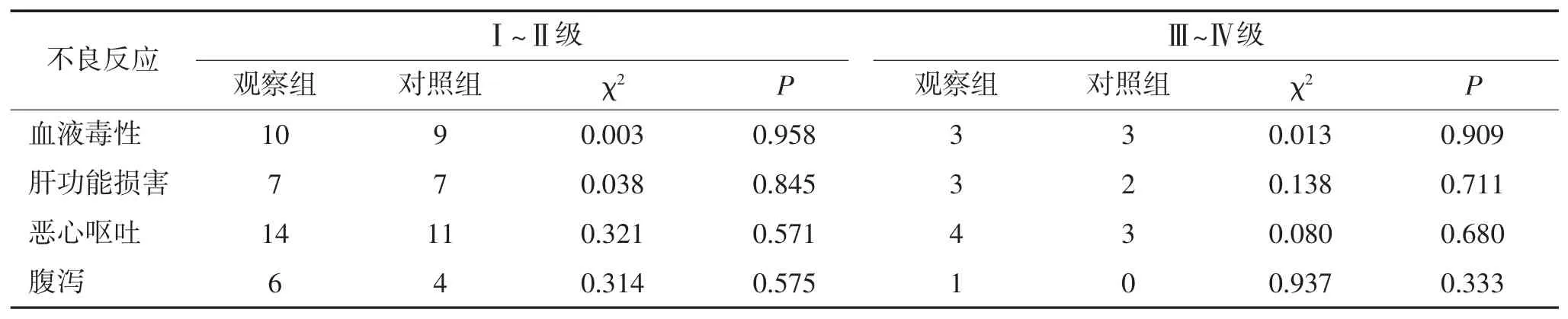
表3 两组患者不良反应发生率比较
本研究采用介入治疗联合替吉奥胶囊治疗晚期胰腺癌,与单纯介入治疗比较,结果观察组在客观有效率、疾病控制率上明显高于对照组,差异有统计学意义(P<0.05);6个月生存率、临床受益率也明显高于对照组,但差异无统计学意义;中位生存时间明显高于对照组,且差异有统计学意义(P=0.013)。观察组的主要不良反应为骨髓抑制反应(包括粒细胞、血小板减少及贫血),以及肝功能损害、恶心呕吐、腹泻等,基本处于临床可耐受范围,与对照组比较差异无统计学意义(P>0.05)。晚期肿瘤的治疗长期以来都面临着如何提高疗效且不增加不良反应的难题,介入治疗及口服替吉奥治疗均为全身不良反应相对较小的治疗方案。我们将两者联合应用,不明显增加治疗相关不良反应,同时提高了近期疗效及生活质量。因肿瘤耐药等原因,远期生存率未见明显增加,但中位生存期有明显提高。
综上所述,替吉奥胶囊联合介入治疗对于晚期胰腺癌优于单纯介入治疗,不良反应无明显增加,耐受性较好,具有较高的临床应用价值,值得推广及进一步研究。
[1]Jemal A,Bray F,Center MM,et al.Global cancer statistics [J].CA Cancer J Clin,2011,61(2):69-90.
[2]Huguet F,Girard N,Guerche CS,et al.Chemoradiotherapy in the management of locally advanced pancreatic carcinoma:a qualitative systematic review[J].J Clin Oncol,2009,27(13):2269-2277.
[3]Hong GB,Zhou JX,Sun HB,et al.Continuous transarterial infusion chemotherapy with gemcitabine and 5-Fluorouracil for advanced pancreatic carcinoma[J].Asian Pac J Cancer Prev,2012,13(6):2669-2673.
[4]Murakami Y,Uemura K,Sudo TA,et al.Impact of adjuvant gemcitabine plus S-1 chemotherapy after surgical resection for adenocarcinoma of the body or tail of the pancreas[J].J Gastrointest Surg,2009,13(1):85-92.
[5]Tanaka T,Sho M,Nishiofuku H,et al.Unresectable pancreatic cancer:arterial embolization to achieve a single blood supply for intraarterial infusion of 5-fluorouracil and fulldose IV gemcitabine[J].AJR Am J Roentgenol,2012,198 (6):1445-1452.
[6]Azizi A,Naguib NN,Mbalisike E,et al.Liver metastases of pancreatic cancer:role of repetitive transarterial chemoembolization(TACE)on tumor response and survival[J].Pancreas,2011,40(8):1271-1275.
[7]Triano LR,Chang BW,Saif MW.New developments in the treatment of locally advanced pancreatic cancer.Highlights from the 45th ASCO annual meeting.Orlando,FL,USA.May 29-June 2,2009[J].JOP,2009,10(4):366-372.
[8]洪国斌,周经兴,许林锋,等.中晚期胰腺癌介入治疗与外周静脉化疗疗效比较的META分析[J].实用放射学杂志,2004,20(4):350-353.
[9]Sasaki T,Isayama H,Nakai Y,et al.Multicenter phase II study of S-1 monotherapy as second-line chemotherapy for advanced biliary tract cancer refractory to gemcitabine[J]. Invest New Drugs,2012,30(2):708-713.
R736.7
B
1006-2440(2015)06-0621-03
2015-09-26
张卫华,E-mail:ntjrzwh321@126.com
