响应面法对金银花叶中绿原酸提取工艺的优化
2015-09-09向福付建强孙白珍等
向福 付建强 孙白珍等


摘要:为了优化金银花(Lonicera japonica)叶中绿原酸醇浸水提工艺,通过单因素试验筛选pH、提取时间、乙醇体积分数等关键影响因素,以绿原酸得率为响应值设计响应面优化试验。结果表明,提取金银花叶绿原酸的最佳工艺为pH 4.5、提取时间25 min、浸析乙醇体积分数65%,该条件下绿原酸的得率可达6.856%。该工艺合理可行,可用于金银花叶中绿原酸提取的产业化生产。
关键词:金银花(Lonicera japonica)叶;响应面;绿原酸;水提法
中图分类号:R284.2 文献标识码:A 文章编号:0439-8114(2015)15-3727-04
DOI:10.14088/j.cnki.issn0439-8114.2015.15.038
Abstract: To optimize the water extraction conditions for chlorogenic acid from flos lonicerae leaves,the key factors such as pH,extraction time,and alcohol concentration were employed to design response surface analysis based on single factor test,with yield of chlorogenic acid as response value.The results showed that the optimum extraction conditions were pH 4.5,extraction time 25 min,and alcohol volume fraction 65%,and under this processtheyield of chlorogenic acid reached 6.856%. So this extraction technology is practically reasonable and suitable for commercial production of chlorogenic acid from flos lonicerae leaves.
Key words: flos lonicerae(Lonicera japonica) leaves; response surface method; chlorogenic acid; water extraction
金银花(Lonicera japonica)是中国一种药食兼用的重要中药材,药用历史悠久,由于其显著的抗菌消炎作用而被誉为“植物抗生素”。绿原酸是金银花的一种主要活性成分,具有抗菌、抗病毒、抗肿瘤、降血压、降血脂、保肝利胆、升高白细胞以及清除自由基等作用[1],广泛用于医药、保健、卫生、化工和食品等领域,也是目前国际公认的“植物黄金”[2]。长期以来,由于金银花叶一直被视为非药用部位而被大量废弃,造成了极大的资源浪费。事实上,金银花叶中绿原酸含量丰富,如湖北省黄冈地区地标产品——罗田金银花的叶中绿原酸的含量高达7%左右[3],且其来源丰富、采集容易,是一种成本更为低廉的绿原酸提取原料。因此,从金银花叶中提取绿原酸已逐渐受到人们的关注。
工艺优化过程中,传统的单因素和正交试验无法在整个区域内寻求因素的最佳组合和响应值的最优值,工程应用的可信度不够。响应面法是一种周期短、精度高、能探讨几种因素间交互作用的回归分析方法,有助于通过较少的试验次数进行快速建模,从而提高工程应用的可信度[4]。因此,本研究以金银花叶为原料,采用醇浸水提法提取绿原酸[5],用紫外分光光度计进行检测,通过响应面分析对金银花叶中绿原酸的提取工艺进行优化,从而为大别山地区金银花高附加值产品的精深加工提供科学依据和技术支持。
1 材料与方法
1.1 材料与仪器
材料与试剂:金银花叶,采于团风县方高坪镇汤铺岭村金银花基地,阴干,粉碎备用;绿原酸标准品(批号20120117),上海源叶生物科技有限公司;浓盐酸、氢氧化钠、无水乙醇均为分析纯,天津市凯通化学试剂有限公司。
仪器设备:紫外可见分光光度计(Varian Cary 100 Scan,美国Varian公司);电子天平(Ax-205 METTLER TOLEDO,瑞士梅特勒-托利多集团);旋转蒸发器(RE-S2AA,上海亚荣生化仪器厂);超声波清洗器(SB 25-12DTDN,宁波新芝生物科技有限公司);pH计[UB-7,赛多利斯科学仪器(北京)有限公司];电热恒温水浴锅(DZKW-D-2,北京西城区医疗器械厂)。
1.2 方法
1.2.1 绿原酸得率测定 最大波峰和标准曲线沿用实验室前期的测定结果[5],即检测波长为323 nm,绿原酸在浓度(X)为5~50 μg/mL范围与吸光度(Y)呈良好线性关系,回归方程为Y=0.043 5X+ 0.021 7,R2=0.999 4。绿原酸得率按式(1)计算:
C=[(A-0.021 7)/0.043 5]×N×V×10-6/m]×100%(1)
式中,C为绿原酸得率,%;V为绿原酸提取液体积,mL;m为金银花叶的质量,g;A为吸光度;N为稀释倍数。
1.2.2 单因素试验 ①提取温度对绿原酸提取的影响。称取5份处理后的金银花叶粉末10 g置于圆底烧瓶,用适量55%乙醇浸泡12 h后,按液料体积质量比20∶1(V∶m,下同)加入pH 4的超纯水,在60、70、80、90℃及沸水条件下水浴25 min提取金银花叶中绿原酸,考察提取温度对绿原酸提取的影响。②pH对绿原酸提取的影响。称取5份处理后的金银花叶粉末10 g置于圆底烧瓶,用适量55%乙醇浸泡12 h后,按液料体积质量比20∶1加入pH为2、3、4、5、6的超纯水,沸水浴加热25 min提取金银花叶中绿原酸,考察pH对绿原酸提取的影响。③提取时间对绿原酸提取的影响。称取7份处理后的金银花叶粉末10 g置于圆底烧瓶,用适量55%乙醇浸泡12 h后,按液料体积质量比20∶1加入pH 4的超纯水,沸水浴分别加热5、10、15、20、25、30、35 min提取金银花叶中绿原酸,考察提取时间对绿原酸提取的影响。④浸析醇体积分数对绿原酸提取的影响。称取5份处理后的金银花叶粉末10 g置于圆底烧瓶,分别用适量体积分数为25%、35%、45%、55%、65%的乙醇浸泡12 h后,按液料体积质量比20∶1加入pH 4的超纯水,沸水浴加热25 min提取金银花叶中绿原酸,考察乙醇体积分数对绿原酸提取的影响。
1.2.3 响应面优化试验 根据单因素试验结果,选取pH、提取时间、浸析醇体积分数3个对金银花叶中绿原酸提取效果影响较为显著的因素,以绿原酸得率为响应值,依据Box-Behnken中心组合试验设计原理设计3因素3水平的响应面优化试验,响应面分析因子与水平如表1所示。
2 结果与分析
2.1 单因素试验结果
2.1.1 提取温度对绿原酸提取的影响 从图1可知,在60~80 ℃时绿原酸提取量迅速增大,然后趋于平缓,直到沸水后达到最高值,表明醇浸水提工艺中短时温度达到80 ℃后渗入细胞内部的乙醇沸腾效果明显,在沸水条件下提取效果最好。
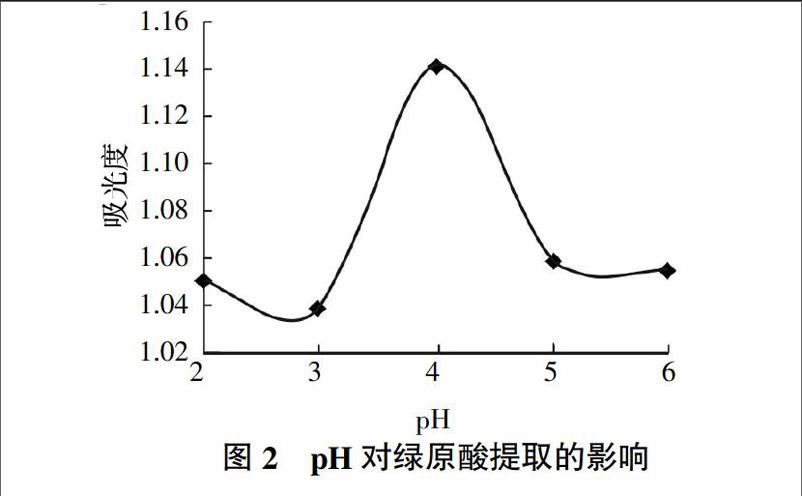
2.1.2 pH对绿原酸提取的影响 由图2可知,随着pH的增大,绿原酸提取量先增加后减少,当pH 4时,金银花叶中绿原酸的提取效果最好,因此适宜条件为pH 4。该结论与向福等[5]的结果一致。
2.1.3 提取时间对绿原酸提取的影响 由图3可知,加热时间10 min时出现第1个峰值,与向福等[5]的结果一致。不同的是在25 min出现了最大的峰值,随后绿原酸量迅速降低。这可能是由于25 min时进入金银花叶孔内的乙醇溶液迅速沸腾而强化了提取效果,随着时间的延长,绿原酸在高温下易分解,且提取物中的多糖等杂质会大量增加,导致绿原酸量迅速降低。因此提取时间以25 min为宜。
2.1.4 浸析醇体积分数对绿原酸提取的影响 由图4可看出,随着乙醇体积分数的增大,绿原酸提取量先是快速上升,在55%浸析醇处出现峰值,之后降低。金银花叶用乙醇进行浸泡的过程相当于细胞内部绿原酸的解析过程,乙醇溶液体积分数不同对细胞内活性物质的解析能力也是不同的。图4结果表明55%乙醇溶液浸析后的金银花叶进行绿原酸提取的效果最佳。需要说明的是,提取过程中涉及到的乙醇用量和提取料液比均参考向福等[5]的结果。
2.2 响应面试验结果
响应面试验结果如表2所示。表2中试验编号1~12为析因试验,13~15为中心试验。15个试验点分为零点和析因点,其中析因点为自变量取值在X1、X2、X3所构成的三维顶点,零点为区域的中心点,零点试验重复3次以估计试验误差。
利用Design Expert 8.0.5b对所得表2数据进行多元回归拟合,得到绿原酸得率(Y)对pH (X1)、提取时间(X2)和浸析醇体积分数(X3)的二次多项回归模型方程:
Y=-1.236 7+1.871 0X1+0.077 3X2+ 0.084 2X3+3.352 5×10-4X1X2-6.142 5×10-4X1X2-3.587 2×10-4X2X3-0.195 2X12-1.185 6×10-3X22-5.480 2×10-4X32
表3中的方差分析结果表明,X1、X2、X3、X2X3、X12、X22、X32对Y的响应值均达到显著或极显著水平,因此,尽管X1、X2、X3 3个因子交互作用对响应值Y的影响较小,但各因子与响应值之间不存在简单的线性关系,绿原酸得率同时也受到二次项的影响。就模型分析结果表明,描述各因子与响应值关系的回归模型F为152.79,P<0.000 1,失拟项F为3.37,P>0.1,且预测拟合度和校正拟合度比较一致,说明该试验方法可靠,模型极显著。就相关系数而言,R2=0.996 4,表明回归方程中99.64%的因变量变化可以由其自变量的变化进行解释,也就是说在该工艺中,未计入回归方程的变量对金银花叶中绿原酸的提取效果影响较小。因此,可用该模型对金银花叶中绿原酸醇浸水提工艺过程进行分析和预测。
图5、图6和图7是根据多元回归方程所生成的响应面及其等高线,比较直观地反映了各因子以及各因子之间的交互作用。各图表示提取时间、pH、浸析醇体积分数这3个因子中任意一个变量取零水平时,其余两个变量对绿原酸得率的影响。从图5~图7可知,就各个因子而言,pH对绿原酸得率的影响最为显著,表现为曲线较陡,而提取时间与浸析醇体积分数次之,表现为曲线较为平滑,且随其数值的增加或减少,响应值变化较小;就交互影响而言,X1X2之间交互作用较为明显(图5中等高线中心呈椭圆状),X1X3、X2X3之间交互作用不明显。3个响应面均为凸面,开口向下,提取时间、pH、浸析乙醇体积分数3个因子与绿原酸得率基本呈抛物线关系,在试验范围内存在最大值。模型预测的最佳提取工艺条件为:pH 4.71,时间23.4 min,乙醇体积分数65%,在此条件下,绿原酸得率可达6.863 7%。
2.3 响应面验证试验
验证时考虑实际操作问题,将最佳条件修正为:pH 4.5、提取时间25 min、浸析乙醇体积分数65%。在浸析12 h、液料体积质量比20∶1以及沸水条件下,利用修正后的最佳条件从金银花叶中用醇浸水提法提取绿原酸,进行了3次平行验证试验,绿原酸实测平均得率为6.856%,与理论预测值吻合度较高。
3 结论
醇浸水提工艺中pH、提取时间和浸析乙醇体积分数对金银花叶中绿原酸的提取影响极显著;在浸析12 h,液料体积质量比20∶1以及沸水条件下提取金银花叶绿原酸的最佳工艺为:pH 4.5、提取时间25 min、浸析乙醇体积分数65%,该条件下绿原酸的得率可达6.856%。该工艺合理可行,可用于工业化生产。
参考文献:
[1] 王 辉,田呈瑞,马守磊,等.绿原酸的研究进展[J].食品工业科技,2009,30(5):341-345.
[2] 单 磊,达超超,呼延晓颖,等.金银花中绿原酸提取工艺研究[J].试验报告与理论研究,2010,13(4):23-25.
[3] 向 福,郭文韬,袁 婷,等.罗田县两种金银花中绿原酸含量的比较[J].黄冈师范学院学报,2013,33(3):36-37.
[4] VOHRA A, SATYANARAYANA T. Statistical optimization of the medium components by response surface methodology to enhance phytase production by Pichia anomala[J]. Process Biochem, 2002,37(9):999-1004.
[5] 向 福,刘 亮,秦 婷,等.罗田金银花叶中绿原酸的提取工艺改进[J].食品与机械,2013,29(6):150-152.
