甲醇随车制氢催化剂Cu-SiO2的制备及性能评价
2015-09-03庆绍军侯晓宁郗宏娟高志贤
庆绍军,侯晓宁,郗宏娟,高志贤
(中国科学院山西煤炭化学研究所,太原 030001)
甲醇随车制氢催化剂Cu-SiO2的制备及性能评价
庆绍军,侯晓宁,郗宏娟,高志贤
(中国科学院山西煤炭化学研究所,太原 030001)
以Cu(NO3)2和水玻璃为原料,采用共沉淀法制备了Cu-SiO2催化剂。在连续流动固定床装置上对Cu-SiO2催化甲醇裂解反应性能进行考察,同时考察反应温度、空速对Cu-SiO2催化性能的影响规律。结果表明:Cu-SiO2催化剂在使用前无需采用H2进行预还原处理,对甲醇裂解反应表现出优异的催化性能,且具有较好的再生性能;在300 ℃、质量空速0.79 h-1、常压的条件下,随反应时间的延长,甲醇转化率由初始的75.8%增加至48 h 时的85.6%,并在144 h内甲醇转化率保持在85%左右,产物以H2和CO为主,并含少量的甲酸甲酯和其它产物;反应温度和空速对催化剂活性影响较大,但对产物分布影响较小;Cu-SiO2催化剂上甲醇转化产物为富氢气体,催化活性稳定,表明催化剂对甲醇随车制氢具有较好的适用性。
甲醇 Cu-SiO2富氢气体 随车制氢
进入21世纪后,能源和环境成为人类社会面临的重要问题,这两大问题已成为制约各国经济持续发展的重要因素,因此,开发新能源、减少环境污染引起了越来越广泛的重视,已成为当前研究的热点。汽车尾气带来的污染约占整个大气污染的42%[1],因此开发清洁替代燃料、实现节能减排具有重要意义。在所有开发的替代燃料中,甲醇具有极大的竞争优势。甲醇是一种来源广泛的化工原料,可以从煤炭、石油、生物中得到,每年的产量较大,便于储备和运输,能量转换效率高,是H2和CO的良好载体,被认为是未来最有希望的高携能绿色燃料[2]。近几十年来,甲醇作为汽车的替代燃料一直是个热门课题,甲醇直接作为燃料使用的效果并不理想,主要是由于其单位体积的热值低,汽化潜热大,制动效率低[3]。如果利用尾气的余热将甲醇随车转化成富氢气体再作为发动机的燃料,则可大大提高发动机的热效率,降低尾气中NOx,HC,CO等的排放量。据研究报道[4-5],甲醇裂解产物的热效率比汽油的热效率高约60%,比甲醇的热效率高约34%,因此使用甲醇裂解产物在节能的同时可降低污染物排放,CO和CH4的排放量减少90%,NOx的排放量减少40%。甲醇随车制氢的核心在于催化剂,对催化剂具有更高的要求:①汽车尾气的余热温度较高,且不稳定,因此催化剂需耐高温及温度波动;②稳定的产物分布有利于发动机的稳定运转;③汽车在行驶过程中,震动较大,因此催化剂应具有较高的强度[6]。现有工业化催化剂均不能满足车载要求。应用于甲醇裂解或重整的催化剂包括贵金属催化剂(如Pd,Pt,Rh)和非贵金属催化剂(如Cu,Ni,Zn,Cr),贵金属催化剂具有较好的催化活性和高温稳定性[7-8],但由于成本高而受到限制;非贵金属催化剂中,镍系催化剂具有较好的稳定性,但高温和低温下产物差别较大[9-10],而Cu系催化剂对甲醇裂解表现出较好的催化性能,且其价格便宜、制备容易。早期用于甲醇裂解的Cu基催化剂以Cu-ZnO[11]、Cu-Cr[12]等研究较多。随后逐步发展为担载型催化剂,其中以CuSiO2的研究较多,制备方法包括浸渍法[13]、离子交换法[14]等,但反应过程中催化剂的失活现象比较明显。本课题选用Cu基催化剂作为研究对象,以廉价的水玻璃为硅源,通过共沉淀法合成Cu-SiO2催化剂,初步探索其对甲醇裂解的催化性能,为开发廉价的、适用于甲醇随车制氢的催化剂提供可参考的基础数据。
1 实 验
1.1 催化剂
配制一定浓度的Cu(NO3)2·3H2O(工业品)溶液,在80 ℃水浴加热、搅拌下,以一定的速率滴加至水玻璃溶液中,经沉淀、老化、洗涤后,在120 ℃下干燥,研磨过筛(200目),加3%的石墨,打片成型,破碎,取10~14目样品用于评价。所得Cu-SiO2催化剂中铜质量分数为33.6%。
1.2 催化剂表征
程序升温还原(H2-TPR)表征在FINESORB-3010C多功能吸脱附仪上进行,还原气体使用10% H2Ar混合气,流速为10 mLmin,热导池检测器。样品先在空气气氛、500 ℃下焙烧30 min,随后切换为Ar降温,当温度低于50 ℃时,开始还原,以10 ℃min升温至400 ℃。
X射线衍射分析(XRD)表征在日本Rigaku MiniFlexⅡX射线衍射仪上进行,Cu Kα靶,工作电压30 kV,工作电流15 mA,2θ为10°~80°,扫描速率为5(°)min。
1.3 甲醇裂解性能评价
甲醇裂解性能评价在10 mL连续流动固定床装置上进行,催化剂装量为5 mL,以工业精甲醇为原料,使用SZB-2双柱塞微量泵进料。催化剂评价前先于空气气氛下(30 mLmin)以3 ℃min的速率升温至500 ℃,处理3 h,随后降温至反应温度,用N2吹扫30 min后开始进料。评价条件:反应温度280~400 ℃、压力0.1 MPa、质量空速0.53~2.37 h-1。反应产物经冷凝后取气体样品和液体样品,用2台分别配有Porapak T柱、TDX-01柱及热导池检测器的气相色谱仪进行分析,计算甲醇转化率以及产物分布。
2 Cu-SiO2催化剂的表征
2.1 H2-TPR表征
Cu-SiO2催化剂的H2-TPR表征结果见图1。由图1可见:Cu-SiO2催化剂的起始还原温度为150 ℃,还原峰温为286 ℃;在同样的条件下,分析纯CuO的还原峰温度为369 ℃。据相关文献报道,纯CuO的还原峰温度约为370 ℃[15-16]。说明Cu-SiO2催化剂中载体SiO2对CuO起到了较好的分散作用,从而使催化剂中CuO变得更易被还原。

图1 Cu-SiO2催化剂的H2-TPR曲线

图2 Cu-SiO2催化剂的XRD图谱▲—SiO2
2.2 XRD表征
Cu-SiO2催化剂焙烧前后样品的XRD谱见图2。由图2可见,焙烧前后样品只在2θ为22°左右有一个弥散的衍射峰。根据文献可知该衍射峰为无定型SiO2的特征峰[17]。XRD谱中未出现铜物种衍射峰,表明催化剂中铜粒子较小或以无定形形式存在,这与H2-TPR表征结果一致。
3 Cu-SiO2催化剂的性能评价
3.1 Cu-SiO2的催化甲醇裂解性能
在300 ℃、质量空速0.79 h-1、常压的条件下,甲醇在Cu-SiO2催化剂上的转化率及产物分布见图3。由图3可见,随反应时间的延长,甲醇转化率由初始的75.8%增加至48 h时的85.6%,并在144 h内甲醇转化率保持在85%左右。在Cu-SiO2催化剂上甲醇转化的产物包括H2、CO、甲酸甲酯(MF)、CH4、H2O、CO2,其中以H2和CO为主,二者的摩尔分数之和在97%以上。在初始反应的48 h内,随反应的进行,甲醇转化产物中H2和MF含量减少,CO含量增加,但变化幅度较小。
由于催化剂在使用前未进行H2预还原处理,催化剂中铜以氧化态的形式存在,当甲醇接触催化剂后开始反应,产生的H2对催化剂进行缓慢还原,从而出现了反应初期甲醇转化率逐渐增加的过程。有关甲醇裂解的文献均表明[18-19],所使用的铜基催化剂在使用前均需进行H2预还原处理,而本研究制备的Cu-SiO2催化剂在使用前无需进行H2预还原处理,这就简化了催化剂的预处理过程,降低了应用成本,且对甲醇随车制氢系统具有更好的适用性。
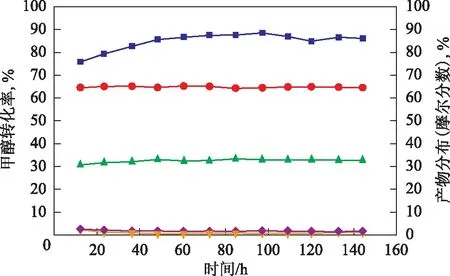
图3 甲醇在Cu-SiO2催化剂上的转化率及产物分布■—甲醇转化率; ●—H2; ▲—CO; ◆—MF; 其它产物(CH4,H2O,CO2)。 图4~图6同
3.2 工艺条件的考察
在上述实验结束后(催化剂已连续运转144 h),保持催化剂的状态不变,考察空速、反应温度等工艺条件对甲醇裂解反应的影响。
3.2.1 空速的影响 在300 ℃、常压的条件下,空速对Cu-SiO2催化甲醇裂解性能的影响见图4。由图4可见,在质量空速为0.53~2.37 h-1的范围内,随空速的增加,甲醇转化率先降低然后经历一个稳定的平台后继续降低;在质量空速由0.53增大到1.32 h-1时,产物分布变化较小,但当空速继续增大时,H2、MF以及其它产物的含量略有增加,CO含量略有减少。表明空速的增加有利于MF的生成。总体来说,空速的变化对产物分布影响不大,比较适用于车载,因为在行车过程中,车速有快有慢(即相当于空速在不断变化),为了保证发动机燃烧稳定,稳定的产物分布是有利的。
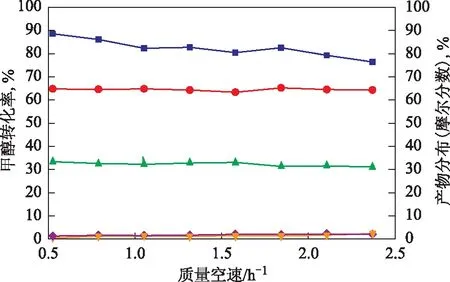
图4 空速对Cu-SiO2催化甲醇裂解性能的影响
3.2.2 温度的影响 在质量空速0.79 h-1、常压的条件下,反应温度对Cu-SiO2催化甲醇裂解性能的影响见图5。由图5可见,随着温度的升高,甲醇转化率先增加,在320 ℃时达到最高,此时甲醇转化率为98.06%,随后开始下降,400 ℃时甲醇转化率为76.73%。在280~400 ℃,随温度的升高,甲醇裂解产物分布变化较小。甲醇随车制氢反应的温度来自于汽车尾气,而尾气的温度较高且波动较大,因此,要求催化剂耐高温且耐温度的波动,在温度的波动过程中,要保证甲醇转化产物的稳定以确保发动机稳定运转。本研究开发的Cu-SiO2催化剂应用在车载系统上具有较大的优势。
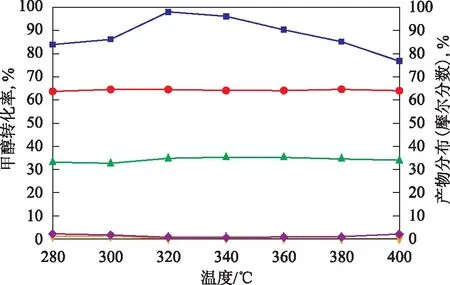
图5 反应温度对Cu-SiO2催化甲醇裂解性能的影响
3.3 Cu-SiO2催化剂的再生性能

图6 Cu-SiO2再生催化剂的甲醇裂解催化性能
由上述研究可知,当温度超过320 ℃后,随温度的升高,催化剂活性下降,可能是生成了积炭,也有可能是铜烧结,因此,对催化剂进行了再生处理。在300 ℃、质量空速0.79 h-1、常压的条件下,再生催化剂的甲醇裂解催化性能评价结果见图6。由图6可见,与新鲜催化剂(图3)相比,催化剂经再生后,活性完全恢复。表明催化剂活性下降后可通过再生处理恢复,由此推测高温导致催化剂失活的主要原因是积炭。再生催化剂与新鲜催化剂的不同之处在于初始阶段未出现甲醇转化率增加以及MF和其它副产物减少的情况。
4 结 论
(1) 以廉价的水玻璃作为硅源,采用共沉淀法制备了对甲醇裂解具有较好催化性能的Cu-SiO2催化剂,该催化剂在使用前无需用H2进行预还原处理,且反应温度和空速对产物分布的影响较小,表明该催化剂对甲醇随车制氢系统具有较好的适用性。
(2) H2-TPR和XRD表征结果表明Cu-SiO2催化剂中铜物种的分散较好。
(3) Cu-SiO2催化剂经再生后,活性可完全恢复,推测高温导致催化剂失活的主要原因是积炭。
[1] 孙康波,王保民.甲醇裂解催化剂的现状及发展[J].科技情报开发与经济,2005,15(13):148-149
[2] 王立奎.甲醇低温裂解催化剂的研究进展[J].浙江工贸职业技术学院学报,2009,9(1):35-39
[3] 彭必先,甘昌胜,闫天堂.非贵金属在甲醇裂解中的应用研究进展[J].化学世界,2004,(6):324-328
[4] 黄朝蔚,董新法.车用甲醇燃料裂解催化剂及其研究概况[J].工业催化,2007,15(2):6-11
[5] Cheng Wu-Hsun.Development of methanol decomposition catalysts for production of H2and CO[J].Acc Chem Res,1999,32:685-691
[6] Johnny W,Leif A K.Catalyst for conversion of methanol:The United States,US4631266[P].1986-12-23
[7] Shen Wenjie,Matsumura Y.Low-temperature methanol decomposition to carbon monoxide and hydrogen catalysed over cationic palladium species in PdCeO2[J].Phys Chem Chem Phys,2000,2(7):1519-1522
[8] Imamuraa S,Higashiharaa T,Saito Y,et al.Decomposition of methanol on Pt-loaded ceria[J].Catalysis Today,1999,50(2):369-380
[9] 席靖宇,吕功煊.NiCuZnO催化剂的甲醇裂解制氢研究[J].分子催化,2001,15(3):191-195
[10]Matsumura Y,Tanaka K,Tode N,et al.Catalytic methanol decomposition to carbon monoxide and hydrogen over nickel supported on silica[J].Journal of Molecular Catalysis A:Chemical,2000,152(12):157-165
[11]Xi Jingyu,Wang Zhifei,Lu Gongxuan.Improvement of CuZn-based catalysts by nickel additive in methanol decomposition[J].Applied Catalysis A:General,2002,225(12):77-86
[12]Cheng Wu-Hsun,Shiau Ching-Yeh,Liu Tzu-Hsieh,et al.Promotion of CuCrMn catalyst by alkali additives in methanol decomposition[J].Applied Catalysis A:General,1998,170(2):215-224
[13]David S J,David S A,Gordon J K,et al.Methanol decomposition over coppersilica:Effect of temperature and co-reactant on carbon deposition[J].Topics in Catalysis,2003,22(34):173-182
[14]Dean B C,Lee Dong-Keun,Mark J S,et al.Infrared studies of the mechanism of methanol decomposition on CuSiO2[J].Journal of Catalysis,1994,150:81-93
[15]周仁贤,蒋晓原,吕光烈,等.CuO在ZrO2上的分散状态及其对催化性能的影响[J].高等学校化学学报,1997,18(11):1854-1857
[16]Shimokawabe M H,Asakawa N T.Characterization of copperzirconia catalysts prepared by an impregnation method[J].Applied Catalysis,1990,59(1):45-58
[17]陈梁锋,朱渊,刘晓钰,等.CuSiO2催化剂制备方法对其草酸二甲酯催化氢解性能的影响[J].化学学报,2009,67(23):2739-2744
[18]张雄伟,储伟,王立楠,等.CeO2对甲醇裂解用Cu-Ir双金属催化剂的影响[J].中国稀土学报,2004,22(Z2):89-92
[19]Cheng W H.Reaction and XRD studies on Cu based methanol decomposition catalysts—Role of constituents and development of high-activity multicomponent catalysts[J].Applied Catalysis A:General,1995,130(1):13-30
PREPARATION AND PERFORMANCE OF Cu-SiO2CATALYST FOR H2PRODUCTION FROM METHANOL ON VEHICLE
Qing Shaojun, Hou Xiaoning, Xi Hongjuan, Gao Zhixian
(InstituteofCoalChemistry,ChineseAcademyofSciences,Taiyuan030001)
Using copper nitrate and sodium water glass as materials, the Cu-SiO2catalyst was prepared by co-precipitation method. The performance of Cu-SiO2for methanol decomposition was studied in a fixed down-flow reactor. The influence of reaction temperature and WHSV were investigated. The evaluation results show that the Cu-SiO2without pre-reduction by H2gives a high catalytic activity for methanol decomposition, and exhibits a good regeneration property. At 300 ℃, WHSV of 0.79 h-1and atmospheric pressure, the conversion of methanol increases from initial 75.8% to 85.6% at 48 h, and then remains at about 85% within 144 h. The main products are hydrogen and carbon monoxide. A few of methyl formate and other products are also found. The influence of the temperature and WHSV on the activity of the catalyst is significant, but small on the products distribution. The test results indicate that the catalyst (Cu-SiO2) has a good applicability for the hydrogen production from the methanol on vehicle.
methanol; Cu-SiO2; hydrogen-rich gas; H2production on vehicle
2014-06-30; 修改稿收到日期: 2014-09-22。
庆绍军,硕士,助理研究员,主要从事甲醇替代燃料的研究工作。
高志贤,E-mail:gaozx@sxicc.ac.cn。
