农业活动干扰下地下水无机碳循环过程研究
2015-08-25刘丛强汪福顺赵志琦河南理工大学资源环境学院河南焦作454000中国科学院地球化学研究所环境地球化学国家重点实验室贵州贵阳55000上海大学环境与化学工程学院上海宝山004
张 东,刘丛强,汪福顺,赵志琦(1.河南理工大学资源环境学院,河南 焦作 454000;.中国科学院地球化学研究所环境地球化学国家重点实验室,贵州 贵阳 55000;.上海大学环境与化学工程学院,上海 宝山 004)
农业活动干扰下地下水无机碳循环过程研究
张 东1,2*,刘丛强2,汪福顺3,赵志琦2(1.河南理工大学资源环境学院,河南 焦作 454000;2.中国科学院地球化学研究所环境地球化学国家重点实验室,贵州 贵阳 550002;3.上海大学环境与化学工程学院,上海 宝山 200433)
为准确识别浅层地下水污染来源及污染过程,选择我国北方某集约化蔬菜种植基地浅层地下水作为研究对象,借助水化学组成、氢氧同位素以及溶解性无机碳(DIC)碳同位素组成,探讨浅层地下水来源以及 DIC来源和迁移转化特征.结果表明:浅层地下水阳离子以Ca2+和Mg2+为主,阴离子以和为主,沿地下水流向,水化学类型由型转变为型;浅层地下水δD组成范围为-69.6‰~-52.7‰,均值为-63.5‰,δ18O组成范围为-9.29‰~-6.80‰,均值为-8.45‰.大气降水是浅层地下水重要补给来源,靠近河水的浅层地下水还接受地表水的补给;浅层地下水δ13CDIC组成范围为-11.76‰~-5.85‰,均值为-10.43‰.浅层地下水DIC来源包括土壤CO2、碳酸盐矿物以及有机质分解.河水DIC侧渗对局部浅层地下水DIC碳同位素造成影响,化学肥料引起的酸性物质参与碳酸盐矿物风化作用以及浅层地下水CO2去气作用对地下水δ13CDIC组成产生影响,在利用DIC碳同位素识别地下水污染来源时需要引起重视.
农业活动;浅层地下水;溶解性无机碳碳同位素;酸化;CO2去气作用
农业活动大量使用化肥和人畜粪肥是浅层地下水污染的重要原因[1-5].地下水硝酸盐因其易被还原为亚硝酸盐,导致婴儿高铁血红蛋白病、肝癌、胃癌及高血压等疾病而倍受关注[3,5-9].我国北方集约化蔬菜基地浅层地下水硝酸盐污染与化学肥料、粪肥和生活污水等关系密切[5,7,10-11].研究地下水污染,一种方法是通过长期地下水水质观测,并结合不同土地利用类型控制下的地下水硝酸盐浓度变化特征来说明地下水潜在污染来源及发生过程[7].一种方法是利用稳定同位素技术示踪地下水污染,如李玉中等[5]采用硝酸盐氮同位素技术研究山东省农村地区地下水硝酸盐污染来源,并计算出不同污染源的贡献比例;李思亮等[12]利用 DIC碳同位素对贵阳城区地下水污染进行研究,结合地下水硝酸盐含量,识别出贵阳市不同地区地下水污染源;刘小龙等[13]结合 DIC碳同位素和锶同位素对六盘水地下水污染进行研究,发现城镇居民区生活污水和农田区化肥肥料、粪肥等是地下水污染重要来源.
DIC碳同位素广泛应用于地表水和地下水碳循环研究[12-19],不同类型水体 DIC来源包括:大气 CO2;根呼吸以及有机质降解产生的生物成因CO2;碳酸盐矿物溶解[20].农业活动对地下水无机碳循环的影响主要表现两个方面:农业活动大量施用人畜粪肥等有机肥是农业区地下水无机碳重要来源.这些有机肥料往往由偏负的碳同位素组成,进入浅层地下水降解后产生CO2碳同位素值也偏负,导致地下水 DIC碳同位素值偏负;农业活动含氮肥料铵化产酸参与地下水环境中碳酸盐岩化学风化改变无机碳同位素组成.农业活动施用大量化学肥料,特别是铵肥,会导致浅层地下水酸化[20-21],反应方程如下:

酸化的结果导致碳酸盐矿物溶解,造成碳同位素组成偏正的 DIC进入浅层地下水,从而改变浅层地下水 DIC碳同位素组成,这一过程在以往的研究中并未受到重视,给利用 DIC碳同位素示踪浅层地下水污染造成一定的干扰.因此如果能准确识别这一过程,有助于更好地利用 DIC碳同位素示踪浅层地下水污染,同时更好地说明农业活动对地下水环境中碳循环的影响过程.
目前我国利用DIC碳同位素辨识农业活动干扰下的浅层地下水DIC的来源及转化过程的研究不多,本研究选择我国北方集约化蔬菜基地地下水作为研究对象,结合水化学组成、氢氧同位素以及DIC碳同位素,探讨农业活动对地下水水化学组成特征的影响以及产酸机制等对地下水无机碳碳循环的影响过程.
1 材料与方法
1.1研究区概况
研究区位于河南省博爱县孝敬镇,是博爱县大地蔬菜种植集中区,不同季节蔬菜种植种类众多.研究区紧邻丹河和沁河,浅层地下水分为2个含水层,上部潜水含水层埋深10m左右,岩性一般为上更新统合全新统中细砂;下部为微承压水,含水层埋深 20~30m,岩性一般为中更新统冲洪积砂砾石,中粗砂和中细砂[22].区内地下水流向为北西-南东向.浅层地下水主要接受大气降水、河渠渗漏、侧向地下水迳流以及农灌水回渗补给[22],大气降水主要集中在7~9月份,占全年降水量的 67.8%,年均降水量最小为 314.40mm,最大为798.30mm[23].
1.2研究方法
区内大地蔬菜种植季节性明显,5月份为是蔬菜生长高峰期,期间使用大量化学肥料和人畜粪肥,灌溉频繁,地下水受污染可能性较大,有利更好地研究区内地下水无机碳碳循环的影响和控制因素.区内长期农业灌溉已经导致上部潜水含水层基本疏干,本次地下水样品主要取自下部微承压含水层,井深在30~40m左右.2013年5月采集研究区浅层地下水样品22个,地表水样品5个,采样布点见图 1.浅层地下水主要取自蔬菜基地正在灌溉的农灌井,现场测定水温、pH值、EC 和DO值.水样24h内用0.45μm混合纤维滤膜过滤,阴离子样品不加任何保护剂,阳离子样品加入1滴超纯硝酸(pH<2),置于 4℃冰箱保存待测.采用盐酸滴定法测定,阳离子采用原子吸收光谱仪(Z5000, Hitachi)测定,阴离子采用离子色谱仪(ICS3000, Dionex)测定,测试精度均优于5%.溶解性无机碳样品过滤后,加入2滴饱和氯化汞溶液密封保存,实验室用 Gasbench IIIRMS(Thermo Fisher)测定碳同位素,Gasbench II前处理装置包括:GC-PAL自动进样器, PoraPlot Q色谱柱;恒温样品盘(控制温度±0.1℃),IRMS为MAT-253(Thermo Fisher Scientific),碳同位素测试以V-PDB为标准计算δ13C值,测试精度优于0.06‰[24].水的氢氧同位素样品过滤后,置于10ml玻璃瓶密封保存,不留空隙,实验室用 Flash 2000HT-IRMS(Thermo Fisher)测定氢氧同位素,配备ConFlo IV连续流动模式同位素质谱仪万用接口,AS3000液体样品自动进样器[25],高温裂解温度为1380℃,IRMS为MAT-253,水的氢氧同位素测试以VSMOW为标准计算δD和δ18O值,测试精度分别优于2‰和0.2‰.上述测试均在河南理工大学生物遗迹与成矿过程省级重点实验室完成.
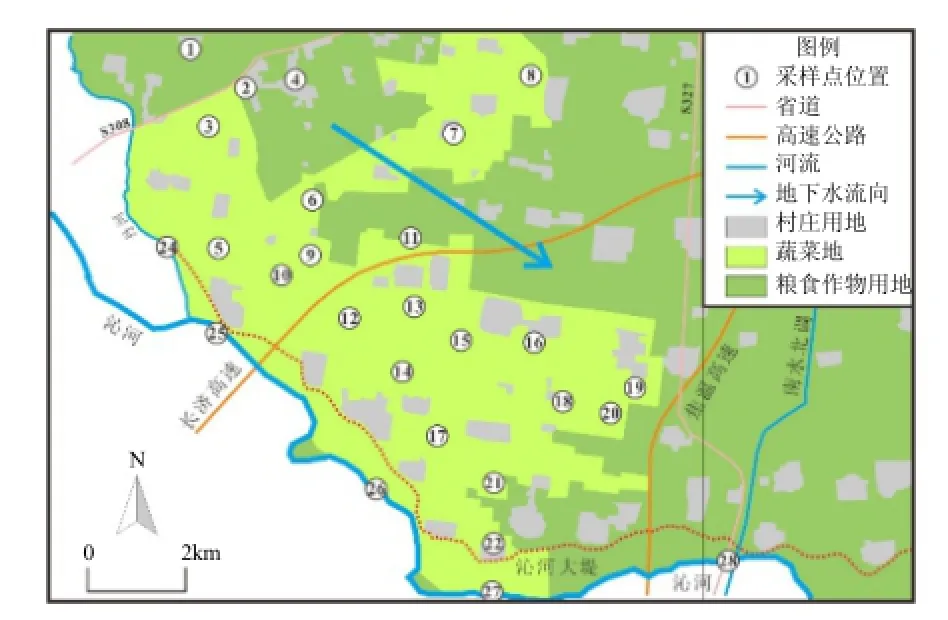
图1 研究区土地利用及采样布点Fig.1 Land use and sampling sites in studied area
根据现场测定的水体pH值和T值,以及室内测试得出的Ca2+、Mg2+、K+、Na+、SO42-、和Cl-的浓度值,借助Visual MINTEQ 3.0软件分别计算水体中方解石和白云石饱和指数以及水体 PCO2值.研究区浅层地下水氢氧同位素、DIC碳同位素以及硝酸盐含量的等值线图借助Surfer 12.0软件绘制,采用的计算方法为克里格(Kriging)法.
2 研究结果
2.1研究区水体主要化学组成特征
研究区浅层地下水pH值范围为6.90~7.68,水温变化范围为 16.2~19.1℃,EC值变化范围为628~1996μS/cm,DO值变 化 范 围 为2.01~6.59mg/L(表1).
总的阳离子当量浓度范围为6.83~19.66meq/L,均值为13.17meq/L.阳离子以Ca2+和Mg2+为主,其中Ca2+浓度范围为1177~4505μmol/L,均值为 2936μmol/L,Mg2+浓度范围为 1423~4414μmol/L,均值为 2891μmol/L, K+浓度范围为18~136μmol/L,均值为60μmol/L,Na+浓度范围为656~2522μmol/L,均值为1456μmol/L.
总的阴离子当量浓度范围为7.56~ 21.84meq/L,均值为14.39meq/L.阴离子以和为主,其中浓度范围为5228~9599μmol/L,均值为 7099μmol/L,浓度范围为 548~4078μmol/L,均值为 2166μmol/L,Cl-浓度范 围为247~2224μmol/L,均值为1322μmol/L ,浓度范围为 333~5571μmol/L,均值为1636μmol/L (表1).沿地下水流动方向,浅层地下水水化学类型由转变为,水化学类型分布规律与附近济源盆地水化学类型分布规律一致[26].
沿地下水流动方向,研究区浅层地下水 pH值逐渐增加(图2a),EC值在12号点附近出现高值,下游浅层地下水EC逐渐降低(图2b),NO3-值与EC值变化趋势接近(图2c).
研究区地表水pH值范围为7.64~8.68,水温变化范围为19.6~24.1℃,EC值变化范围为1008~1192μS/cm,DO 值变化范围为 3.10~10.89mg/L(表 1).总的阳离子当量浓度范围为 11.95~13.45meq/L,阳离子以Ca2+和Mg2+为主,总的阴离子当量浓度范围为 13.08~14.41meq/L,阴离子以和为主.丹河 (24号点)水化学类型为型,沁河水化学类型均为Mg2+-Ca2+.

图2 研究区浅层地下水pH值(a)、EC值(b)和NO3-浓度(c)空间变化Fig.2 Spatial variations of pH values (a), EC values (b) and nitrate concentrations (c) of local shallow groundwater
2.2研究区水体同位素组成特征
研究区浅层地下水δD组成范围为-69.6‰~-52.7‰,均值为-63.5‰,δ18O组成范围为-9.29‰~-6.80‰,均值为-8.45‰,δ13CDIC组成范围为-11.76‰~-5.85‰,均值为-10.43‰.
研究区浅层地下水氢氧同位素空间分布基本一致(图3a,3b),沿地下水流动方向,浅层地下水δD和δ18O值逐渐偏负,与沁河距离越近,浅层地下水δD和δ18O值越正(图3a,3b).研究区浅层地下水氘盈余(d=δD-8δ18O)值范围为 1.56‰~8.61‰,均值为4.11‰(表1),空间变化与氢氧同位素空间变化相反,氢氧同位素组成偏正的区域 d盈余值偏负,反之,氢氧同位素组成偏负的区域,d盈余值偏正(图 3c),说明浅层地下水氢氧同位素偏正的区域,受到蒸发作用影响或者受蒸发影响的河水补给作用的影响.

图3 研究区浅层地下水δD(a)、δ18O值(b)和氘盈余(c)空间变化Fig.3 Spatial variations of δD (a), δ18O (b) and d-excess (c) of local shallow groundwater

图4 研究区浅层地下水DIC值(a)、δ13CDIC值(b)和PCO2(c)空间变化Fig.4 Spatial variations of DIC values (a), δ13CDICvalues (b) and PCO2(c) of local shallow groundwater
研究区浅层地下水DIC浓度高值区集中在16号和18号点,上游1号点DIC浓度也较高(图4a).δ13CDIC值沿着地下水流动方向逐渐偏正(图4b),靠近沁河,浅层地下水δ13CDIC值偏正,形成以17号点和16点为中心的高值区,再往下游,浅层地下水δ13CDIC值偏负(图4b).浅层地下水PCO2值沿地下水流动方向逐渐降低,16号和17号点PCO2也较高(图4c).
研究区地表水 δD 组成范围为-74.8‰~-53.5‰,均值为-59.3‰,δ18O组成范围为-9.93‰~-5.37‰,均值为-7.26‰,δ13CDIC组成范围为-8.98‰~-5.88‰,均值为-7.26‰(表1).

表1 研究区地下水和地表水水化学及稳定同位素组成Table 1 Chemical and isotopic compositions for local ground water and river water samples
3 讨论
3.1研究区浅层地下水溶解组分来源
控制浅层地下水水化学组成的因素包括物质来源和反应过程[27-28],研究区浅层地下水溶解组分来源包括矿物岩石溶解、大气干湿沉降以及人为输入,可能产生的化学反应包括溶解沉淀、氧化还原、阳离子交换以及生物作用等[28].
3.1.1水-岩作用 水-岩作用是控制地下水水体水化学组成的重要因素,不同类型岩石中矿物溶解产物的离子摩尔比是不同的.碳酸盐矿物溶解产物Ca2+/Na+、Mg2+/Na+和物质的量比分别为50、10和120[29],硅酸盐矿物溶解产生Ca2+/Na+、Mg2+/Na+和物质的量比分别为0.35±0.15、0.24±0.12和2±1[29-30],蒸发盐矿物溶解产生的 Ca2+/Na+、Mg2+/Na+和物质的量比分别为 0.17±0.09、0.02±0.01和 0.3±0.3[30].研究区地下水和地表水不同离子物质的量比值位于碳酸盐矿物溶解和硅酸盐矿物溶解之间(图 5a,5b),说明研究区水-岩作用主要以碳酸盐矿物和硅酸盐矿物溶解为主,蒸发盐溶解对水体水化学组成的影响不大.

图5 研究区地下水和地表水离子摩尔浓度比值关系Fig.5 The plots of ion ratios of local groundwater and river water samples
3.1.2人为输入 研究区人类活动对浅层地下水水化学组成影响较大浓度范围为333μmol/L~5571μmol/L,均值为 1636μmol/L,其中超过世界卫生组织标准(=45mg/L, 726μmol/L)的样品比例为77.3%(表1).该研究结果与山东省惠民县蔬菜大棚区浅层地下水硝酸盐浓度均值 (1961μmol/L)[3]和山东寿光市集约化蔬菜种植区地下水硝酸盐平均含量(1640μmol/L)[1]接近,高于北京市集约化农区地下水硝酸盐平均含量(460μmol/L)[7]、巢湖流域地下水硝酸盐平均含量(946μmol/L)[31]以及滇池流域地下水硝酸盐平均含量(434μmol/L)[6],说明蔬菜种植区长期人为活动对地下水影响更大,硝酸盐含量更高.研究区地下水Cl-与和之间具有较好的相关性(图5c,5d),说明这些离子存在共同来源,结合研究区人为活动情况,化学肥料以及人畜粪肥等的使用可能是导致地下水硝酸盐浓度升高的重要因素.研究区浅层地下水硝酸盐含量高值区集中在研究区中部,如 10号点,12号点,且蔬菜地浅层地下水硝酸盐含量普遍高于粮食作物用地的浅层地下水硝酸盐含量(图 2c),说明蔬菜地化学肥料及人畜粪肥使用量频繁,使用量较大.
3.2研究区地下水和地表水之间的水力联系
焦作地区大气降水直线方程为 δD= 8.032δ18O+12.68[32],研究区地下水和地表水氢氧同位素组成均位于当地大气降水直线下方,说明大气降水是研究区浅层地下水和地表水的主要来源.邻近新乡地区北部山前洪积斜地浅层地下水δ18O均值为-8.54‰,δD均值为-65.5‰[33],与研究区浅层地下水δ18O均值(-8.45‰)和 δD均值(-63.5‰)接近,说明太行山区是研究区浅层地下水的补给区.地表水经历强烈蒸发后,氢氧同位素富集,结合研究区地表水氢氧同位素组成,当地蒸发线方程为 δD=4.661δ18O-25.49.蒸发线与当地大气降水线的交点(δ18O=-11.32‰, δD=-78.3‰)为研究区浅层地下水补给源的年平均降水的氢氧同位素组成(图6a)[34].浅层地下水17号点和22号点与地表水氢氧同位素组成接近(图6a),说明二者存在水力联系,结合浅层地下水氢氧同位素空间分布图(图2a,2b),17号点和22号点距离沁河较近,富集氢氧同位素的河水混入是导致浅层地下水氢氧同位素升高的重要原因.地表水(28号)氢氧同位素组成更接近当地大气降水直线(图6a),与浅层地下水混入有关.
氘盈余“d”主要受空气相对湿度控制[34],蒸发作用越强,氘盈余越偏负.研究区浅层地下水氘盈余值范围为 1.56‰~8.61‰,均值为 4.11‰(表1),地表水氘盈余为-13.21‰~4.66‰,均值为-1.24‰(表 1),地表水氘盈余值偏负与蒸发作用有关.地表水样28号点氘盈余为 4.66‰,与研究区浅层地下水氘盈余均值接近,也说明其混入浅层地下水(图 6b).大气降水以及农田灌溉水在下渗补给浅层地下水的过程中,氘盈余变化很小,但补给过程会发生溶滤作用,大量可溶离子进入地下水,导致浅层地下水 TDS值升高.研究区浅层地下水12号、10号、01号以及05号等TDS值较高(图 6b),NO3-含量均大于2580μmol/L(表1),说明大气降水以及灌溉水等在下渗过程中溶解大量盐类进入浅层地下水(图6b).浅层地下水17号点和22点氘盈余值均较低,但是17号点TDS值较高,除地表水混入外,还与溶滤作用有关,22 点 TDS值较低,氘盈余较低,可能与地表水混入有关.

图6 研究区地下水和地表水氢氧同位素组成及氘盈余与TDS关系Fig.6 The plots of hydrogen and oxygen isotopes and d excess and TDS of local groundwater and river water samples
3.3研究区浅层地下水DIC来源及控制因素
3.3.1研究区浅层地下水DIC来源 地下水中DIC主要包括和,其中由CO2(aq)和H2CO3(aq)组成[35].DIC来源包括大气CO2、土壤CO2、碳酸盐矿物以及人为输入等[36].不同来源的碳同位素组成差异明显:大气CO2碳同位素值为-7‰左右[20];土壤CO2碳同位素与上覆植物种类碳同位素密切相关,C3植物和 C4植物碳同位素均值分别为-27‰和-12.5‰[37];碳酸盐矿物碳同位素值在-2‰~+2‰[38];人为输入主要包括生活污水和工业废水,如西安地区污水 δ13CDIC均值为-14.5‰[19],六盘水地区污水δ13CDIC均值为-12.91‰[13].
CO2进入水体过程中发生的分馏包括:根呼吸产生的土壤CO2受到分子扩散作用影响产生分馏,分馏系数最大为+4.4‰[20],导致土壤CO2碳同位素较植物碳同位素偏正;土壤水中 δ13CDIC值不但与土壤CO2气体碳同位素值有关,而且与土壤水pH值有关.在pH<4时,水中DIC主要以H2CO3形式存在,分馏系数(εH2CO3-CO2)在-1‰左右(10℃)[14,39],pH值在 6.5~8.0时,水中 DIC主要以形式存在,10℃时分馏系数(εHCO3--CO2)为9.3‰[39],25℃时分馏系数(εHCO3--CO2)为 7.7‰[39];开放体系中,当水体PCO2高于周围大气CO2分压时,水中溶解的CO2气体会逸出,导致剩余水体 DIC碳同位素发生变化.Doctor等[16]研究发现,河水PCO2从6倍降至2倍大气CO2压力的过程中,河水中DIC碳同位素富集约+3‰.方解石过饱和发生沉淀,增加水体 CO2量,水体CO2去气作用导致水体PCO2降低,DIC含量降低,剩余河水DIC碳同位素富集约0~3‰[40-41];光合作用,地表水中藻类利用DIC进行光合作用,导致剩余DIC碳同位素值偏正[42].

图7 研究区地下水和地表水δ13CDIC值与和关系及[Ca2++Mg2+]值与和关系Fig.7 The plots of δ13CDIC, δ13CDICvs.[Ca2++Mg2+] vs.and [Ca2++Mg2+] vs.of local groundwater and river water samples
我国北方小麦和玉米轮作地区土壤有机碳同位素值约在-21‰左右[43],研究区种植蔬菜种类较多(以C3植物为主),土壤CO2碳同位素较小麦和玉米轮作地区土壤有机碳碳同位素偏负.李思亮等[12]研究认为南方土壤有机碳以C3植物为主,碳同位素值在-23‰左右.研究区周边夏玉米种植范围广泛,考虑C4植物的影响(约占10%),故研究区土壤有机碳碳同位素值在-22‰左右.我国北方寒武系和奥陶系灰岩中碳同位素范围在-2‰~0‰左右[44-45].
土壤有机碳直接分解产生的土壤 CO2碳同位素与原有机物碳同位素接近,在-22%左右,但土壤 CO2扩散过程会发生富集(+4.4%),故土壤CO2碳同位素值在-17%左右(Line 1,图7).相对封闭的地下水环境中(有限的土壤CO2参与岩石化学风化),土壤 CO2参与硅酸盐矿物风化产生的碳同位素值为-17‰(Line 1,图 7),参与碳酸盐矿物(碳同位素均值为 0‰)风化产生的HCO3-碳同位素值为-8.5‰(Line 3,图 7).相对开放的地下水环境中(无限的土壤CO2进入地下水环境),来自粪肥和生活污水等有机质分解产生的DIC碳同位素值约为-14‰(Line 2,图7).大气CO2溶于地下水产生的碳同位素值为0‰(Line 4,图7),但由于地下水PCO2数倍于大气CO2分压,因此大气CO2对地下水的贡献可以忽略.
3.3.2酸化机制对浅层地下水δ13CDIC值的影响研究区浅层地下水硝酸盐含量较高,与化学肥料过多施入有关.化学肥料中酰胺态氮和铵态氮等最终后被氧化为酸性物质,进入地下水引起地下水酸化[21].酸性物质(如硝酸和硫酸)参与碳酸盐矿物化学风化产生的碳同位素值在0‰左右[46],混入地下水后导致地下水 δ13CDIC值升高,同 时]值 (Line5,图7a)和]值(Line5,图 7b)升高.研究区浅层地下水硝酸盐含量较高的地下水δ13CDIC值也较高,如12号、11号、10号以及5号点等,同时随着]值 和值 增加,[Ca2++Mg2+]含量分别升高(相关系数分别为0.58和0.50,图7c,7d),说明化学肥料带来的酸性物质参与了碳酸盐矿物的风化,产生的HCO3-混入地下水,导致地下水δ13CDIC值升高.
3.3.3CO2去气作用对浅层地下水δ13CDIC值的影响 除了酸化机制引起浅层地下水δ13CDIC值升高外,CO2去气作用也会导致剩余地下水δ13CDIC值升高.研究区浅层地下水 DIC含量升高,PCO2值升高(图8a),δ13CDIC值降低(图8b),说明有机质降解产生CO2对浅层地下水PCO2产生很大影响.研究区浅层地下水方解石饱和指数多数大于0.1(表 1),说明方解石处于过饱和状态,CO2不能被利用来溶解方解石.因此过多的CO2会发生去气作用,图 8a中浅层地下水 1号,10号,16号,17号和18号点均存在这种现象.浅层地下水中转变为 CO2气体溢出,导致剩余水体碳同位素富集 0~3‰[40-41],因此上述浅层地下水δ13CDIC值偏正(图8b).
3.3.4研究区浅层地下水 DIC混入比例 研究区浅层地下水δ13CDIC值范围为-14~-8.5‰ (Lin2 和Line3之间,图7a),除土壤CO2参与碳酸盐矿物风化以及有机质降解两个浅层地下水 DIC重要来源外,河水DIC对部分浅层地下水也有贡献(4.2部分),如17号点和22号点.因此研究区浅层地下水 DIC来源可能主要包括:碳酸盐溶解、有机质降解以及河水DIC.土壤 CO2参与碳酸盐矿物风化产生的DIC碳同位素在-8.5‰左右(产生的DIC含量接近研究区北部山区岩溶地下水 DIC含量3500μmo/L)[47],有机质降解产生的DIC碳同位素在-14‰左右(产生的DIC含量选取研究区浅层地下水DIC含量上限,约10000μmol/L,河水DIC碳同位素值约为-6.5‰(DIC含量均值约4500μmol/L),从图9可以看出,大部分浅层地下水位于上述 3个来源的混合范围内,但是也有一些点不在这些范围内,如浅层地下水 1号,10号,14号,16号,17号以及18号点,这些区域的δ13CDIC主要受到硝酸参与碳酸盐矿物化学风化以及CO2去气作用的影响,导致δ13CDIC值升高.20号点受到有机质降解的影响DIC碳同位素值偏低.
考虑到浅层地下水DIC含量受到河水DIC影响不大,仅局限在 17号点附近,因此采用二元混合模型来估算不同来源对浅层地下水DIC的贡献,混合模型如下[12]:

式中:δ13CDIC为浅层地下水 DIC碳同位素实测值;mCi为第i来源的DIC含量;δ13Ci为第i来源对应的碳同位素值.
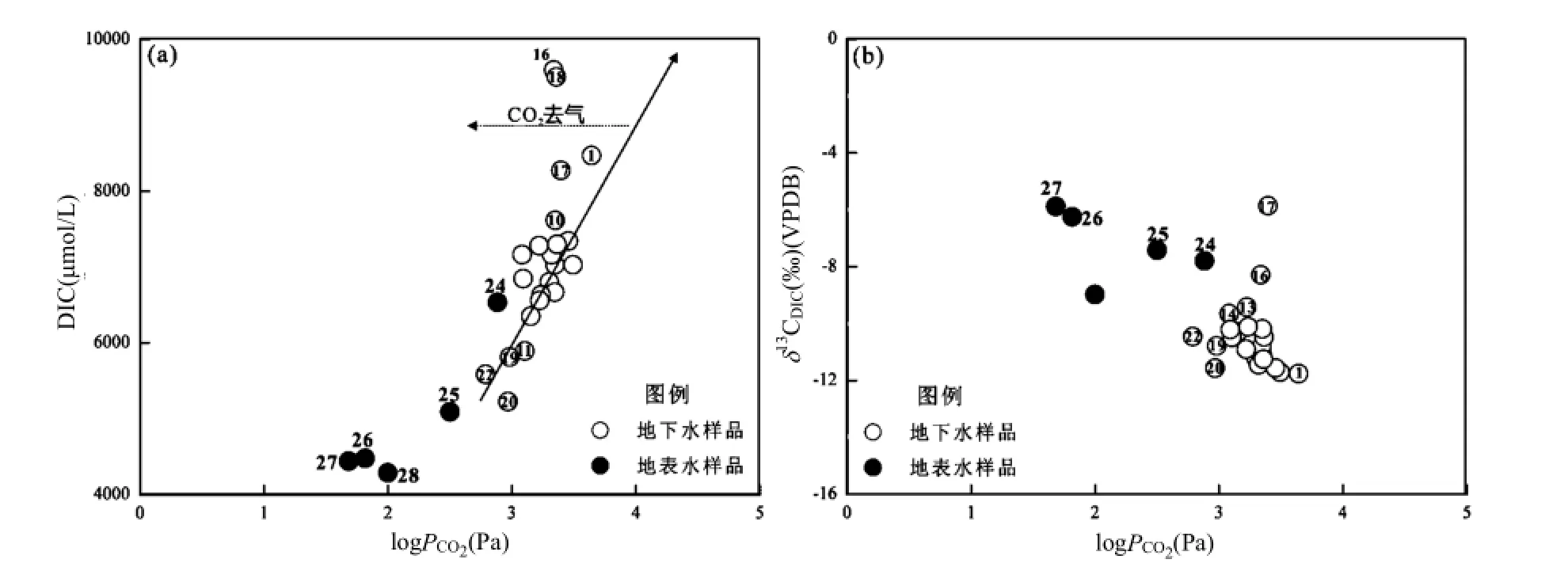
图8 研究区地下水和地表水logPCO2值与DIC值和δ13CDIC值关系Fig.8 The plots of logPCO2vs. δ13CDICand logPCO2vs. DIC of local groundwater and river water samples
根据上述公式,计算得出:来自土壤CO2参与碳酸盐矿物风化的DIC比例范围为 41%~83%,均值为59%,有机质分解产生的DIC比例范围为17%~59%,均值为 41%.浅层地下水 16号点δ13CDIC值为-8.29%,其受到 CO2去气作用影响,δ13CDIC值变化较大,不能再用上述二元混合模型进行计算.

图9 研究区地下水和地表水DIC值和δ13CDIC值关系Fig. 9 The plots of δ13CDICvs. DIC of local groundwater and river water samples
3.4研究区地表水溶解性无机碳来源及影响因素
研究区地表水DIC来源与地下水类似,沁河和丹河上游广泛分布奥陶纪和寒武纪石灰岩[28],因此碳酸盐矿物化学风化是河水DIC重要来源.参与风化的CO2主要来自土壤CO2,大气CO2直接参与碳酸盐风化,贡献很小.因此河水 δ13CDIC值介于-8.5‰~0‰之间.河水 PCO2值较地下水值低,但是方解石饱和指数高于地下水(表 1),CO2去气作用可能发生在地表水环境,导致地表水δ13CDIC值升高(图 8b).同时地表水光合作用往往导致河水 DIC浓度降低,δ13CDIC值升高(Line 6,图 7a,7b),DO含量升高(表 1)[42],因此地表水δ13CDIC值升高与 CO2去气作用和光合作用有密切联系.地表水 28号点由于混入 PCO2值较高但δ13CDIC值较低的地下水,δ13CDIC值有所降低,PCO2有所升高(表1).
4 结论
4.1研究区水-岩作用主要以碳酸盐矿物和硅酸盐矿物溶解为主,蒸发盐溶解对水体水化学组成的影响不大,人为输入的影响主要包括化学肥料以及粪肥等.
4.2研究区浅层地下水主要补给来源为大气降水,地表水和地下水水力联系密切,溶滤作用是控制浅层地下水离子含量的重要因素.
4.3研究区浅层地下水 DIC来源包括土壤CO2、碳酸盐矿物以及人为输入的有机物,其中人为输入有机质对地下水DIC的贡献比例范围为17%~59%,同时化学肥料带来的酸性物质参与碳酸盐矿物风化以及浅层地下水 CO2去气作用是影响地下水DIC碳同位素组成的重要因素.
4.4研究区丹河和沁河地表水DIC来源包括大气CO2、土壤CO2和碳酸盐矿物.CO2去气作用和水体光合作用是控制河水DIC碳同位素的重要因素.
[1] 董章杭,李 季,孙丽梅.集约化蔬菜种植区化肥施用对地下水硝酸盐污染影响的研究—以“中国蔬菜之乡”山东省寿光市为例 [J]. 农业环境科学学报, 2005,24(6):1139-1144.
[2] Kaown D, Koh D-C, Mayer B, et al. Identification of nitrate and sulfate sources in groundwater using dual stable isotope approaches for an agricultural area with different land use(Chuncheon, mid-eastern Korea) [J]. Agriculture, Ecosystems & Environment, 2009,132(3/4):223-231.
[3] 张丽娟,巨晓棠,刘辰琛,等.北方设施蔬菜种植区地下水硝酸盐来源分析——以山东省惠民县为例 [J]. 中国农业科学, 2010, 43(21):4427-4436.
[4] 杨广容,Xiying H,李春莉,等.集约化生产对农田土壤碳氮含量及 δ13C和δ15N同位素丰度的影响 [J]. 应用生态学报, 2012, 23(3):751-757.
[5] 李玉中,贾小妨,徐春英,等.山东省地下水硝酸盐溯源研究 [J].生态环境学报, 2013,22(8):1401-1407.
[6] 史 静,张乃明,褚素贞,等.滇池流域地下水硝酸盐污染特征及影响因素研究 [J]. 农业环境科学学报, 2005,24(S1):104-107.
[7] 李文娟,赵同科,张成军,等.北京市集约化农区地下水硝酸盐含量变化分析 [J]. 农业环境科学学报, 2013,32(7):1445-1450.
[8] 徐志伟,张心昱,于贵瑞,等.中国水体硝酸盐氮氧双稳定同位素溯源研究进展 [J]. 环境科学, 2014,35(8):3230-3238.
[9] 张亚丽,张依章,张 远,等.浑河流域地表水和地下水氮污染特征研究 [J]. 中国环境科学, 2014,34(1):170-177.
[10] 巩建华,柯尊伟,李 季.河北省藁城市蔬菜种植区化肥施用与地下水硝酸盐污染研究 [J]. 农村生态环境, 2004,20(1):56-59.
[11] 刘 瑾,费宇红,张兆吉,等.华北平原某集约化种植区地下水污染探讨 [J]. 地球学报, 2014,35(2):197-203.
[12] 李思亮,刘丛强,陶发祥,等.碳同位素和水化学在示踪贵阳地下水碳的生物地球化学循环及污染中的应用 [J]. 地球化学,2004,33(2):165-170.
[13] 刘小龙,刘丛强,李思亮,等.碳与锶同位素在六盘水地下水研究中的应用 [J]. 生态学杂志, 2010,29(5):978-984.
[14] Barth J A C, Cronin A A, Dunlop J, et al. Influence of carbonates on the riverine carbon cycle in an anthropogenically dominated catchment basin: evidence from major elements and stable carbon isotopes in the Lagan River (N. Ireland) [J]. Chemical Geology, 2003,200(3/4):203-216.
[15] 李甜甜,季宏兵,江用彬,等.赣江上游河流水化学的影响因素及DIC来源 [J]. 地理学报, 2007,62(7):764-775.
[16] Doctor D H, Kendall C, Sebestyen S D, et al. Carbon isotope fractionation of dissolved inorganic carbon (DIC) due to outgassing of carbon dioxide from a headwater stream [J]. Hydrological Processes, 2008,22(14):2410-2423.
[17] 李干蓉,刘丛强,陈 椽,等.猫跳河流域梯级水库夏-秋季节溶解无机碳(DIC)含量及其同位素组成的分布特征 [J]. 环境科学,
2009,30(10):2891-2897.
[18] 贾国东,陈法锦,邓文锋.北江河水溶解无机碳同位素的季节变化 [J]. 地球科学(中国地质大学学报), 2012,37(2):365-369.
[19] 郭 威,李祥忠,刘卫国.西安周边河流溶解无机碳浓度及同位素组成初探 [J]. 环境科学, 2013,34(4):1291-1297.
[20] Brunet F, Potot C, Probst A, et al. Stable carbon isotope evidence for nitrogenous fertilizer impact on carbonate weathering in a small agricultural watershed [J]. Rapid Communications in Mass Spectrometry, 2011,25(19):2682-2690.
[21] 王见月,刘庆花,李俊良,等.胶东果园土壤酸度特征及酸化原因分析 [J]. 中国农学通报, 2010,26(16):164-169.
[22] 蒋 辉.河南省博爱县平原区地下水环境质量数字化综合评价[J]. 水文地质工程地质, 2004,31(3):46-50.
[23] 孙长才,毋先进,张苍松,等.博爱县水资源利用现状及对策研究[J]. 河南水利与南水北调, 2007,(9):33,67.
[24] 吴 夏,涂林玲,杨 会,等.水样中溶解性无机碳同位素测试前处理方法对比研究 [J]. 岩矿测试, 2013,32(4):659-664.
[25] 袁红朝,张丽萍,耿梅梅,等.Flash HT和GasBench Ⅱ-IRMS分析水中氢氧同位素的方法比较 [J]. 质谱学报, 2013,34(6):347-352.
[26] 焦艳军,王广才,崔霖峰,等.济源盆地地表水和地下水的水化学及氢、氧同位素特征 [J]. 环境化学, 2014,33(6):962-968.
[27] 郎赟超,刘丛强,赵志琦,等.贵阳市地表水地下水化学组成:喀斯特水文系统水-岩反应及污染特征 [J]. 水科学进展, 2005, 16(6):826-832.
[28] 张 东,黄兴宇,李成杰.自然与人为控制下河流水化学组成演变过程 [J]. 干旱区资源与环境, 2012,26(12):75-80.
[29] Gaillardet J, Dupré B, Louvat P, et al. Global silicate weathering and CO2consumption rates deduced from the chemistry of large rivers [J]. Chemical Geology, 1999,159(1):3-30.
[30] Li S-L, Chetelat B, Yue F, et al. Chemical weathering processes in the Yalong River draining the eastern Tibetan Plateau, China[J]. Journal of Asian Earth Sciences, 2014,88(0):74-84.
[31] 王庆锁,顾 颖,孙东宝.巢湖流域地下水硝态氮含量空间分布和季节变化格局 [J]. 生态学报, 2014,34(15):4372-4379.
[32] 裴建国,陶友良,童长水.焦作地区天然水环境同位素组成及其在岩溶水文地质中的应用 [J]. 中国岩溶, 1993,12(1):48-56.
[33] 林 云,潘国营,靳黎明,等.氢氧稳定同位素在新乡市地下水研究中的应用 [J]. 人民黄河, 2007,29(10):53-54.
[34] 葛 涛,储婷婷,刘桂建,等.淮南煤田潘谢矿区深层地下水氢氧同位素特征分析 [J]. 中国科学技术大学学报, 2014,44(2):112-118,170.
[35] Spence J, Telmer K. The role of sulfur in chemical weathering and atmospheric CO2fluxes: Evidence from major ions, δ13CDIC, and δ34SSO4in rivers of the Canadian Cordillera [J]. Geochimica et Cosmochimica Acta, 2005,69(23):5441-5458.
[36] Li S-L, Calmels D, Han G, et al. Sulfuric acid as an agent of carbonate weathering constrained by δ13CDIC: Examples from Southwest China [J]. Earth and Planetary Science Letters, 2008, 270(3/4):189-199.
[37] Brookman T, Ambrose S. Kangaroo tooth enamel oxygen and carbon isotope variation on a latitudinal transect in southern Australia: implications for palaeoenvironmental reconstruction [J]. Oecologia, 2013,171(2):403-416.
[38] Galy A, France-Lanord C. Weathering processes in the Ganges-Brahmaputra basin and the riverine alkalinity budget [J]. Chemical Geology, 1999,159(1):31-60.
[39] Hendy C H. The isotopic geochemistry of speleothems—I. The calculation of the effects of different modes of formation on the isotopic composition of speleothems and their applicability as palaeoclimatic indicators [J]. Geochimica et Cosmochimica Acta, 1971,35(8):801-824.
[40] Wachniew P. Isotopic composition of dissolved inorganic carbon in a large polluted river: The Vistula, Poland [J]. Chemical Geology, 2006,233(3/4):293-308.
[41] 彭 希,刘丛强,王宝利,等.筑坝对喀斯特河流水体溶解性无机碳地球化学行为的影响 [J]. 科学通报, 2014,59(4/5):366-373.
[42] Aucour A-M, Sheppard S M F, Guyomar O, et al. Use of13C to trace origin and cycling of inorganic carbon in the Rhône river system [J]. Chemical Geology, 1999,159(1-4):87-105.
[43] 孟凡乔,匡 星,杜章留,等.不同土地利用方式及栽培措施对土壤有机碳及 δ13C值的影响 [J]. 环境科学, 2010,31(8):1733-1739.
[44] 景秀春,邓胜徽,赵宗举,等.塔里木盆地柯坪地区寒武-奥陶系界线附近的碳同位素组成与对比 [J]. 中国科学(D辑:地球科学),2008,38(10):1284-1296.
[45] 左景勋,彭善池,朱学剑.扬子地台寒武系碳酸盐岩的碳同位素组成及地质意义 [J]. 地球化学, 2008,37(2):118-128.
[46] Li S-L, Liu C-Q, Li J, et al. Geochemistry of dissolved inorganic carbon and carbonate weathering in a small typical karstic catchment of Southwest China: Isotopic and chemical constraints[J]. Chemical Geology, 2010,277(3/4):301-309.
[47] 黄平华,陈建生,宁 超,等.焦作矿区地下水水化学特征及其地球化学模拟 [J]. 现代地质, 2010,24(2):369-376.
Inorganic carbon cycling in subsurface environment influenced by agricultural activities.
ZHANG Dong1,2*, LIU Cong-qiang2, WANG Fu-shun3, ZHAO Zhi-qi2(1.Institute of Resource and Environment, Henan Polytechnic University,Jiaozuo 454000, China;2.State Key Laboratory of Environmental Geochemistry, Institute of Geochemistry, Chinese Academy of Science, Guiyang 550002, China;3.School of Environmental and Chemical Engineering, Shanghai University, Shanghai 200433, China).
China Environmental Science, 2015,35(11):3359~3370
To accurately elucidate the pollution sources and pollutant transformations in subsurface environment, shallow groundwater affected by intensive cultivation of vegetables on open land in North China was selected as objective. Hydrochemical compositions, hydrogen and oxygen isotopes, and dissolved inorganic carbon isotopes of shallow groundwater samples were utilized to delineate the sources of groundwater and to illuminate the sources and transformations of dissolved inorganic carbon. The results demonstrated that Ca2+and Mg2+were dominated cations, andandwere dominated anions in local groundwater. Along groundwater flow path, hydrochemistry types varied fromto; Hydrogen and oxygen isotope values of shallow groundwater varied from -69.6‰ to -52.7‰ with the average value of -63.5‰ and from -9.29‰ to -6.80‰ with the average value of -8.45‰, respectively. It could be found that atmospheric precipitation was the main recharge source of local groundwater,meanwhile shallow groundwater located near the river water were also recharged from surface water. Dissolved inorganic carbon isotope values of shallow groundwater varied from -11.76‰ to -5.85‰ with average value of -10.43‰. Dissolved inorganic carbon in local groundwater was mainly derived from soil carbon dioxide, carbonate minerals and organic matters. It also indicated that some groundwater samples had been influenced by infiltration of river water. Fertilizer-induced acid participating carbonate minerals weathering and CO2outgassing in shallow groundwater were two important factors controlling inorganic carbon isotopic compositions in groundwater, which should be paid more attentions during identification of groundwater pollution sources by dissolved inorganic carbon isotopes.
agricultural activities;shallow groundwater;dissolved inorganic carbon isotopes;acidification;CO2outgassing
X523,P597
A
1000-6923(2015)11-3359-12
2015-04-15
国家自然科学基金资助项目(41573095,41173030);河南省高校科技创新团队支持计划(15IRTSTHN027)
* 责任作者, 副教授, zhangdong@hpu.edu.cn
张 东(1978-),男,山东泰安人,副教授,博士,主要从事环境地球化学方面的研究.发表论文10余篇.
