催化还原法深度处理污水中硝态氮的研究
2015-08-25云玉攀李子富周晓琴白晓凤高瑞玲王雪梅北京科技大学土木与环境工程学院工业典型污染物资源化处理北京市重点实验室北京100083
云玉攀,杨 鑫,李子富,周晓琴,白晓凤,高瑞玲,王雪梅 (北京科技大学土木与环境工程学院,工业典型污染物资源化处理北京市重点实验室,北京 100083)
催化还原法深度处理污水中硝态氮的研究
云玉攀,杨 鑫,李子富*,周晓琴,白晓凤,高瑞玲,王雪梅 (北京科技大学土木与环境工程学院,工业典型污染物资源化处理北京市重点实验室,北京 100083)
为有效降低城市污水处理厂出水硝态氮的含量,减轻氮素污染,依次进行了基础性试验和验证性试验.基础性试验以Fe0为还原剂,以配置的KNO3溶液为试验用水对分别添加H+、Fe2+、Cu2+、Pd/Al2O3等后的脱氮效果进行了对比研究.试验结果表明,系统pH值为2.1,Fe2+、Cu2+投加量分别为1000mg/L时,系统均可获得较好的脱氮效果,分别为92%、41%、61%,产物均以氨氮为主;当投加10g/L催化剂Pd/Al2O3,调节系统pH值为3.02时,系统脱氮率可达48%,且其产物以氮气为主,副产物较少.在此基础上,验证性试验以北京市某污水处理厂出水为试验用水,对上述各方法的脱氮效果进行了试验验证,并对其可行性进行了分析.结果表明,在一定条件下,各方法均可达到理想的脱氮效果,其去除率分别可达到87%、36%、50%、46%.但综合脱氮效果、产物分析、出水水质等考虑,相比较而言,添加催化剂的化学催化还原法在去除污水中的硝态氮时具有更好的可行性.
污水处理;硝态氮去除;化学催化还原
随着工农业的发展,水体中硝酸盐污染已成为亟待解决的环境问题.污水中硝酸盐的过量排放可直接造成水体的富营养化及水质的下降,污染破坏生态环境,从而对人类的生产生活造成极大的影响.资料显示,由于高含氮污水排放导致的地下水硝酸盐污染已愈发严重,相当多地区硝酸盐含量甚至已严重超标[1],如美国、法国部分地区的地下水硝酸盐浓度已达到 40~50mg/L,而我国有些地区的地下水硝酸盐浓度甚至已超过100mg/L,远高于规定的饮用水中硝态氮含量10mg/L[2].
污水中氮素主要以氨氮、硝态氮、亚硝态氮等形式存在.在我国,城镇的生活污水及工业废水排入外部环境前都需先经过污水处理厂处理.污水厂主要通过生物法来脱氮.实际运行时,在生物反硝化阶段,需要外加碳源,而受到污水水质及处理工艺的限制,其处理效果不理想,出水硝态氮含量往往较高.根据调查[3],某污水厂出水总氮(20.6mg/L)中80.6%以硝态氮的形式存在,氨氮仅占19.4%.
因此,采用何种技术有效降低污水厂出水硝态氮以减少氮素污染成为广大学者亟需解决的难题.
目前,污水中硝态氮的去除方法主要有物化法、生物法及化学法[4-6].其中,物化法主要包括离子交换、反渗透、电渗析等[7],主要通过选择性吸附及膜的选择透过性等作用去除水体中的硝态氮.而生物法脱氮则是基于反硝化理论,即硝态氮在一定条件下,通过反硝化过程被转化为氮气而从水体中去除[8].化学法则利用易被氧化的金属或化合物将硝酸盐还原为氨氮、氮氧化物或氮气,从而达到脱氮目的[9].化学法主要有活泼金属还原法[10]与催化还原法[11]等.前者多以铝、铁等还原性较强的金属单质作为还原剂,将硝态氮转化为氨氮等其它形式的氮[12-13].而催化还原法是以氢气、甲酸等为还原剂,在特定催化剂作用下,将硝酸盐氮还原为氮气[14].
物化法虽易于操作实施,处理效果好,但其不能彻底去除硝酸盐,易造成二次污染,而且成本也较高.生物法脱氮真正意义上实现了氮从水体的去除,但作为尾水的深度处理,生化法工艺复杂,成本较高,且去除效果不稳定.而化学法虽受到pH值影响,但由于操作简单、处理周期短、处理效果稳定等仍受到广大学者的关注[15],尤其是催化还原法,理论上还原剂在适宜催化剂作用下,可将水体中大部分硝态氮转化为氮气,这为真正去除污水中硝态氮,减少氮素污染提供了可能.
综合以上考虑,本文以去除污水中硝态氮作为出发点,以化学催化脱氮的相关理论为指导,以 Fe0为还原剂,通过添加不同化学试剂,依次进行了基础性试验和验证性试验.本文首次提出了应用Fe0+催化剂的化学催化还原法处理污水厂尾水中的硝态氮,并对其技术的可行性进行了深入探讨分析.
1 材料与方法
1.1试验仪器与试剂
试验仪器:恒温振荡器、紫外/可见分光光度计、马弗炉、真空干燥箱、高压灭菌锅、旋转蒸发仪、pH计等.
试验药剂:试验所采用的试剂除特殊说明外,均为分析纯.还原性铁粉、KNO3、FeSO4·7H2O、CuCl2·2H2O、NaBH4、HCl、Al2O3、PdCl2.
1.2试验方法
1.2.1基础试验 用 KNO3试剂配置所需试验用水,硝态氮浓度为20mg/L.取100mL该溶液于250mL锥形瓶中,而后分别加入一定量的还原剂和相关试剂,放入恒温振荡器于250r/min条件下反应2h.具体方案如下:
(1)投加还原性铁单质Fe0,调节系统pH值;(2)投加Fe0,加入不同量的FeSO4·7H2O;(3)投加Fe0,加入不同量的CuCl2·2H2O;(4)投加Fe0,加入不同量的催化剂Pd/Al2O3.
根据最终的脱氮效果,确定各方案的最佳反应条件,包括:Fe0投加量、Fe2+、Cu2+的投加浓度、催化剂的投加量、系统pH值等,为后续的可行性研究打下基础.
1.2.2验证试验 为探讨化学法去除污水中硝态氮的可行性,选取北京市某污水处理厂的出水作为试验用水.用水水质如表1所示.

表1 试验用水水质Table 1 water quality for test
根据上述基础试验的结果,选取各方案的最佳反应条件,而后以污水处理厂的出水为试验用水,在最佳反应条件下进行验证性试验.根据试验结果,综合多方面因素,对各方案用于污水脱氮的可行性进行分析探讨,为实际应用提供理论依据.
2 结果与讨论
2.1基础试验
基础试验以实验室配制的硝酸钾溶液为试验用水,以还原性铁粉(Fe0)为还原剂,为方便对比试验效果,各方案的Fe0投加量均为5g/L,而后分别投加不同量的 H+、Fe2+、Cu2+及 Pd/Al2O3,根据试验效果选取各方案的最佳操作条件.试验结果如下.
2.1.1投加Fe0+H+由表2可知,当系统pH值为2.1时,硝态氮去除率达到92%,而未调pH值时(pH值为7.1),其去除效率较低,仅为6%.系统在酸性条件下对水体中硝态氮的去除效率较高,这和Chen等[16]的研究结果一致.另外,随着反应的进行,系统中H+被消耗,pH值呈现上升的趋势.由图1可发现,反应的最终产物主要以氨氮为主,还有少量的亚硝态氮和氮气.王迪使用还原铁粉去除水体中的硝态氮时也发现,pH值是影响硝态氮去除效率的关键,其最终产物主要以氨氮为主[17].
表2 系统pH值对去除效果的影响Table 2 Effect of pH onremoval

表2 系统pH值对去除效果的影响Table 2 Effect of pH onremoval
反应前pH值去除率(% )反应后pH值2.1924.63.3705.94.1456.55.2256.96.3117.47.167.8
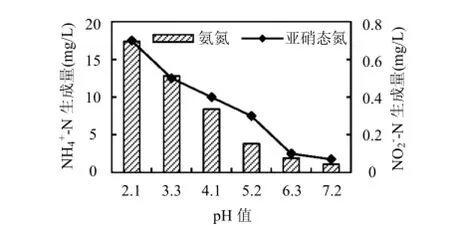
图1 pH值对氨氮和亚硝态氮生成量的影响Fig.1 Effect of pH on production ofand
从原理分析,单质铁在与硝酸盐反应的过程中,会消耗大量的氢离子.由反应方程式[18]可以发现,理论上,系统在酸性条件下,利于化学反应顺利进行,使硝酸盐转化为氨氮、氮气及亚硝酸盐氮等物质,从而提高硝酸盐的去除率.

2.1.2投加 Fe+Fe2+由表 3可知,Fe2+投加浓度为1000mg/L时,硝态氮的去除率达到41%,投加浓度增至1200mg/L时,硝态氮去除率增加不大,仅为46%.系统反应后,pH值维持在6~8.根据图 2所示,反应产物仍主要以氨氮为主,其生成量为 0.6~8.1mg/L,亚硝态氮的生产量总体较低,其生成量为 0.03~0.33mg/L.从原理分析,Fe0主要作为电子供体,NO3-作为电子受体,其参与的反应如下:

表3 Fe2+浓度对去除效果的影响Table 3 Effect of Fe2+concentration onremoval

表3 Fe2+浓度对去除效果的影响Table 3 Effect of Fe2+concentration onremoval
投加浓度(mg/L)去除率(%)反应后pH值20096.6400146.9600237.2800316.91000417.31200467.4

图2 投加浓度对氨氮和亚硝态氮生成量的影响Fig.2 Effect of Fe2+concentration on production ofand
由上述反应方程式不难发现,系统反应过程中伴随 H+的消耗和产生.通过试验测定,反应前后,系统的pH仍维持在7左右,差别不大.反应结束后,有黄色沉淀物生成,通过对生成物的XRD测试分析,其为Fe3O4.有资料认为[19],在反应过程中,铁表面生成的Fe3O4有较低的电阻,是很好的半导体. Xu等[20]研究发现,在Fe0还原硝态氮的反应中,系统pH值中性条件下,一定量的Fe2+能增加铁表面的腐蚀,同时产生 Fe3O4和 H+.Fe3O4一定程度上能够促进电子从供体 Fe0到受体的转移,从而加速硝态氮的还原,促进硝酸盐氮的去除效率.而 Fe2+过量可能会包裹于 Fe0表面,形成胶状物质,减少Fe0的反应活性.因此,Fe2+选取的适宜投加浓度为1000mg/L.
2.1.3投加Fe0+Cu2+由表4发现,随着Cu2+投加浓度的增加.硝态氮的去除率逐步升高.当Cu2+投加浓度为 100mg/L时.硝态氮的去除率仅为15%左右,投加浓度增至 1000mg/L时,去除效果有一定程度的提高,去除率达到61%,投加浓度为1250mg/L时,其去除率增加不太显著,仅为64%.另外,在试验中我们发现,随着不同浓度Cu2+的投加,系统 pH值均出现下降趋势.究其原因,CuCl2·2H2O是强酸弱碱盐,在系统中易发生水解,导致系统 pH值降低.由上面试验可知,低pH值有利于系统的反应,促进硝态氮的去除.而且随着反应的进行,系统H+有消耗,系统pH值又有上升,维持在7~9范围内.由图3可知,系统反应完全后,其产物主要以氨氮为主,其生成量为1.2~11.1mg/L,亚硝态氮生成量较少,其生成量为0.02~0.41mg/L.
表4 Cu2+浓度对去除效果的影响Table 4 Effect of Cu2+concentration onN removal

表4 Cu2+浓度对去除效果的影响Table 4 Effect of Cu2+concentration onN removal
投加浓度(mg/L)去除率(%)反应后pH值100157.3250217.4500327.3750457.51000617.91250648.3
从原理分析,Fe0还原性较好,在反应中相当于电子供体[21],其失去电子,从而触发硝态氮的氧化还原.而反应中 Fe0会与 Cu2+发生氧化还原反应,生成的单质铜会附着于铁表面,一定程度上起到催化剂的作用,加速反应过程中电子的转移,从而促进系统中硝态氮的氧化还原,而系统酸性条件则有利于 Fe0失去电子.另一方面,溶液中硝态氮会首先扩散并吸附于铜界面的活性吸附位,而后在催化作用下,硝态氮发生脱氧反应,逐步被去除,同时伴随氨氮及氮气的产生.

图3 Cu2+浓度对氨氮和亚硝态氮生成量的影响Fig. 3 Effect of Cu2+concentration on production ofand
2.1.4投加Fe0+ Pd/Al2O3由表5发现,当催化剂的投加量为3g/L时,硝态氮去除率为29%,投加量增至15g/L时,去除率增至53%.对反应前后pH值测定发现,pH值较反应前有所增加,这是因为反应过程中,有一定量的OH-生成.另外通过与不调节pH值的去除率对比,酸性条件下,系统硝态氮去除效果更好,而系统不调pH值时,硝态氮去除率有限,仅为 10%左右,基本未发生反应.因为,酸性条件一方面可防止铁的氧化,另一方面可提供催化反应所需的活性 H,从而有效推进催化反应的发生.由图4发现,随催化剂投加量的增加,系统生成的氨氮及亚硝态氮量也逐步增加,分别在0.4~2.6mg/L及0.01~0.26mg/L内.为探究氮的转化形态,我们对系统总氮进行了测定,并由此推断,去除的硝态氮中约70%左右被转化为了氮气.
表5 催化剂投加量对去除效果的影响Table 5 Effect of catalyst dosage on removal

表5 催化剂投加量对去除效果的影响Table 5 Effect of catalyst dosage on removal
注:反应的pH值为3.02,括号内为未调节pH值(7.1)的去除率
投加量(g/L)去除率(%)反应后pH值329(7)7.4538(9)7.81048(11)8.21553(12)8.4
至今为止,化学催化法去除硝酸盐的反应机理还不是很清楚,但普遍认为反应的发生是通过多个步骤完成的.催化剂催化脱氮过程是一个典型的多相催化反应.在反应中,Fe0作为电子供体在酸性条件下失去电子,而电子则可结合系统中的H+成为活性H,反应方程式如下:


图4 投加量对氨氮和亚硝态氮生成量的影响Fig.4 Effect of dosage on the production ofand
生成的活性H易被吸附于催化剂金属表面,水体中的硝态氮可与其逐步发生脱氧反应,从而被还原去除,主要的反应方程式如下:

NO被认为是脱氧反应的关键中间产物.反应过程中,催化剂金属表面吸附的H可与O反应生成OH-,而NO则可与H生成NH,而后与另外的H结合生成,或者与另外一个NH生成.硝酸盐的催化还原反应机理示意图如下所示.
由图5发现,在催化剂作用下,通过向系统添加还原性铁(Fe0)和H+,理论上存在将硝态氮转化为氮气的可能.而在反应中,适宜的催化剂及 H+浓度对提高氮气转化率尤为重要.适宜的H+浓度有助于H的生成,从而促进硝态氮的选择性还原;而催化剂一方面可加强电子的转移,并激发 H2O中的氢产生H[23],另外,其还能选择性的促进硝态氮向氮气反应的发生,提高氮气的转化率.
通过以上几组试验对比,我们发现以 Fe0作为良好的还原剂,而后通过调节系统 pH或分别添加 Fe2+、Cu2+等,虽然一定程度上可达到去除部分硝态氮的目的,但其反应只是发生了氮形态的不同转化(多转化为氨氮),N仍停留在水体中.但采用Fe0+Pd/Al2O3的方法,在一定条件下,其硝态氮可大部分转化为氮气,从而真正意义上实现了水体中硝态氮的去除.

图5 催化还原脱氮反应机理Fig.5 Hypothetical mechanism of catalytic nitrate reduction
2.2验证试验
通过基础试验选取了各方案的最佳运行条件,而后以北京某城市污水厂出水为试验用水,对以上各方法进行验证试验.经测定污水浓度为12.7mg/L浓度为0.1mg/L,TN浓度为 16.9mg/L,NH4+-N浓度为3.3mg/L.试验结果见表6.

表6 验证性试验结果Table 6 Experimental results of proving tests
2.2.1脱氮效果 A组硝态氮去除率较高,达到87%,但出水 pH较低,若正常排放需进行后续处理.B组效果相对较差,仅为 36%.四组中,相比于基础性试验的单纯溶液反应,采用污水后的试验脱氮效果略有下降.可能是因为,污水水质(如水体中的相关有机物、悬浮物、阴阳离子等)对反应造成了一定程度的影响,而C组和D组,其去除效果相当,去除率均在50%左右.
2.2.2产物分析 前 3组硝态氮大都转化为氨氮,造成了二次污染,实际中若直接排放还需对氨氮及总氮进行处理(均超过一级 A排放标准5mg/L,15mg/L),增加了处理成本.而采用催化剂催化去除硝态氮,合理选择还原剂和催化剂可将大部分硝态氮转化为氮气,一定程度上实现了氮素从水体中真正意义上的去除.
2.2.3最终水体的物理特性 前 3组由于添加了相关的试剂,反应完全后,水体较浑浊,色度很高,不能直接排放,需进行混凝处理,处理成本较高.相比较而言,本试验所采用催化剂稳定性较好,而且反应完全后,水体不致较浑浊,色度不高.
通过对 4组方案去除污水中的硝态氮的可行性分析发现,4种方法中,D组的化学催化法去除污水的中硝态氮时有更好的可行性.另外,应用化学催化法脱氮时,还原剂及催化剂的选取是能否取得良好脱氮效果的关键.还原剂可诱导催化反应的发生,而催化剂则对反应的发生起到了关键的引导和催化作用.催化剂有一定的催化活性和选择性.催化活性可由硝态氮的去除效率表征,而选择性可由生成的氨氮或氮气来衡量.因此,在保证一定的催化活性条件下,如何选取载体和催化组分以保证催化剂有较好的选择性,从而使系统硝态氮转化为氮气,将是以后研究的重点.
2.3化学催化法脱除污水中硝态氮的影响因素
2.3.1催化剂性质 催化剂的性质对其活性和选择性起着至关重要的作用.催化剂由催化活性组分和载体构成. Hoerold等[24]对多种金属试验研究后发现,Pd金属的活性和选择性最高.另外,催化剂的活性组分含量一定程度上会影响催化效果.本文仅对 Pd催化剂进行了初步探索研究,后续还将对更多的金属催化剂进行深入系统的研究,本试验中Pd催化剂的设计负载量为5%,催化剂可通过浸渍法获得.而在二元催化剂中,助催化剂的添加一定程度上可改善其催化性能.研究发现,在主催化剂中(如Pd)分别添加Sn、In、Cu等金属,催化效果均可得到明显改善[25].
2.3.2水体中的离子 与硝酸盐配成的水溶液相比,处理实际污水时,催化剂的活性和选择性都有不同程度的下降.其原因在于,污水水质组成对催化剂催化脱氮的活性和选择性有不同程度的影响,如水体中阳离子可影响硝酸根和氢氧根在水中的迁移速度,而阴离子则可与硝酸根竞争表面吸附或活性位置,在催化剂表面形成沉淀或污垢,降低催化剂的有效表面积[26].Pintar等[27]研究后发现,具有和硝态氮类似结构,会与其发生竞争吸附,降低催化剂的活性和选择性,而Ca2+、Mg2+则不会对其产生明显的影响. Lemaignen[28]也提出与同样存在竞争吸附,会降低硝态氮的去除效果.
2.3.3水体的DO及pH值 水体中的DO一定程度上也会影响硝态氮的去除效果.污水经过生物处理后,水体中会有一定量的DO存在,一方面,氧通过与硝态氮争夺电子而抑制其还原;另一方面,其一定程度上会导致铜等金属催化剂及铁等还原剂被氧化,降低脱氮效果[29].为消除DO的不利影响,可适当调节系统pH值,使系统维持在酸环境,其既能防止还原剂及催化剂被氧化,又能提供催化反应所需的活性H,有效维持系统的pH值平衡.
2.3.4其他因素 温度对反应速率有一定的影响,升高温度能有效打破硝酸盐还原反应中的能量壁垒,提高硝酸盐还原的反应速率[30].实际工程中在常温下,还原反应同样能发生,因此不需要提高温度.另外,化学催化脱氮是一个异相催化还原过程,主要发生在催化剂的表面,因此,若保证良好的去除效果,还需使催化剂的活性表面与溶液内部保持良好的传质效果,如加强搅拌、使用粉末状催化剂、添加酸性物质等.
3 结论
3.1基础性试验以配制的KNO3为试验用水.系统 pH为 2.1值时,硝态氮去除率可达 92%;当Cu2+、Fe2+投加浓度为1000mg/L时,去除率达到61%和41%;Pd/Al2O3投加量为10g/L时,硝态氮去除率达到48%.就产物而言,当向系统分别投加H+、Fe2+、Cu2+时,产物均以氨氮为主,亚硝态氮及氮气次之;投加Pd/Al2O3时,其产物主要以氮气为主,伴有少量氨氮及亚硝态氮.
3.2验证试验以北京某城市污水厂出水为试验用水.通过对去除效果、产物分析、最终水体的物理特性等方面综合考虑,4种去除污水中硝态氮的方法中,添加催化剂的化学催化法有更好的可行性. 3.3 实际应用中,催化剂性质、污水中的阴阳离子、污水的DO及pH值等都将直接或间接影响硝态氮的去除效果.因此,用催化还原法去除污水中硝态氮时应控制好反应条件,综合考虑多方因素选择合理方案.
[1] 孙彩霞,王 琴,何云峰,等. 催化还原地下水中硝酸盐的研究[J]. 环境科学动态, 2003,2:6-9.
[2] 张 燕.催化还原去除地下水中硝酸盐的研究 [D]. 浙江大学,2003.
[3] 陈云峰,文 辉,张彦辉.不同固态碳源用于反硝化去除污水处理厂尾水中硝态氮的研究 [J]. 给水排水, 2010(11):140-143.
[4] Ahn Jae-Hee, Choo Kwang-Ho, Park Hak-Soon. Reverse osmosis membrane treatment of acidic etchant wastewater: effect of neutralization and polyelectrolyte coating on nitrate removal [J]. J. Membr. Sci., 2008,310:296-302.
[5] Rivett M Q, Buss S R, Morgan P, et al. Nitrate attenuation in groundwater: a review of biogeochemical controlling processes [J]. Water Res., 2008,42:4215-4232.
[6] Prusse U, Vorlop K D. Supported bimetallic palladium catalysts for water-phase nitrate reduction [J]. J. Mol. Catal. A: Chem.,2001,173,313-328.
[7] Luo G Z, Li L, Liu Q, et al. Effect of dissolved oxygen on heterotrophic denitrification using poly (butylene succinate) as the carbon source and biofilm carrier [J]. Bio-resource Technology, 2014,171:152-158.
[8] 张希衡.废水厌氧处理工程 [M]. 北京:中国环境科学出版社,1996.
[9] 高建峰.水中硝酸盐氮复合催化还原无害化的原理和技术研究[D]. 天津:南开大学, 2004.
[10] Fax X M, Guan X H, Ma J, et al. Kinetics and corrosion production of aqueous nitrate reduction by iron powder without reaction conditions control [J]. J.Environ.Sci., 2009,21:1028-1035.
[11] Machesni F A, Irusta S, Querini C, et al. Nitrate hydrogenation over Pt, In/Al2O3and Pt, In/SiO2: effect of aqueous media and catalyst surface properties upon the catalytic activity [J]. Catal Commun., 0089:1021-1026.
[12] Murphy A P. Chemical removal of nitrate from water [J]. Nature,1991,350:223-225.
[13] Huang C P, Wang H W, Chiu P C, Nitrate reduction by metallic iron [J]. Water Res., 1998,32:2254-2257.
[14] 张 富.催化还原去除水中硝酸盐新型催化剂的研究 [D]. 大庆:大庆石油学院, 2009.
[15] 赵 群.废水中硝态氮来源、转化及去除方法 [J]. 山东理工大学学报(自然科学版), 2014,28(4):53-56.
[16] Chen Yiming, Li Chiwang, Chen Shiaoshing. Fluidized zero valent iron bed reactor for nitrate removal [J]. Chemosphere,2005,753-759.
[17] 王 迪.还原铁粉去除地下水中硝酸盐及亚硝酸盐的研究 [D].东北林业大学, 2013.
[18] Yang Gordon C C, Lee Hsaio-Lan. Chemical reduction of nitrate by nanosized iron Kinetics and pathways [J]. Water Research,2005,39:884-894.
[19] Schlicker O, Ebert M, Fruth M, et al. Degradation of TCE with iron: the role of competing chromate and nitrate reduction [J]. Ground Water, 38(2000):403-409.
[20] Xu Jiang, Hao Zhiwei, Xie Chunsheng. Promotion effect of Fe2+and Fe3O4on nitrate reduction using zero-valent iron [J]. Desalination, 2012,284:9-13.
[21] Hu Hong-Ying, Goto Naohiro, Fujie Koichi. Effect of pH on the reduction of nitrite in water by metallic iron [J]. Water Research,2001,35(11):2789-2793.
[22] 杜志强,陈万喜,徐铸德,等.氮氧化合物在铜、银、镍、钯、铂面的吸附、脱附理论研究 [J]. 化学物理学报, 1999,12(5):633-640.
[23] S. Mossa Hosseini, B.Ataie-Ashtiani, M. Kholghi. Nitrate reduction by nano-Fe/Cu particles in packed column [J]. Desalination, 2011,276,214-221.
[24] Hoerold S, Tacke T, Vorlop K D. Catalytic removal of nitrate and nitrite from drinking water-1:screening for hydrogenation catalysts and influence of reaction conditions on activity and selectivity [J]. Environ. Technol., 1993,14:931-945.
[25] 王 颖,辛 杰,李 雪,等.化学催化还原地下水中硝酸盐的研究进展 [J]. 水处理技术, 2010,36(7):14-19.
[26] 崔宝臣,张 富,徐胜利,等.催化还原法去除饮用水中硝酸盐氮研究进展 [J]. 应用化工, 2008,37(9):1081-1085.
[27] Pintar A, Levec J. Hardness and salt effects on catalytic hydrogenation of aqueous nitrate solutions [J]. J. Catal., 1998,1(15):72-87.
[28] Lemaignen L, Tong C, Begon V, et al. Catalytic denitrification of water with palladium-based catalysts supported on activated carbons [J]. Catal. Today, 2002,75:43-48.
[29] 李胜业,金朝晖,金晓秋,等.还原铁粉反应柱去除地下水中硝酸盐氮的研究 [J]. 农业环境科学学报, 2004(6):1203-1206.
[30] Se Chang Ahn, Seok-Young Oh, Daniel K Cha. Enhanced reduction of nitrate by zero-valent iron at elevated temperatures [J]. Journal of Hazardous Materials, 2008(156):17-21.
Study on advanced treatment for removing nitrate in wastewater through chemical catalytic reduction.
YUN Yu-pan, YANG Xin, LI Zi-fu*, ZHOU Xiao-qin, GAO Rui-ling, WANG Xue-mei (Beijing Key Laboratory on Resource-oriented Treatment of Industrial Pollutants, School of Civil and Environmental Engineering, University of Science and Technology Beijing, Beijing 100083, China).
China Environmental Science, 2015,35(11):3310~3316
In order to effectively reduce the concentration ofin the effluent of the municipal wastewater treatment plant, the basic experiments and proving tests were conducted in order. The KNO3solution prepared was sampled for evaluatingremoval efficiency by adding H+、Fe2+、Cu2+and Pd/Al2O3,respectively. Results showed that certain removal performances could get (92%、41%、61%), when the pH was 2.1, or with the dosage of 1000mg/L for Fe2+and Cu2+,respectively; one thing we could not neglect was thatdominated in the products. However, 48% removal efficiency could be reached and N2was predominant in the products with dosage of 10g/L of the catalysts (Pd/Al2O3) and pH of 3.02. The effluent of the wastewater treatment plant was used for the proving tests. It can be concluded that under certain condition,ideal efficiency could be obtained through the above mentioned ways. Taking nitrate removal efficiency, byproducts, water properties into consideration, the chemical catalytic reduction of nitrate in wastewater could be more practicable.
wastewater treatment;nitrate removal;chemical catalytic reduction
X703.1
A
1000-6923(2015)11-3310-07
2015-04-10
* 责任作者, 教授, zifulee@aliyun.com
云玉攀(1985-),男,河北石家庄人,北京科技大学博士研究生,主要从事水污染控制方面研究.
