3D腹腔镜下逆时针全结直肠切除术治疗FAP患者一例(附视频)
2015-08-23马天翼黄睿汤庆超乔天宇袁子铭陈瑛罡
马天翼 黄睿 汤庆超 乔天宇 袁子铭 陈瑛罡
·名家手术·
3D腹腔镜下逆时针全结直肠切除术治疗FAP患者一例(附视频)
马天翼 黄睿 汤庆超 乔天宇 袁子铭 陈瑛罡

陈瑛罡 副教授、副主任医师。主要研究方向是结直肠癌以手术为主的综合治疗,肿瘤患者肠内、肠外营养支持治疗的临床及基础研究,低位直肠肿瘤患者TEM治疗。现任哈尔滨医科大学附属第二医院结直肠肿瘤外科副主任、《中华结直肠疾病电子杂志》编辑部主任。主要学术兼职:中国抗癌协会肿瘤营养与支持治疗专业委员会委员、中华医学会外科医师分会肠内肠外营养治疗专业委员会委员、中国抗癌协会大肠癌专业委员会TEM学组副组长、黑龙江省抗癌协会肠内肠外营养治疗专业委员会委员。主持承担省自然科学基金1项,参与及完成国家自然科学基金2项。主编著作1部,参编人民卫生出版社著作1部,参编卫生部音像教材3部。在国内外期刊发表论文20余篇。
家族性腺瘤性息肉病(familial adenomatous polyposis,FAP)是一种常染色体显性遗传的结直肠疾病[1-2]。因其具有癌变倾向,外科手术是治疗该疾病的有效治疗手段[3]。自1991年Jacobs等[4]首次用腹腔镜行结直肠手术成功以来,随着腹腔镜技术的不断发展,腹腔镜结直肠癌根治术在许多有条件的医院得以开展,近日哈尔滨医科大学附属第二医院结直肠肿瘤外科收治了1例此类患者,其手术特点为全结肠标本经会阴部切口取出,腹部无辅助切口,现将该患者的治疗汇报如下。
一、一般资料
患者男性,38岁,主因“腹泻便血3年,腹部不适感1月”入院,既往无高血压及糖尿病病史,2013年3月曾于其他医院行痔切除术。该患者存在明确家族史,其母亲、姨母,祖母均为肠癌患者。肠镜检查提示:进境后观察肠管黏膜可见多发息肉样隆起,可见全结肠百余枚息肉样隆起,最大者直径约3 cm,表面分叶状,在降结肠乙状结肠交界处(距肛门28 cm),距肛门10 cm及距肛门1 cm处分别见一较大肿物(图1),病理回报均为腺癌。术前CEA为20.23 ng/ml,CA199为40.34 U/ml,其余检查无著征。腹部查体:腹平坦,未见肠型及蠕动波,腹部未触及明显包块,叩诊呈鼓音,听诊肠鸣音3~4次/分。肛诊:胸膝位,距肛缘1 cm左侧壁可触及一肿物,活动度良好,所触及肛管及直肠管腔黏膜有广泛息肉样隆起,数量不可数。退出指套染血。患者术前诊断为直肠癌、结肠癌、家族性腺瘤性息肉病。经术前讨论,对患者拟3D腹腔镜下全结肠切除术、经腹会阴联合直肠癌根治术、回肠造口术。
二、手术过程
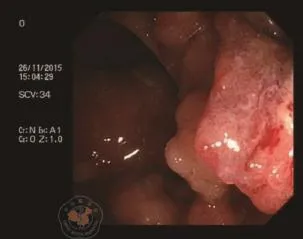
图1 患者结肠镜检查结肠黏膜图像
患者麻醉满意后,取头低足高分腿平卧位,常规消毒铺无菌巾,术者站位于患者右侧,第一助手站位于患者左侧,持镜者站位于术者同侧。在脐下置入10 mm Trocar,安置30°斜面3D腹腔镜头,在镜头的引导下,与右脐旁腹直肌外缘置入5 mm Trocar。右下腹、左脐旁腹直肌外缘置入12 mm Trocar作为主操作孔,左下腹置入5 mm Trocar用于辅助操作孔。设置气腹机压力12 mmHg。探查腹腔未见远处转移及种植,可见结肠息肉恶变肿瘤位于降结肠乙状结肠交界处,大小约4×4 cm,侵出浆膜,直肠息肉恶变肿瘤位于腹膜返折下。拟先行游离肠系膜下血管及直肠,然后逆时针方向游离降结肠、横结肠及升结肠,直肠肿瘤距离肛门较近,且直肠及肛管内息肉多,不可数,需行直肠癌Miles术,遂所切除标本拟从会阴处切口取出体外,腹部可无辅助切口。
于左右髂血管分叉处用超声刀先切开乙状结肠右侧腹膜,向下切开至直肠前的腹膜反折处,转而向上切口游离,显露肠系膜下血管,在其根部,即距离腹主动脉起源处1~2 cm处裸化血管壁,清扫血管根部淋巴结,用Hem-o-lok血管夹夹闭,超声刀切断。沿腹主动脉及左侧髂血管表面即Toldtʹs筋膜间隙向左侧处理,此时后腹膜的疏松结缔组织显露,保护左侧输尿管,显露左侧生殖血管。超声刀打开乙状结肠外侧腹膜,使内外侧想通,游离直肠系膜并保持其完整性,保护双侧输尿管,镜下于盆筋膜的壁层和脏层之间进行锐性分离,沿骶前间隙到达盆底,继续向下游离达到肛提肌平面,超声刀切断直肠侧韧带,游离直肠前壁,靠近盆壁向下游离直肠,使直肠周围方向都达到肛提肌平面,至此完成直肠的游离。
将腹腔镜屏幕做小幅度调整,移动至患者头侧,术者站位于患者两腿间,沿降结肠外侧旁沟向上游离至结肠脾曲,充分显露仔细游离切断脾结肠韧带,同时注意保护脾下级及胰腺尾部。顺势游离横结肠系膜及大网膜,用血管夹夹闭供血血管。
变换腹腔镜屏幕位置至患者右侧,术者站位于患者左侧,右半结肠切除采用内侧入路方式,按由内向外、从上到下的原则,先处理血管,沿肠系膜上动静脉走行打开结肠系膜,首先解剖出回结肠血管,在血管根部裸化1~2 cm血管,用Hem-o-lok血管夹夹闭,超声刀切断。然后向下以超声刀游离小肠系膜至距回盲部10 cm处预切断小肠肠壁,备用。以此前回结肠血管切断处作为指示,沿十二指肠表面、Toldtʹs筋膜间隙,向外、向上分离,分离至胰头表面可见右结肠动静脉,于根部以血管夹夹闭、切断。胃网膜血管弓外侧分离切断胃结肠韧带,沿胃网膜右动静脉弓向十二指肠、胰头游离,清扫第6组淋巴结至胃网膜右动静脉血管根部。向外侧游离以超声刀切断肝结肠韧带,然后从升结肠旁沟自肝曲处向下锐性切开后腹膜,将升结肠从腹后壁游离,在游离过程中注意保护右侧输尿管、肾脏。此时小肠预切断处血运分界清晰,以镜下线型切割闭合器在小肠预切线处切断回肠。先全结肠均已处于游离状态。关闭气腹机。
肛门口作荷包缝合,环绕肛门梭形切开皮肤,电刀游离皮下脂肪,向盆腔方向游离至肛提肌,在直肠后壁切开肛尾韧带,进入直肠后间隙,与盆腔相通。从底部向两侧向上游离直肠两侧壁,沿直肠前间隙分离直肠,保护尿道及前列腺被膜,将直肠切除。通过会阴部切口取出全部结肠及直肠标本(图2)。会阴部冲洗,确切止血,留置骶前引流管一枚,经臀部引出体外,缝合会阴部切口。
在右侧髂前上棘与脐孔连线的中、外1/3处做一直径约2.5 cm的圆形切口,切除皮肤及皮下组织,顺肌纤维方向分开腹内、外斜肌,切开腹膜,从该切口将切断的回肠断端拉出体外,将近端肠壁与腹膜间断环形缝合固定,再以771D可吸收缝线将肠壁边缘全层与周围皮肤外翻拟括约肌间断缝合一周。确定缝合完整,再次建立气腹,检查手术创面无出血,检查造口处肠管顺畅,用温蒸馏水浸泡冲洗腹腔,吸净,脾窝处留置引流管一枚经附近戳卡控引出体外,停止气腹,排尽积气。拔除Trocar,关闭戳孔,开放造口,手术结束。
三、术后结果
患者手术用时7小时30分,术中出血50 ml,现患者术后6 d,病理尚未回报。患者于术后第1 d排气排便,引流管尚未拔除,会阴部切口愈合尚可。患者术后第2日已离床活动。尿管已经拔除,现排尿通畅。已进流食,排便通畅,尚不成型。术后对症处置,无发热、感染等症状发生。
四、讨论
(一)FAP的临床特征
1. FAP的大肠内表现:FAP的共同特征是结肠腺瘤性息肉,息肉开始生长的平均年龄是15岁,在患者青少年期整个大肠有成百上千的腺瘤性息肉,直径一般小于1 cm,多数是宽基底,大于2 cm的息肉通畅有蒂。组织学类型包括管状及绒毛管状腺瘤,如不预防性切除大肠,100%都可以癌变。
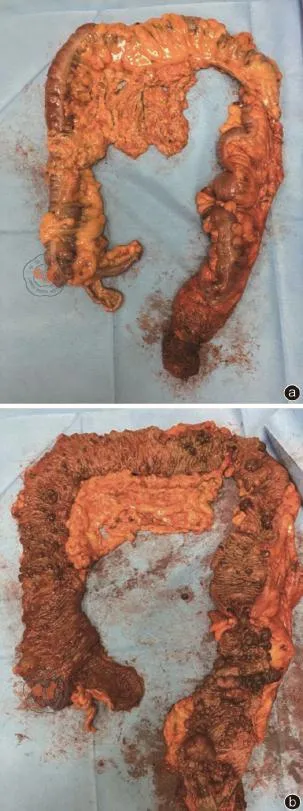
图2 患者术后切除标本图像
2. FAP的大肠外表现:FAP常伴发两种类型胃息肉,基底腺息肉和腺瘤性。前者的发生率约为50%,位于胃体或胃底,散发于胃窦部,病理特征是腺体的扩张及囊性变,即使有异常增生也不会癌变。腺瘤性息肉的发生率为6%,弥漫整个胃粘膜,属于癌前病变[5]。
10%的FAP患者可在四肢末端、腹壁和肠系膜发生硬纤维瘤(DT),一般呈多发性,腹腔内多发于腹壁。DT为良性纤维性肿块,主要来源于间质基底的干细胞层,由高分化成熟的成纤维细胞组成并伴有大量胶原性基质。DT不会发生转移,但呈无规则及侵润性生长,切除后易复发甚至加速生长[6]。
(二)FAP的外科治疗
预防性的手术是当今外科界普遍采用的治疗及预防其癌变的方法。目前主要有三种手术方式[7]:(1)全结肠切除、回肠直肠吻合术(IRA),(2)全结直肠切除、回肠储袋肛管吻合术(IPAA),(3)全结直肠切除、回肠末端造口术。国内较多采用传统开腹手术,对于腹腔镜辅助下行腹腔大范围的结肠游离切除手术,其可行性和安全性尚不能统一意见。Marcello等[8]与Seshadri等[9]对腹腔镜下全结肠切除与传统开腹手术进行了对比研究,发现肠道功能运动恢复时间,住院天数明显短于传统开腹手术,长期的术后并发症显著减少。腹腔镜全结肠切除在治疗FAP患者上技术是可行的,同时具有微创、安全,术中出血少,住院时间短等优点[10]。
进年来3D腹腔镜技术在肠道手术中的应用逐渐增多,但应用3D腹腔镜性全结肠切除术的报道较少,尚无法形成比较。其3D腹腔镜的立体解剖层次清晰、术者的纵深感好等优点在此例患者的治疗中都有体现。同时该患者未行腹部辅助切口,日后对患者的生理和心理的康复均是有益的,这与王锡山教授[11]提出的类Notes术式类似。本例患者采用逆时针方向游离肠管,较少变换腹腔镜屏幕的频率和次数,给术者带来了较为流畅和舒适的操作感受。同类患者笔者认为应推荐此种手术方式。
[ 1 ] Rustgi AK. The genetics of hereditary colon cancer. Genes Dev,2007,21(20):2525-2538.
[ 2 ] 董立国,蒲永东,何建苗.家族性结肠息肉病患者的诊断及治疗.中国优生及遗传杂志,2008,16(11):111-112.
[ 3 ] 赵摇亮,何若冲,畅任伟,等.家族性腺瘤息肉病6例报告并国内文献复习.山西医科大学学报,2011,42(7):586-588.
[ 4 ] Jacobs M,Verdeja JC,Goldstein HS. Minimally invasive colon resection(laparoscopic colectomy). Surg Laparosc Endosc,1991,1(3):144-150.
[ 5 ] Kashiwagi H,Spigelman AD.Gastroduodenal lesions in familial adenomatous polyposis.Surg Today,2000,30:675-682.
[ 6 ] 于恩达,徐晓东,孟荣贵.家族性腺瘤性息肉病的临床特点及研究现状.第二军医大学学报,2006,27(4):349-352.
[ 7 ] Church J,Simmang C. Practice parameters for the treatment of patients with dominantly inherited colorectal cancer (familial adenomatous polyposis and hereditary nonpolyposis colorectal cancer). Dis Colon Rectum,2003,46(8):1001-1012.
[ 8 ] Marcello PW,Milsom JW,Wong Sk,et al.Laparoscopic total colectomy for acute colitis:a case-control study.Dis Colon Rctum,2001,44:1441-1445.
[ 9 ] Seshadri PA,Poulin EC,Schlachta CM,et al.Does a laparoscopic approach to total abdominal colectomy and proctocolectomy offer advantage?Surg Endosc,2001,15:837-842.
[ 10 ] 冯波,郑敏华,陆爱国,等.腹腔镜全结直肠切除治疗家族性腺瘤性息肉病伴癌变.中华消化内镜杂志,2004,21(1):9-12.
[ 11 ] 王锡山.结直肠肿瘤类-NOTES术之现状及展望[J/CD].中华结直肠疾病电子杂志,2015,4(4):367-372.
(本文编辑:杨明)
马天翼, 黄睿, 汤庆超, 等. 3D腹腔镜下逆时针全结直肠切除术治疗FAP患者一例(附视频) [J/CD].中华结直肠疾病电子杂志.2015, 4(6):682-685.
10.3877/cma.j.issn.2095-3224.2015.06.27
150086 哈尔滨医科大学附属第二医院 哈尔滨医科大学大肠癌研究所
陈瑛罡,Email:chygang777@163.com
(2015-12-14)
