经硫脲改性后的酸化缓蚀剂的研究
2015-08-20李克华杨冰冰兰志威
李克华,杨冰冰,兰志威
(长江大学化学与环境工程学院,湖北荆州 434023)
酸化处理是提高油井采收率的重要措施,但酸液的注入会严重腐蚀石油管道及设备,因此,合成具有优异缓蚀性能的缓蚀剂具有重要意义[1-2]。传统的酸化缓蚀剂如炔醇类、铬酸盐及砷酸盐类由于对环境污染较大,已逐渐被限制使用[3-4]。曼尼希碱缓蚀剂是一种典型的吸附膜型缓蚀剂,由醛酮胺缩合而成,是目前油气田开采过程常用缓蚀剂之一,可有效阻止酸液对金属材料的腐蚀且对环境危害较小,具有良好的研究前景。
缓蚀性能良好的缓蚀剂大多是含杂原子(如O,N,S)类的有机化合物,正是由于杂原子的存在才使这些有机化合物吸附在钢铁表面上,从而起到保护铁的作用。从分子的结构上来说,分子中同时含N和S的一类化合物比只含单一的N或S的一类化合物缓蚀性能好[5-7]。硫脲因其分子结构中含硫代碳酰(C=S)键和N原子,可提供孤对电子与金属表面生成配位键,阻止腐蚀反应的进行对铁具有很好的缓蚀效果,因此,常用作金属缓蚀剂。笔者根据Mannich反应原理,探索了以硫脲、肉桂醛和苯乙酮为原料合成曼尼希碱的方法,评价该缓蚀剂的缓蚀性能并探讨其吸附行为。
1 实验
1.1 实验基材及其前处理
腐蚀实验测试钢片为N80钢片,其组成成分为:0.24%C,0.22%Si,1.19%Mn,0.013%P,0.004%S,0.036%Cr,0.021%Mo,0.028%Ni,剩余部分由 Fe组成。试片用 200#,400#,800#,1200#金相砂纸打磨,于丙酮溶液中除去油污,再放入无水乙醇中浸泡1 min,吹干,干燥待用。电化学测试中工作电极是N80钢,工作电极表面用环氧树脂进行封涂处理,测试面积0.3 cm2。
硫脲、苯乙酮、肉桂醛,均为分析纯;15%HCl溶液,由质量分数为37%分析纯盐酸用蒸馏水稀释得到。
1.2 缓蚀剂的合成
在装有冷凝管、温度计、磁力搅拌器的三口烧瓶中,加入一定量的肉桂醛、硫脲(0.025 mol)和苯乙酮,再加入10 mL无水乙醇做溶剂,滴加浓盐酸调节pH。将三口烧瓶置于恒温水浴锅中,在一定温度下搅拌加热,回流数小时后,所得的液体即为曼尼希碱缓蚀剂。
1.3 缓蚀剂的测试与表征
失重法采用的实验材质是N80钢片,参照中华人民共和国石油与天然气行业标准SY/T 5405—1996《酸化用缓蚀剂性能试验方法及评价指标》中的静态挂片失重法,在15% 盐酸介质中加入一定质量分数的缓蚀剂,4 h后在60℃下测定N80钢试片的腐蚀速率,以此评价缓蚀性能。每组实验平行测量3次取平均值。腐蚀速率(ν)的计算公式为:

式中,ν为腐蚀速率,g/(m2·h);w0和w分别为反应前和失重后钢片的质量,g;s为钢片的面积,m2;t为反应时间,h。
通过腐蚀速率的计算,缓蚀效率(η)的计算公式为:

式中,v0和v分别为空白和加入缓蚀剂后的腐蚀速率。
电化学测试采用传统的三电极体系[8]。测试仪器为辰华CHI660C电化学工作站,辅助电极为铂电极,参比电极为饱和甘汞电极,工作电极由N80钢加工而成,测试温度20℃,极化曲线测试扫描范围-200~-500 mV,扫描速率5 mV/s,交流阻抗测试的频率范围为0.1~10 kHz,交流激励信号幅值5 mV,极化曲线参数和交流阻抗参数分别由Cview和Zview软件拟合得到。
2 结果与讨论
2.1 合成条件的优化
试验结果见表1。
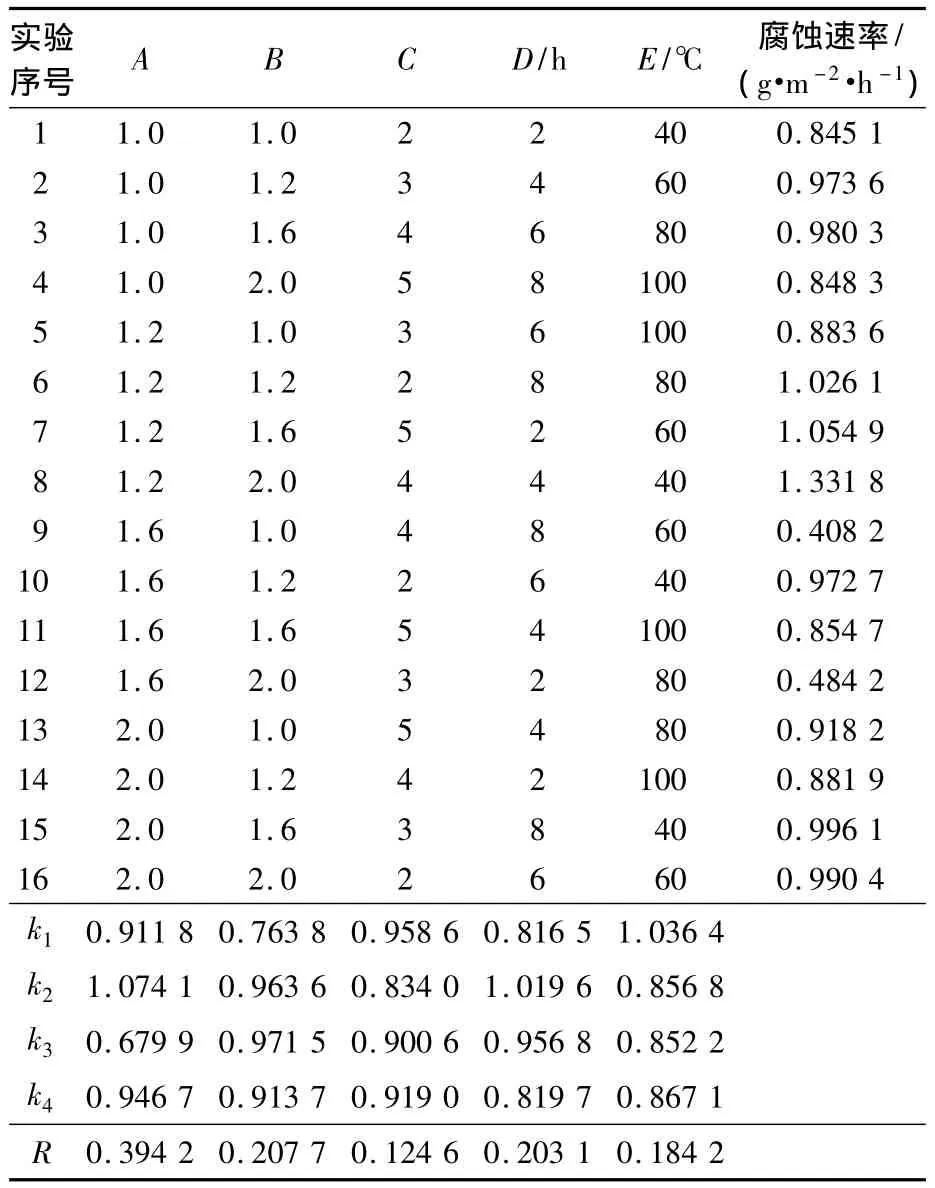
表1 正交试验设计及分析
表1参数说明:以质量分数为15%的盐酸中N80钢片的腐蚀速率为评价指标,挂片腐蚀温度为60℃,腐蚀时间为4 h,缓蚀剂加量为1.0%,确定醛胺物质的量比(A)、酮胺物质的量比(B)、反应体系pH(C)、反应时间(D)、反应温度(E)5个因素,设计5因素4水平正交试验,试验结果见表1。
由表1可知,各因素对腐蚀速率的影响顺序为:A>B>D>E>C。最佳合成条件为:A3B1C2D1E3,按照最佳条件合成的缓蚀剂M-17腐蚀速率为0.852 3 g/(m2·h)。综合考虑,确定最佳合成条件为:n(醛)∶n(胺)=1.6,n(酮)∶n(胺)=1,体系pH为4,反应时间为8 h,反应温度为60℃。
2.2 缓蚀剂性能评价
2.2.1 盐酸质量分数对缓蚀性能的影响
以最佳合成条件制备曼尼希碱缓蚀剂,缓蚀剂加量1.0%,试验温度60℃,试验时间4 h,试验压力为常压的条件下,考察盐酸质量分数对腐蚀速率的影响,结果见图1。

图1 盐酸质量分数对腐蚀速率的影响
从图1看出,随着盐酸质量分数增加,腐蚀速率逐渐增大。当盐酸质量分数小于25%时,腐蚀速率小于0.926 4 g/(m2·h),优于石油天然气行业标准中一级酸化缓蚀剂指标。表明该缓蚀剂能满足现场低浓度酸化施工的要求。
2.2.2 缓蚀剂加量对缓蚀性能的影响
固定其他条件,盐酸质量分数为15%,考察曼尼希碱缓蚀剂加量对腐蚀速率的影响,结果见图2。随着缓蚀剂加量增加,腐蚀速率明显下降。当缓蚀剂加量(质量分数,下同)大于1.0%时,腐蚀速率降至0.401 3 g/(m2·h)以下,优于SY/T 5405—1996《酸化用缓蚀剂性能试验方法及评价指标》中一级标准。

图2 缓蚀剂加量对腐蚀速率的影响
2.2.3 缓蚀剂的极化曲线图
在15%HCl体系中,分别加入不同加量的曼尼希碱缓蚀剂,测其极化曲线,以极化电位E对极化电流密度的对数lg[I]作图,结果见图3,表2为其极化曲线参数。
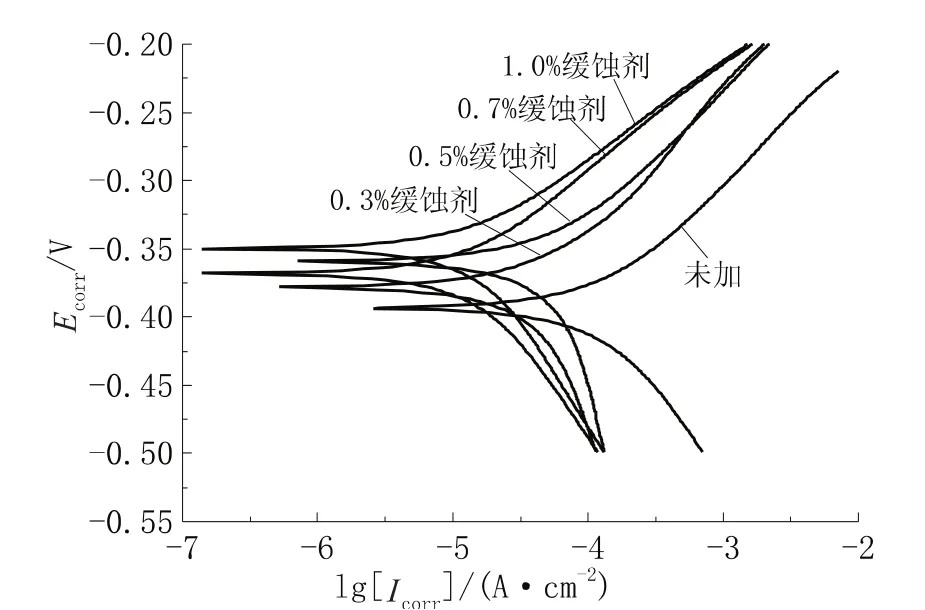
图3 15%盐酸中不同加量的曼尼希碱缓蚀剂的极化曲线
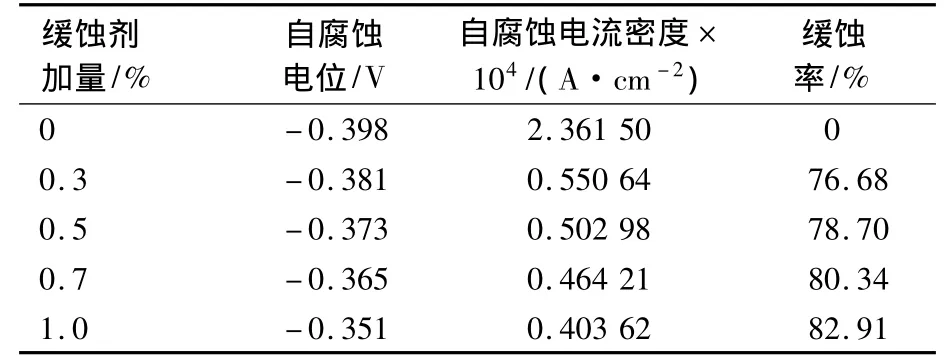
表2 15%盐酸中不同加量缓蚀剂的极化曲线参数
由图3可知,在15%HCl中添加缓蚀剂后,N80钢的自腐蚀电流减小,说明腐蚀反应速率减小;由表2可知,加入缓蚀剂后,N80钢的自腐蚀电位与空白比较,发生了正移,说明该缓蚀剂是抑制阳极腐蚀过程为主的混合型缓蚀剂。随着缓蚀剂加量增大,缓蚀能力加强。当缓蚀剂加量为1.0%时,缓蚀效果最好。
2.2.4 交流阻抗实验结果
20℃时在15%盐酸中分别加入不同加量缓蚀剂,进行交流阻抗实验,结果见图4。

图4 15%盐酸中不同加量缓蚀剂的交流阻抗Nyquist图
由图4可知,在Nyquist图中均出现了较规则的半圆容抗弧,随着缓蚀剂加量增大,容抗弧半圆直径增大,说明缓蚀效率随着缓蚀剂加量增大而显著增加。缓蚀剂加量为1.0%时,缓蚀效果最好,这与极化曲线的结论相符。
2.3 缓蚀剂在N80钢表面的吸附机理研究
2.3.1 缓蚀剂对N80钢的吸附行为
为了研究缓蚀剂在N80钢表面的吸附热力学,60℃下用挂片失重法测定N80钢片在添加不同加量缓蚀剂的15%盐酸中的腐蚀速率。通常情况下,实验测得的缓蚀率η近似等于表面覆盖率θ[9]。假设缓蚀剂分子在N80钢表面的吸附规律服从Langmuir吸附等温公式:

式中,c为缓蚀剂的浓度,mol/L;θ为缓蚀剂在金属表面的覆盖率,%;K为Langmuir吸附平衡常数。将吸附等温公式变形得到以下公式:

若以上假设成立,c/θ与c应为线性关系,以c/θ为纵坐标,c为横坐标作图,并对数据进行线性拟合得到一条相关系数为0.999 8的直线,如图5所示。当温度为60℃时c/θ与c作图为一条直线,表明该温度下缓蚀剂在N80钢表面的吸附符合Langmuir吸附等温式。缓蚀剂在碳钢上形成单分子层吸附,从而起到缓蚀作用。

图5 缓蚀剂在N80钢片的等温吸附曲线
2.3.2 缓蚀剂的加入对腐蚀体系活化能的影响
为了研究加入缓蚀剂后腐蚀体系活化能的改变,在15%盐酸溶液分别不加和加入1%的缓蚀剂,测试其在30~70℃下的腐蚀速率。腐蚀速率与温度间的关系符合Arrhenius公式,则有:

式中,vcorr为腐蚀速率,g/(m2·h);Ea为表观活化能,kJ/mol;R为摩尔气体常量;T为热力学温度,K;A为指前因子,也称频率因子。将(1)式两边取对数得:lnvcorr=lnA-Ea/RT,以1/T为横坐标,lnvcorr为纵坐标,作图得直线,由直线的斜率可得表观活化能,由截距可得指前因子。曼尼希碱缓蚀剂的Arrhenius曲线见图6。

图6 缓蚀剂的Arrhenius曲线
根据图6的拟合参数,未加和加入缓蚀剂的活化能分别为 12.030,20.089 kJ/mol。这表明随着缓蚀剂的加入,增加了反应的活化能,从而减小腐蚀速率,有效地抑制反应的进行。
3 结论
1)以硫脲、肉桂醛、苯乙酮为原料合成曼尼希碱,试验结果表明,该缓蚀剂在酸性介质中具有优良的缓蚀性能。正交试验结果得其合成条件为:n(醛)∶n(胺)=1.6,n(酮)∶n(胺)=1,体系pH为4,反应时间为8 h,反应温度为60℃。
2)极化曲线测试表明:以硫脲为原料合成的曼尼希碱缓蚀剂是以抑制阳极腐蚀过程为主的混合型缓蚀剂。交流阻抗测试表明:随着缓蚀剂加量增大,半圆容抗弧的直径变大,缓蚀剂的缓蚀效率显著增加。
3)曼尼希碱缓蚀剂在N80钢铁表面的吸附符合Langmuir吸附等温方程。
[1]胡鹏程,李克华,李久启,等.新型酸化缓蚀剂的合成及性能[J].断块油气田,2011,18(2):261 -263.
[2]吴兰兰,李克华,金明皇,等.曼尼希碱酸化缓蚀剂的合成及性能评价[J].精细石油化工进展,2012,13(5):40 -42.
[3]何新快,陈白珍,张钦发.缓蚀剂的研究现状与展望[J].材料保护,2003,36(8):1 -3.
[4]杨雪莲,常青.缓蚀剂的研究与进展[J].甘肃科技,2004,20(1):79-81.
[5]Ali S A,Al-Muallem H A,Saeed M T,et al.Hydrophobictailed bicycloisoxazolidines:a comparative study of the newly synthesized compounds on the inhibition of mild steel corrosion in hydrochloric and sulfuric acid media[J].Corrosion Science,2008,50(3):664 -675.
[6]Singh A K,Quraishi M A.Inhibiting effects of 5 -substituted isatin-based Mannich bases on the corrosion of mild steel in hydrochloric acid solution[J].Appl Electrochem,2010,40(7):1293-1306.
[7]Ali S A,Saeed MT,Rahman S U.The isoxazolidines:a new class of corrosion inhibitors of mild steel in acidic medium[J].Corrosion Science,2003,45(2):253 -266.
[8]曹楚南.腐蚀电化学原理[M].3版.北京:化学工业出版社,2008:211-212.
[9]王招娣,司云森,余强,等.一种曼尼希碱在酸性介质中对碳钢缓蚀行为的研究[J].表面技术,2011,40(1):59 -62.
