电驱动膜过程在氨基酸发酵液处理中的研究进展
2015-08-19柴萍王建友卢会霞
柴萍,王建友,卢会霞
(南开大学环境科学与工程学院,天津300071)
氨基酸是蛋白质分子的基本组成单位,是生物有机体的重要组成部分,其在食品、制药、化工等领域有广泛的应用[1]。氨基酸的生产方法有蛋白质水解法、酶促转化法、微生物发酵法等多种。其中,微生物发酵法是最常见的氨基酸生产方法[2]。由于发酵液中含有各种微生物、原料、无机盐及中间产物,因此需要后续工艺对发酵液进行分离纯化以提取目标产物。传统的沉淀、酸化、结晶、蒸馏、离子交换和吸附等工艺都不同程度地存在工艺流程长、收率低、能耗高、化学试剂消耗、环境污染等问题[3]。因此,需要进一步研究开发经济性好、环境友好的发酵液分离纯化新技术,以减少环境污染、缩短处理工艺、提高生产效率,此举具有重要的社会、环境与经济价值。
氨基酸是一种两性电解质,同时含有酸性官能团—COOH和碱性官能团—NH2,其荷电性主要取决于溶液的pH值。当溶液pH值在其等电点(isoelectricpoint,pI)时,氨基酸所带的正负电荷数相等,此时其呈现电中性;当溶液pH值大于等电点时,氨基酸以阴离子形式存在;反之则以阳离子形式存在[4-5]。该特性使得电驱动膜分离技术可以用于氨基酸发酵液处理。
电驱动膜过程(electro-membraneprocess,EMP)是一类基于电渗析技术(electrodialysis,ED)的膜分离过程的统称。ED是以电位差为推动力,利用阴、阳离子交换膜的选择透过性,实现溶液中电解质的脱除或富集,其在废水处理、海水淡化、重金属回收、有机酸制备等领域已有诸多报道[2,6-8]。近年来,随着离子交换膜的发展及膜堆构型的改进,双极膜电渗析(bipolarmembraneelectrodialysis,BMED)、离子取代电渗析(ion-substitution electrodialysis,ISED)、电 复 分 解 反 应 器(electrometathesis,EMT)等一系列新的电膜过程逐渐出现[6,9]。如图1所示,其在氨基酸生产中的研究报道呈逐渐上升的趋势。本文介绍了国内外近年来电膜过程在氨基酸生产中的分离、脱盐、浓缩和转化等方面的研究进展,并对其发展趋势及应用前景进行了展望。
1 膜堆构型
1.1 普通电渗析
普通电渗析即两电极间阴阳离子交换膜交替排列,其常用于电解质溶液的脱盐或浓缩。图2(a)所示的普通电渗析可以用于混合氨基酸的分离,氨基酸等电点的差异使得在同一pH值条件下不同类型的氨基酸所呈现的荷电性相同。原料液pH值为中性时,酸性氨基酸(AA-)以阴离子形态存在,可以透过阴离子交换膜向酸室迁移;碱性氨基酸(AA+)以阳离子形态存在,可以透过阳离子交换膜向碱室迁移;而中性氨基酸(AA±)呈电中性,不发生迁移,仍保留在原料液中。
普通电渗析还可用于发酵液中无机盐的去除[图2(b)]。调节发酵液pH值至其等电点附近,其中的氨基酸盐转化为电中性的氨基酸(AA±),此时无机盐离子在电场作用下向相邻隔室迁移而氨基酸仍保留在原料液中,实现了发酵液中无机盐的去除。与传统的离子交换法除盐相比,ED脱盐有效地避免了树脂再生所需的酸碱消耗。
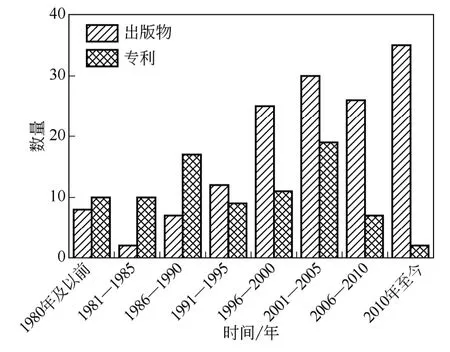
图1 电驱动膜过程在氨基酸生产中应用的发展趋势
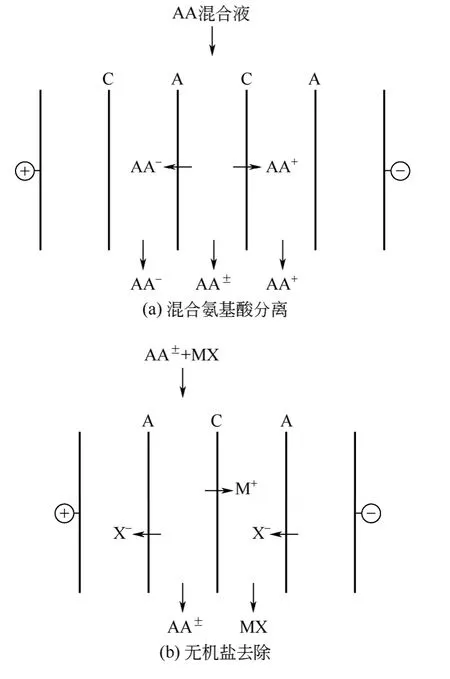
图2 ED原理示意图
1.2 双极膜电渗析
在采用ED进行氨基酸分离及脱盐时需要消耗酸碱试剂或者缓冲溶液以调节发酵液pH值,在这一过程中,难免会引入其他杂质离子,不仅影响了产品纯度还增加了处理负荷。双极膜是一种新型的离子交换复合膜,其可以使水分子解离成H+和OH-,因此双极膜电渗析(bipolarmembrane electrodialysis,BMED)可以在不引入新组分的情况下有效地调节溶液的pH值。如图3(a)所示,将氨基酸混合液通入碱室,双极膜水解离产生的OH-使得碱室pH值升高,此时酸性氨基酸将以阴离子形态存在透过阴膜进入到酸室中,而碱性氨基酸将保留在碱室,实现了氨基酸的分离。
此外,BMED也可将氨基酸盐转化为氨基酸。以酸性氨基酸为例,采用BP-C-BP的膜堆构型[图3(b)]将发酵产物——氨基酸盐(Na-AA)通入酸室,Na+将透过阳膜进入碱室,酸室中即可得到对应的氨基酸。同理,采用BP-A-BP的膜堆构型也可实现碱性氨基酸的转化。然而,两室BMED所存在的问题在于所得到的产品液(氨基酸)与原料液(氨基酸盐)处于同一隔室中,若无机盐离子迁移不彻底,将影响产品纯度。BP-A-C-BP的三室BMED构型可有效解决这一问题。原料液从中间隔室进入,无机盐离子及氨基酸盐离子分别向两侧隔室迁移,所得产品纯度可大幅提高。
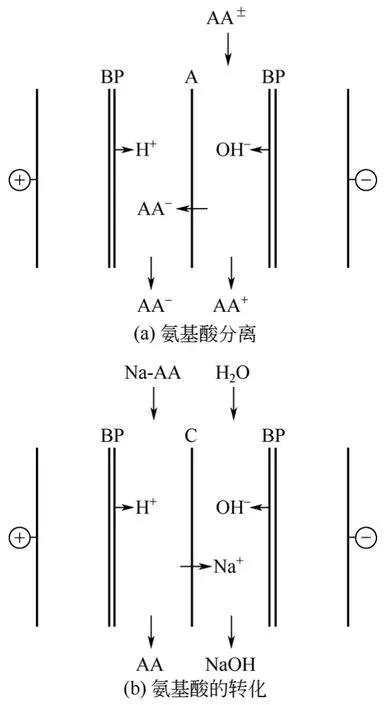
图3 BMED原理示意图
1.3 离子取代电渗析
氨基酸盐到氨基酸的转化实际上即是以H+或OH-取代其中的无机盐离子的过程,该过程也可在不使用双极膜的情况下,通过膜堆构型的调整,利用无机酸碱或电极反应提供的H+和OH-得以实现,此类电渗析被称之为离子取代电渗析(ion-substitutionelectrodialysis,ISED),如图4(a)所示。此外,电复分解反应器(electrometathesis,EMT)也是ISED的一种变形,其中含有原料液、产品液各两种,可以实现两种原料液间的复分解反应,其反应可简述为:AX+BY—→AY+BX。
2 在氨基酸生产中的应用
2.1 混合氨基酸分离
表1列出了文献中介绍的电驱动膜过程在混合氨基酸分离中的应用。由表1可见,EMP技术对于等电点相差较大的混合氨基酸的分离可取得良好的效果。且等电点相差越大,分离效果越好。
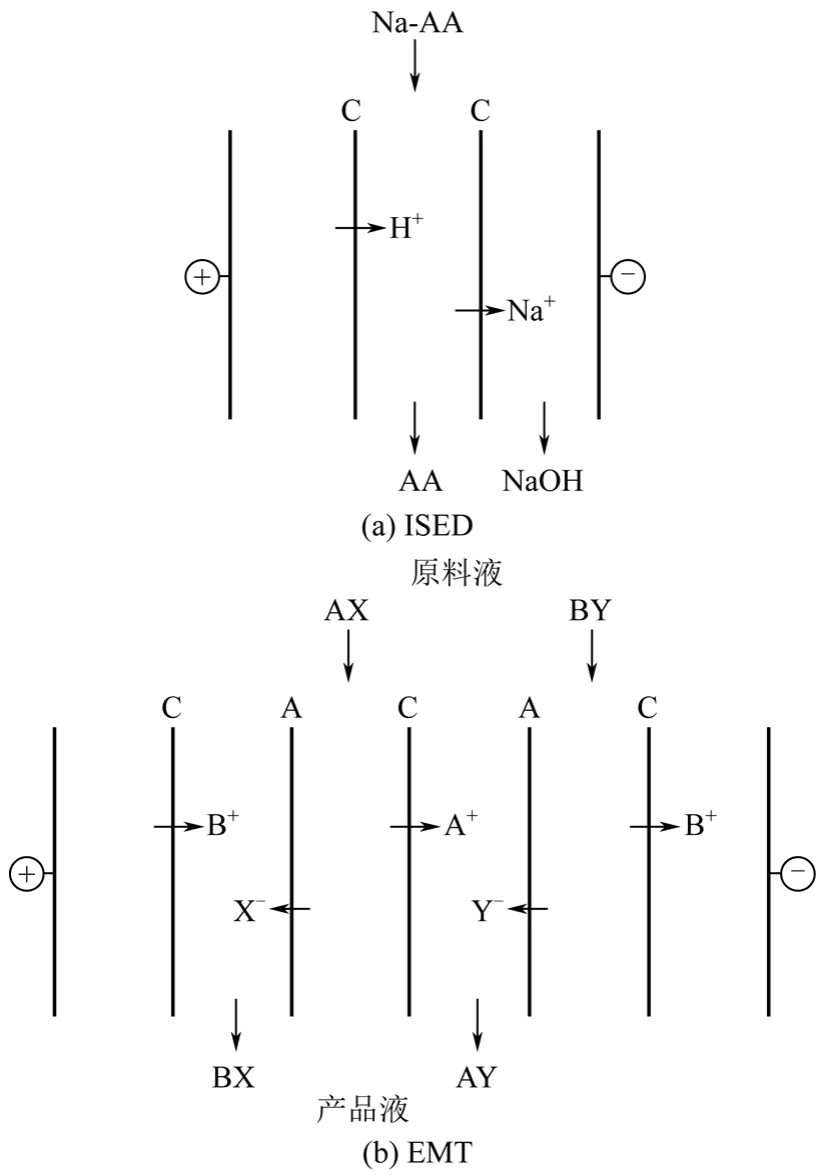
图4 ISED及EMT原理示意图
然而,在ED分离混合氨基酸的过程中,屏蔽效应(barriereffect)[12,15]是影响分离过程的一个重要因素,其原理如图5所示。随着分离过程的进行,原料室中的离子数量减小,原料室侧膜表面浓差极化加剧,发生水解离。在阴膜表面,水解离产生的OH-透过阴膜,H+被拦截,致使原料室侧阴膜表面pH值降低。酸性氨基酸在原料室pH值呈中性时带负电荷,透过阴膜向正极移动。在发生水解离之后,阴膜附近pH值降低,酸性氨基酸所带负电荷减少甚至呈中性或者带正电荷,此时,其又会改变迁移方向向负极移动。在阳膜表面,水解离使得其膜表面pH值呈碱性,氨基酸荷电性又发生改变。如此循环往复,氨基酸的迁移受到抑制,电流效率降低[16]。这一屏蔽效应的发生会降低装置的分离性能、增加能耗,因此应尽量避免。提高流速、强化传质、降低边界层厚度、提高极限电流密度是避免屏蔽效应发生的有效方法,此外,及时调整操作电流、保证在极限电流密度下运行也可以有效防止屏蔽效应的产生[4,7]。

图5 屏蔽效应原理示意图[4]
2.2 无机盐去除
电渗析技术在溶液脱盐领域已经发展的较为成熟,在此利用图2(b)的膜堆构型也可以实现发酵液中无机盐的去除。谷氨酰胺(Gln)是谷氨酸(Glu)的γ-羧基酰胺化物,在生命活动中起着重要作用,其生产方法以微生物发酵法为主。离子交换法可以有效地分离发酵液中的Gln,然而发酵液中存在的硫酸铵严重影响了Gln的分离效果。为此Shen等[17]利用ED技术预先对Gln发酵液中的硫酸铵进行脱除。结果表明,控制溶液pH值在Gln等电点5.65附近,此时硫酸铵的去除率达到96.01%,Gln的损失率仅有0.0467%。此外,Elisseeva等[18]和Aghajanyan等[19]也分别研究了ED用于甘氨酸(Gly,5.97)和脯氨酸(Pro,6.30)发酵液中无机盐的去除,也获得良好效果。值得注意的是,在混合氨基酸分离时对过程不利的屏蔽效应在脱盐过程中又能有效地避免氨基酸的损失。因此,电流密度等操作参数的选择应视实验目的而定。

表1 电驱动膜过程在氨基酸分离中的应用
2.3 氨基酸制备
谷氨酸广泛应用于食品、制药等领域。目前工业上常用等电结晶工艺从发酵液中提取谷氨酸,但是等电母液中残留1%~2%的谷氨酸盐。Kumar等[20]提出利用ISED技术回收等电母液中的谷氨酸,同时采用了两种不同膜堆构型的ISED进行对比实验研究,一种是仅含有阳离子交换膜的3室ISED,另一种是同时含有阴阳离子交换膜的4室ISED。后者在两张阳离子交换膜中间放置一张阴离子交换膜以获得纯度更高的产品,然而结果发现虽然4室ISED所得产品纯度较高,但由于有机离子的迁移性较弱,其能耗较高、收率较低。
ISED技术不仅可用于酸性氨基酸的转化,也可用于碱性氨基酸的转化。赖氨酸是一种碱性氨基酸,是人体第一必需的氨基酸。其不易存储,通常以赖氨酸盐酸盐(L-Lys·HCl)的形式存在,使用前需将Cl-去除。Zhang等[21]利用阴极室电解水产生的OH-,将L-Lys·HCl转化为赖氨酸(L-Lys,pI=9.74)。该作者考察了操作电压、Lys·HCl溶液浓度和初始Lys·HCl溶液pH值对过程的影响,结果发现在Lys·HCl溶液pH值为其等电点为9.74时,Lys的回收率达到最大值93.2%。
Cauwenberg等[22]采用BP-C-BP结构的BMED将氨基酸钠盐转化为氨基酸。酸室中加入待处理的氨基酸钠盐溶液(pH值为10~11),其中的Na+在电场作用下透过CEM进入到碱室,与BPM水解离产生的OH-结合形成NaOH。酸室中,BPM水解离产生H+使得氨基酸钠盐转化为氨基酸。然而,由于该作者使用的氨基酸的pI值在5~6范围内,在原料液pH值呈碱性时,氨基酸以阴离子形态存在,其会在电场作用下向双极膜的阳膜侧迁移;而此处水解离产生的H+使得pH值降低,氨基酸易在BPM的阳膜侧结晶析出产生沉淀。为解决此问题,该作者提高了溶液温度以增加氨基酸的溶解度,待溶液流出电渗析装置,再降低温度使其结晶析出。
Zhang等[23]采用BP-A-BP结构的BMED从谷氨酸发酵液等电结晶后的上清液中回收谷氨酸。原料液中的谷氨酸根离子在电场力作用下透过阴膜向酸室迁移,并在此与双极膜水解离产生的H+结合形成HGA,可保证产品液的纯度。在初始GA-浓度为13g/L条件下,20V恒压运行3h,GA的收率为72.1%,纯度较高。
在利用ISED或BMED将氨基酸盐转化为氨基酸的过程中,都存在一个产品液与原料液同处于一个隔室中的问题,影响产品纯度。该问题可以通过调整膜堆构型使氨基酸盐离子从原料室迁移出,在转化的同时实现氨基酸的分离,提高产品纯度。然而,由于有机离子的迁移性较弱,在相同收率条件此举会增加过程能耗。Fu等[24]比较了不同构型的BMED在相同条件下将琥珀酸钠转化为琥珀酸的性能,虽然其处理对象并非氨基酸,但同样都是分子量较大、迁移性较弱的有机酸,得到了相似的结果。
采用BMED制备氨基酸无需额外添加其他化学试剂以提供H+。据理论计算,制备1mol/L25℃的酸和碱,双极膜的理论电势只有0.83V,而电解需2.1V[25]。因此,BMED制备有机酸较利用电极反应提供H+或OH-的ISED可降低能耗。此外,BMED在得到产品氨基酸的同时会生成NaOH、氨水等副产物,可以将其回流至发酵罐用于发酵液pH值的调节,节约了生产成本。然而,双极膜的成本要远高于普通的离子交换膜,这也在一定程度上限制了其发展。
2.4 氨基酸盐制备
为从谷氨酸发酵液(主要成分为谷氨酸铵)中直接提取谷氨酸钠(味精),避免传统等电结晶、离心分离、离子交换、酸碱中和等复杂工序,丛威[26]和李方伟[27]分别采用图4(b)所示的EMT技术以模拟发酵液和无机钠盐(NaCl或Na2SO4)为原料制备谷氨酸钠。该技术可大幅缩短工艺流程,实现发酵液到产品的一步转化,同时还避免了传统提取工艺的酸碱消耗及对环境的二次污染,所得副产物硫酸铵或者氯化铵又可用于化肥的生产。实验结果表明,在谷氨酸铵浓度为115g/L、Na2SO4浓度为0.7mol/L、电流密度为15mA/cm2条件下,制取1kg NaGA的 能 耗 为1.21kW·h,膜 通 量 约 为2 mol/(m2·h)。
本文作者所在课题组樊改肖[28]尝试采用电去离子(electrodeionization,EDI)技术实现该过程,即在原料室中填充混床离子交换树脂以促进GA-迁移,提高过程性能。在相似实验条件下,能耗可降至0.938kW·h/kg谷氨酸钠,膜通量升至3mol/(m2·h)。EMT技术为NaGA的清洁生产提供了新的思路。
此外,Boniardi等[29]和Wang等[30]分别以乳酸钠(乳酸铵)和H2SO4为原料利用EMT技术制备乳酸,同时副产(NH4)2SO4,说明该技术也同样适用于其他有机酸碱的制备。
3 工艺优化与集成
3.1 工艺改进
对于等电点相差较大的氨基酸,通过溶液pH值的调节可以比较容易地实现分离,然而对于等电点相近的氨基酸分离效果不佳。为此,研究者提出了利用酶转化法,使得某一种氨基酸在特定的脱羧酶的作用下转化为不带电或者荷电性与另一种氨基酸不同的胺类化合物,再进一步实现二者的分离。为分离Glu(3.22)和Asp(5.41),KattanReadi等[4]将Glu在谷氨酸脱羧酶(GAD)的作用下转化为γ-氨基丁酸(GABA),在pH值为6时Asp带负电荷GABA不带电,可通过ED进一步实现Asp的分离,Asp的回收率可达到90%。类似地,Teng等[31]将Lys在赖氨酸脱羧酶(LDC)的作用下转化为1,5-戊二胺(PDA),在pH值大于11时,Arg呈电负性,PDA呈电中性,经过ED可以实现Arg的分离。酶转化法与ED的结合为等电点相近的氨基酸的分离提供了新的思路。
袁中伟等[32]采用多级连续电渗析技术分离Ser(5.68)和Pro(6.30)。如图6所示,多级电渗析是一个类似于精馏的过程,透膜阴离子流和料液流彼此逆向流动,经过逐级透膜迁移,迁移较多的Ser在左侧富集,而迁移较少的Pro在右侧富集。级数、电流及NaOH浓度的变化都将影响产品的纯度。为了使二者都保持较高的产品纯度,该作者又增加了回流液[33],回流液中的Ser可以将透膜迁移的Pro-转化为Pro±,使之随物料往下游流动,以提高Ser产品的纯度。最终所得Ser及Pro产品纯度都达到了90%以上。
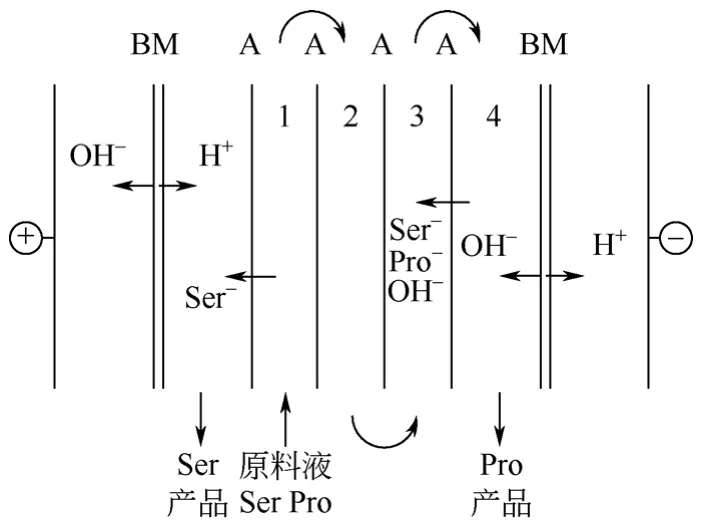
图6 多级连续电渗析原理示意图[32]
3.2 膜的改进
在电驱动膜过程中,离子交换膜的性能是影响实验结果的关键因素之一,为了得到理想的处理效果,在进行工艺改进的同时,研究者也在不断开发研究新型膜材料。
3.2.1 荷电镶嵌膜
在用ED脱除发酵液中的无机盐过程中,发酵液pH值的控制是一个重要影响因素。若pH值控制不当,氨基酸也将以氨基酸盐离子形态存在,在无机盐离子去除的同时会损失氨基酸。为此,Sato等[34]为提高无机盐的去除率同时降低氨基酸的损失,使用了含有荷电镶嵌膜(charge-mosaic membrane)的ED分别对含有NaCl的谷氨酸(Glu)溶液和精氨酸(Arg)溶液进行脱盐,同时采用普通电渗析进行对比实验研究。
荷电镶嵌膜是一种两性膜,其中含有一系列规则排列的阴阳离子交换基团,其原理如图7所示。阳极室和阴极室中分别通入H2SO4和NaOH溶液。在电场的作用下,混合液中的Na+透过荷电镶嵌膜的阳离子交换区域进入到阴极室;阴极室中的OH-透过阴离子交换区域进入到脱盐室中。Cl-和H+的迁移同理。OH-的迁入使脱盐室中靠近阴极侧的区域pH值较高,氨基酸带负电荷;而H+的迁入使脱盐室中靠近阳极侧的区域pH值较低,氨基酸带正电荷。在电场作用下脱盐室中的氨基酸都会向远离膜表面方向迁移,进而可降低氨基酸透过膜而造成的损失。
实验结果表明,采用含有荷电镶嵌膜的ED对Glu和NaCl混合液脱盐,过程运行120min时脱盐率达到97%,Glu的损失率只有8%。与此相比,CED在过程运行80min时脱盐率亦达到98%,但同时损失了80%的Glu。其对Arg和NaCl混合溶液脱盐也得到了相似的实验结果。由此可见,荷电镶嵌膜的使用可以明显改善CED脱盐过程中氨基酸的损失,但由于其制作成本高于普通的离子交换膜,投资成本也随之提高。
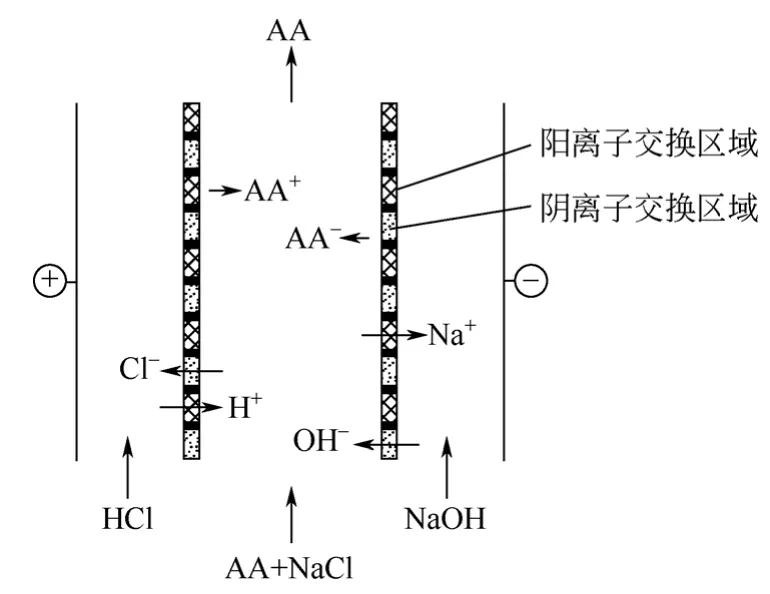
图7 含有荷电镶嵌膜的ED工作原理示意图[34]
3.2.2 sBPM膜
由于氨基酸的两性特性,pH值的微小改变就可能引起氨基酸荷电性的变化,这将会降低产品的回收率或者纯度,KattanReadi等[35]提出了一种sBPM膜(segmentedbipolarmembrane),其中单极区域与双极区域交替排列。这使得Etn+能透过单极区域,而双极区域的水解离又可同时调节pH值。在中性pH值条件下从Ala中分离Etn+。结果发现使用sBPM后,产品收率、能耗与传统CEM相当,产品纯度可达到100%,Ala全部保留在原料液中。然而其单极区域与双极区域的比例分布还需进一步优化。
3.2.3 MMMs膜
酶转化法可以实现等电点相近的氨基酸的分离,然而酶转化与后续的分离需在两个独立的反应器中进行。KattanReadi等[36]提出了一种MMMs膜(mixedmatrixmembranes),如图9所示,其可为酶转化提供一个平台,将其放置在电渗析其中可以使酶转化与分离同时完成。该作者以Glu为例,在该装置中Glu的转化率可达33%,电流效率和能耗分别为40%和3kW·h/kg。此膜的开发可以进一步缩短处理工艺,但其酶转化效果还有待于进一步提高。
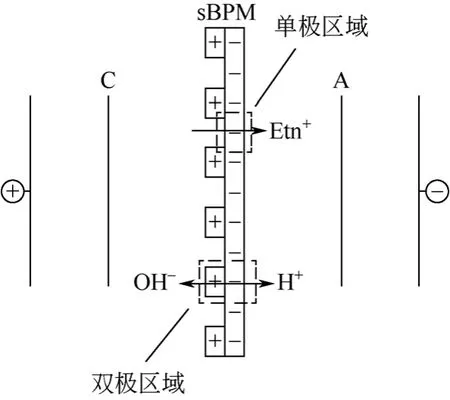
图8 sBPM-ED原理示意图[35]
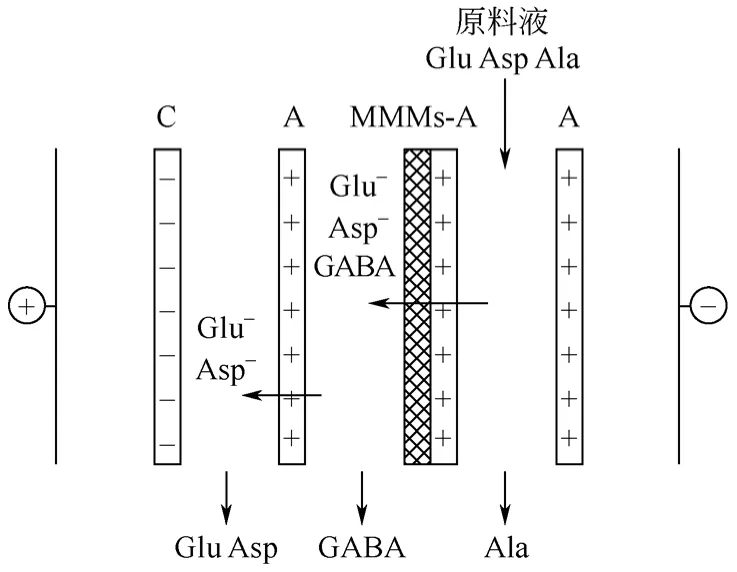
图9 MMMs-ED原理示意图[36]
3.3 工艺集成与规模化
前述的大部分实验研究都是以模拟发酵液为研究对象进行的实验室规模小试研究,其主要目的是探索技术可行性及优化操作参数,提高过程性能。然而实际发酵液成分复杂,因此需要预处理等多工艺集成以实现在生产中的应用。Zhang等[23]从实际的谷氨酸等电母液中回收谷氨酸。等电母液经微滤去除生物体等杂质,然后经三室BMED脱盐去除硫酸铵,预处理后的等电母液进入到两室BMED以回收谷氨酸。然而该作者重点研究的是BMED对谷氨酸的回收,对预处理过程只是作了简要描述。工艺集成在氨基酸生产领域的报道还不多见,然而在其他有机酸如葡萄糖酸[37]、乳酸[38]的发酵液处理方面已有相关报道。Wang等[38]考察了间歇操作模式下的BMED与发酵罐原位集成的可行性。Li等[34]提出了一种电动反应器(electrokineticbioreactor)生产乳酸,即在该反应器中,发酵过程在BMED的碱室中进行,通过pH值的在线监测及电流控制系统来调节操作电流。双极膜产生的OH-可以中和发酵过程生产的乳酸,维持发酵液pH值稳定。发酵产生的乳酸也会在电场作用下向酸室迁移,源源不断地进行分离浓缩,实现了发酵与分离同时进行。然而在氨基酸的发酵工艺中,还未见此类报道。对于规模化应用,文献[39]报道指出国内有单位在D-对羟基苯甘氨酸、牛磺酸、甘氨酸等氨基酸母液脱盐方面实现了从小试、中试到产业化的应用,但文中并未给出更多细节。
4 结语与展望
电驱动膜技术在混合氨基酸分离、发酵液脱盐、氨基酸盐与氨基酸转化等过程中均有重要应用价值。与传统氨基酸发酵液处理工艺相比,电膜过程存在工艺流程短、占地面积小、产品纯度高、环境友好、产能易于控制等显著优点,使其在发酵法生产氨基酸过程中存在显著的竞争性。然而,目前该领域的研究仍主要处于实验室阶段,研究对象多以模拟发酵液为主。为实现工业应用,还需要更多的参数优化、过程集成方面的研究。
由于实际发酵液成分复杂,膜污染将是工业应用的重大障碍。除对发酵液作适当的预处理之外,也可通过采用倒极电渗析、改善隔室内水力条件、控制操作电流等手段来加以控制。现有离子交换膜大多针对无机盐离子的迁移,而氨基酸盐的迁移性相对较弱,因此可尝试开发用于氨基酸盐乃至有机酸盐迁移的特种离子交换膜。此外,已有研究表明隔室内离子交换树脂的填充对谷氨酸盐离子的迁移有促进作用,可以提高膜通量降低能耗,因此还应探索离子交换树脂对其他氨基酸盐离子迁移的影响。可以预计,经过进一步发展改进的电驱动膜技术将会为氨基酸发酵液的处理带来重大的变革。
[1]Sikder J,Chakraborty S,Pal P,etal.Purification of lactic acid from m icrofiltrate fermentation broth by cross-flow nanofiltration[J].BiochemicalEngineeringJournal,2012,69:130-137.
[2]Abels C,Carstensen F,Wessling M.Membrane processes in biorefinery applications[J].JournalofMembraneScience,2013,444:285-317.
[3]Huang H J,Ramaswamy S,Tschirner U W,et al.A review of separation technologies in current and future biorefineries[J].SeparationandPurificationTechnology,2008,62(1):1-21.
[4]Kattan ReadiOM,MengersH J,WirathaW,etal.On the isolation of single acidic amino acids for biorefinery applications using electrodialysis[J].JournalofMembraneScience,2011,384(1-2):166-175.
[5]Tsukahara S,Nanzai B,IgawaM.Selective transportof am ino acids across a double membrane system composed of a cation-and an anion-exchangemembrane[J].JournalofMembraneScience,2013,448:300-307.
[6]Moon S H,Yun S H.Process integration of electrodialysis for a cleaner environment[J].CurrentOpinioninChemicalEngineering,2014,4:25-31.
[7]Nikonenko V V,Kovalenko A V,Urtenov M K,etal.Desalination at overlim iting currents:State-of-the-art and perspectives[J].Desalination,2014,342:85-106.
[8]Reig M,Casas S,Aladjem C,et al.Concentration of nacl from seawater reverse osmosis brines for the chlor-alkali industry by electrodialysis[J].Desalination,2014,342:107-117.
[9]Huang CH,Xu TW,Zhang Y P,etal.Application of electrodialysis to the production of organic acids:State-of-the-art and recent developments[J].JournalofMembraneScience,2007,288(1-2):1-12.
[10]Kattan ReadiO M,Giron SM,Nijmeijer K.Separation of complex m ixtures of am ino acids for biorefinery applications using electrodialysis[J].JournalofMembraneScience,2013,429:338-348.
[11]KumarM,TripathiB P,ShahiV K.Electro-membrane process for the separation of am ino acids by iso-electric focusing[J].Journalof ChemicalTechnology&Biotechnology,2010,85(5):648-657.
[12]Bukhovets A E,Savel’Eva AM,Eliseeva TV.Separation of am ino acids m ixtures containing tyrosine in electromembrane system[J].Desalination,2009,241(1-3):68-74.
[13]Habe H,Yamano N,Takeda S,etal.Useofelectrodialysis to separate and concentrateγ-am ino butyric acid[J].Desalination,2010,253(1-3):101-105.
[14]Choi JH,Oh S J,Moon SH.Structural effects of ion-exchange membrane on the separation of L-phenylalanine(L-phe)from fermentation broth using electrodialysis[J].JournalofChemical TechnologyandBiotechnology,2002,77(7):785.
[15]Shaposhnik V A,Eliseeva T V.Barrier effect during the electrodialysis of ampholytes[J].JournalofMembraneScience,1999,161(1-2):223-228.
[16]Bazinet L.Electrodialytic phenomena and their applications in the dairy industry:A review[J].CriticalReviewsinFoodScienceand Nutrition,2004,44(7-8):525-544.
[17]Shen JY,Duan JR,Liu Y S,etal.Demineralization ofglutamine fermentation broth by electrodialysis[J].Desalination,2005,172(2):129-135.
[18]Elisseeva TV,Shaposhnik V A,Luschik IG.Dem ineralization and separation of am ino acids by electrodialysis w ith ion-exchange membranes[J].Desalination,2002,149(1-3):405-409.
[19]Aghajanyan A E,Hambardzumyan A A,Vardanyan A A,et al.Desalting of neutral am ino acids fermentative solutions by electrodialysisw ith ion-exchangemembranes[J].Desalination,2008,228(1-3):237-244.
[20]Kumar M,Tripathi B P,Shahi V K.Electro-membrane reactor for separation andinsituion substitution of glutam ic acid from its sodium salt[J].ElectrochimicaActa,2009,54(21):4880-4887.
[21]Zhang Y P,Chen Y,Yue M Z,et al.Recovery of L-lysine from L-lysine monohydrochloride by ion substitution using ion-exchange membrane[J].Desalination,2011,271(1-3):163-168.
[22]Cauwenberg V,Peels J,Resbeut S,et al.Application of electrodialysis w ithin fine chem istry[J].SeparationandPurification Technology,2001,22-23:115-121.
[23]Zhang X Y,LuW H,Ren H Y,etal.Recovery of glutam ic acid from isoelectric supernatant using electrodialysis[J].Separationand PurificationTechnology,2007,55(2):274-280.
[24]Fu L L,Gao X L,Yang Y,etal.Preparation of succinic acid using bipolar membrane electrodialysis[J].SeparationandPurification Technology,2014,127:212-218.
[25]徐芝勇,张建国.双极膜电渗析技术在有机酸生产中的应用进展[J].膜科学与技术,2007(3):75-79.
[26]丛威.从谷氨酸发酵液直接制取谷氨酸单钠:中国,102126974A[P].2011-07-20.
[27]李方伟.电渗析盐复分解生产谷氨酸钠溶液的方法:中国,1896051A[P].2007-01-17.
[28]樊改肖.电去离子(EDI)技术清洁制备谷氨酸钠[D].天津:南开大学,2012.
[29]Boniardi N,Rota R,Nano G,et al.Lactic acid production by electrodialysis:Part I:Experimental tests[J].JournalofApplied Electrochemistry,1997,27(2):125-133.
[30]Wang QH,Cheng GS,Sun X H,etal.Recovery of lactic acid from kitchen garbage fermentation broth by four-compartment configuration electrodialyzer[J].ProcessBiochemistry,2006,41(1):152-158.
[31]Teng Y L,Scott EL,Van Zeeland A N T,etal.The use of L-lysine decarboxylase as a means to separate am ino acids by electrodialysis[J].GreenChemistry,2011,13(3):624-630.
[32]袁中伟,钟玉江,余立新.多级连续电渗析分离丝氨酸和脯氨酸[J].化工学报,2009,60(5):1199-1203.
[33]袁中伟,余立新.带回流的多级连续电渗析分离氨基酸[J].膜科学与技术,2010(5):84-88.
[34]SatoK,SakairiT,YonemotoT,etal.Thedesalinationofamixed solutionofanaminoacidandaninorganicsaltbymeansof electrodialysiswithcharge-mosaicmembranes[J].Journalof MembraneScience,1995,100(3):209-216.
[35]KattanReadiOM,KuenenHJ,ZwijnenbergHJ,etal.Novel membraneconceptforinternalphcontrolinelectrodialysisofamino acidsusingasegmentedbipolarmembrane(Sbpm)[J].Journalof MembraneScience,2013,443:219-226.
[36]KattanReadiOM,RolevinkE,NijmeijerK.Mixedmatrix membranesforprocessintensificationinelectrodialysisofamino acids[J].JournalofChemicalTechnology&Biotechnology,2013,89(3):425-435.
[37]WangYM,ZhangX,XuTW.Integrationofconventional electrodialysisandelectrodialysiswithbipolarmembranesfor productionoforganicacids[J].JournalofMembraneScience,2010,365(1-2):294-301.
[38]WangXL,WangYM,ZhangX,etal.Insitucombinationof fermentationandelectrodialysiswithbipolarmembranesforthe productionoflacticacid:Operationalcompatibilityanduniformity[J].BioresourceTechnology,2012,125:165-171.
[39]谢柏明,楼永通,方丽娜,等.膜分离技术在氨基酸生产上的应用[J].发酵科技通讯,2006(1):40-42.
