丙冬甘宁中药方剂发酵前后成分的变化
2015-08-18范作良刘英龙李汝春山东畜牧兽医职业学院山东潍坊261061贾慧卿潍坊诺达药业有限公司山东青州
范作良 刘英龙 鞠 雷 李汝春 (山东畜牧兽医职业学院 山东 潍坊 261061)贾慧卿 (潍坊诺达药业有限公司 山东 青州)
丙冬甘宁中药方剂发酵前后成分的变化
范作良 刘英龙 鞠 雷 李汝春 (山东畜牧兽医职业学院 山东 潍坊 261061)
贾慧卿 (潍坊诺达药业有限公司 山东 青州)
丙冬甘宁中药方经枯草芽孢杆菌发酵52h后,通过液相测定发现,发酵后甘草次酸、黄芩素含量升高,而甘草酸和黄芩苷含量降低。
中药 发酵 成分变化 质量研究
肝脏作为动物体内重要而具有特殊功能的代谢器官,对体内的代谢、消化、排泄、解毒以及免疫等过程具有重要作用。病毒、代谢毒物、药物、各种理化因素等均可导致肝脏损伤或者肝功能障碍,动物肝脏疾病的防治已经成为当前人们关注的热点之一[1]。近年来,由于各种因素导致肝脏疾病的频发,给养殖户带来了巨大的经济损失。微生物发酵的中药产品与传统中药产品相比有起效快,用量少,有效成分含量高,并且可以减少中药的不良气味等优点。栀子,甘草,柴胡,五味子、丹参等中药作为保肝药物已经有很长的应用历史[2-6],将这几味药组方为丙冬甘宁,利用芽孢杆菌将其发酵活化,本文对丙冬甘宁中药方剂发酵前后成分的变化进行分析,为临床用药提供依据。
1 材料
1.1供试药品
中药提取液由潍坊诺达药业有限公司提供;中药发酵液由潍坊诺达药业有限公司提供;甘草次酸对照品、黄芩素对照品、柴胡皂苷对照品由中国药品生物制品检验所提供;乙腈、色谱纯由天津市大茂化学试剂厂提供;甲醇、优级纯由天津市福晨化学试剂厂提供;硅胶G板由青岛海洋化工厂分厂生产,批号080411。
1.2仪器
Agilent12000型高效液相色谱仪(四元泵、柱温箱、在线脱气机、自动进样器、紫外检测器由美国安捷伦公司生产);Agilent ZORBOX SB-C18色谱柱(5μm,4.6mm× 150mm由美国安捷伦公司提供);XS105十万分之一电子分析天平由瑞士梅特勒公司提供;WFH-204B便携式紫外灯。
2 方法与结果
2.1发酵前后柴胡皂苷薄层分析变化
取中药发酵液10ml、中药提取液10ml,分别离心6000r/min,离心10min,取上清液,分别加乙醚15ml萃取3次,混合萃取液,在水浴中挥干乙醚,残渣加95%醇2ml使溶解,供点样用。柴胡皂苷a,柴胡皂苷b,分别用95%的乙醇溶解,供点样用。分别将提取液10μl,发酵液10ul和标准品溶液10ul点样于同一薄层板上,展开剂分别为氯仿:甲醇:水(70:25:5)展开5cm,挥干溶剂,喷洒10%的硫酸加热显色。分别在可见光和365nm的在外观下观察,结果如图1。
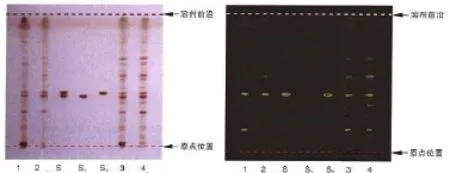
图1 柴胡皂苷薄层分析结果
从薄层层析图可以看出,中药提取液和中药提取发酵液中都存在柴胡皂苷a和柴胡皂苷d的薄层点,提取液和发酵液中均存在2种成分,在中药发酵液的薄层点中还存在2个明显的点,跑在了柴胡皂苷a和柴胡皂苷d的前面,说明该物质的极性比柴胡皂苷a和d的极性差,根据文献报道,上述几个物质为柴胡皂苷的苷元。
2.2发酵前后甘草次酸含量变化
2.2.1色谱条件 色谱柱Chromsphere C18柱(150mm× 4.6mm,5μm)、流相乙腈-水-甲醇(7:2:1)、流速0.8ml/ min、检测波长268nm、柱温室温、进样量20μl。
2.2.2标准品溶液的配置 精密称取甘草次酸对照品约10mg,用甲醇适量超声溶解,加甲醇至刻度,摇匀,配成甘草次酸对照品溶液。再精密吸取0.5、1.0、2.0、4.0、6.0、8.0ml,置量瓶中,配成各个浓度的甘草次酸标准品溶液。
2.2.3标准曲线的绘制 分别取各个浓度的甘草次酸对照品溶液20μL,依次进样,测定峰面积,记录色谱图及色谱峰面积,以进样量(μg)对峰面积进行线性回归,得标准曲线方程为Y=1341206.1X+87543.5(相关系数r=0.9996),线性范围为0.0768~1.2288μg。
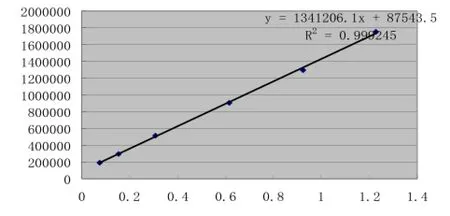
图2 甘草次酸标准曲线
2.2.4样品处理方法 中药提取液、发酵液的处理方法:分别取中药提取液和发酵液10ml,加入5%的盐酸20ml,摇匀10min,分别离心10min,6000r/min。取上清液10ml,用氯仿萃取3次,20ml/次。合并萃取液,蒸干,用甲醇溶解,定容到50ml容量瓶中。
2.2.5精密度试验 取标准品溶液,分别连续进样5次,每次进样20μl,记录吸收峰面积,测定结果RSD为0.22%。
2.2.6稳定性试验 取供试样品溶液,室温放置,每2h上样1次,记录锋面积,测定结果RSD为1.87%。说明样品在12h内稳定。
2.2.7重现性试验 根据样品处理方法,分别制备供试样品,每个样品制备6分。分别测定含量,测定结果药渣的RSD为1.74%,发酵产物的RSD为1.58%。
2.2.8加样回收试验 取已知含量的提取液和发酵产物样品,精密称定5份,置于锥形瓶中,分别加入甘草次酸对照品溶液,分别处理样品。测定样品中甘草次酸含量,结果如表1、2。
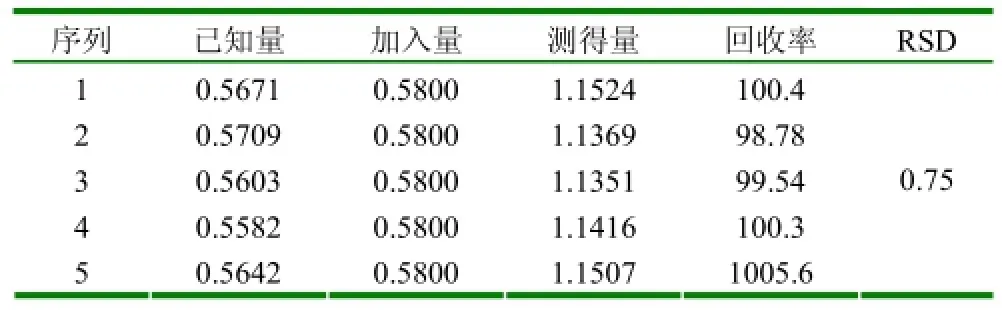
表1 提取液加样回收率 (mg、%)

表2 发酵液的加样回收率 (mg、%)
2.2.9含量测定 按照设定的色谱条件和标准曲线计算,提取液和发酵产物中各3批产品中甘草次酸的含量,结果如表3。

表3 甘草次酸含量 (mg/ml)
2.3发酵前后黄芩苷、黄芩素的变化
2.3.1色谱条件 色谱柱Chromsphere C18柱(150mm× 4.6mm,5μm)、流动相为甲醇-0.4%磷酸溶液(51:49)、检测波长277nm、流速1.0ml·min-1、柱温25℃,理论塔板数按黄芩苷峰,黄芩素峰计算应不低于2500。
2.3.2对照品溶液的制备 黄芩苷对照品溶液制备:取黄芩苷对照品适量,精密称定,加70%乙醇制成每1ml含25μg 黄芩苷的对照品溶液,摇匀,既得。黄芩素对照品溶液制备:取黄芩素对照品适量,精密称定,加70%乙醇制成每1ml含100μg 黄芩素的对照品溶液,摇匀,既得。
2.3.3供试样品的制备 中药提取液、发酵液的处理方法:分别取中药提取液和发酵液,分别离心10min,6000r/min。取上清液5ml,转移置于25ml容量瓶中,加无水乙醇5ml超声溶解,加入无水乙醇定容。从容量瓶中移取5ml至50ml容量瓶中,用70%的乙醇定容。
2.3.4检测波长的确定 黄芩苷与黄芩素对照品经DAD检测器进行紫外吸收光谱扫描,二者均在277nm处有最大吸收,故检测波长确定为277nm。
2.3.5专属性试验 按处方比例配制缺黄芩的阴性样品,制备样品溶液,根据色谱条件测定,结果黄芩苷和黄芩素对照峰处均未出现色谱峰,说明发酵液和提取液中其他成分对黄芩中黄芩苷和黄芩素的测定均无干扰。
2.3.6线性关系考察 (1)黄芩苷的标准曲线:精密称取黄芩苷对照品4.08mg,置100ml量瓶中,加70%乙醇溶解并稀释至刻度,配制成浓度为40.8μg/ml的溶液。分别稀释成浓度为10.2、15.3、20.4、25.5、30.6、35.7μg/ml。精密吸取上述6个浓度对照品溶液10μl,注入液相色谱仪,按色谱条件测定峰面积。以进样量(μg)为横坐标(X),峰面积为纵坐标(Y),绘制标准曲线。结果表明:黄芩苷在0.102~0.357μg范围内与峰面积呈良好的线性关系,其回归方程Y=33309.29X+2233.611(r=0.9999)。结果见图3。(2)黄芩素的标准曲线:精密称取黄芩素对照品13.43mg,置25ml量瓶中,加70%乙醇溶解并稀释至刻度,配制成浓度为0.537mg/ml的溶液。分别稀释成浓度为53.7、107.4、214.8、322.2、429.6、537.0μg/ml。精密吸取上述6个浓度对照品溶液10μl,注入液相色谱仪,按色谱条件测定峰面积。以进样量(μg)为横坐标(X),峰面积为纵坐标(Y),绘制标准曲线。结果表明:黄芩素在0.537 ~5.370μg范围内与峰面积呈良好的线性关系,回归方程为Y=51392.68X-666.28(r=0.9998)。结果见图4。
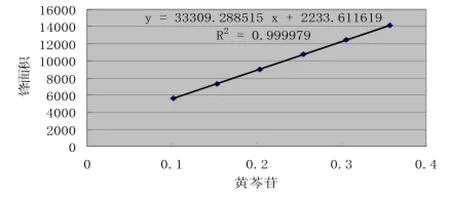
图3 黄芩苷的标准曲线
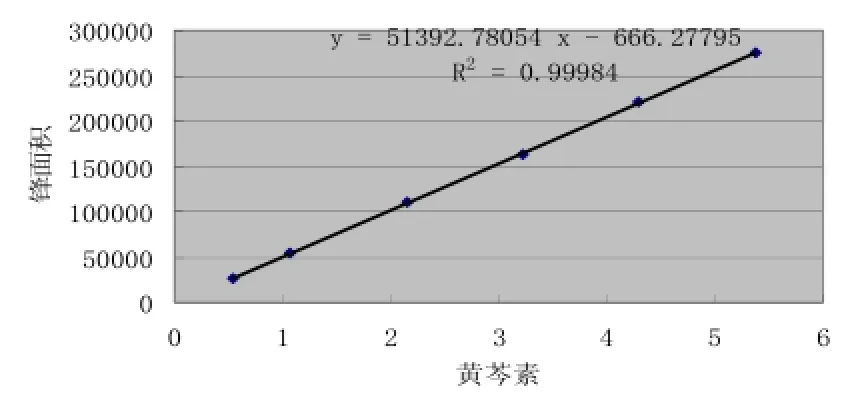
图4 黄芩素的标准曲线
2.3.7稳定性试验 制备供试品溶液,室温下放置,分别于0、1、2、4、6、8、10、12、24h后依次注入液相色谱仪,测定黄芩苷与黄芩素的峰面积并计算RSD值。黄芩苷与黄芩素的RSD分别为0.22% 和0.52%,结果表明供试品溶液在24h内基本稳定。
2.3.8精密度试验 取样品,制备供试品溶液,连续进样6次,测定峰面积值并计算RSD值。黄芩苷和黄芩素的RSD分别为0.26%和0.53%,结果表明仪器的精密度良好。
2.3.9重复性试验 取同一批号样品,制备供试品溶液6份,测定其含量及RSD值。黄芩苷和黄芩素的含量分别为1.31mg/g(RSD=1.09%),8.43mg/g(RSD =0.48%)。结果表明该方法重现性良好。
2.3.10回收率试验 (1)黄芩苷回收率试验:称取已知含量的同一批供发酵液和提取液各1ml(5份),精密称定,分别精密加入黄芩苷对照品,测定黄芩苷含量,计算回收率,结果见表4、5。(2)黄芩素回收率试验:称取已知含量的同一批发酵液1ml(5份),精密称定,分别精密加入黄芩素对照品,测定黄芩素含量,计算回收率。结果见表6、7。
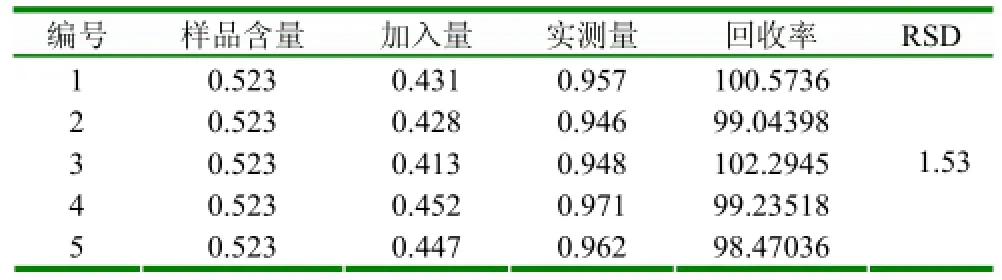
表4 发酵液中黄芩苷加样回收试验结果 (mg、%)

表5 提取液中黄芩苷加样回收试验结果 (mg、%)

表6 发酵液中黄芩素加样回收试验结果 (mg、%)
2.3.11黄芩苷、黄芩素在发酵液和提取液中的含量 分别取3批中药发酵液和提取液各2ml,处理样品,进入高效液相,测定含量。

表8 黄芩苷在发酵液和提取液中的含量

表9 黄芩素在发酵液和提取液中的含量 (mg/ml)
3 结论
从试验结果来看,发酵液和提取液中均有柴胡皂苷a,柴胡皂苷d的薄层特征,并且发酵液中的薄层点要比提取液多两个,并且特有的斑点移动距离大于柴胡皂苷a和d,这说明这两种物质的极性、分子量小于柴胡皂苷,根据相关文献报道,这两种物质疑似柴胡皂苷a和d的苷元。从液相测定的甘草次酸、黄芩素、甘草酸、黄芩苷的含量来看,通过发酵后甘草次酸、黄芩素含量升高,而甘草酸和黄芩苷含量降低,通过研究发现甘草次酸和甘草酸的区别就是,甘草次酸比甘草酸少了一个葡萄糖,而黄芩苷和黄芩素的区别也是如此,黄芩素、甘草次酸、柴胡皂苷苷元,在肠道内可以不经过肠道微生物的分解,直接吸收进入血液,药效要比黄芩苷、甘草酸、柴胡皂苷快,因此,通过生物发酵提高了中药的药效,加快了中药的作用速度。
[1] 王丽宏, 吉红, 张宝彤等. 中草药保肝作用的研究进展[J]. 饲料博览, 2012, 11: 41-45.
[2] 胡元亮. 中兽医学[M]. 北京: 中国农业出版社, 2006.
[3] 刘钟杰, 许剑琴. 中兽医学[M]. 北京: 中国农业出版社, 2010.
[4] 钟秀会, 刘占民. 兽医中药学[M]. 北京: 中国农业出版社, 2009.
[5] 汪德刚. 兽医中药学[M]. 北京: 中国农业大学出版社, 2008.
[6] 李时珍. 本草纲目[M]. 北京: 华夏夏出版社.
S853.92
A
1007-1733(2015)06-0009-03
