TiO2-C纳米复合材料负载钯催化剂的制备及其对甲酸的电催化氧化
2015-08-09刘金杭
杨 鑫,刘金杭,崔 影
(1.信阳师范学院 a.工商管理学院;b.化学化工学院,河南 信阳 464000; 2.漯河食品职业学院 质量监测系,河南 漯河 462300)
0 引言
如何提高钯基催化剂在甲酸氧化过程中的反应活性和稳定性已经变成了一个重要的研究课题[1-2].与普遍使用的铂基催化剂相比,钯具有储量丰富、价格便宜的优点.更重要的是,钯基催化剂更适用于甲酸催化氧化,这是由于在甲酸直接氧化过程中经过脱氢可直接生成CO2,能够克服催化剂的CO中毒[3].不过与Pt催化剂相比,Pd催化剂的稳定性较差,这是由于Pd在酸性溶液中的溶解[4].此外,最新研究表明Pd基催化剂在甲酸电化学氧化过程中失活的主要的原因是Pd对CO的吸附[5].
载体材料在提高燃料电池催化剂的催化活性和稳定性方面扮演着重要的角色[6].最近,由XC-72炭黑和金属氧化物制备的纳米复合材料用于担载Pd催化剂,对甲酸氧化反应的催化活性和稳定性得到了显著的提高.例如,Qu等[7-9]利用XC-72炭黑和金属氧化物制备了Pd/Al2O3-C,Pd/ZrO2-C和Pd/TiO2-C三种Pd基催化剂,并用于直接甲酸燃料电池电催化剂,这些催化剂与Pd/C催化剂相比对甲酸电化学氧化表现出更强的催化活性和稳定性.此外,最新研究表明通过控制催化金属在金属氧化物-碳纳米复合材料上的结构可以提高催化剂的催化活性和稳定性[10].例如,Jiang等[11]制备的Pd/TiO2-C催化材料中所用的碳是将葡萄糖进行高温煅烧所得到的,而且得到的催化剂显示了很强的稳定性.本文研究了Pd/TiO2-C催化剂的制备及其对甲酸氧化反应的催化性能.
1 实验部分
1.1 试剂和仪器
三聚氰胺 (99%), 钛酸异丙酯 (99.0%), PdCl2(AR, Pd ≥ 59.0%), NaBH4(98%) 和乙醇 (95%)购于国药集团化学试剂有限公司.Vulcan XC-72炭黑购买于E-TEK公司. Nafion (10 wt%) 购买于Sigam-Aldrich公司.实验室用水均经微孔净化系统净化.日立H-7650 透射电子显微镜;日立S-4800 扫描电子显微镜;Rigarku Mini Flex 600 X-射线衍射仪;CHI 850C电化学工作站(上海辰华仪器公司),三电极体系:修饰的玻碳电极为工作电极,铂丝电极为对电极,Ag/AgCl/3 mol/L KCl 为参比电极.
1.2 样品的制备
1.2.1 TiO2-C纳米复合材料的制备
取2.5 mL钛酸异丙酯滴加至50 mL含5.0 g三聚氰胺的95%乙醇溶液,然后搅拌过夜,抽滤后得到含有TiO2和三聚氰胺的混合物,并在真空干燥箱中80 ℃烘干,之后把烘干的混合物放置于管式炉中,900 °C氩气保护下加热2 h,升温过程为 5 ℃/min.
1.2.2 Pd/TiO2-C催化材料的制备
称取50 mg TiO2-C加到50 mL的蒸馏水中超声分散30 min,之后加入2 mL含有21 mg的PdCl2的盐酸溶液 (1.0 mmol/L),搅拌1 h,冰水浴中滴加10 mL现配的0.1 mol/L的NaBH4水溶液,室温搅拌6 h,然后抽滤,分别用蒸馏水和无水乙醇洗涤,最后在真空干燥箱中70 ℃下干燥6 h,制得Pd/TiO2-C催化剂.此外,以TiO2和XC-72作为载体,利用上述方法制得另外两种催化剂,分别用Pd/TiO2和Pd/XC-72表示.
1.3 电化学测试
电化学测使用CHI 850C电化学工作站进行,采用三电极体系,分别为工作电极、参比电极和对电极.称取5 mg制备的Pd/TiO2-C催化剂加到1 mL的蒸馏水中,并加入5 μL Nafion溶液,超声分散2 h,之后取5 μL分散的溶液滴加到抛光的玻碳电极上,然后放置在红外灯下烤干.循环伏安测试在0.5 mol/L的H2SO4溶液中氩气保护下进行,扫描范围为0~1.0 V,扫描速率为50 mV/s.
CO溶出实验在0.5 mol/L的H2SO4溶液中进行的,具体操作为先充氩气30 min,然后充入高纯度的CO气体15 min使CO气体吸附在催化剂的表面,之后再充入氩气30 min排除溶液中的CO气体,然后进行循环伏安测试,扫描范围为-0.2~1.0 V,扫描速率为50 mV/s.
2 结果与讨论
2.1 XRD分析
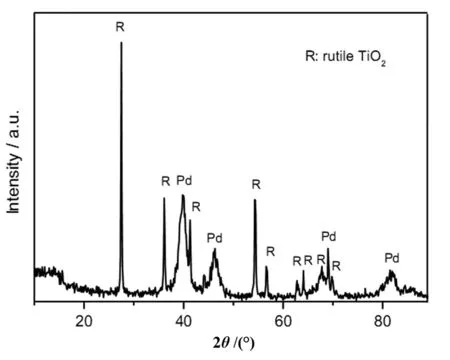
图1 Pd/TiO2-C催化材料的XRDFig. 1 XRD patterns of Pd/TiO2-C
图1是催化材料Pd/TiO2-C的XRD图谱.2θ= 27.5°、36.1°、41.3°、54.3°、56.6°、62.7°、64.0°、67.8°及69.8°的衍射峰分别对应金红石TiO2的(101)、(111)、(211)、(220)、(002)、(310)、(301)和(112)晶面(JCPDS 78-2485),这表明经过900 ℃的高温煅烧TiO2全部以金红石晶相存在[12].通过Scherrer公式可推算出TiO2晶粒尺寸大约为10 nm.此外,2θ= 39.9、46.2、69.0和82.0°处的衍射峰对应于面心立方结构Pd的 (111)、(200)、(220)、(311)晶面(JCPDS 05-0681)[13].
2.2 TEM和EDS分析
通过图2a和2b可清楚地看到金属Pd负载在TiO2-C纳米复合材料表面,Pd的平均粒径为5 nm.图2c是催化剂的HRTEM图.由图可知,0.23 nm对应于Pd (111)面的晶格间距,0.33 nm和0.25 nm对应于红金石TiO2(110)和(101)晶面,0.34 nm对应于石墨(002)晶面,表明碳来自三聚氰胺的炭化[14].通过观察可以发现,Pd负载于碳与TiO2的界面.由XRD图谱可以看出,谱图中除了Cu元素峰外,其余的全部为TiO2和Pd的峰.
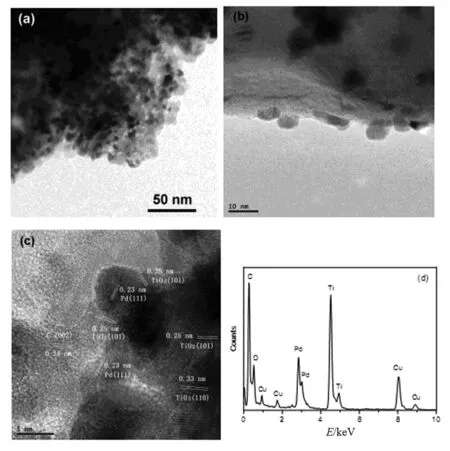
图2 Pd/TiO2-C催化材料的 TEM (a、b),HRTEM (c)和EDS(d)Fig. 2 TEM (a and b), HRTEM (c) images and energy dispersive X-ray spectroscopy (EDS)(d) of Pd/TiO2-C
2.3 循环伏安测试
图3是不同Pd催化剂在0.5 mol/L硫酸溶液测试的循环伏安曲线,a、b、c分别代表材料Pd/TiO2-C、Pd/XC-72和Pd/TiO2.循环伏安图上在-0.2 V和0.1 V左右,有两对明显的峰,分别为H的吸附和脱附.当阳极电位>0.5 V 时,Pd开始被氧化,阴极扫描电位为 0.6~0.25 V时,表面氧化物被还原.在Pd/TiO2-C上,Pd氧化物的还原峰电位为0.45 V,而在Pd/XC-72上则为0.41 V.说明在Pd/TiO2-C表面,Pd氧化物的还原更容易进行[15].此外,在Pd/TiO2-C材料上,CO吸附/脱附电流明显大于Pd/XC-72.这说明在TiO2-C载体上,Pd含有高密度的台阶原子和扭曲原子[16].
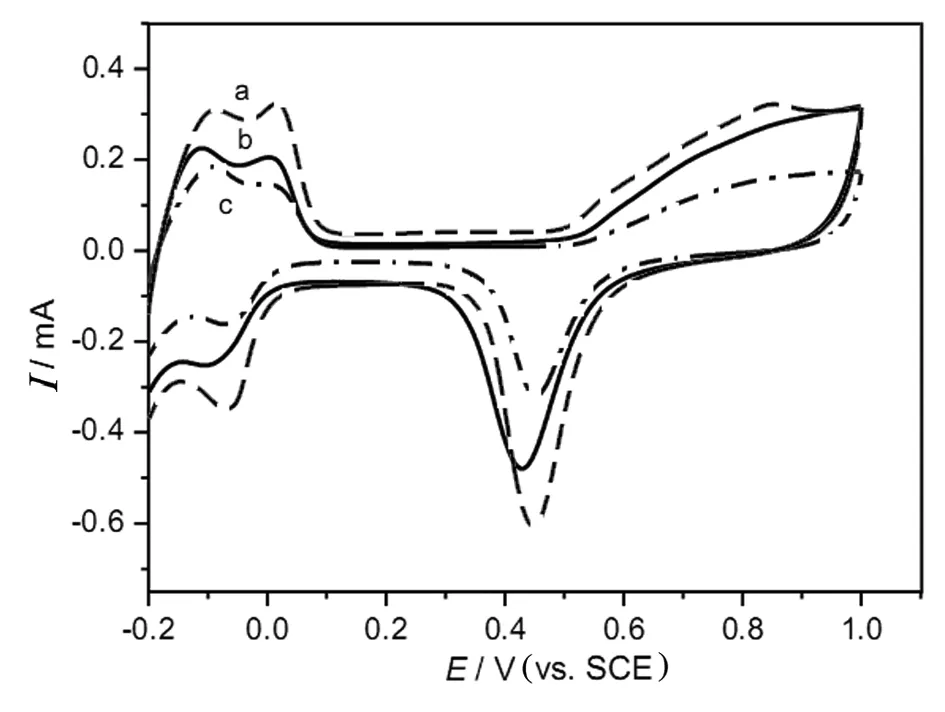
图3 不同修饰电极在0.5 M硫酸中的循环伏安Fig. 3 CVs of Pd/TiO2-C (a), Pd/XC-72 (b) and Pd/TiO2 (c) in an Ar-saturated 0.5 mol/L H2SO4 solution at a scan rate of 50 mV/s
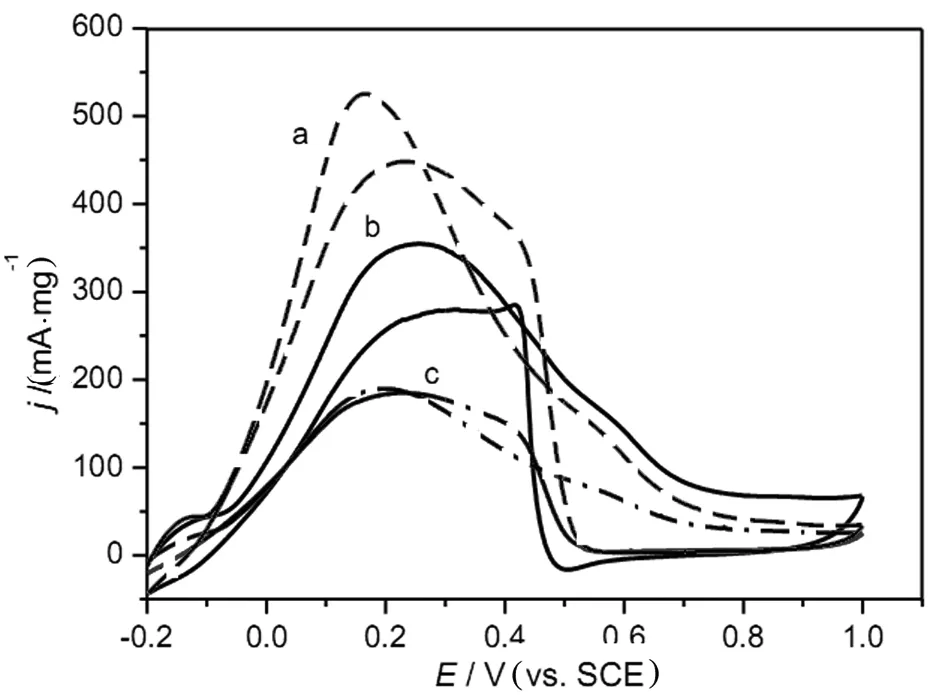
图4 不同修饰电极对甲酸的循环伏安Fig. 4 CVs of Pd/TiO2-C (a), Pd/XC-72 (b) and Pd/TiO2 (c) in an Ar-saturated 0.5 mol/L H2SO4 solution containing 0.5 mol/L formic acid at a scan rate of 50 mV/s
不同Pd催化剂对FAO的电催化活性在含有0.5 mol/L甲酸的硫酸溶液中进行测试.图4所示为不同电极对甲酸氧化的循环伏安.由图4a可以看出,Pd催化剂的循环伏安曲线在0.16~0.26 V间有一个主峰,在0.55 V处有一个次峰,表现出Pd催化剂对 FAO的电化学行为特性.Pd/TiO2-C、Pd/XC-72和Pd/TiO2的峰电流密度分别为 525 mA/mgPd(0.16 V vs. SCE),356 mA/mgPd(0.26 V vs. SCE) 和190 mA/mgPd(0.20 V vs. SCE).Pd/TiO2-C对甲酸氧化显示了较低的峰电位和较高的电流密度,表明其对FAO较高的电催化活性.根据文献报道,第一个峰位对应为脱氢过程,第二个峰对应为脱水过程[17-18].本实验中,第二个峰电位为0.55 V,近似于CO溶出伏安图中的起始电位 (0.50 V),说明这与CO的氧化反应有关.第一个峰电流和第二个峰电流的比值可以用来说明FAO的主要反应路径.Pd/TiO2-C的两个峰电流比值比Pd/XC-72和Pd/TiO2相应的比值高得多,说明Pd/TiO2-C能显著增强脱氢过程.
2.4 CO溶出实验
这些Pd催化剂对CO的抗中毒性能通过CO-溶出实验进行研究.通过CO-溶出特征曲线观察Pd催化剂的性能,如图5所示.H的吸附/脱附完全被抑制直到CO的吸附/脱附反应终止.Pd/TiO2-C上吸附的CO氧化峰电位为0.75 V,低于 Pd/XC-72 (0.80 V)和Pd/TiO2(0.84 V) 上CO氧化峰电位.相对于Pd/XC-72和Pd/TiO2,CO在Pd/TiO2-C上氧化的起始电位较低.这表明吸附的CO更容易在Pd/TiO2-C上被氧化.Pd基催化剂的电化学表面积 (ESA) 由CO氧化峰计算.Pd/TiO2-C的ESA值为75.5 m2g,大于Pd/XC-72 (65.0 m2/g) 和Pd/TiO2(39.5 m2/g),说明在Pd/TiO2-C催化剂上有更多的催化活性位点.
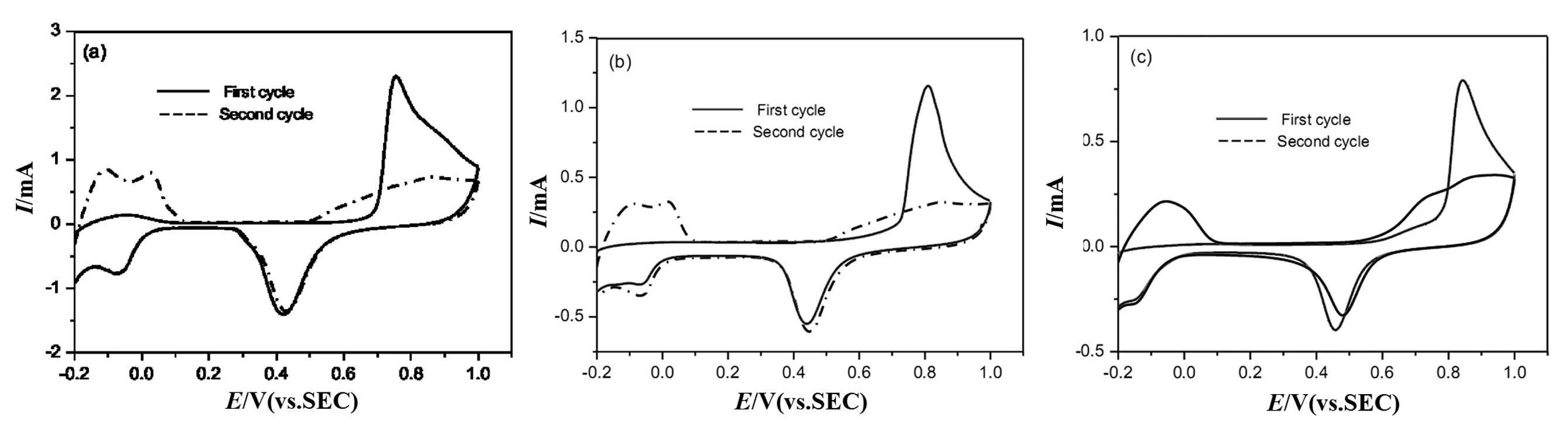
图5 不同修饰电极测试的CO溶出伏安Fig. 5 CO-stripping voltammograms of Pd/TiO2-C (a), Pd/XC-72 (b) and Pd/TiO2 (c) in 0.5 mol/L H2SO4solution at a scan rate of 50 mV/s
这些Pd催化剂对CO的抗中毒性能通过CO-溶出实验进行研究.通过CO-溶出特征曲线观察Pd催化剂的性能,如图5所示.H的吸附/脱附完全被抑制直到CO的吸附/脱附反应终止.Pd/TiO2-C上吸附的CO氧化峰电位为0.75 V,低于 Pd/XC-72 (0.80 V)和Pd/TiO2(0.84 V) 上CO氧化峰电位.相对于Pd/XC-72和Pd/TiO2,CO在Pd/TiO2-C上氧化的起始电位较低.这表明吸附的CO更容易在Pd/TiO2-C上被氧化.Pd基催化剂的电化学表面积 (ESA) 由CO氧化峰计算.Pd/TiO2-C的ESA值为75.5 m2/g,大于Pd/XC-72 (65.0 m2/g) 和Pd/TiO2(39.5 m2/g),说明在Pd/TiO2-C催化剂上有更多的催化活性位点.
2.5 计时电流测试
用计时电流测试对Pd催化剂的活性和稳定性进行进一步研究,如图6所示.Pd/TiO2-C具有较高的初始电流密度和极限电流密度.3000 s时,Pd/TiO2-C的电流密度为87 mA/mgPd,明显高于Pd/XC-72(60 mA/mgPd)和Pd/TiO2(35 mA/mgPd)的电流密度.Pd/TiO2-C催化剂较强的电催化活性主要是由于TiO2-C载体协同作用.来源于三聚氰胺炭化的石墨提高了TiO2-C载体的电导性和比表面积.TiO2较强的稳定性提高了载体的耐久性.最重要的是,Pd沉积在TiO2-C异质界面上,能够极大地提高金属-载体的相互作用,从而增强了Pd对FAO的催化活性和稳定性.
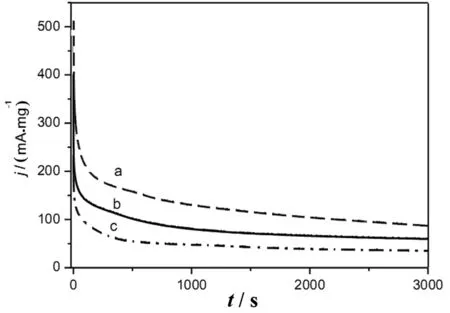
图6 不同修饰电极的计时电流曲线Fig. 6 Chronoamperometric curves of Pd/TiO2-C (a), Pd/XC-72 (b) and Pd/TiO2 (c) recorded at 0.3 V in an Ar-saturated 0.5 mol/L H2SO4 solution containing 0.5 mol/L formic acid
3 结论
我们通过高温煅烧法制备出TiO2-C纳米复合材料,并将其负载Pd粒子合成出Pd/TiO2-C催化剂.这种方法简单有效,可以广泛应用于Pd负载型催化剂复合材料的合成.Pd/TiO2-C催化剂相对于Pd/XC-72和Pd/TiO2,对FAO的催化活性和稳定性明显增强,这归因于TiO2-C载体的特性和Pd/TiO2-C独特的异质结构.
