基于新型固相萃取-高效液相色谱法灵敏测定牛奶中的药物残留
2015-08-09王玲玲吴志伟
王玲玲, 吴志伟
(信阳师范学院 化学化工学院,河南 信阳 464000)
0 引言
还原氧化石墨烯(Gr)是由碳原子单层通过共价键合的一种六方对称二维晶体,厚度仅为0.335 nm,而比表面积理论值则达到2 630 m2/g[1-3],是目前备受研究者关注的一种新型二维碳材料.由于Gr具有大的比表面积,且机械性能优良、化学性质稳定,其对物质的吸附主要是基于π-π电子之间的相互作用及其疏水性,被证明是一种很好的固相萃取吸附剂.但是,由于单纯的Gr易于聚集,作为萃取柱填料容易造成塌陷,堵塞柱子,从而使得萃取效率下降.因此对于石墨烯进行表面修饰非常必要.硅胶是由二氧化硅的无定形体构成的非晶型的多孔状物质,具有性质稳定、耐酸、不易碎、不溶胀等优点,是一种良好的吸附剂材料[4-5].但是硅胶的颗粒一般较大,比表面积较小,因此限定了它的应用.
本文通过水热法,将还原性石墨烯与硅胶相结合制备了两者的复合物用作固相萃取柱的填料.该复合物结合了石墨烯和硅胶两者的优点,具有机械性能好、不易坍陷、比表面积大、吸附力强等优点.磺胺类药物是兽药的一种,常残留于食品中,通过食物链富集于人体中,对人的健康造成危害[6-7].在本工作中我们将该新型萃取柱与高效液相色谱法相结合, 成功地测定了牛奶中的磺胺类药物残留,实验结果令人满意.
1 实验部分
1.1 仪器与试剂
安捷伦1200高效液相色谱仪,安捷伦C18分离柱(250 mm×4.6 mm, 5 μm)和1 mL固相萃取小柱;日立公司S4800扫描电子显微镜;KQ50E型超声波清洗器(昆山市超声仪器有限公司);Mettler Toledo DELTA 320 pH计(瑞士梅特勒-托利多公司).
石墨粉、肼、氨水、硅胶等均购于上海试剂厂;磺胺类(对羧基苯磺酰胺SMB、磺胺嘧啶SDZ、磺胺甲基嘧啶SMR、磺胺甲噁唑SMZ、邻甲基苯磺酰胺O-T)和3-氨丙基三乙氧基硅烷购于上海晶纯试剂公司;5种磺胺类物质分别溶于乙酸-甲醇的混合溶液中,配制成1 g/L的储备液,在4 ℃下储存.
1.2 还原氧化石墨烯-硅胶复合物的制备
首先采用Hummers方法制备氧化石墨[8-9].分别将3 g石墨粉、2.5 g (NH4)2S2O8和2.5 g P2O5加入到80 ℃的12 mL浓硫酸中,恒温4.5 h后,冷却,用水稀释后放置12 h.经过过滤、洗涤、烘干后得到预氧化石墨.将氧化石墨加到120 mL的浓硫酸中,在冰浴下缓慢加入15 g的KMnO4,搅拌均匀.然后升温至35 ℃,搅拌2 h后逐滴加入250 mL水,并在50 ℃下搅拌2 h.用水稀释后,加入100 mL的30%的过氧化氢至产物呈亮黄色并产生气泡.将所得的混合物抽滤并用10%的HCl和水反复洗涤,干燥后得氧化石墨.在氧化石墨中加入适量蒸馏水,超声至溶液呈现均一透明状,得到氧化石墨烯水溶液.
将5.0 g 60目硅胶置于6 mol/L HCl中加热回流4 h,冷却后过滤,洗涤至中性,并在80 ℃下烘干.加入75 mL甲苯,加热至回流,再逐滴加入5 mL的3-氨丙基三乙氧基硅烷,回流12 h后,冷却,抽滤, 80 ℃下烘8 h后加入150 mL氧化石墨烯水溶液,再加入2.5 g N, N- 二环己基碳酰亚胺,回流24 h,抽滤,洗涤,烘干.称取上述产物0.2 g置于圆底烧瓶中,加入100 mL的蒸馏水,加热回流,加入0.2 g NaBH4,继续回流12 h,抽滤,洗涤,烘干后得到还原氧化石墨烯-硅胶复合物.
所制备的还原氧化石墨烯和还原氧化石墨烯-硅胶复合物的扫描电镜图如图1中的A和B所示.由A图可以看到石墨烯典型的片状褶皱结构,在B图中可以看到硅胶和石墨烯紧密地结合在一起.

图1 还原氧化石墨烯(A)和还原氧化石墨烯-硅胶复合物(B)的扫描电子显微镜图Fig. 1 SEM images of reduced graphene (A) and reduced graphene-silica gel composites
1.3 固相萃取柱的制备
将商品化的1 mL的固相萃取小柱上筛板取出,倒出柱填料,取20 mg还原氧化石墨烯-硅胶复合物填入柱中,盖上上筛板.柱子在使用前分别用5 mL的蒸馏水与甲醇活化.萃取结束后,柱子分别用甲醇与蒸馏水洗涤即可进行下次进样.
1.4 色谱条件及样品制备
对色谱分离条件进行优化,确定如下分离条件:色谱柱为C18分离柱,流动相为甲醇-乙酸混合溶液(pH 3.2),体积比为27∶73,流速为1 mL/min,紫外检测波长为275 nm.
牛奶为蒙牛牌纯牛奶(无菌包装).将铁氰化钾与牛奶混合液置于100 mL锥形瓶中,再加入5 mL硫酸锌,搅拌均匀后加热到75 ℃,直至牛奶中蛋白质大量沉淀.然后向混合溶液中加入10 mL乙腈,并超声一段时间,最后通过0.2 μm的滤膜进行过滤,得到的滤液转移到容量瓶中,4 ℃下保存备用.
2 结果与讨论
2.1 萃取条件优化
磺胺类药物在不同溶剂中的溶解度差异较大,因此需要对溶剂进行优化.分别考察了乙腈、乙醇、甲醇、碱性甲醇、酸性甲醇这5种有机溶剂对5种磺胺类药物洗脱能力的影响.结果表明,当5种磺胺类药物的浓度为100 μg/L,且溶液体积为50 mL时,乙腈、乙醇和甲醇3种洗脱液基本没有出峰,说明洗脱效果不好.而酸性甲醇和碱性甲醇洗脱液的信号峰较强,但碱性甲醇洗脱液中有杂质峰存在,干扰检测,而且硅胶在碱性条件下易溶解,对色谱柱造成损害,因此选择酸性甲醇为洗脱剂.
考察了洗脱剂的体积对萃取效率的影响.当酸性甲醇的量小于0.1 mL时,不足以覆盖萃取填料,所以洗脱剂使用最小量选择为0.1 mL.将洗脱剂0.1 mL逐渐增加到0.6 mL.所得结果如图2所示,随着洗脱剂的增多,峰面积逐渐减小,所以选择0.1 mL的酸性甲醇为洗脱剂.

图2 洗脱剂体积的影响Fig. 2 The effect of elution volume
考察了样品溶液的体积对峰面积的影响.分别测试了6个不同体积(25、50、75、100、125、150 mL)的样品溶液.所得结果如图3所示.对于5种磺胺类药物,当溶液体积由25 mL增大到75 mL时,它们的峰面积随之增大.而当样品溶液超过75 mL时,其峰面积随之减少.因此选择75 mL为最佳样品溶液体积.

图3 样品体积的影响Fig. 3 The effect of samples volume
由于磺胺类物质的溶解度受pH影响较大,所以样品溶液的pH也是影响萃取效率的重要因素.在pH 3~8范围内考察了样品溶液pH对的各个磺胺类药物峰面积的影响,结果如图4所示.综合考虑后,选择pH 5为最佳溶液pH值.
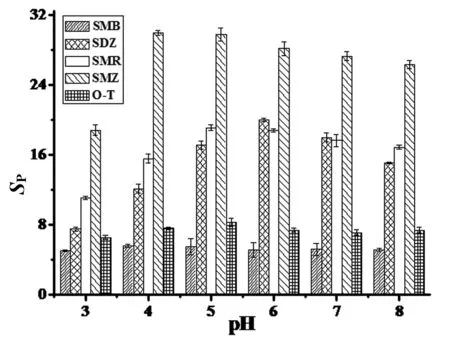
图4 样品溶液pH的影响Fig. 4 The effect of samples pH value
酸性甲醇中乙酸和甲醇的含量比也影响洗脱效率.如图5所示,通过改变两者的比率,得到的各个磺胺类药物的峰面积也不一样,当乙酸体积与甲醇的体积比为1∶1.5时,所得到的各个药物的峰面积最大,因此选择该比率配置洗脱液.
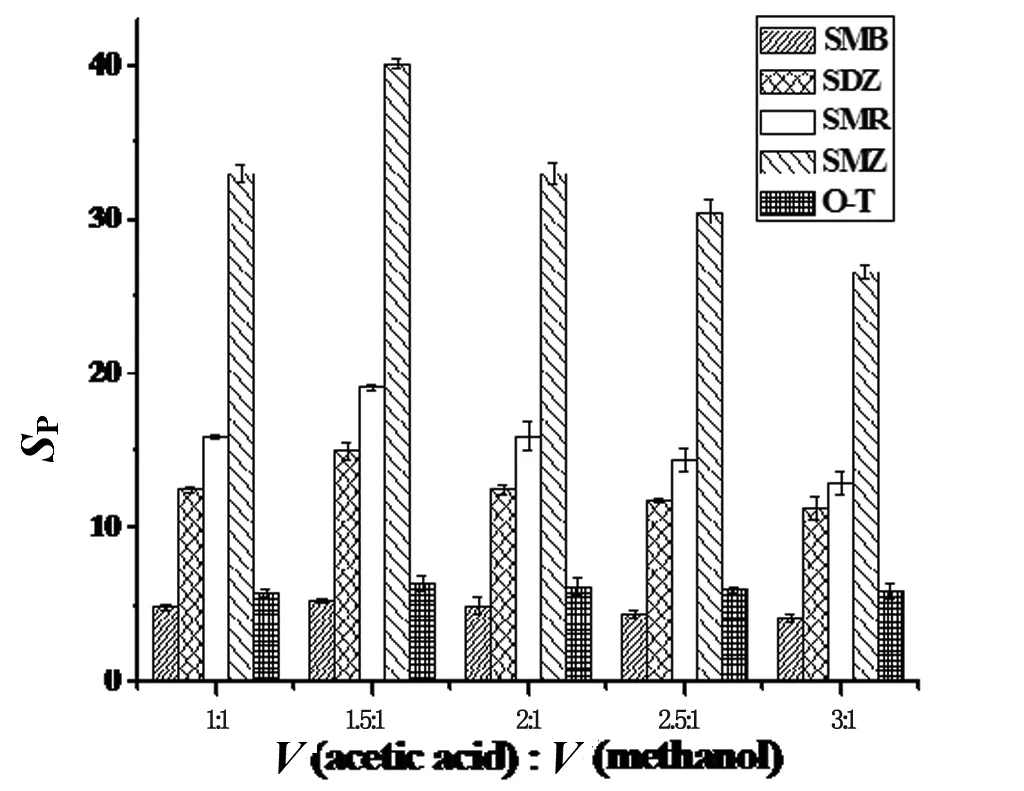
图5 乙酸与甲醇体积比的影响Fig. 5 The effect of the ratio of methanol to acetic acid
2.2 分析参数
在上述的优化条件下,利用固相萃取-高效液相色谱法测定了不同浓度的磺胺类药物,5种分析物的标准色谱图如图6所示,从图中可以看出5种物质得到了良好的基线分离.所建立的分析方法的线性范围、检测限(LOD)、相关系数、相对标准偏差等相关参数如表1所示.
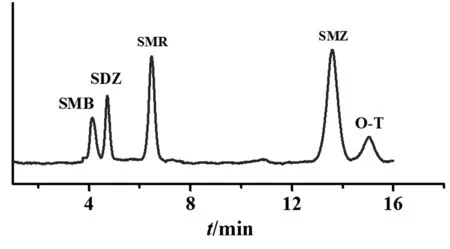
图6 五种磺胺类药物的标准色谱图 样品溶液pH:5,样品溶液体积:50 mL, 各物质浓度均为25 μg/L,洗脱剂:0.2 mL的酸性甲醇.Fig. 6 The chromatogram of five sulfonamides表1 分析方法的分析参数Tab. 1 Analytical parameters of the developed method
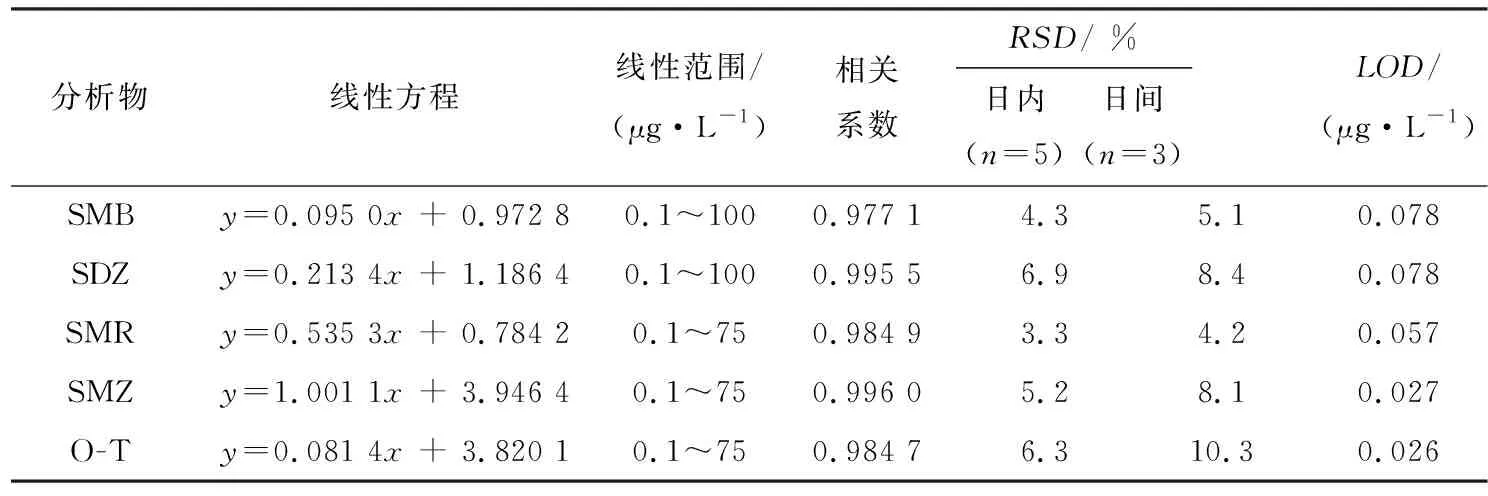
分析物线性方程线性范围/(μg·L-1)相关系数RSD/ %日内(n=5)日间(n=3)LOD/(μg·L-1)SMBy=0.095 0x + 0.972 80.1~1000.977 14.35.10.078SDZy=0.213 4x + 1.186 40.1~1000.995 56.98.40.078SMRy=0.535 3x + 0.784 20.1~750.984 93.34.20.057SMZy=1.001 1x + 3.946 40.1~750.996 05.28.10.027O-Ty=0.081 4x + 3.820 10.1~750.984 76.310.30.026
2.3 实际样品分析
按实验部分对牛奶样品进行预处理,然后将不同浓度的磺胺类药物标准品加入到处理好的牛奶样品中,用所建立的新方法进行测定,结果如表2所示.回收率在88.3%~113.6%之间,说明所建立的方法可用于实际样品分析.
3 结论
本文将还原氧化石墨烯-硅胶复合材料作为新型固相萃取吸附剂与高效液相色谱法相结合用于磺胺类药物分析,该方法展现出收率高,重现性好,灵敏度高等优点.并且萃取柱的制备简单、成本低、操作简便,可用于实际样品分析.
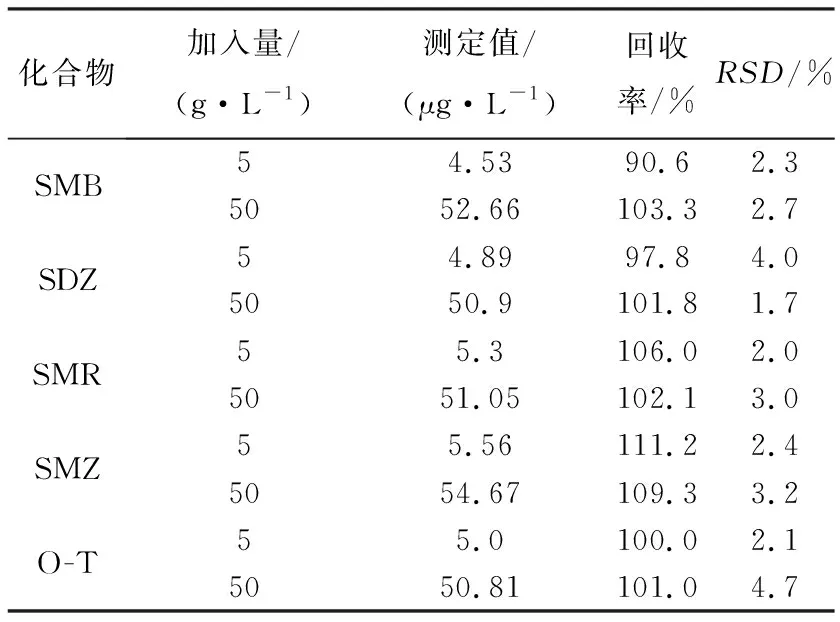
表2 加标回收实验结果Tab. 2 The results of the covery test
