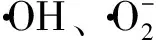响应面法优化薤白多糖的羧甲基化修饰工艺及抗氧化活性研究
2015-08-08夏新奎豆成林
夏新奎,豆成林
(信阳农林学院 食品科学系,河南 信阳 464000)
0 引言
薤白是百合科植物小根蒜AlliummacrostemonBge.或薤AlliumchinensisG. Don. 的干燥鳞茎.有通阳散结、行气导滞之功效[1],其原植物既入药又可食用,是常见的药食两用中药材.药理研究表明,薤白具有抑菌、抗氧化、抗肿瘤等作用.薤白中的化学成分已分离到的有甾体皂苷、挥发油和酚酸类等,但对薤白多糖的研究报道较少,尤其对薤白多糖(PAM)结构修饰的研究还未见报道.
多糖分子修饰是指通过物理、化学和生物学等方法对多糖分子结构进行改造,以得到理化性质改变或产生新的生物学功能的多糖衍生物[2].多糖经羧甲基化后可提高其水溶性.同时对其生物活性的提高和改进具有极其重要的作用.张丽华等[3]用碱性条件的氯乙酸法对冬花多糖进行羧甲基化修饰,其修饰产物清除DPPH自由基的能力明显提高.曹宇等[4]对羧甲基化茯苓多糖(CMP)的研究结果表明,羧甲基化后其水溶性得到很好改善,对·OH的清除率提高.
本文在前期研究的基础上[5-6],对所得的薤白多糖纯品采用碱性条件的氯乙酸法进行羧甲基化修饰,用响应面设计法确定羧甲基化的最佳条件,并对修饰前后的薤白多糖清除超氧阴离子自由基、羟自由基能力进行研究,旨在筛选出羧甲基化的最佳条件,为薤白多糖的开发应用提供理论依据.
1 实验部分
1.1 材料与仪器
薤白多糖及分级纯品:由本实验室提供.利用水溶醇沉法得薤白粗多糖,经木瓜蛋白酶+Sevag法脱蛋白处理得薤白多糖,再经DEAE-纤维素柱层析和SephadexG-150柱层析得薤白多糖的三种级分(PAM-Ⅰb、PAM-Ⅱa、PAM- III’)[5-6].
主要仪器与试剂:HH-S6恒温水溶锅,上海普渡生化科技有限公司;GL-20C高速冷冻离心机,上海安婷科学仪器厂;UV-7502PCS紫外-可见光分光光度计,上海欣茂仪器有限公司;PHS-3C 型 pH 计,上海精密科学仪器有限公司.
氯乙酸、异丙醇、氢氧化钠、盐酸、邻二氮菲、邻苯三酚、三羟甲基氨基甲烷(Tris)等均为国产分析纯.
1.2 实验方法
1.2.1 薤白多糖的羧甲基化修饰
采用氢氧化钠-氯乙酸反应体系[7]对薤白多糖进行羧甲基化修饰.
将1.0 g薤白多糖置于三颈瓶中,加入20 mL异丙醇,搅拌30 min后加入20%NaOH溶液4 mL,继续搅拌碱化50 min,形成均匀的混悬液;然后加入20 mg的氯乙酸,升温至60 ℃,醚化3 h,反应结束后,冷却至室温并加入适量蒸馏水,用0.5 mol/L的盐酸调pH至7.0.最后将混合液置于透析袋中透析3 d,浓缩后用95%乙醇沉淀多糖,所得沉淀干燥后得到羧甲基化薤白多糖(cPAM).
根据文献报道,氯乙酸浓度、反应温度、反应时间对羧甲基化产物的取代度影响较大[3].因此,本实验根据单因素实验结果,以氯乙酸浓度(A)、反应时间(B)和反应温度(C)为自变量,产物的羧甲基取代度(DS)为响应值,利用Box-Benhnken Design中心组合实验设计原理,设计3因素3水平的响应面分析实验,以确定羧甲基化修饰的最佳工艺条件.
1.2.2 羧甲基取代度的测定
薤白多糖羧甲基取代度测定采用碱滴定法[8]进行.准确称取羧甲基多糖样品10 mg,干燥后加入 3 mL70%乙醇,混合后放置 5 min.依次加入10 mL蒸馏水,50 mL 0.5 mol/L的NaOH后混合搅拌,直至样品溶解.然后以酚酞做指示剂用0.1 mol/L盐酸滴定,计算每克羧甲基多糖所需的盐酸的毫摩尔数(n) :
n=(V0M0-(V2-V1)M)/W,
式中:V0为加入NaOH的体积,mL;V2为样品测定所消耗HCl的体积,mL;V1为空白测定所消耗HCl的体积,mL;M0为加入的NaOH浓度(0.5 mol/L);M为测定所用盐酸的浓度(0.1 mol/L).
羧甲基取代度(DS)的计算:
DS=0.162n/(1-0.058n).
1.2.3 薤白多糖羧甲基化修饰前后体外抗氧化活性测定
2 结果与分析
2.1 薤白多糖羧甲基化修饰
2.1.1 薤白多糖羧甲基化修饰工艺条件优化
根据单因素实验结果,以氯乙酸浓度(A)、反应温度(B)和反应时间(C)为自变量,产物的羧甲基取代度(DS)为响应值,利用Box-Benhnken Design中心组合实验设计原理,设计3因素3水平的响应面分析实验,实验因素水平见表1,实验及分析结果见表2和表3.

表1 实验因素水平Tab.1 Factors and leves of test
由表3可以看出,模型P<0.000 1,表明该模型方程达到极显著水平;说明该方法是准确可靠的,使用该方程模拟真实点分析可行.
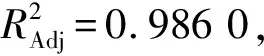
利用Design Expert 8.0.5.0软件对表2数据进行多元回归拟合,得到羧甲基化薤白多糖的羧甲基取代度(DS)与氯乙酸浓度(A)、反应时间(B)、反应温度(C)的回归方程为:
DS= -7.931 75+0.893 50A+0.561 50B+
0.237 55C+7.500 0×10-3AB-
8.750 00×10-3AC+4.250 00×10-3BC-
0.147 75A2-0.132 75B2-1.927 50C2.
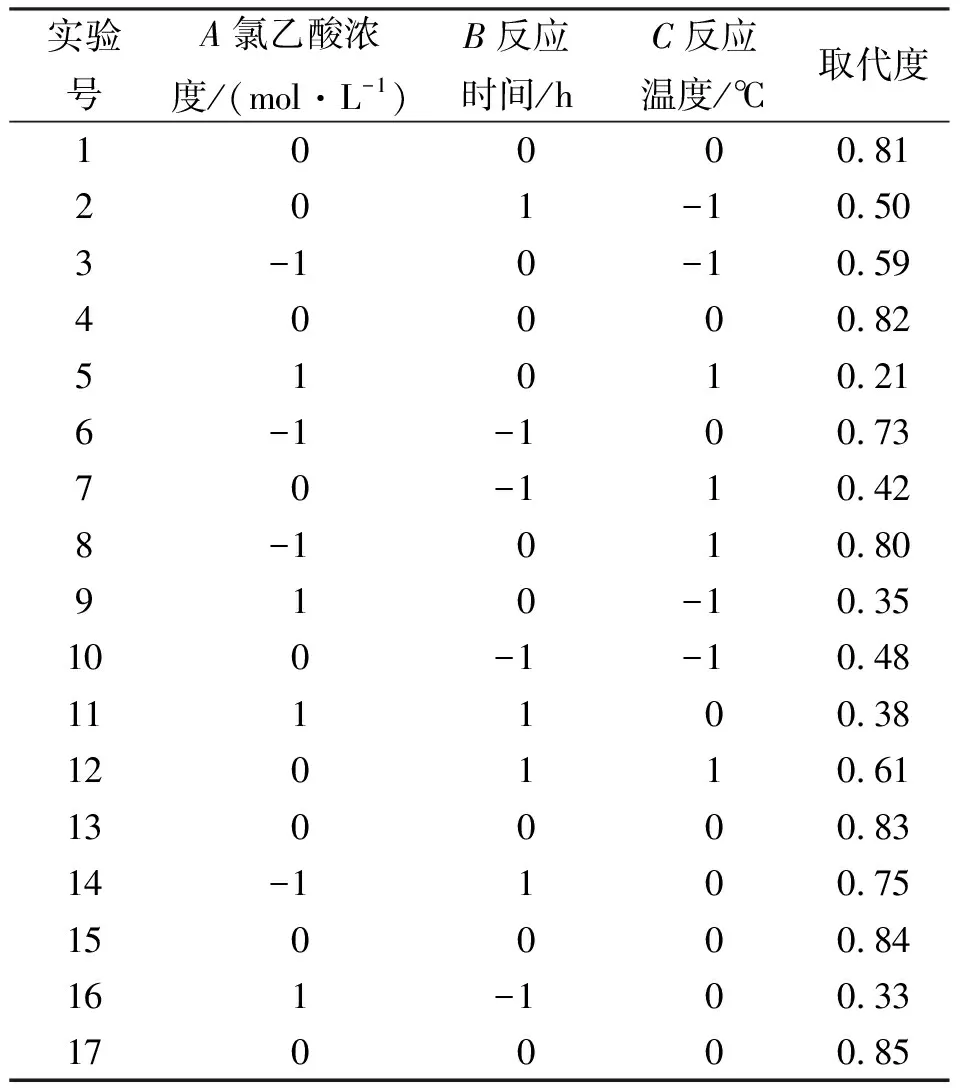
表2 响应面分析实验设计及结果Tab.2 Respond surface experimental design and results
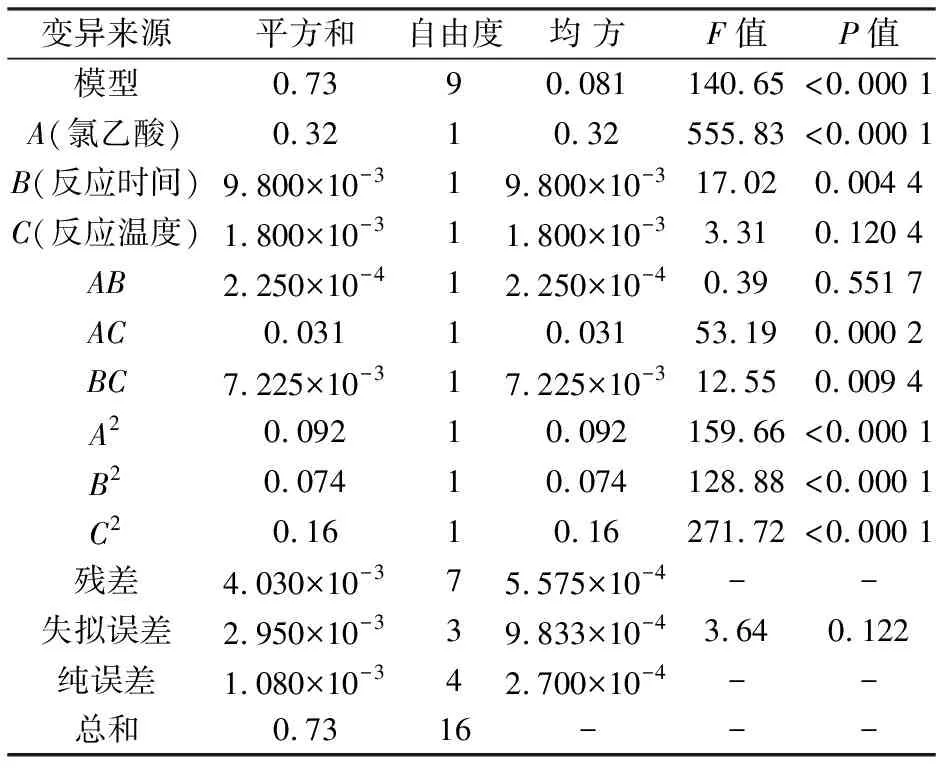
表3 方差分析结果Tab.3 The results of variance analysis
由表3可以看出,各因素对实验结果的影响大小为A>B>C, 即氯乙酸浓度对薤白多糖羧甲基取代度的影响最大,其次为反应时间,反应温度影响最小.因素A、B、A2、B2、C2对薤白多糖羧甲基取代度的影响极显著(P<0.01),AC、BC对薤白多糖羧甲基取代度的影响显著(P< 0.05),C、AB对薤白多糖羧甲基取代度的影响不显著(P>0.05).
采用Design-Expert8.0.5.0软件做出3个因素之间的响应曲面图,结果如图1、图2和图3所示.
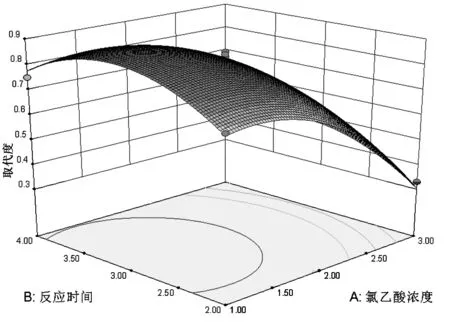
图1 氯乙酸浓度与反应时间对取代度的影响Fig.1 Effects of chloroacetic acid and reaction time on DS
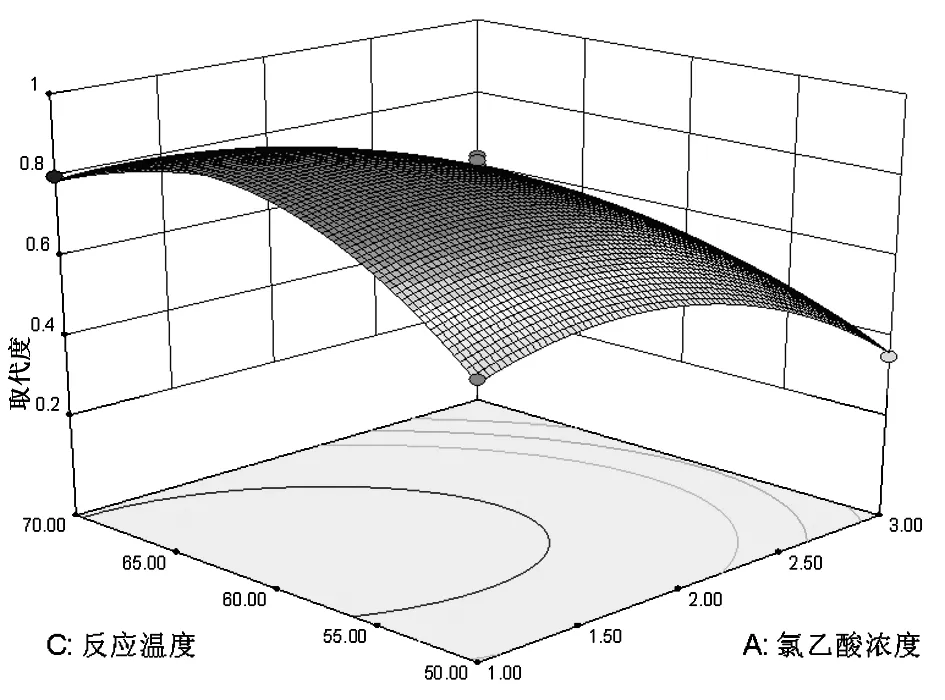
图2 氯乙酸浓度与反应温度对取代度的影响Fig.2 Effects of chloroacetic acid and reaction temperature on DS
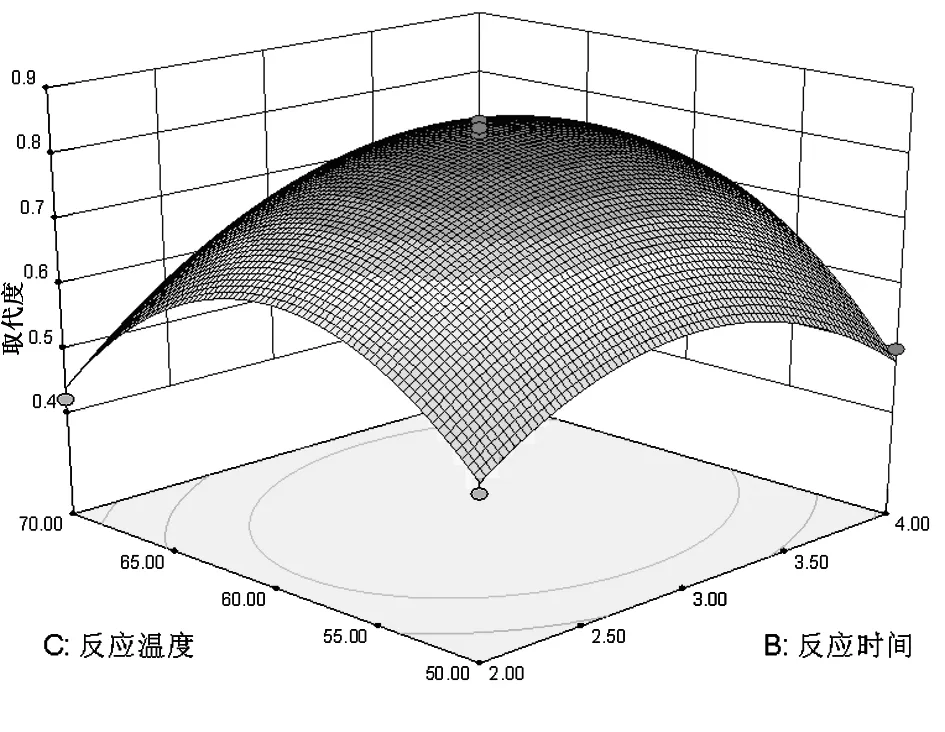
图3 反应时间与反应温度对取代度的影响Fig.3 Effects of reaction time and reaction temperature on DS
2.1.2 模型的优化和验证
利用Design Expert 8.0.5.0软件进行优化,回归模型预测的薤白多糖羧甲基化修饰的最佳条件为:氯乙酸浓度1.26 mol/L,反应温度62.24 ℃,反应时间3.15 h,在此条件下羧甲基取代度为0.883.根据实际情况,考虑到可操作性,校正最佳工艺为:氯乙酸浓度1.3 mol/L,反应温度63 ℃,反应时间3.2 h,此条件下羧甲基取代度为0.882,与预测值接近,说明该模型可以很好地预测薤白多糖羧甲基化条件与羧甲基取代度之间的关系.同时也证明了该方法的可行性.
2.2 薤白多糖羧甲基化修饰产物体外抗氧化活性
2.2.1 薤白多糖羧甲基化修饰前后对·OH的清除作用
薤白多糖及各组分羧甲基化修饰前后对·OH的清除率见表4.
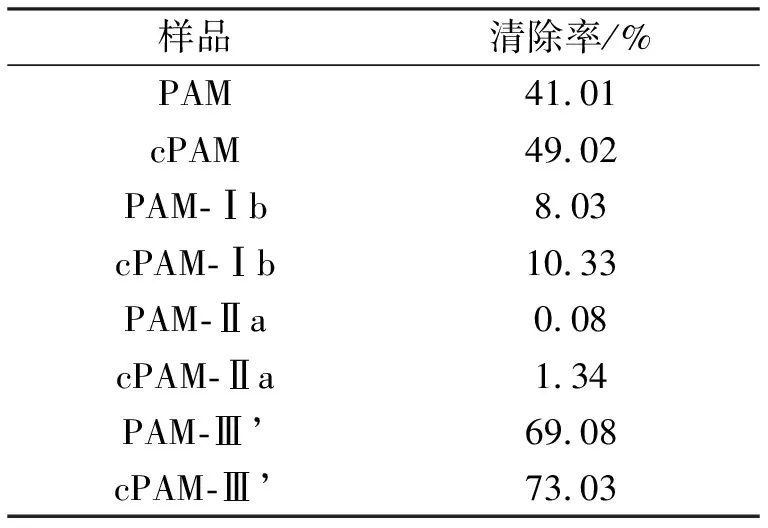
表4 薤白多糖羧甲基化修饰前后对·OH的清除率Tab.4 Scavenging effect of PAM and cPAM on· OH
从表4可以看出,薤白多糖羧甲基化修饰后对H2O2/Fe2+体系通过Fenton反应产生的·OH清除率都有所提高,说明羧甲基化修饰可改变或增加多糖的生物学活性.
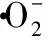
表5 薤白多糖羧甲基化修饰前后对的清除率Tab.5 Scavenging effect of PAM and cPAM on
3 结 论