超声辅助碱解萃取-气相色谱-电子捕获检测器测定海洋沉积物中8种多溴联苯醚
2015-08-03王国光张大海杨丹丹彭佳琳李先国
王国光, 张大海, 杨丹丹, 彭佳琳, 李先国
(中国海洋大学,海洋化学理论与工程技术教育部重点实验室,山东青岛266100)
添加型溴系阻燃剂多溴联苯醚(PBDEs)价格便宜、阻燃效率高、热稳定性好,被广泛应用于电子、电器、塑料、纺织、建材和石油等领域[1]。商业生产的PBDEs阻燃剂主要分为五溴、八溴和十溴联苯醚。PBDEs与塑料等制成品之间不以稳定的化学键相连,而以分子间作用力相结合[2],在产品的生产、使用和废弃过程中,易进入周围环境,在大气[3]、水体[4]、沉积物[5]、人[6]和动物组织[7]中都有检出。PBDEs具有较高的脂溶性、持久性和生物累积性,对环境[8]和生物体[9]具有极大的毒性,属于持久性有机污染物。
PBDEs在水生环境中主要聚集于沉积物,世界各地的河流[10,11]、湖泊[12]和海洋沉积物[13,14]中都有检出。PBDEs在沉积物中的低含量和干扰物质(有机农药、色素等)的存在使得检测困难,因此PBDEs的纯化是其检测的关键。目前,关于沉积物中 PBDEs的提取方法主要有索氏提取法[15,16]、加速溶剂提取法[17]、微波辅助萃取法[18]、超声辅助萃取法[19]等。其中,索氏提取法最经典,但溶剂用量大且耗时,不适合批量样品的前处理。加速溶剂萃取和微波辅助萃取需要专门的萃取仪器,价格比较昂贵。超声辅助萃取法省时、省溶剂且不需要专门仪器,可用于批量处理样品。
对沉积物样品中PBDEs的净化,一般采用浓硫酸洗涤,但回收率明显偏低。碱液处理样品的效果优于酸洗样品,采用NaOH水溶液洗脱萃取液还可以消除色素的干扰[20],但是该法无法有效除去有机氯农药(OCPs)对GC-ECD检测PBDEs的干扰,且回收率也不理想。
本工作在超声辅助条件下,利用NaOH甲醇溶液作为碱解介质,OCPs在碱溶液中分解,再结合有机溶剂萃取沉积物中的PBDEs,达到净化和萃取同时进行的目的,解决了 GC-ECD检测PBDEs时OCPs的干扰问题。该方法成本低廉、操作简便且回收率稳定,可满足批量样品的检测需求。
1 实验部分
1.1 仪器与试剂
气相色谱-电子捕获检测器(GC-2010 plus,Shimadzu);旋转蒸发仪(Laborota 4000,Heidolph Instruments GmbH &Co KG);超声波仪(KS-3000,宁波科生仪器厂);正己烷、二氯甲烷、丙酮、甲醇、异辛烷均为色谱纯,购自北京百灵威化学技术有限公司。PBDEs混合标准品(BDE-CSM)、回收内标PCB-209 和2,4,5,6-四氯间二甲苯(TCmX)及内标3,3′,4′,4-四 溴 联 苯 醚 (BDE-77)均 购 自 美 国AccuStandard公司。BDE-CSM包括美国环保署(US-EPA)1614方法(草案)中列出的环境中优先关注的 8 种 PBDEs 单体:2,4,4′-三溴联苯醚(BDE-28)、2,2′,4,4′-四溴联苯醚(BDE-47)、2,2′,4,4′,5-五溴联苯醚(BDE-99)、2,2′,4,4′,6-五溴联苯 醚 (BDE-100 )、2,2′,4,4′,5,5′-六 溴 联 苯 醚(BDE-153)、2,2′,4,4′,5,6′-六 溴 联 苯 醚 (BDE-154)、2,2′,3,4,4′,5′,6-七溴联苯醚(BDE-183)和十溴联苯醚(BDE-209)。其中BDE-209的质量浓度为25.00 μg/mL,其他单体的质量浓度均为2.50 μg/mL。
1.2 样品的采集与处理
1.2.1 样品的采集
表层(2~3 cm)沉积物样品搭载国家自然科学基金委员会黄渤海公共航次,于2013年11月用箱式采泥器采集,采样站位见图1。样品用锡纸包裹,于-20℃冷冻保存。
1.2.2 样品前处理
将沉积物样品解冻,去除砾石、贝壳等杂物后冷冻干燥,研磨后过80目筛备用。
样品用正己烷-二氯甲烷(1∶1,v/v)混合溶剂萃取至无PBDEs检出,于60℃烘干作为空白基质。
准确称取沉积物样品10.00 g,加入0.50 g铜粉和 10 μL 100 ng/mL 回收内标(TCmX、PCB-209)以及 30 mL 2.00 mol/L NaOH 甲醇溶液,混合均匀后超声30 min,碱液中加入45 mL水、50 mL正己烷涡旋萃取后离心,分离出有机相,萃取液旋转蒸发浓缩至2 mL左右,得到超声辅助碱解萃取样品。

图1 渤海表层沉积物采样站位图Fig.1 Sampling sites of the surface sediments in Bohai Sea
1.2.3 样品柱层析
选用30 cm×1.5 cm玻璃层析柱,用正己烷湿法装柱,自下而上分别为7.00 g活化硅胶(含质量分数为5%的H2O,去活化)和3.00 g无水硫酸钠。用40 mL正己烷润洗之后将浓缩后的提取液转移至层析柱,50 mL正己烷一次性洗脱并收集洗脱液。洗脱液旋转蒸发至0.5 mL左右,转移至样品瓶中,氮吹吹干,加入20 μL 100 ng/mL定量内标 BDE-77,异辛烷定容至100 μL后进GC-ECD检测。
1.3 色谱条件
三溴~七溴PBDEs采用DB-5MS毛细管色谱柱(30 m×0.25 mm×0.25 μm)分析。升温程序如下:初始柱温100℃,保留1 min,以10℃/min升至190℃;5℃/min升至255℃,保留0.5 min;2℃/min升至300℃,保留10 min。载气为高纯氮气,流速为3.0 mL/min;检测器温度315℃,进样口温度280℃,无分流进样,进样量1 μL。
BDE-209采用DB-5毛细管色谱柱(15 m×0.25 mm×0.10 μm)测试分析。升温程序如下:初始温度100℃,保留1 min,以10℃/min升至200℃,保留0.5 min;以 5℃/min升至 265℃;以10℃/min升至300℃,保留12 min。载气为高纯氮气,流速3.0 mL/min;检测器温度315℃,进样口温度290℃,无分流进样,进样量1 μL。
2 结果与讨论
2.1 样品萃取方法的优化
准确称取干沉积物样品10.00 g,加入0.50 g铜粉和 10 μL 100 ng/mL 回收内标(TCmX、PCB-209),50 mL 正己烷-丙酮(1∶1,v/v)混合溶剂超声萃取30 min,离心分离出有机相,重复3次,合并萃取液,旋转蒸发浓缩至2 mL左右,然后分3次加入15 mL正己烷淋洗,进行溶剂置换,最终旋转蒸发浓缩至2 mL左右得到普通超声辅助萃取样品。将普通超声辅助萃取与超声辅助碱解萃取对同一沉积物样品的提取效果进行了比较。普通超声辅助萃取样品的色谱图基线严重漂移,目标物几乎被杂质峰所掩盖(见图2a)。经超声辅助碱解萃取处理样品后,杂质影响显著减少,基线稳定,典型PBDEs目标峰比较明显(见图2b),符合样品测试的要求。本文选用超声辅助碱解萃取处理样品,并进一步优化了萃取条件。
加强电力工程输电线路施工管理有利于施工中各环节和各部门的主动配合和积极协作,要在制度上和管理上确保施工的协调有序进行,在实质上缩短电力工程输电线路施工的期限,提高电力工程输电线路建设的工作效率。
2.2 超声辅助碱解萃取方法的条件优化
2.2.1 NaOH 甲醇溶液的浓度
OCPs可以在强碱性溶液中发生分解[21]。本实验室在前期测定沉积物中PCBs的研究中发现,在浓度大于1.5 mol/L的 NaOH甲醇溶液中,OCPs能够完全分解[22]。
将10 μL 50 ng/mL PBDEs混合标准溶液直接加入30 mL 2.0 mol/L NaOH甲醇溶液中,超声萃取30 min后加入45 mL水、50 mL正己烷涡旋萃取,离心分离有机相,浓缩定容至1 μL进行检测。作为对比,将10 μL 50 mg/L PBDEs混合标准溶液加入10.00 g沉积物样品中,经过与上述相同的超声碱解萃取、离心、浓缩定容步骤后测定。实验结果如图3所示,PBDEs各单体的回收率在66.0%~116.9%之间,随单体差异有所不同,且在2.00 mol/L NaOH甲醇溶液中各单体的回收率达到最大,确定2.00 mol/L NaOH甲醇溶液为超声辅助碱液。
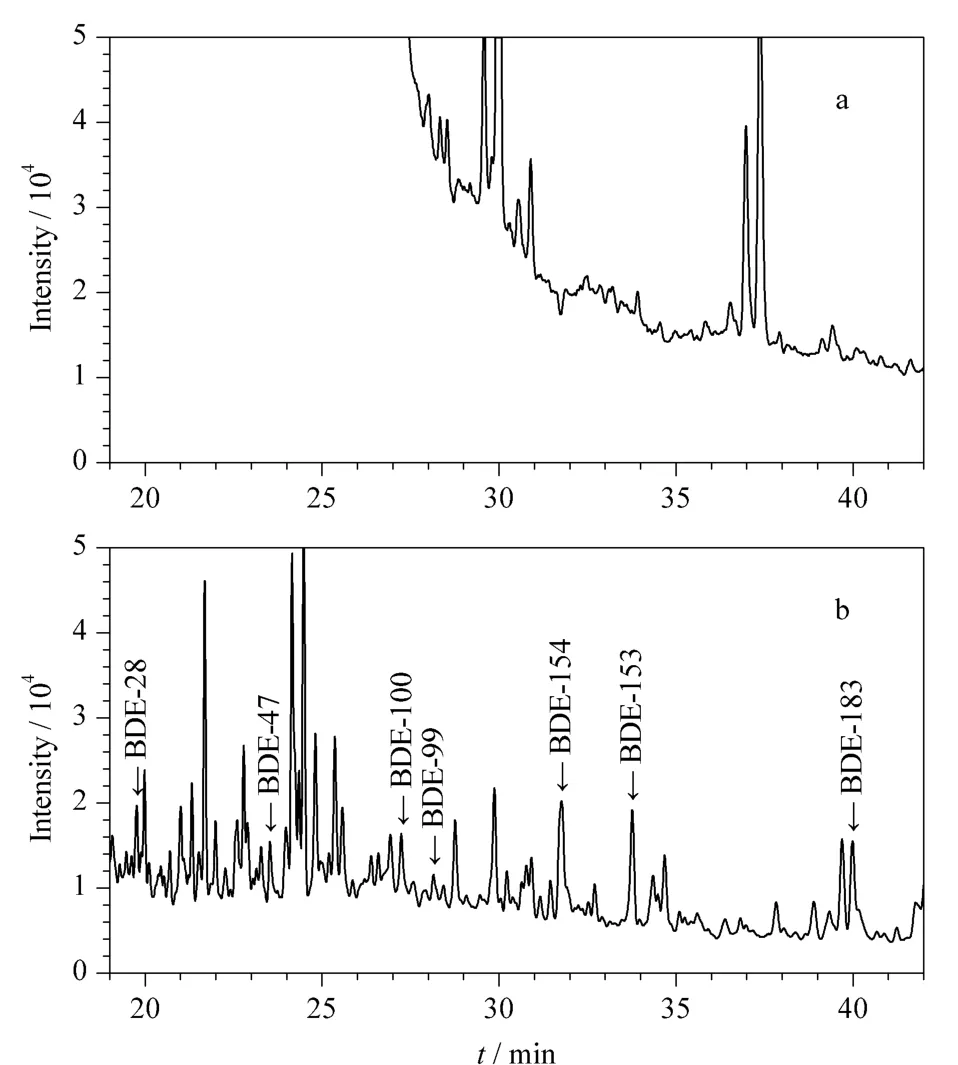
图2 同一沉积物样品经(a)超声辅助萃取和(b)超声辅助碱解萃取后的GC-ECD色谱图Fig.2 GC-ECD chromatograms of a sediment sample after(a)ultrasonically assisted extraction and(b)ultrasonically assisted alkaline hydrolysis extraction
2.2.2 萃取溶剂的选择
沉积物中PBDEs的萃取多采用正己烷或正己烷和其他极性溶剂的混合物作为萃取剂,本实验分别选取正己烷和正己烷-二氯甲烷(1∶1,v/v)对同一样品进行萃取测试。采用正己烷-二氯甲烷(1∶1,v/v)萃取的色谱图中基线明显漂移,杂质峰较多(见图4a);而正己烷萃取的色谱图中基线得到明显改善,目标物峰的分离度较好(见图4b),能够满足测试要求,因此选择正己烷为最优萃取溶剂。检测效果的差异性主要受二氯甲烷中氯元素的影响,同时由于其极性比较大,萃取能力增强导致杂质增多,对PBDEs的检测干扰很大。
2.2.3 柱层析净化填料的选择
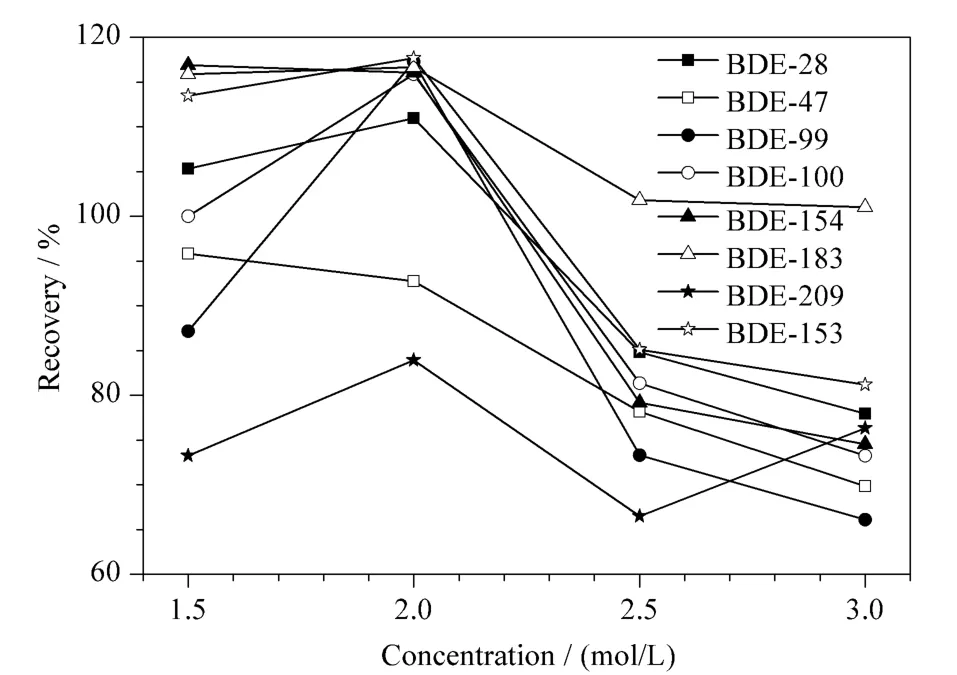
图3 不同浓度的NaOH甲醇溶液中超声30 min时PBDEs各单体的回收率Fig.3 Recoveries of BDE congeners treated in NaOH menthanol solution with different concentration by ultrasonification for 30 min

图4 同一沉积物样品经(a)正己烷-二氯甲烷(1∶1,v/v)和(b)正己烷萃取后的GC-ECD色谱图Fig.4 GC-ECD chromatograms of a sample extracted by (a)n-hexane-dichloromethane (1∶1,v/v)and (b)n-hexane
PBDEs单体种类多,在样品中的含量低,受到杂质的干扰严重。为了消除杂质的影响,分别选用硅胶、氧化铝-硅胶-NaOH 硅胶-硅胶-硫酸硅胶-硅胶、硅胶-硫酸硅胶-硅胶(自下而上)3种填料方式对同一样品进行净化测试分析。样品经过超声辅助碱解萃取后,采用3种填料方式的净化效果基本相同,杂质含量均较少、目标物峰较明显(见图5)。但后两种净化方法的填料制备过程繁琐,其净化效果易受硅胶柱的装填及洗脱速度影响,测试结果重现性较差,不利于批量样品的处理。因此选用单层硅胶作为净化材料即能满足分析测试要求。

图5 同一沉积物样品采用(a)硅胶、(b)氧化铝-硅胶-NaOH 硅胶-硅胶-硫酸硅胶-硅胶和(c)硅胶-硫酸硅胶-硅胶净化后的GC-ECD色谱图比较Fig.5 GC-ECD chromatograms of one sample purified by (a)silica gel,(b)alumina-silica-sodium hydroxide silica-silica-sulfuric acid silica-silica gel and (c)silica-sulfuric silica-silica gel
考察了正己烷和正己烷-二氯甲烷(1∶1,v/v)为洗脱溶剂时样品中PBDEs的洗脱效果,综合评价后选择正己烷为洗脱剂。当极性大的二氯甲烷为洗脱剂时,样品的GC-ECD色谱图基线严重漂移,目标物峰多数被杂质峰掩盖,难以进行定量分析(见图6a);正己烷为洗脱剂时基线平稳且杂质少,目标物峰明显,符合定量分析要求(见图6b)。
2.2.5 气相色谱柱的选择

图 6 同一样品采用(a)正己烷-二氯甲烷(1∶1,v/v)和(b)正己烷洗脱后的GC-ECD色谱图Fig.6 GC-ECD chromatograms of a sample eluted by (a)n-hexane-dichloromethane (1∶1,v/v)and (b)n-hexane

图7 同一样品采用(a)15 m和(b)30 m色谱柱分离的GC-ECD 色谱图Fig.7 GC-ECD chromatograms of a sample separated on (a)15 m and (b)30 m capillary columns
PBDEs的沸程宽(310 ~425 ℃)[23],分流歧视严重,即在色谱柱上后出峰组分的响应值比先出峰的组分低较多,无法准确定量,因此选用30 m和15 m的色谱柱分别对同一样品各组分进行测定,评价其对各组分的检测效果。由于BDE-209的相对分子质量大,对温度比较敏感,高温下易发生降解,导致其在30 m色谱柱上的响应值极低(见图7a),而在15 m的短色谱柱上,BDE-209的响应值得到较大的提高,并且出峰时间早(见图7b),降低了其在色谱柱上的降解。但对三溴~七溴联苯醚,15 m色谱柱相比于30 m色谱柱分离效果差,重复性差,且一些低溴联苯醚(BDE-28、BDE-47)的响应值低,无法满足定量检测要求。因此,选用30 m色谱柱检测三溴~七溴联苯醚,15 m色谱柱检测BDE-209。
2.3 方法学考察
2.3.1 线性关系和检出限
将8种PBDEs混合标准溶液用异辛烷进行逐级稀释,分别配制 1.0、5.0、12.5、50、80、100、200 ng/mL的混合标准液(其中BDE-209的质量浓度分别为 10、50、125、500、800、1 000、2 000 ng/mL),且每个浓度的混合标准液中定量内标BDE-77的质量浓度均为20 ng/mL。以目标化合物与BDE-77的峰面积之比y对二者的质量浓度比x进行线性回归;以信噪比(S/N)为3时GC-ECD检出PBDEs的含量为检出限(LOD),结果见表1。PBDEs各单体在各自的浓度范围内线性关系良好,相关系数r2为0.998 4~0.999 8;三溴~七溴联苯醚的检出限为0.002~0.011 ng/g,BDE-209的检出限为0.097 ng/g。

表1 8种PBDEs组分混合标准溶液的线性范围、回归方程、相关系数及检出限Table 1 Linear ranges,regression equations,correlation coefficients (r2)and limits of detection (LODs)of the eight PBDEs
2.3.2 准确度和精密度
在空白对照沉积物样品中添加PBDEs混合标准品,考察方法的准确度和精密度。BDE-209进行3 个水平(10.0、125.0、1 000.0 ng/mL)的加标回收试验,其他各组分分别进行 5个水平(1.0、5.0、12.5、50、80、100 ng/mL)的加标回收试验,各水平均进行5次平行测定。PBDEs各单体的加标回收率范围为63.6%~110.3%,相对标准偏差(RSD)为1.7%~15.5%。方法回收率高,精密度好,稳定可靠,能够满足样品定量分析的要求。
2.4 实际样品的检测
采用优化的方法测定渤海表层沉积物中PBDEs的含量,样品测定结果见表2。所测样品中,∑8PBDEs(8种单体含量总和)为1.566~6.760 ng/g,其中 BDE-209 的含量为1.461 ~6.438 ng/g。各站位中 BDE-209是主要的检出物质,含量是∑7PBDEs的20~60倍,这与我国大量使用商业十溴联苯醚阻燃剂相吻合。与国内外其他地区表层沉积物中 PBDEs的含量(见表3)相比,该地区的∑7PBDEs的含量与长江口和韩国沿海表层沉积物中大致相当,略低于我国台湾沿海、东海、南海和美国五大湖地区,远低于珠江口(电子垃圾拆解区)和香港近海地区(港口和工业区),表明渤海地区∑7PBDEs污染处于中低水平。渤海表层BDE-209的含量除与南海和台湾近海地区相当外,远低于其他研究地区,表明BDE-209在该地区污染处于低水平。但是,考虑到PBDEs对环境和人体的危害,一些防御和管理措施在渤海地区应得到加强。
其他7种单体中,BDE-99、BDE-100和 BDE-183含量比较高,这与BDE-99和BDE-100、BDE-183分别是商业五溴、八溴联苯醚阻燃剂的主要组成成分[31]相对应,进一步表明这两种阻燃剂在所研究区域也有一定程度的使用。除 P4站位外,PBDEs含量整体呈现出由近岸向远岸递减的趋势,说明陆地的人为活动、表层冲刷和河流的输入对渤海地区PBDEs的污染有着非常大的影响。

表2 渤海表层沉积物中8种PBDEs单体的含量Table 2 Contents of the eight PBDE congeners in the surface sediments in Bohai sea
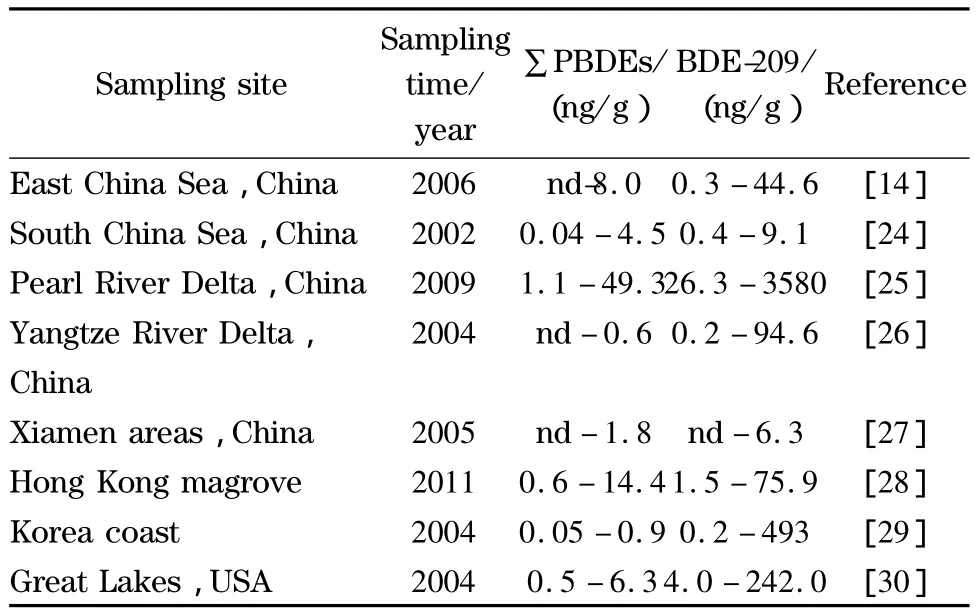
表3 世界其他地区表层沉积物中PBDEs的含量Table 3 PBDE levels in the surface sediments from other regions around the world
P1~P4站位于莱州湾附近,∑8PBDEs和BDE-209的含量均高于M1~M4站位,主要受近岸人为活动的影响。著名的山东潍坊滨海经济开发区位于莱州湾的沿岸,是重要的化工业生产基地,并且有中国最大的溴系阻燃剂生产工厂。此外,莱州湾是许多内陆河入海聚集区,如白浪河、胶莱河、弥河和小清河等,由河流输入带来大量的工业和生活废水导致近岸PBDEs含量的增加。
3 结论
本文建立了超声辅助碱液分解杂质与正己烷萃取相结合,单层硅胶净化、正己烷洗脱和GC-ECD检测沉积物中8种PBDEs的方法。该方法处理样品的效果明显优于普通超声萃取,杂质含量显著减少,基线稳定,PBDEs各单体出峰明显,同时PBDEs回收率良好,能够满足样品中PBDEs定量检测的要求。运用该方法测定渤海表层沉积物中的8种PBDEs,结果表明BDE-209为主要检出物质,其他三溴 ~七溴代联苯醚中以 BDE-99、BDE-100和BDE-183为主,含量总体呈现出由近岸向远岸递减的趋势。
[1] Huang F F,Li J G,Zhao Y F,et al.Environmental Chemistry(黄飞飞,李敬光,赵云峰,等.环境化学),2011,30(2):418
[2] Rakkestad K E,Dye C J,Yttri K E,et al.J Environ Monit,2007,9(12):1419
[3] Chen D H,Bi X H,Liu M,et al.Chemosphere,2011,82(9):1246
[4] Qiu X H,Zhu T,Hu J X.Chemosphere,2010,80(10):1207
[5] Nouira T,Risso C,Chouba L,et al.Chemosphere,2013,93(3):487
[6] Frouin H,Lebeuf M,Hammill M,et al.Chemosphere,2011,82(5):663
[7] Rochman C M,Lewison R L,Eriksen M,et al.Sci Total Environ,2014,476/477:622
[8] Hong W,Wei D Y,Dong H M.Chemical Engineering&Equipment(洪伟,魏东洋,董洪梅.化学工程与设备),2012(12):150
[9] McDonald T A.Chemosphere,2002,46:745
[10] Chen C E,Zhao H X,Chen J W,et al.Chemosphere,2012,88(7):791
[11] Zou Y M,Ran Y,Gong J,et al.Environ Sci Technol,2007,41(24):8262
[12] Zhou P,Lin K F,Zhou X Y,et al.Chemosphere,2012,88(11):1375
[13] Pan X H,Tang J H,Li J,et al.J Environ Monit,2010,12(6):1234
[14] Li Y Y,Lin T,Chen Y J,et al.Environ Pollut,2012,171:155
[15] Chen L G,Huang Y M,Peng X C,et al.Chemosphere,2009,76(2):226
[16] Chen S J,Mai B X,Zeng Y P,et al.Acta Scientiae Circumstantiae(陈社军,麦碧闲,曾永平,等.环境科学学报),2005,25(9):1255
[17] You Z Z,Kong D X,Xu J,et al.Environmental Chemistry(由宗政,孔德祥,许静,等.环境化学),2013,32(7):1410
[18] Wan X,Wang B,Zhao S M,et al.Environmental Chemistry(万幸,王彬,赵世民,等.环境化学),2011,30(10):1781
[19] Tang Z W,Huang Q F,Cheng J L,et al.Environ Sci Technol,2014,48(3):1508
[20] EPA Method 1668
[21] GB 13015-91
[22] Duan X Y,Li X G,Li Y X,et al.Environmental Chemistry(段晓勇,李先国,李艳霞,等.环境化学),2012,31(10):1645
[23] Huang F F,Zhao Y F,Li J G,et al.Chinese Journal of Chromatography(黄飞飞,赵云峰,李敬光,等.色谱),2011,29(8):743
[24] Mai B X,Chen S J,Luo X J,et al.Environ Sci Technol,2005,39(10):3521
[25] Chen S J,Feng A H,He M J,et al.Sci Total Environ,2013,444:205
[26] Chen S J,Gao X J,Mai B X,et al.Environ Pollut,2006,144(3):651
[27] Jiang J J,Lee C L,Fang M D,et al.Mar Pollut Bull,2011,62(4):815
[28] Zhu H,Wang Y,Wang X,et al.Sci Total Environ,2014,468:130
[29] Moon H B,Kannan K,Lee S J,et al.Chemosphere,2007,66(2):243
[30] Song W,Ford J C,Li A,et al.Environ Sci Technol,2005,39(15):5600
[31] Chen S J.[PhD Dissertation].Guangzhou:Guangzhou Institute of Geochemistry,Chinese Academy of Sciences(陈社军.[博士学位论文].广州:中国科学院广州地球化学研究所),2005
