O-磺化/O-季铵化-N,N-双烷基壳聚糖混合单分子膜及 自组装囊泡性质
2015-07-25毛扬帆李明春辛梅华
毛扬帆,李明春,辛梅华
(华侨大学材料科学与工程学院,环境友好功能材料教育部工程中心,福建 厦门 361021)
自组装是指由分子之间的非共价相互作用驱动以及分子形状自发识别而形成超分子结构[1]。自组装的形成一般由一种作用力为主或几种作用力共同作用,其中静电作用较其他二级作用力更强[2]。壳聚糖及其衍生物常用于具有静电作用的自组装中,Wang 等[3]制备了N,N-二甲基-N-十八烷基-赖氨酸改性壳聚糖(OQLCS),分别接枝聚乙二醇单甲醚(mPEG)和叶酸(FA),制得mPEG-OQLCS 和FA-OQLCS,将三者与胆固醇混合利用水化法制得自组装囊泡,囊泡对钙黄绿素具有低渗透率,可应用于亲水性药物的包载。Fan 等[4]制备了两亲性的O-羧甲基-N-烷基化壳聚糖,研究了产物与阳离子表面活性剂十六烷基三甲基溴混合体系的自组装行为,结果表明,混合体系能自发形成囊泡,静电作用和疏水作用是囊泡形成的主要驱动力。Shu 等[5]制备了N-(2-羟基)丙基-3-三甲基壳聚糖季铵盐与硫酸葡聚糖自组装纳米球,以牛血清蛋白为模型药物,研究了蛋白质药物在口服给药领域的应用,结果表明,在酸性条件下其纳米球具有缓释效果。Valente等[6]以壳聚糖和硫酸葡聚糖为原料制备载牛血清蛋白的纳米粒,并与间充质干细胞共同封装至海藻酸钠纳米粒中形成新型双药物递送系统,结果表明,纳米粒通过静电自组装,具有粗糙的表面,有利于细胞迁移和黏附,载药纳米粒50h 的累积释放率为10%,900h 释放平衡的累积释放率为35%左右。Martins 等[7]制备N,N,N-三甲基壳聚糖,与海藻酸钠复合制备聚电解质复合物,研究其对姜黄素的释放,结果表明,其在模拟胃液中30h 释放平衡的累积释放率为20%。综上所述,静电作用对壳聚糖及其衍生物自组装行为及药物释放行为具有一定的影响,目前静电作用的自组装研究主要集中在囊泡、纳米粒等方面。在天然高分子共组装领域,聚阳离子以壳聚糖及季铵化壳聚糖研究较多,聚阴离子则以海藻酸钠、硫酸葡聚糖研究较多,且研究多为水溶性产物,油溶性产物的共组装研究鲜有报道。磺化壳聚糖作为水溶性阴离子壳聚糖衍生物,不仅具有海藻酸钠、硫酸葡聚糖所具有的生物相容性和生物可降解性,还具有抗病毒性、抗凝血性、抗菌性和成骨活性等优点。本文制备了油溶性的O-磺化-N,N-双十二烷基化壳聚糖(HSDLCS)和O-季铵化-N,N-双十二烷基化壳聚糖(QADLCS),合成路线见图1。考虑双亲分子单分子膜的性质在一定条件下可预测自组装囊泡的结构与性质[8],本文研究了HSDLCS/QADLCS 混合单分子膜和自组装囊泡的性能,为进一步研究其自组装行为提供依据。

图1 壳聚糖衍生物HSDLCS 和QADLCS 的合成路线图
1 实验部分
1.1 主要试剂及仪器
O-磺化-N,N-双十二烷基化壳聚糖(HSDLCS)和O-季铵化-N,N-双十二烷基化壳聚糖(QADLCS),实验室自制(壳聚糖的相对分子质量为500000;HSDLCS 磺化度为21.67%,烷基化度为177.10%;QADLCS 季铵化度23.69%,烷基化度为178.59%。两个产物均溶于THF、DMF 和氯仿)[9];维生素B12,上海国药集团;其他试剂,均为市售分析纯。
JML04S 型双驱动膜天平,上海中晨数字技术设备有限公司;UV-3 系列紫外可见分光光度计,上海美谱达仪器有限公司;HITACHI S-3500N 扫描电镜,日本Hitachi 公司;ZEN3600 纳米激光粒度及Zeta 电位分析仪,英国malvern 公司。
1.2 HSDLCS/QADLCS 混合单分子膜的π-A 等温线测定
将壳聚糖主链相对分子质量为500000 制得的HSDLCS 和QADLCS 分别溶解于氯仿中,于25mL容量瓶中配制成10-3mol/L 的溶液,按带电基团摩尔比1∶1 混合于10mL 容量瓶中。以二次水为亚相进行实验,用微量进样器取40μL 样品溶液,缓慢、均匀地滴加在亚相表面上,待溶液在亚相表面上铺展并挥发约30min 后进行压缩,用Wilhelmy 吊片法测定π-A 等温线。压膜速率为20mm/min,室温(20±1)℃, 实验重复3 次。配制相同浓度HSDLCS 和QADLCS 溶液,同样方法测定单组分π-A 等温线。
1.3 HSDLCS/QADLCS 复合囊泡的制备
0.1g 摩尔比为1∶1 的HSDLCS 和QADLCS 溶解于24mL 氯仿中,加入8mL 浓度为4mg/mL 的维生素B12溶液,冰浴超声30min 形成W/O 乳液,低温旋转蒸发至胶状半固体,放置过夜除氯仿。在冰浴下强力超声10min,冷冻离心40min,分离载药囊泡和未包封的药物。同样方法制备QADLCS、HSDLCS 载药囊泡及空白囊泡。
1.4 囊泡的粒径和Zeta 电位测定
将 1.3 节制得的 QADLCS、HSDLCS 及HSDLCS/QADLCS 自组装囊泡制成囊泡-水悬混液,采用纳米激光粒度及Zeta 电位分析仪在25℃下测定空白囊泡的粒径分布及Zeta 电位。
1.5 自组装囊泡的载药性能和药物释放行为
将载药囊泡放入透析袋并置于25mL 纯水中,间隔1h 取出3mL 透析液,再补充3mL 蒸馏水。透析液在UV361nm 测定吸光值,根据B12标准曲线方程计算药物释放量( C=0.05829A-0.00036 ,r=0.9995,线性范围5.36×10-3~5.36×10-2mg/mL),绘制载药囊泡释放曲线。由公式包封率=(M1+M2)/M×100%和载药量=(M1+M2)/M3(其中M1、M2、M3和M 分别为释药平衡时药物总释放量、未释放药物的质量、囊材的质量和总投药量;M2是由乙醇破坏囊泡后离心得到的上清液,采用UV 测定吸光值并由B12标准曲线方程计算得到),计算包封率和载药量。
2 结果与讨论
2.1 HSDLCS/QADLCS 混合单分子膜性质
2.1.1 混合单分子膜的π-A 等温线
按照实验部分1.2 的操作测得产物单分子膜的π-A 等温线如图2 所示,a、b、c 分别为O-磺化-N,N-双十二烷基壳聚糖(HSDLCS)、O-季铵化-N,N-双十二烷基壳聚糖(QADLCS)及HSDLCS/QADLCS混合单分子膜的π-A 曲线。由图2 可见,HSDLCS、QADLCS 及混合单分子膜的π-A 等温线都较为平滑,无明显的液态扩张相-液态凝聚相(LE-LC)转变,崩溃压均在35mN/m 以上,说明三者均可在水面上形成稳定的单分子膜。从π-A 曲线得到相应的崩溃压和极限分子面积见表1。由图2 和表1 可以看出,HSDLCS 的分子极限面积较QADLCS 低,这是因为与 HSDLCS 的磺酸盐基团相比较,QADLCS 的季铵盐基团空间阻碍作用较大,且基团间存在静电作用及水化层[10],从而影响了单分子膜分子间距离,导致QADLCS 的分子平均占有面积增大,所成的单分子膜较为扩张。与单组分产物相比,HSDLCS/QADLCS 混合单分子膜的崩溃压(46.14mN/m)和极限分子面积较大,这可能是因为二者在形成单分子膜时,亲水基团进入水相中,基团之间易形成静电相互作用,使膜压缩至崩溃时需要的压力更大,故崩溃压更大。但季铵盐阳离子周围有3 个甲基的屏蔽,在一定程度上阻碍了阴阳离子表面活性剂极性头基相互靠近,使得分子的平均占有面积更大,形成的单分子膜较为扩张[11]。
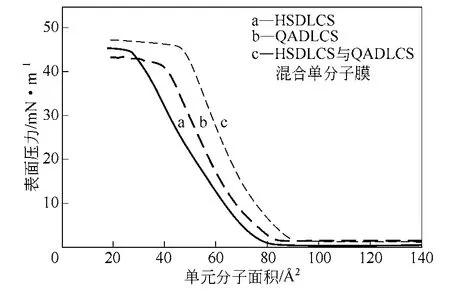
图2 HSDLCS、QADLCS 及其混合单分子膜的π-A 等温线 (1Å2=10-20m2)

表1 HSDLCS、QADLCS 及其复合单分子膜的崩溃压、极限分子面积和最大压缩模量
2.1.2 混合单分子膜的Cs-1-A 曲线
2.2 HSDLCS/QADLCS 复合囊泡的性质
2.2.1 自组装囊泡的SEM 图
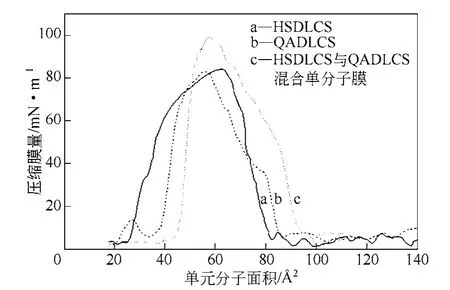
图3 HSDLCS、QADLCS 及其混合单分子膜的Cs-1-A 曲线
按照实验部分1.3 节的方法制备HSDLCS/ QADLCS 复合囊泡。囊泡的SEM 图如图4 所示,可见,复合自组装形成的囊泡接近于球形,粒径在200~400nm。

图4 HSDLCS/QADLCS 复合自组装囊泡的SEM 图
2.2.2 囊泡的粒径大小、分布及Zeta 电位
按照实验部分1.4 节的操作测得囊泡的粒径分布及Zeta 电位见表2。QADLCS、HSDLCS 和HSDLCS/QADLCS 自组装囊泡的Zeta 电位分别为49.4mV、-42.4mV 和-6.94mV,单组分囊泡的Zeta电位绝对值均大于 30mV,说明 QADLCS 和HSDLCS 自组装囊泡能够稳定存在。 而HSDLCS/QADLCS 复合囊泡的Zeta 电位较小,说明复合囊泡进行自组装时HSDLCS 的—SO3-基团与QADLCS 的—N(CH3)3+基团间存在静电作用[12],二者按比例复合后Zeta 电位不为0,则因为两者均由高相对分子质量壳聚糖制备而成,长链分子本身容易形成缠结和嵌套等结构,在空间位阻效应、静电作用及疏水作用的共同作用下,HSDLCS 分子链上的负电荷未能完全与QADLCS 分子链中的正电荷静电结合,导致两者形成囊泡时的电位不符合两者完全复合的化学计量比[13]。
由表2 可以看出,QADLCS、HSDLCS 和HSDLCS/QADLCS 自组装囊泡粒径分别为345.6nm、344.3nm 和 359.9nm,比SEM 中粒径略大。HSDLCS/QADLCS 复合囊泡的粒径较单组分囊泡略大,这可能是因为季铵盐基团为正四面体结构,空间位阻较大,在一定程度上阻碍了阴阳离子表面活性剂极性头基相互靠近[11]。3 种囊泡的多分散系数均在0.1~0.2,说明囊泡的粒径比较均匀,具有单分散性。
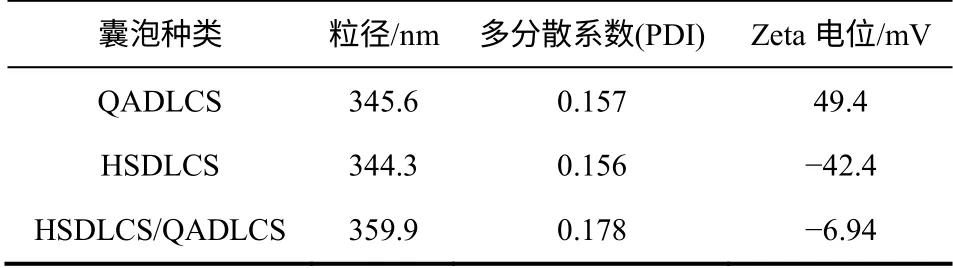
表2 自组装囊泡的粒径大小、分布及Zeta 电位
2.2.3 囊泡的载药性能及释放行为
以维生素B12为模型药物,按照实验部分1.3节的方法制备载药囊泡,测得载药量和包封率如表3 所示,与单组分囊泡相比,复合囊泡的载药量和包封率较高。

表3 HSDLCS、QADLCS 及其复合囊泡的载药量和包封率
载药囊泡的释放行为见图5,a、b、c 分别为QADLCS、HSDLCS 载药囊泡以及 HSDLCS/ QADLCS 复合载药囊泡的释放曲线。可见,3 种囊泡均有缓释作用,在30h 左右达到释药平衡,其平衡释放率分别为42.14%、38.16%和23.68%,药物释放速率和平衡释放量顺序为QADLCS>HSDLCS>HSDLCS/QADLCS 载药囊泡,说明三者中复合囊泡的通透性最低,膜结构较为紧密,这与单分子膜结果一致。与HSDLCS 结构中的磺酸盐基团相比,季铵盐基团由于空间占有较大且基团间存在一定的静电排斥作用,使得QADLCS 囊泡结构较为疏 松[14]。而HSDLCS/QADLCS 复合囊泡由于正、负离子极性头基之间存在强烈的静电作用,容易形成离子对结构[4],在静电作用和疏水作用的共同驱动下,复合囊泡具有更有序的结构,药物通透性降低。
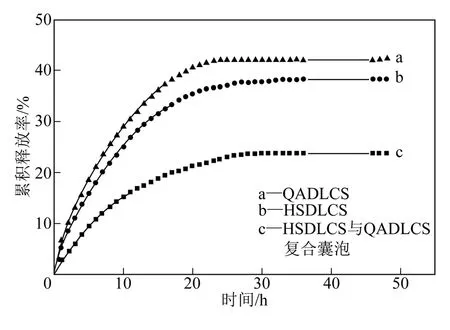
图5 自组装囊泡的药物释放曲线
2.3 囊泡性质与相应单分子膜性质的关系
囊泡的释放行为取决于囊泡分子膜的药物通透性,而单分子膜的最大压缩模量可以在一定程度上反映囊泡膜结构的紧密程度,通过对两者关系的考察可以建立单分子膜与相应自组装囊泡性质间的联系[8,15],为进一步研究产物结构、单分子膜、囊泡三者之间的关系提供理论依据。壳聚糖衍生物QADLCS、HSDLCS 及HSDLCS/QADLCS 单分子膜的最大压缩模量与其相应自组装载药囊泡药物平衡释放率关系如图6 所示。从图6 中可以看出,随着产物单分子膜最大压缩模量的增加,其相对应自组装载药囊泡的药物平衡释放率降低,并呈现一定的线性关系,说明壳聚糖衍生物结构不同会导致单分子膜性质及囊泡性质的改变,通过产物单分子膜的最大压缩模量能在一定程度上对囊泡结构紧密程度进行预测。

图6 产物单分子膜性质与相应自组装囊泡性质之间的关系
3 结 论
制得 O- 磺化-N,N- 双十二烷基壳聚糖(HSDLCS)和O-季铵化-N,N-双十二烷基壳聚糖(QADLCS),研究HSDLCS/QADLCS 混合单分子膜和自组装囊泡性质的关系。结果表明,与单组分产物单分子膜性质相比,HSDLCS/QADLCS 混合单分子膜具有较大的崩溃压和压缩模量;自组装囊泡HSDLCS 和QADLCS 的Zeta 电位绝对值大于30mV,能够稳定存在,而HSDLCS/QADLCS 复合囊泡的Zeta 电位较低;HSDLCS/QADLCS 复合囊泡具有较高的载药量和包封率,较低的药物释放率和平衡释放量。3 种单分子膜的最大压缩模量与其相应载药囊泡药物平衡释放率呈一定的线性关系。这些结果为进一步研究HSDLCS/QADLCS 混合自组装行为提供依据。
[1] Stephanopoulos Nicholas,Ortony Julia H,Stupp Samuel I,et al. Self-assembly for the synthesis of functional biomaterials[J]. Acta Materialia,2013,61:912-930.
[2] Fajardo André R,Piai Juliana F,Rubira Adley F,et al. Time- and pH-dependent self-rearrangement of a swollen polymer network based on polyelectrolytes complexes of chitosan/chondroitin sulfate[J]. Carbohydrate Polymers,2010,80:934-943.
[3] Wang H J,Zhao P Q,Liang X F,et al. Folate-PEG coated cationic modified chitosan-Cholesterol liposomes for tumor-targeted drug delivery[J]. Biomaterials,2010,31:4129-4138.
[4] Fan Yaxun,Liu Yan,Xi Juqun,et al. Vesicle formation with amphiphilic chitosan derivatives and a conventional cationic surfactant in mixed systems[J]. Journal of Colloid and Interface Science,2011,360:148-153.
[5] Shu Shujun,Zhang Xinge,Wu Zhongming,et al. Delivery of protein drugs using nanoparticles self-assembled from dextran sulfate and quaternized chitosan[J]. Journal of Controlled Release,2011,152:170 -172.
[6] Valente J F A,Gaspar V M,Antunes B P,et al. Microencapsulated chitosan-dextran sulfate nanoparticles for controlled delivery of bioactive molecules and cells in bone regeneration[J]. Polymer,2013,54:5-15.
[7] Martins Alessandro F,Bueno Pedro V A,Almeida Elizangela A M S,et al. Characterization of N-trimethyl chitosan/alginate complexes and curcumin release[J]. International Journal of Biological Macromolecules,2013,57:174-184.
[8] Kuo An-Tsung,Li Wei-Ta,Tseng Chia-Yao,et al. Probing the alkyl chain length effects on molecular packing characteristics of mixed ion pair amphiphile/double-chained cationic surfactant vesicular bilayers with the Langmuir monolayer approach[J]. Colloids and Surfaces A: Physicochem. Eng. Aspects,2014,454:23-31.
[9] 关品燊,辛梅华,李明春,等. O-季铵化-N,N-双烷基壳聚糖的单分子膜性质研究[J]. 化工进展,2011,30(12):2671-2675.
[10] 赵国玺,肖进新. 十二烷基季铵盐及其与十二烷基硫酸钠混合体系的表面活性[J]. 物理化学学报,1995,11(9):785-790.
[11] 余娜. 囊泡的自发形成与及其稳定性的研究[D]. 长春:吉林大学,2007.
[12] Fang Jianjun,Zhang Yun,Yan Shifeng,et al. Poly(L-glutamic acid)/chitosan polyelectrolyte complex porous microspheres as cell microcarriers for cartilage regeneration[J]. Acta Biomaterialia,2014,10:276-288.
[13] 何嫄,於麟,谭松巍,等. 壳聚糖-O-聚(聚乙二醇甲醚甲基丙烯酸酯)接枝共聚物的ATRP 合成及其自组装研究[J]. 高分子学报,2010,7(7): 897-902.
[14] Li Rong,Chen Qibin,Zhang Dazhi,et al. Mixed monolayers of Gemini surfactants and stearic acid at the air/water interface[J]. Journal of Colloid and Interface Science,2008,327:162-168.
[15] Li Mingchun,Su Sheng,Xin Meihua,et al. Relationship between N,N-dialkyl chitosan monolayer and corresponding vesicle[J]. Journal of Colloid and Interface Science,2007,311:285-288.
