盐水液滴降压蒸发析盐过程数值模拟
2015-07-24刘璐舒盼盼王茉刘彦丰
刘璐,舒盼盼,王茉,刘彦丰
(华北电力大学能源动力与机械工程学院,河北 保定 071003)
盐水降压蒸发技术可以广泛地应用于海水淡化[1-3]以及工业制盐[4-5]等领域,同时随着我国航天航空技术的发展,空间宇航员的活动日益频繁,太空中排放的很多液体都是盐水的混合物,因此研究盐水溶液的降压蒸发问题,可以有助于解决我国宇航员在太空生活垃圾的排放问题,更好地为航天员提供舒适的环境。
骆骞等[6]实验测得盐水溶液在降压环境下蒸发过程的温度变化情况,分析了不同压力、不同质量浓度和不同初始直径下的液滴温度变化情况,但是并没有给出盐析的蒸发率以及盐析对液滴温度的影响关系。Gopalakrishna 等[7]从实验和理论上研究了盐水溶液的闪蒸问题,分析了初始液膜浓度的影响以及过热度对盐水液膜的影响。Muthunayagam 等[8]建立了蒸发扩散模型,研究降压环境下盐水液滴直径和温度变化。Ebrahimian 等[9]建立双组分液滴蒸发模型,计算了盐水液滴在蒸发过程中温度和直径的变化,并分析了重力的影响因素。Liu 等[10]实验研究了真空环境下盐水液滴的温度变化情况,并分析了其影响因素。
本文对盐水液滴降压蒸发析盐过程进行模型研究,获得了盐析率与液滴温度随时间的变化关系,并分析了影响析盐率及液滴温度的主要因素。
1 盐水液滴降压蒸发析盐过程模型
模型简化假设如下:①液滴假设为理想球形,液滴温度仅沿径向变化;②液滴表面气相处于准稳态;③忽略环境气体的化学反应和可溶性;④忽略液滴和环境的辐射换热问题。
1.1 数学模型
液滴内部能量守恒方程见式(1)。

式中,T 为液滴的温度,K;ρl为液滴密度,kg/m3;Cpl为定压比热容,J/(kg·K);r 为液滴半径,m;λeff= χλλl是液滴内的有效导热系数,W/(m·K)。
液滴表面的气流运动加速了液滴内部混合,故引入修正系数χλ,见式(2)~式(5)。
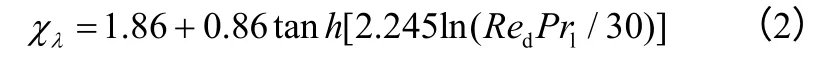
初始条件:

边界条件:


式中,rs为液滴表面半径,m;r0为液滴的初始半径,m;qm为蒸发换热的热流密度,见式(6),W/m2;qh为液滴和空气的对流换热密度,W/m2;qy为析盐放热的热流密度,W/m2。

式中,LV为水的蒸发潜热,单位为J/kg;m˙为质量蒸发率,kg/s,可由式(7)得到。
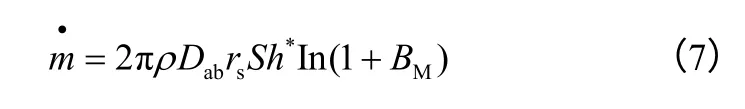
式中,ρ 为蒸气和空气混合气体的平均密度, kg/m3;Dab为水蒸气在空气中的传质扩散系数, m2/s;Sh*为修正舍伍德数,计算过程见文献[11];BM为Spalding 传质系数,可由式(8)计算得到。

Yv,s是液滴表面蒸气质量分数,Yv,a是空气中蒸气质量分数;Yv,s和Yv,a可由式(9)和式(10)得出。

式中,Pv,s为纯水液滴表面温度所对应的饱和蒸汽压,Pa,可由克劳修斯-克拉伯龙方程获得;Mv为水蒸气的摩尔质量;Pv,a为环境空气中水蒸汽分压力,Pa;Ma为空气的摩尔质量;αw为盐水溶液中水的活度系数,可由式(11)得到。

式中,Y2s是盐水中盐的质量分数。

式中,Td,s为液滴表面温度,K;Ta为环境空气温度,K;h 对流换热表面的传热系数,W/(m2·K)。

式中,s 为液滴温度下盐水的饱和度;Lc为析出单位质量盐分所释放的热量,取值为 6.3× 105J/kg[12]。
1.2 数值计算方法
随着液滴蒸发进行,液滴尺寸逐渐减少,引入量纲为1 参数η(η=rs/r0捕捉移动边界)。η的变化范围为0~1,在液滴的中心η=0,在液滴的表面η=1。对方程式(1)进行坐标转换,得到能量方程式(14)。
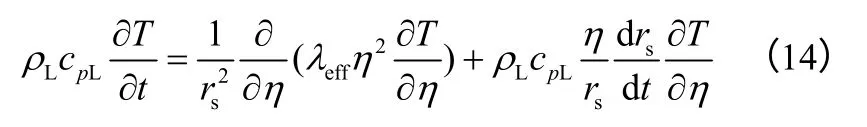
在本文计算过程中,沿液滴径向划分网格数150,时间步长为0.01ms,数值求解方法采用三角对阵法。
2 数值结果和讨论
2.1 模型验证
通过模型计算,获得了盐水在降压环境蒸发过程中的中心温度的变化。图1 中的初始条件和环境参数为:盐水浓度为26%,液滴直径为2.0mm,液滴的初始温度为10℃,环境压力由0.1MPa 降为3000Pa,数值模拟计算的结果和文献[11]实验数据进行对比,误差为2%左右,吻合较好。图2 中的初始条件和环境参数为:盐水浓度为26%,液滴直径为2.0mm,液滴的初始温度为10℃,环境压力由0.1MPa 降为4000Pa,数值模拟计算的结果和文献 [11]实验数据进行对比,误差为14%,证明了本文模型的有效性。

图1 计算结果和文献[11]实验数据比较
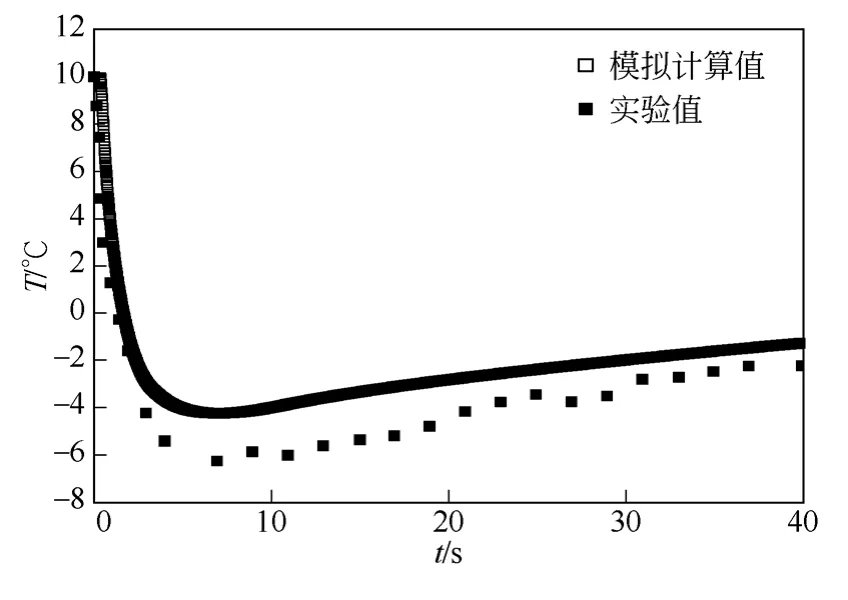
图2 计算结果和文献[11]实验数据比较
2.2 盐水液滴降压环境下析盐过程温度变化
如图3~图5 所示,所采用的工质为饱和盐水,液滴初始质量分数为26.416%,液滴初始温度为20℃;液滴的初始直径D0为2mm,环境压力由0.1MPa降为2000Pa。由图3 可以看出压降的变化过程,由0.1MPa 迅速下降,在3s 左右,液滴的压力迅速降到最低压力2000Pa 左右,之后压力不再发生变化。图4 为降压环境下的盐析率m 随时间的变化,由图4 可以看出,液滴的析盐率迅速下滑,在3s 左右进入稳定状态,主要由于压力的迅速下降,液滴和空气强制对流换热显著,加速了液滴中的水分大量迅速蒸发,导致盐分大量的析出,但是随着时间的推移,压力下降的速率减缓,直到3s 左右,对流热量不断地减少,导致蒸发速率的减少,盐析的速率也呈现快速下降的趋势,最后进入稳定阶段。由图5 得出液滴的温度在降压环境下迅速下降,液滴在5s 左右达到最低温度,之后有回升趋势,主要是受环境空气对流和盐析放热的影响,液滴的吸热量大于液滴蒸发的散热量,液滴温度有一定的回升。在降压蒸发过程中,由于水的汽化潜热远远大于析盐所放出的热量,并且水蒸发的速率大于盐分析出的速率,因此在降压环境中,析盐放热对液滴温度并不是影响很大,液滴的温度主要是受到空气对流和蒸发散热的影响。
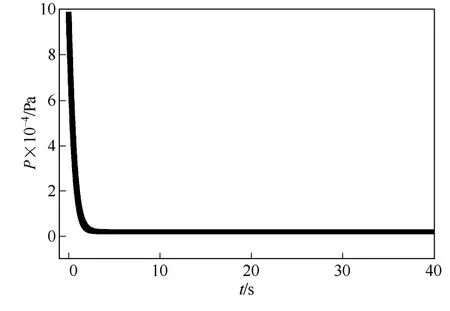
图3 环境压力随时间的变化

图4 盐析率随时间的变化

图5 液滴表面温度随时间变化
2.3 液滴初始直径对盐析率和温度变化的影响

图6 初始直径对盐析率的影响

图7 初始直径对液滴温度的影响
如图6、图7 所示,液滴的初始直径分别为1.2mm、1.6mm、2mm,液滴初始温度为20℃,盐的质量分数26.416%,环境压力由0.1MPa 降至2000Pa。由图6 可知,液滴直径越大,在初始阶段前3s 左右,液滴的析盐率越大,随着时间的推移,液滴的析盐率都迅速的下降,最后趋于一致。原因 是受蒸发速率的影响,液滴初始直径越大,蒸发速率越快,析盐越多。图7 所示为析盐过程中液滴温度的变化情况,在降压环境下,液滴温度迅速下降,直径越小,其蒸发过程中液滴所能达到的温度越低,之后液滴温度都有回升的趋势。主要是由于受到环境温度的影响,液滴的对流换热量和盐析放出的热量大于液滴蒸发所放出的热量,液滴温度回升。
2.4 液滴初始温度对盐析率和温度变化的影响
如图8、图9 所示,所用工质为饱和盐水,液滴初始直径1.6mm,初始温度分别为20℃、15℃、10℃,环境压力由0.1MPa 降至2000Pa。由图8 可以看出,液滴初始温度越高,其盐析率在初始时刻越高,但是随着时间的推移,由于液滴温度下降,盐析率逐渐趋于一致,可见初始温度对盐析率的影响主要在初期阶段,最终盐析率趋于一致。由图9可以看出,液滴初始温度越高,降压阶段液滴的蒸发速率越快,温度下降也越快,但是液滴最终的温度却趋于一致,可见初始温度主要影响蒸发初始阶段的质量蒸发率。
2.5 压降速率对盐析率和液滴温度变化的影响
如图10、图11 所示,所用工质为饱和盐水,液滴初始直径为1.6mm,液滴初始温度分别为20℃、15℃、10℃、环境压力由0.1MPa 降至2000Pa,10 000Pa、20 000Pa。由图10 可以看出,环境压力对液滴盐析率的影响很大,压降速率越大,降压初期盐析率越高,但在压力稳定后,盐析率基本趋于一致。由图11 可以看出,压降速率越大,液滴所能达到的最低温度越低,蒸发的速率也越快。上述情况的原因主要是由于压降速率越快,降压阶段液滴对流换热更加剧烈;此外环境压力越低,传质扩散越强,蒸发速率更快,液滴所能达到的温度也越低。

图8 初始温度对盐析率的影响

图9 初始温度对表面温度变化的影响
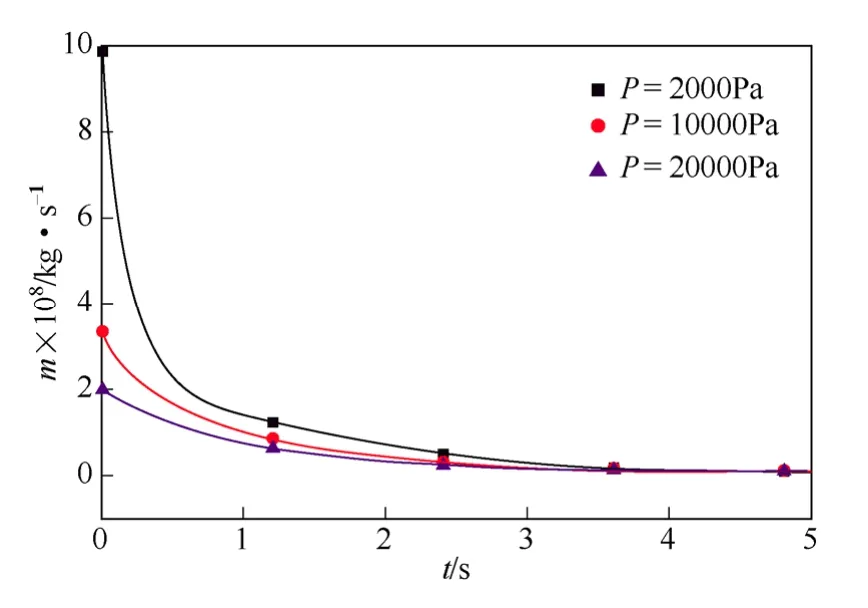
图10 压降对盐析率的影响

图11 压降对液滴表面温度变化的影响
3 结 论
(1)盐水液滴直径越大,蒸发初期阶段,盐析率越高,液滴温度受环境温度的影响变化越慢。
(2)液滴初始温度越高,液滴蒸发速率越快,蒸发初期盐析率越高,但随着液滴温度的下降,盐析率逐渐趋于一致,液滴温度最后趋于一致。
(3)压降速率越快,盐析率越大,蒸发速率越快,液滴所能达到的温度也越低。
[1] Liu Z,Yi J. Falling film evaporation heat transfer of water/salt mixtures from roll-worked enhanced tubes and tube bundle[J]. Applied Thermal Engineering,2002,22(1):83-95.
[2] Muthunayagam A E,Ramamurthi K,Robert Paden J. Modelling and experiments on vaporization of saline water at low temperatures and reduced pressures[J]. Applied Thermal Engineering,2005,25(5-6):941-952.
[3] Yang L,Shen S. Experimental study of falling film evaporation heat transfer outside horizontal tubes[J]. Desalination,2008,220(1-3):654-660.
[4] Akridge D G. Methods for calculating brine evaporation rates during salt production[J]. Journal of Archaeological Science,2008,35(6):1453-1462.
[5] KilIc A M. Recovery of salt co-products during the salt production from brine[J]. Desalination,2005,186(1-3):11-19.
[6] 骆骞,毕勤成,韩彦宁,等. 盐水液滴降压环境下蒸发过程[J]. 化工学报,2013,64(6):2001-2006.
[7] Gopalakrishna G,Purushothaman V M,Lior N. An experimental study of flash evaporation from liquid pools[J]. Desalination,1987,65(11):139-151.
[8] Muthunayagam A E,Ramamurthi K R,Paden J R. Modelling and experiments on vaporization of saline water at low temperatures and reduced pressures[J]. Appl. Therm. Eng.,2005,25(5-6):941-952.
[9] Habchi C,Ebrahimian V. Gravitational effects on multi-component droplet evaporation[J]. Microgravity Sci. Technol.,2012,24(3):229-235.
[10] Liu L,Bi Q C,Li H X. Experimental investigation on flash evaporation of saltwater droplets released into vacuum[J]. Microgravity Sci. Technol.,2009,21(1):255-260.
[11] 刘璐. 降压过程中及低压环境下液滴相变传热传质的机理研究 [D]. 西安:西安交通大学,2010.
[12] 迪安 J A. 兰氏化学手册[M]. 第13 版. 尚久方等译. 北京:科学出版社,1991:1520-1521.
