HPLC法同时测定化妆品中多种生物还原剂
2015-07-19冯亚男王梦丽谢红英宁欣陈芙蓉张玉霞徐小平
冯亚男,王梦丽,谢红英,宁欣,陈芙蓉,张玉霞,徐小平
(四川大学华药学院,四川成都610041)
HPLC法同时测定化妆品中多种生物还原剂
冯亚男,王梦丽,谢红英,宁欣,陈芙蓉,张玉霞,徐小平
(四川大学华药学院,四川成都610041)
建立同时测定嫩肤-01(NF-01)中维生素C、绿原酸和咖啡酸等多个生物还原剂的HPLC测定法。采用ODS(4.6mm×150mm×5μm)为色谱柱,流动相A为甲醇,流动相B为0.1%磷酸,进行梯度洗脱(A相0min→5min,0→0;5min→15min,0→30%;15min→30 min,30%→30%);检测波长为290 nm;流量为1mL/min。维生素C、绿原酸和咖啡酸在质量浓度43.5~636.0μg/mL,4.2~66.4μg/mL和4.3~68.8μg/mL内线性关系良好(线性方程分别为y=2 871.4x+ 1221.7,r=0.9995;y=45 240x+1089.5,r=0.999 4和y=103271x+41823,r=0.9999);连续3周考察溶液的稳定性,3个组份在1d内稳定,在6 d内基本稳定,在3周后出现较明显的变化。所建立的HPLC法能同时分离并定量该护肤品中极性差异较大的3种生物还原剂,可用于化妆品中类似配方的质量控制。
维生素C;绿原酸;咖啡酸;HPLC
1 实验部分
1.1 仪器与试药
仪器:LC-2010高效液相色谱仪(日本岛津仪器公司);品成纯水器(成都品成科技有限公司);KL 10260D超声清洗器;BT 125D电子天平(德国赛多利斯公司);漩涡震荡器。
试药:维生素C、绿原酸和咖啡酸对照品均购于中检所;NF-01嫩肤水(自制);甲醇为色谱纯(天津市科密化学试剂有限公司);磷酸为分析纯(重庆茂业化学试剂有限公司);超纯水(自制)。
1.2 溶液的制备
1.2.1 对照品溶液
精密称取维生素C对照品87.0mg,绿原酸对照品8.3mg,咖啡酸对照品8.6mg,置于100mL容量瓶中,加水溶解并稀释至刻度,摇匀即得对照品储备液。精密量取储备液2mL,置于10mL容量瓶,加水稀释定容,摇匀即得。
1.2.2 供试品溶液
精密量取供试品1mL,置于10mL容量瓶中,用水稀释至刻度,摇匀后精密量取2mL于10mL容量瓶中,用水稀释至刻度,摇匀即得。
1.3 色谱条件的筛选
1.3.1 梯度程序的筛选
流动相A:甲醇;流动相B:0.1%甲酸;分别在3种不同梯度程序下对化妆品进行了测定,梯度程序见表1(A+B=100%);色谱测定结果见图1。
1.3.2 不同酸的筛选
在流动相B分别为0.1%甲酸、0.1%磷酸、0.1%乙酸、水时,测定化妆品,结果见图2。
1.3.3 波长的筛选
维生素C、绿原酸、咖啡酸分别在波长为240, 270,290,323nm对化妆品进行了测定,最大吸收波长分别为245,324,323nm,结果见图3。

表1 3种不同梯度条件
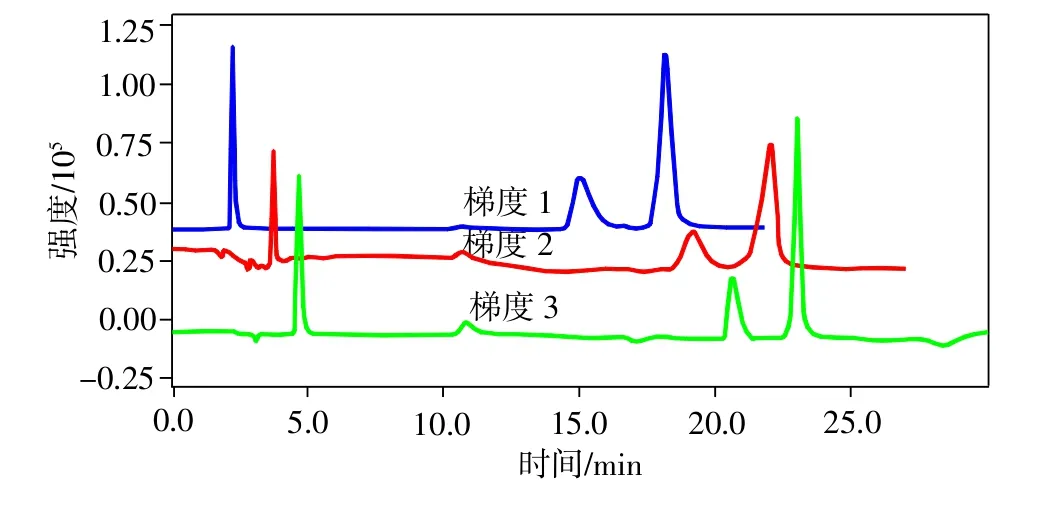
图1 不同梯度程序对本品分离的影响HPLC图
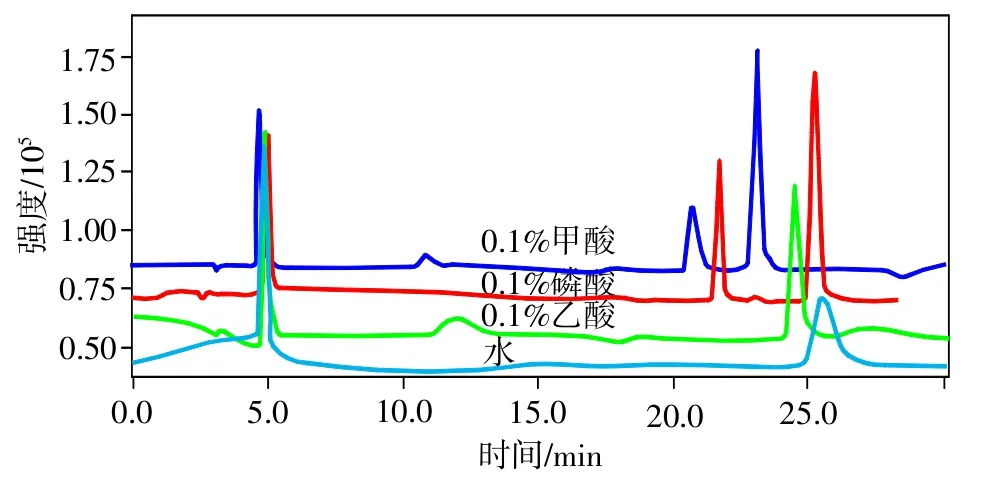
图2 不同酸对本品HPLC分离的影响
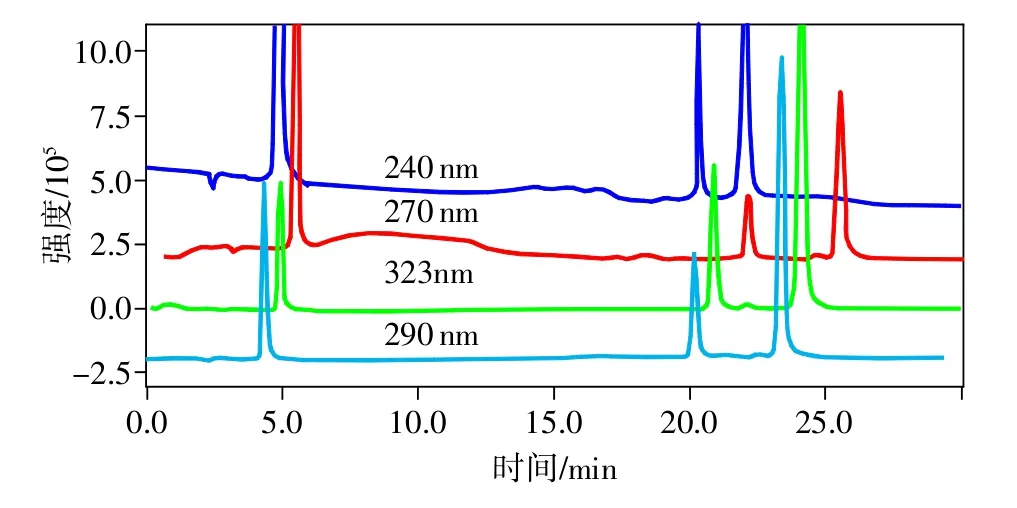
图3 不同波长的本品HPLC图
1.4 色谱条件
色谱柱:Sepax GP-C18(4.6mm×150mm×5μm);检测波长:290nm;流量:1mL/min;进样量:20μL;柱温:25℃;采用梯度洗脱法,流动相A:甲醇;流动相B:0.1%磷酸;梯度洗脱程序:A相0%,保持5min,15min升至30%,保持到30min;色谱图见图4。
1.5 方法学考查
1.5.1 线性、检出限和定量限
精密量取对照品储备液适量,分别置于10mL容量瓶中,加水稀释制成6个不同质量浓度的标准溶液,按1.4下色谱条件分别进样测定,记录色谱图。分别以各自的质量浓度与峰面积回归计算3个组份的标准曲线和相关系数,以信噪比>3为检测限,信噪比>10为定量限,结果见表2,VC、绿原酸和咖啡酸分别在43.5~636.0μg/mL,4.2~66.4μg/mL,4.3~68.8μg/mL范围内,线性关系良好。
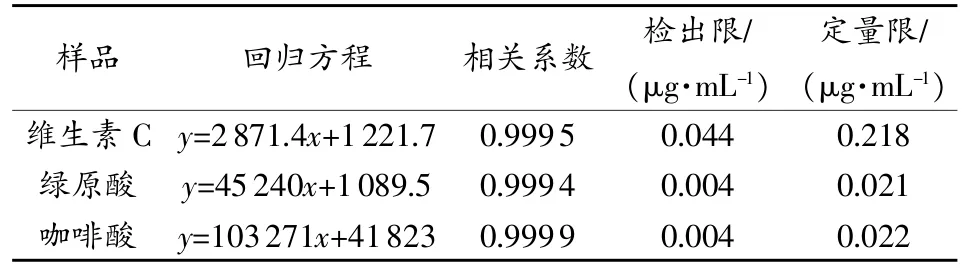
表2 维生素C、绿原酸、咖啡酸的回归方程、相关系数及线性范围
1.5.2 精密度
取对照品溶液,按1.4下条件,连续重复进样6次,测定峰面积,以维生素C、绿原酸、咖啡酸各自的峰面积计算进样精密度分别为1.05%、1.57%、0.64%。取同一批样品6份,按1.2.2制成供试品溶液,按外标法测定被测组分含量,以VC、绿原酸、咖啡酸的含量计算各自的重复性精密度分别为1.79%、1.80%、0.85%。分别于6d,按外标法每天测定同一批样品的含量,VC、绿原酸,咖啡酸各自的日间精密度分别为0.42%、0.75%、0.69%。
1.5.3 加样回收
精密量取已知量的供试品溶液适量,用水稀释10倍作为背景溶液,精密量取9份1mL背景溶液,分别加入适量对照品储备液,加水稀释制成高中低3个质量浓度各3份,精密量取各溶液10μL,注入液相色谱仪,记录色谱图,计算各自含量,经扣除背景后与加入的对照品量进行比较,计算出各自的回收率,结果见表3。
1.6 NF-01的稳定性考察
介于生物还原剂稳定性较差的特点,本文针对化妆品溶液进行了3周的稳定性考察,其中第1d分别每小时采样一次,检测了12h,然后在第1周的每天采样一次,检测了6 d,之后的第1个月的每周采样一次,检测了3周,对同一供试品进行含量测定,考查稳定性。结果表明:维C、绿原酸、咖啡酸12h内的最大变化率分别为:0.3%,0.4%,0.3%;6 d的最大变化率分别为3.7%,5.6%,3.3%;3周的最大变化率分别为15.4%,13.8%,5.3%。3组分在3周后都出现了较大的变化,变化率见图5。
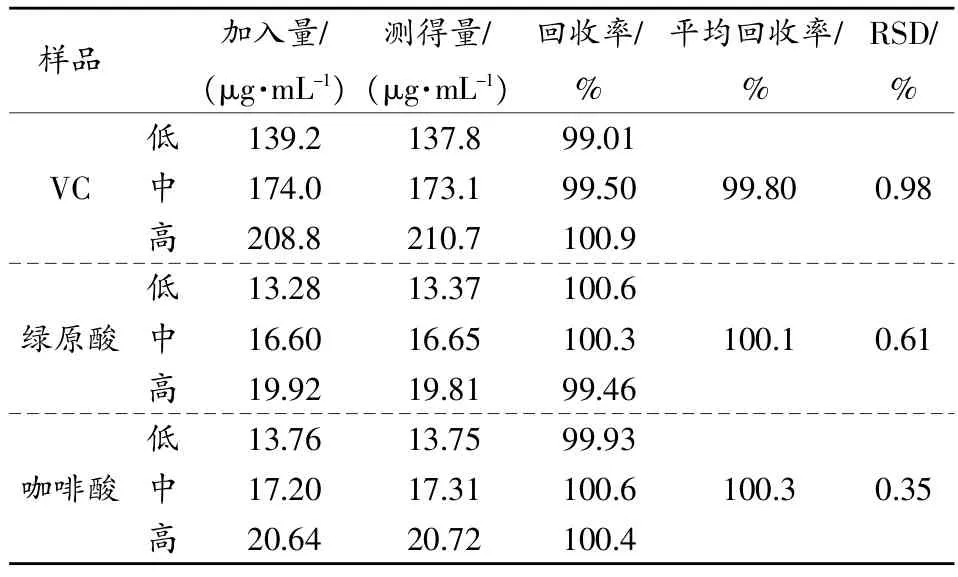
表3 加样回收试验结果(n=3)
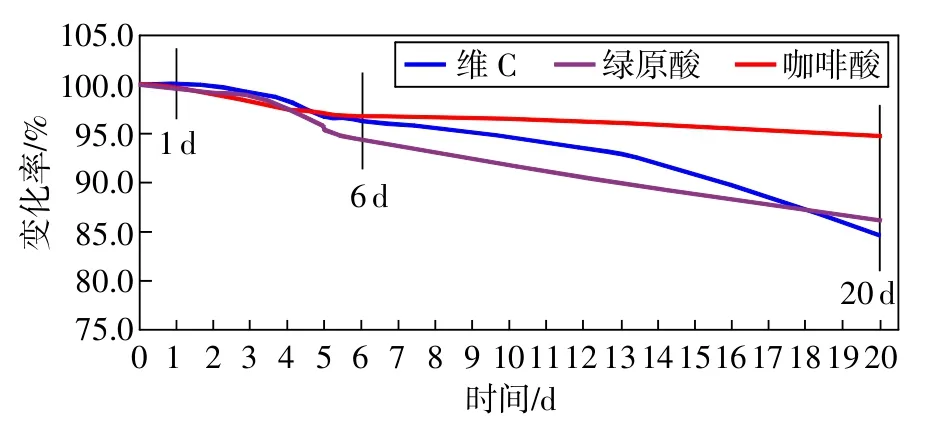
图5 20d内稳定性考察含量变化图
2 结果与讨论
2.1 实验结果
维C、绿原酸和咖啡酸在质量浓度范围分别为43.5~636.0μg/mL,4.2~66.4μg/mL,4.3~68.8μg/mL,线性关系良好;检出限分别为0.044,0.004,0.004μg/mL,定量限分别为0.218,0.021,0.022μg/mL。进样精密度分别为1.05%,1.57%,0.64%,重复性精密度分别为1.79%,1.80%,0.85%,日间精密度分别为0.42%,0.75%,0.69%,其精密度均小于2%,符合要求。加样回收试验中,3者的平均回收率分别为99.80%,100.1%,100.3%,均在要求的98.0%~102.0%范围内;其RSD分别为0.98%、0.61%和0.35%,3者均小于2.0%;该方法具良好的准确度。综上,该实验条件具有良好的方法学特性,可以用来测定护肤品中还原剂成分的含量。
对化妆品进行稳定性考察,维C、绿原酸、咖啡酸12 h内的最大变化率分别为:0.3%,0.4%,0.3%; 6 d的最大变化率分别为3.7%,5.6%,3.3%;3周的最大变化率分别为15.4%,13.8%,5.3%。结果表明3者的含量在3周后均出现了较大的变化,由图5可知3者中咖啡酸的变化最缓,而维C的变化最快,这与维C易氧化特性具一定的关系。后期可考虑成分中加入适宜的抗氧剂,使之更为稳定。
2.2 实验条件对分离的影响
2.2.1 梯度对分离的影响
由3种梯度程序所得的色谱图(见图1),可以得知,甲醇开始加入的时间越早,维C出峰的时间越早,而流动相中甲醇比例越大,绿原酸和咖啡酸出峰也就越早,为避免维C出峰过早,最终选择在5min时开始加入甲醇,而在此条件下,绿原酸和咖啡酸的分离效能也较高。
2.2.2 不同酸对分离的影响
由于测定的3种物质都是偏酸性的物质,所以认为在酸性条件下,3种物质能够更好地游离出来,所以考察了在流动相B分别为0.1%甲酸、0.1%磷酸、0.1%乙酸和水时,色谱峰的分离情况。由图2可知,在水和0.1%乙酸条件下绿原酸不出峰,且咖啡酸的柱效较低,而在酸性更大的0.1%甲酸和0.1%磷酸条件下,3种物质均出峰,且能良好分离,而0.1%磷酸具有更好的分离效能,且pH在2~8之间,所以最终选择了0.1%磷酸作为流动相B。
2.3 波长对检测的影响
维生素C、绿原酸、咖啡酸的最大吸收波长分别在245,324,323nm左右,分别在4个波长处对化妆品进行了测定。由图3可知,在240nm时维C的响应太高,而323 nm时维C的响应又太低,所以选择了两个中间波长进行考察,结果发现270nm时绿原酸和咖啡酸的响应太小而维C响应又过高,而323nm和290 nm时绿原酸和咖啡酸响应差异不大,而在290 nm时,维C能有更高的响应,所以最终选择290 nm为检测波长。
3 结束语
本文分别探索了不同波长、酸以及梯度程序对化妆品中3种生物还原剂测定的影响,从而建立了1种较优的HPLC梯度洗脱法使之能同时定量测定样品中极性差异较大的3种生物还原剂。连续3周溶液的稳定性考察,3个组份在1d内稳定,在6 d内基本稳定,在3周后出现较明显的变化,为后期的配方优化提供了有利条件。此方法简便灵敏,可用于化妆品中类似配方的质量控制,并为化妆品的现代化质量控制提供技术支持。
[1]谷雪贤.维生素C衍生物的制备及其在化妆品中的应用[J].化学试剂,2011,33(4):325-328.
[2]欧阳玉祝,吕程丽,易银辉,等.植物多酚复配物对水包油型膏霜化妆品抗氧化性能的影响[J].日用化学工业,2010,40(3):190-193.
[3]徐良,步平.美白祛斑化妆品及其未来发展[J].日用化学工业,2001(2):42-45.
[4]丁素君,张会芬.碘量法测定不同种类茶叶中的维生素C含量[J].中国当代医药,2014,21(5):156-157.
[5]李元玲,贺龙强.紫外分光光度法测定新鲜蔬菜中维生素C的含量[J].焦作大学学报,2011,25(3):93-94.
[6]华永有.HPLC法测定保健食品中维生素C含量[J].海峡药学,2014(10):19.
[7]黄京燕,刘占通,雷伟,等.反相高效液相色谱法测定双黄连注射液中咖啡酸的含量[J].中国当代医药,2011,18(1):41-42.
[8]朱旭松,包丽萍,郭炜毅.HPLC法测定银花感冒冲剂中绿原酸的含量[J].特别健康(下),2014(7):557-558.
[9]李德鑫,高源.HPLC法测定桂蒲肾清片中咖啡酸含量[J].药物与人,2014(8):95.
[10]张进,何鑫,姚思童,等.漫反射傅里叶变换红外光谱法测定维生素C制剂中抗坏血酸的含量[J].化学分析计量,2013(5):51-54.
[11]白雁,李珊,王星,等.近红外光谱法快速测定金银花中绿原酸的含量[J].中国实验方剂学杂志,2011,17(5):66-69.
[12]徐东升,高言明,杨春,等.高效毛细管电泳内标法测定山银花中绿原酸含量[J].江西中医药,2014(10):31.
Determ ination of bio-reductive agents in NF-01 by HPLC
FENG Ya’nan,WANG Mengli,XIE Hongying,NING Xin,CHEN Furong,ZHANG Yuxia,XU Xiaoping
(West China School of Pharmacy,Sichuan University,Chengdu 610041,China)
A HPLC measurement has been established to simultaneously determine the vitamin C,chlorogenic acid and caffeic acid in NF-01.The method comprises the following steps:conduct gradient elution on a ODS column(4.6mm×150mm×5μm),along with the mobile phase A-methanol and the mobile phase B-0.1%phosphate(phase A:0 min→5 min,0→0;5 min→15 min,0→30%;15min→30min,30%→30%);set the wavelength as 290nm and the flow rate as 1ml/min. The calibration curves of the vitamin C,the chlorogenic acid and the caffeic acid were linear in the ranges of 43.5-636.0μg/mL,4.2-66.4μg/mL and 4.3-68.8μg/mL respectively(y=2871.4x+1 221.7,r=0.999 5;y=45 240x+1 089.5,r=0.999 4;y=10 3271x+41 823,r=0.999 9).After three consecutive weeks’observation on the stability of the solution,the above three components remains stable within a day,basically stable within 6 days,and changed significantly after 3 weeks.The established HPLC method can simultaneously determinate three bio-reductive agents of large polarity difference in NF-01 and can also control the quality of similar cosmetic formulations.
vitamin C;chlorogenic acid;caffeic acid;HPLC
A文章编号:1674-5124(2015)06-0052-04
10.11857/j.issn.1674-5124.2015.06.012
0 引言
随着人们对皮肤的日益重视,美白嫩肤类化妆品倍受青睐,最为常见的有维生素类[1]和植物多酚类[2]。这些生物还原剂无论是天然的还是合成的对皮肤表面的色斑和损伤都表现出较好的祛斑和修复作用,成为化妆品中常用的添加剂[3]。维生素C、E,茶多酚、咖啡酸和绿原酸等,更是药物化妆品质量控制的指标之一。然而这些共存的生物还原剂由于结构和性质的差异较大,加之含量较低以及赋形剂的干扰,使得定量检测较为困难,特别是同时检测这些组分更加困难。有关这些组分的单一检测方法已有不少报道,如容量法[4]、紫外光谱法[5]、HPLC法[6-9]、红外光谱法[10-11]、电泳法[12]等。但是在化妆品中同时检测这3种不同性质的生物还原剂尚未见报道。本文建立了同时测定化妆品VC、绿原酸和咖啡酸的HPLC分析法,为护肤品多指标质量控制以及稳定性研究提供了较为可行的分析方法。
2015-01-29;
2015-03-18
冯亚男(1991-),女,四川成都市人,硕士研究生,专业方向为药物质量控制。
