近α型Ti600合金吸氢热力学的研究
2015-07-18
(西华大学材料科学与工程学院,四川 成都 610039)
·先进材料及能源·
近α型Ti600合金吸氢热力学的研究
王小丽, 廖慧敏
(西华大学材料科学与工程学院,四川 成都 610039)
根据钛合金吸氢的热力学性质,通过管式氢处理炉,在不同的温度条件下利用连续多步吸氢法进行Ti600合金的吸氢热力学试验,建立不同温度条件下的PCT热力学曲线。研究结果表明:Ti600合金吸氢的平衡氢压随氢含量和温度的增加而增加,在较低温度下,PCT曲线存在一个很短的平台;当吸入Ti600合金中的氢超过其溶解度时,生成氢化物相,氢在氢化物相中的溶解度与其平衡氢压满足Sieverts’定律;根据Van’t Hoff定律,近α型的Ti600合金中αH→氢化物相变的焓变和熵变分别为-55.99 kJ/mol和-131.585 J/(K·mol)。
近α型高温Ti600合金;热力学;溶解焓;氢化反应
Ti600合金为近α型高温钛合金[1-2],在使用温度高于600 ℃的条件下,具有优异的高温性能、抗蠕变性能和抗疲劳裂纹扩展性能等,满足航空、航天发动机对材料的要求;然而,高温Ti600合金与其他高温钛合金一样,由于高温变形抗力大,其热加工性能较差,限制其应用。近年来,研究者们发现热氢处理技术可改善Ti600合金的热加工性。
钛及钛合金与氢具有很高的亲和力,氢在钛合金中具有很高的迁移能力和扩散能力。近年来,利用氢在钛合金中的可逆性,研究者们把氢作为一种临时合金元素来改善钛合金的加工性能、高温性能、超塑性能等[3-11]。在一定的温度范围内,合金化氢可以增加α、α+β和金属间化合物合金的韧性,降低其流变应力,允许在较低的温度下进行大的变形。Li M.Q.等[12]和Niu Yong等[13-15]研究了氢的质量分数为0.16%~0.45%的Ti600合金在温度为800~1 000 ℃,应变速率为0.001~10.0 s-1下的等温压缩,研究发现,Ti600合金的应变硬化指数随着氢含量的增加而减小,在α+β相区内,氢的加入降低其应变激活能约30%。Zhang Xuemin等[16-17]研究了氢的质量分数为0.1%~0.5%的Ti600合金的超塑性,研究表明,氢可降低Ti600合金的变形温度约80℃,提高一个数量级的应变速率。Zong Yingying等[18]的研究表明,当Ti600合金中加入质量分数0.3%的氢,其流变应力和变形抗力都小于未加氢的Ti600合金,主要是因为氢的加入改变了Ti600合金高温变形时的相变温度、位错运动、动态回复与再结晶。这些研究结果表明氢的加入可改善高温Ti600合金的高温变形能力。
本文作者利用氢的吸附与扩散作用研究初始吸氢温度、初始放氢温度和吸氢与放氢过程中氢压的变化[19]。研究表明,Ti600合金的初始吸氢温度和初始放氢温度分别为573 ℃和578.5 ℃,吸氢过程中氢压先降低后升高,说明Ti600合金的吸氢过程是一个逆过程。根据Ti600合金的初始吸氢温度,本文利用PCT曲线研究了Ti600合金在吸氢过程中的热力学行为和热力学参数。
1 试验材料与试验方法
1.1试验材料
试验的材料为西北有色金属研究院提供近α型Ti600高温合金,合金材料名义成分为Ti-6Al-2.8Sn-4Zr-0.4Mo-0.4Si-0.1Y。试验材料按名义成分配料,经过两次真空自耗电弧炉熔炼成铸锭,开坯锻造成φ60 mm的圆棒,然后进行退火处理,退火处理工艺为850 ℃/1h+AC。
1.2试验方法
固态吸氢的理论基础是Sievert’s定律,在温度一定的条件下,试样中的氢含量与氢压的平方根成正比,并且钛合金吸氢是一个放热的反应,氢压一定的条件下,试样中的氢含量会随温度的升高而降低;因此,可以通过控制氢压和温度来控制试样中的氢含量。通过比较分析,利用等容差压原理设计制作L2210Ⅱ/ZM型管式氢处理炉,其结构如图1所示。
钛合金吸氢的热力学性质主要反应合金的吸氢量和热力学函数,P-C-T曲线是热力学研究的基础[20]。测试钛合金吸氢的热力学实验过程如图2所示。
通过管式氢处理炉,利用连续多步吸氢法在不同的温度条件下进行固态吸氢热力学试验,建立不同温度条件下的PCT热力学曲线。试验过程中氢压随时间的变化如图3所示,其中试验共分n步,第i步初始氢压为p1i,平衡氢压为p2i。试验过程中氢流量为5 L/min。
1 氢气入气口;2 氩气入气口;3 氢气阀;4 氮气阀;5 进气阀;6 放空阀;7 安全阀;8 直联泵;9 分子泵;10 高真空阀;11 隔离阀;12 电离规;13 电阻规;14 加热阀。
图1 L2210Ⅱ/ZM型管式氢处理炉结构简图
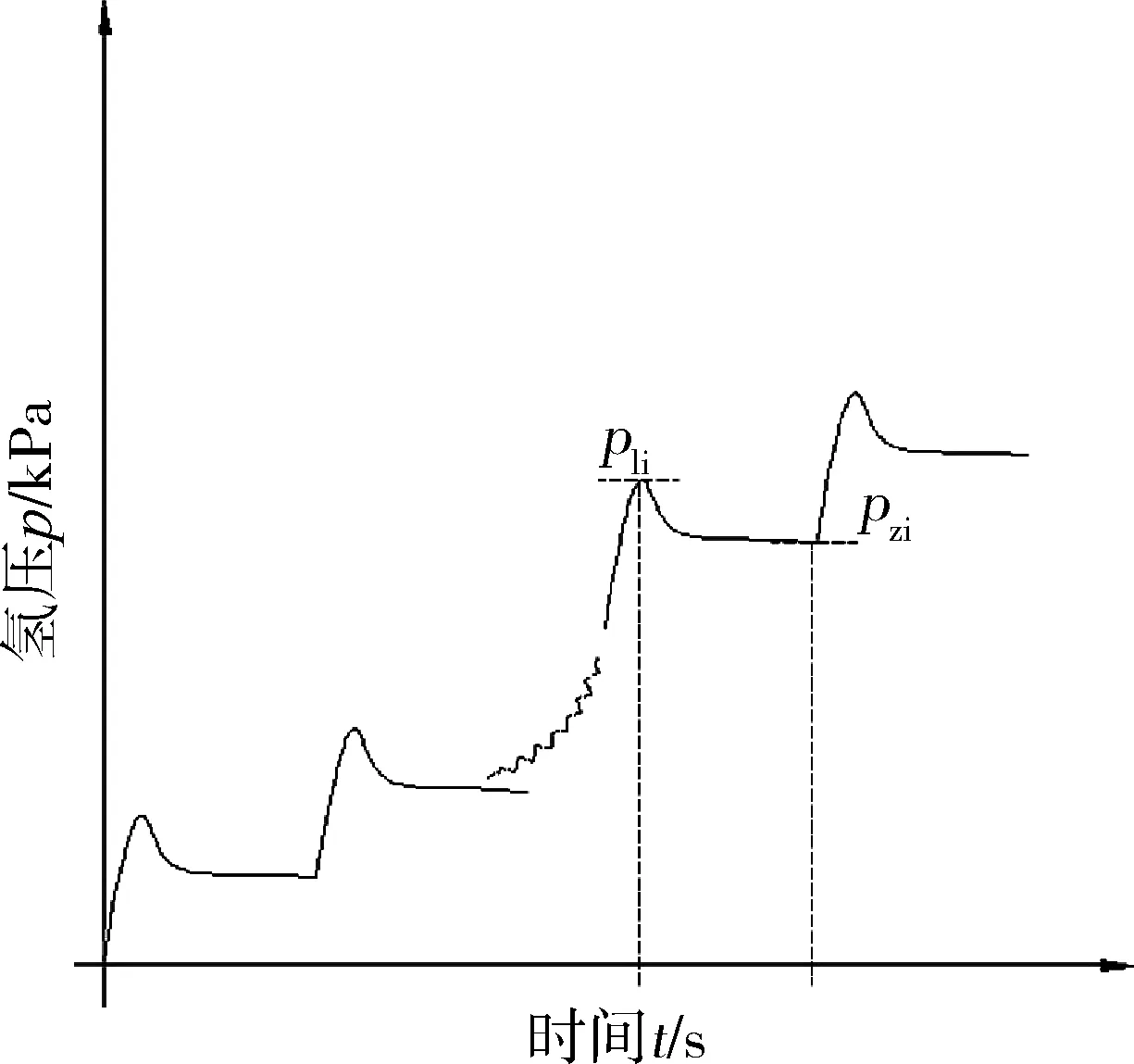
图3 连续多步吸氢过程中氢压随时间的变化
根据波马定律,第i步吸氢试验氢压变化Δpi与吸氢量Δni关系可以用式(1)表示:
ΔpiV=ΔniRT。
(1)
式中:Δpi为氢压变化,Δpi=p1i-p2i;V为管式氢处理炉体积,m3;Δni为试样吸氢摩尔量,mol;R为气体常数,8.31 J/(K·mol);T为吸氢温度,K。
因此第1~i步试样的总吸氢量可以表示为
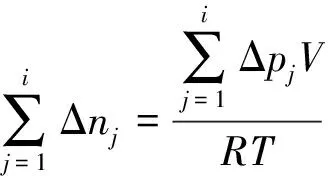
(2)
总吸氢量可以表示为
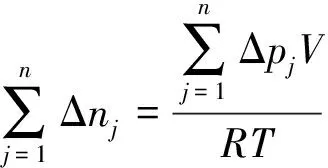
(3)
式(2)与式(3)相比可得
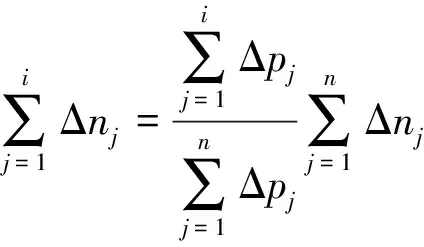
(4)
因此第i步试样氢含量Ci可以表示为
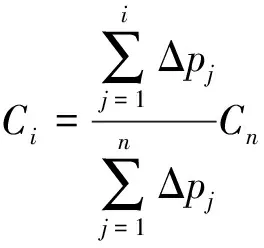
(5)
通过计算获得第(1)~(n-1)步氢含量(C1~Cn-1),建立P-C-T热力学曲线。
2 试验结果与讨论
2.1钛合金吸氢的P-C-T曲线
根据钛合金吸氢热力学试验得到的平衡氢压和公式(5),计算得到某一点的氢含量,与对应的平衡氢压作图,可得到一定温度下的P-C-T曲线图。
图4为Ti600合金在不同温度下吸氢的P-C-T曲线,其中横坐标H/M为氢原子/金属原子的原子比。可以看出:在吸氢过程中,Ti600合金的平衡氢压随氢含量的增加而增加,在675 ℃时只存在一个很短的平台,其平衡氢压约为0.06 atm;随着吸氢温度的升高,平台特征愈不明显,说明此时的吸氢温度高于P-C-T曲线的临界温度。根据Ti-H相图,氢在α-Ti中的溶解度很低,并随温度的升高而降低。氢在Ti600合金中的最大溶解度约为0.208% (约580 ℃)[14],吸附在合金表面的氢原子通过扩散迅速占据α相的间隙位置,发生αH→βH相变和δ氢化物相的析出,随后氢不断的固溶于βH和δ氢化物相中,氢压增大。
从图4可以看出,Ti600合金在吸氢过程中的P-C-T曲线出现1个平台区,这与黄刚等[21]和郭青苗等[22]在纯钛和TC4粉末研究中出现2个平台区存在差异。其中第1个平台区为αH和βH的共存区,第2个平台区为βH与氢化物的共存区。该差异主要是因为本文的试验材料钛合金块体材料吸氢过程中的阻碍较大,在相同氢压下吸氢的氢含量明显小于粉末材料。Ti600合金中只观察到较短的αH、βH和δ氢化物相共存的平台区。
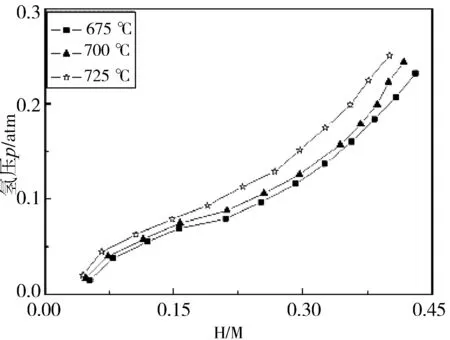
图4 Ti600合金吸氢的P-C-T曲线
2.2钛合金吸氢的热力学参数计算
2.2.1 氢固溶于氢化物中溶解焓的计算
若氢在合金中的溶解度达到极限溶解度时满足Sieverts’定律,则由平衡时1/2H2(g)=Hdiss可得到
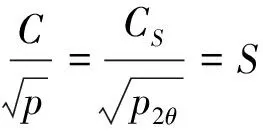
(6)
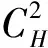
2.2.2 氢化反应平台区的热力学参数计算
在平台区,根据Van’t Hoff定律,lnpH2=ΔH/RT-ΔS/R,对平台区的平衡氢压和温度作图,可以计算平台区的熵变与焓变。 但由于试验过程中的平台区并非一条直线, 为了减小平台区平衡氢压的计算偏差,取其平均数。作lnPH2-1/T图(见图6),求其焓变和熵变,相关数据见表2。近α型Ti600合金中αH→氢化物相变的焓变和熵变分别为-55.99 kJ/mol和-131.585 J/(K·mol)。
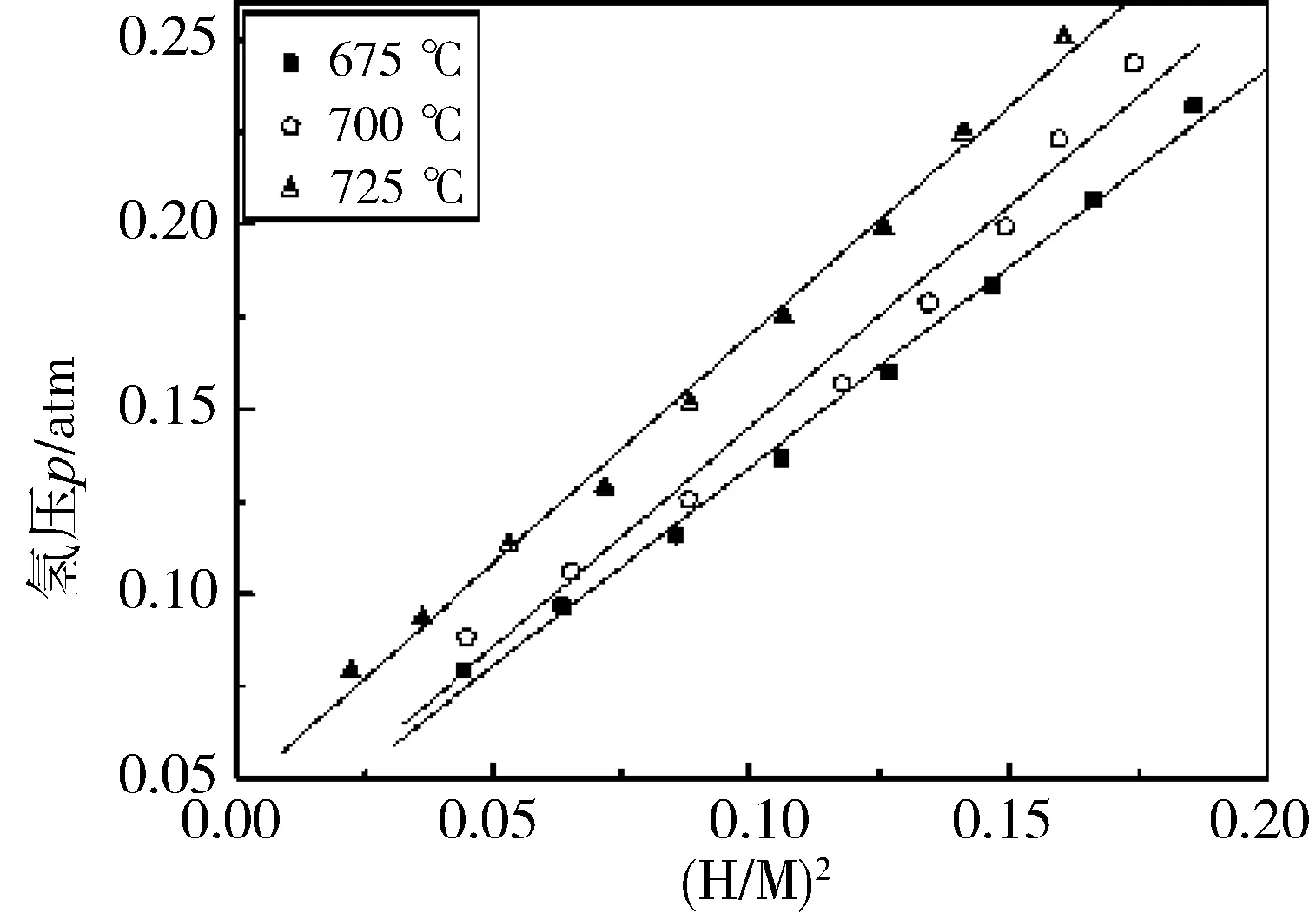
图5 氢固溶于氢化物中的氢含量与平衡氢压的关系
表1 氢在βH和氢化物相中溶解的Sieverts’常数
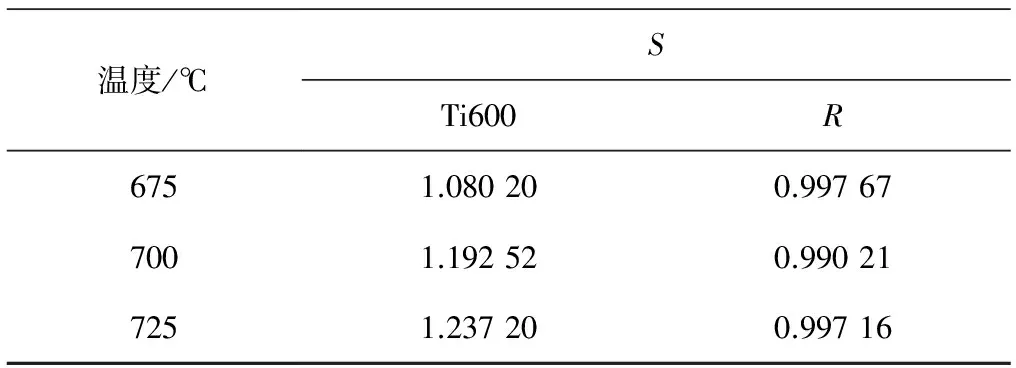
温度/℃STi600R6751.080200.997677001.192520.990217251.237200.99716
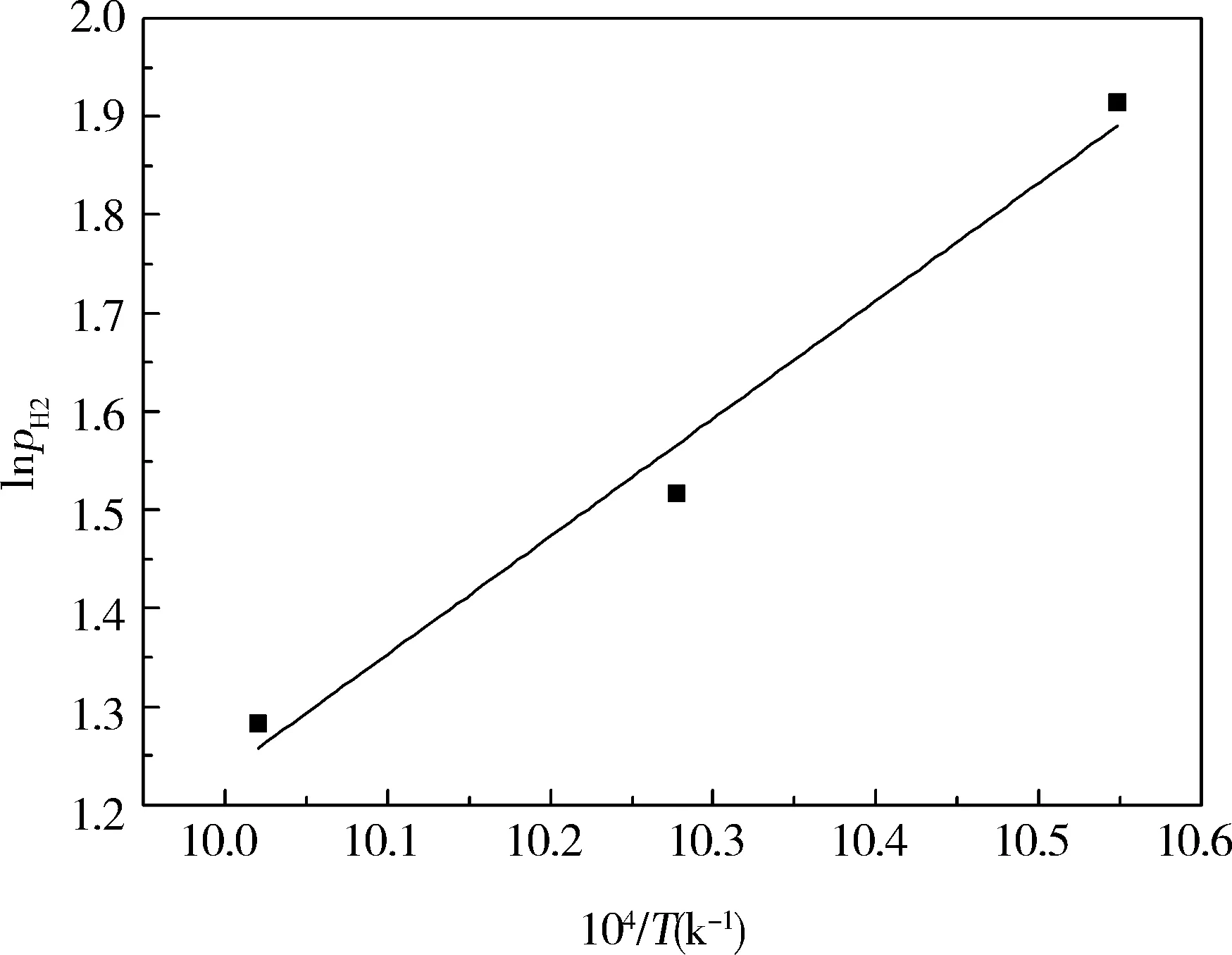
图6 lnpH2-1/T关系图
表2 钛合金吸氢平台热力学参数
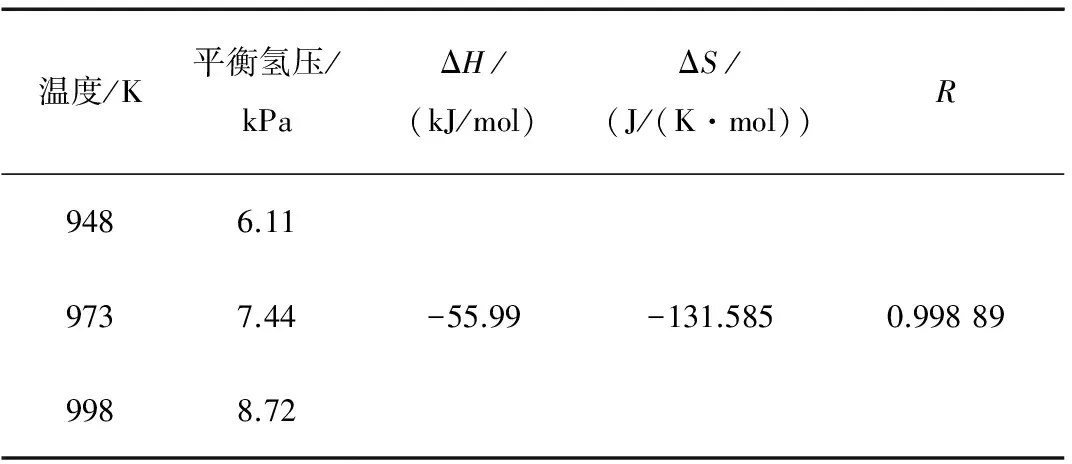
温度/K平衡氢压/kPaΔH/(kJ/mol)ΔS/(J/(K·mol))R9486.119737.449988.72-55.99-131.5850.99889
3 结论
1)近α型Ti600合金在一定温度下可以吸氢,其吸氢的平衡氢压随氢含量和温度的增加而增加;在较低温度下,P-C-T曲线存在一个很短的平台,随着吸氢温度的升高,平台特征愈不明显。
2)Ti600合金的显微组织为大量的α相和少量的β相,氢在α相中的溶解度很低,当吸入的氢超过其溶解度时,将析出氢化物相。氢固溶于氢化物相中,其溶解度与平衡氢压满足Sieverts’定律。在不同温度下,氢在氢化物中溶解的Sieverts’常数随温度的升高而升高。
3)在平台区,其吸氢规律满足Van’t Hoff定律。根据Van’t Hoff定律,计算出Ti600合金中αH→氢化物相变的焓变和熵变分别为-55.99 kJ/mol和-131.585 J/(K·mol)。
[1]Wang X L, Zhao Y Q, Wei X W, et al. Effect of Hydrogen on Phase and Microstructure of Ti600 Alloy [J]. Phase Transit, 2012, 85(9): 781-790.
[2]辛社伟, 洪权, 卢亚峰,等. Ti600 高温钛合金600 ℃下组织稳定性研究[J].稀有金属材料与工程, 2010, 39(11): 1918-1922.
[3]Froes F H , Senkov O N , Qazi J I. Hydrogen as a Temporary Alloying Element in Titanium Alloys: Thermohydrogen Processing[J]. Int Mater Rev , 2004, 49: 227.
[4]Wang Xiaoli , Zhao Yongqing , Hou Hongliang ,et al.Effect of Hydrogen Content on Superplastic Forming/Diffusion Bonding of TC21 Alloys [J]. J Alloys Compd, 2010, 503: 151-154.
[5]Zong Y Y, Shan D B , Lü Y, et al.Effect of 0.3 wt%H Addition on the High Temperature Deformation Behaviors of Ti-6Al-4V Alloy [J]. Int J Hydrogen Energy, 2007, 32: 3936-3940.
[6]Chen Yexin, Wan Xiaojing, Li Fang, et al. The Behavior of Hydrogen in High Temperature Titanium Alloy Ti-60 [J]. Mater Sci Eng A, 2007, 466: 156-159.
[7]He W J, Zhang S H, Song H W ,et al. Hydrogen-induced Hardening and Softening of a B-titanium Alloy [J]. Scripta Mater. 2009, 61: 6-19.
[11]Zong Yingying, Liang Yingchun, Yin Zhongwei, et al. Effects of Hydrogen Addition on the High Temperature Deformation Behavior of TC21 Titanium Alloy[J]. Int J Hydrogen Energy, 2012, 37: 13631-13637.
[12]Li M Q , Luo J , Niu Y. Effect of the Hydrogen Content on the Deformation Behavior in the Isothermal Compression of Ti600 Alloy [J]. Mater Sci Eng A, 2010, 527: 6626-6632.
[13]Niu Yong, Li Miaoquan. Effect of 0.16 wt% Hydrogen Addition on High Temperature Deformation Behavior of the Ti600 Titanium Alloy [J]. Mater Sci Eng A, 2009, 513-514: 228-232.
[14]Niu Yong , Hou Hongliang , Li Miaoquan, et al. High Temperature Deformation Behavior of a Near Alpha Ti600 Titanium Alloy [J]. Mater Sci Eng A, 2008, 492: 24-28.
[15]Niu Yong, Luo J, Li M Q. The Correlation Model between the Hydrogen Content and the Flow Stress in the Isothermal Compression of Ti600 Alloy [J]. Int J Hydrogen Energy, 2011, 36: 1006-1013.
[16]Zhang Xuemin, Zhao Yongqing, Zeng Weidong. Effect of Hydrogen on the Superplasticity of Ti600 Alloy [J]. Int J Hydrogen Energy, 2010, 35: 4354-4360.
[17]Zhang Xuemin, Cao Leilei, Zhao Yongqing ,et al. Superplastic Behavior and Deformation Mechanism of Ti600 Alloy [J].Mater Sci Eng A, 2013, 560: 700-704.
[18]Zong Yingying, Huang Shuhui, Feng Yingjuan,et al.Hydrogen Induced Softening Mechanism in Near Alpha Titanium Alloy [J]. J Alloys Compd , 2011, 528: 60-64.
[19]Wang Xiaoli, Zhao Yongqing, Zeng Weidong, et al. Behavior of Hydrogen Absorption/Desorption of Ti600, TC21 and Ti40 Alloys [J]. Rare Metal Materials and Engineering , 2010, 39(9): 1509-1512.
[20]Payá J, Linder M , Laurienb E, et al. Mathematical Models for the P-C-T Characterization of Hydrogen Absorbing Alloys [J].J Alloys Compd, 2009, 484(1/2): 190-195.
[21]黄刚, 曹小华, 龙兴贵.钛-氢体系的物理化学性质[J]. 材料导报, 2006, 20(10): 128-133.
[22]郭青苗, 刘彪, 侯红亮,等. 氢在TC4合金粉末压坯中的扩散行为及固结增效作用研究[D]. 北京:北京科技大学, 2009: 56-105.
(编校:夏书林)
ResearchonThermodynamicsofHydrogenObsorptioninNearαTi600Alloy
WANG Xaio-li,LIAO Hui-min
(SchoolofMaterialScienceandEngineering,XihuaUniversity,Chengdu610039China)
According to thermodynamics of hydrogen absorption in titanium alloys, thermodynamic experiments of hydrogen absorption in Ti600 alloy were carried out at different temperatures by continuous multistep hydrogen absorption through tube hydrogen treatment furnace. PCT curves were set up at different temperatures. The results show that equilibrium hydrogen pressure increases with the increase of hydrogen content and temperature. PCT curves exist a short plateau region at low temperature. As hydrogen contents in Ti600 alloy exceed solubility, hydride phases precipitate. The solubility of hydrogen in hydride phase and equilibrium hydrogen pressure adhere to Sieverts’ Law. According to Van’t Hoff Law, enthalpy and entropy of αH→hydrides phase transformation in near α Ti600 alloy are -55.99kJ/mol and -131.585 J/K·mol respectively.
near α high temperature Ti600 alloy; thermodynamics; solution enthalpy; hydrogenation
2014-11-23
四川省教育厅项目(12201453);西华大学校人才引进项目(Z1120117);四川省特种材料及制备技术重点实验室开放基金项目(S2jj2012-019)。
王小丽(1982-),女,讲师,博士,主要研究方向为金属结构材料的制备、组织及性能。
TG146.2+3
:A
:1673-159X(2015)04-0088-05
10.3969/j.issn.1673-159X.2015.04.018
