聚焦分散系五大考点
2015-07-13刘晓春
刘晓春

例2下列物质分类正确的是( )。
A.SO2、SiO2、CO均为酸性氧化物
B.稀豆浆、硅酸、氯化铁溶液均为胶体
C.烧碱、冰醋酸、四氯化碳均为电解质
D.福尔马林、水玻璃、氨水均为混合物
解析从常见物质的组成、结构、性质角度分析,利用题给的分类方法分析解决问题。A项中,SO2、SiO2是酸性氧化物,而CO为不成盐氧化物;B项中,稀豆浆属于胶体,氯化铁溶液不是胶体;C项中,烧碱和冰醋酸为电解质,四氯化碳是有机物,为非电解质;D项中,福尔马林是甲醛的水溶液,水玻璃是硅酸钠的水溶液,氨水为氨溶于水的溶液,均为混合物。则D项正确。答案:D。
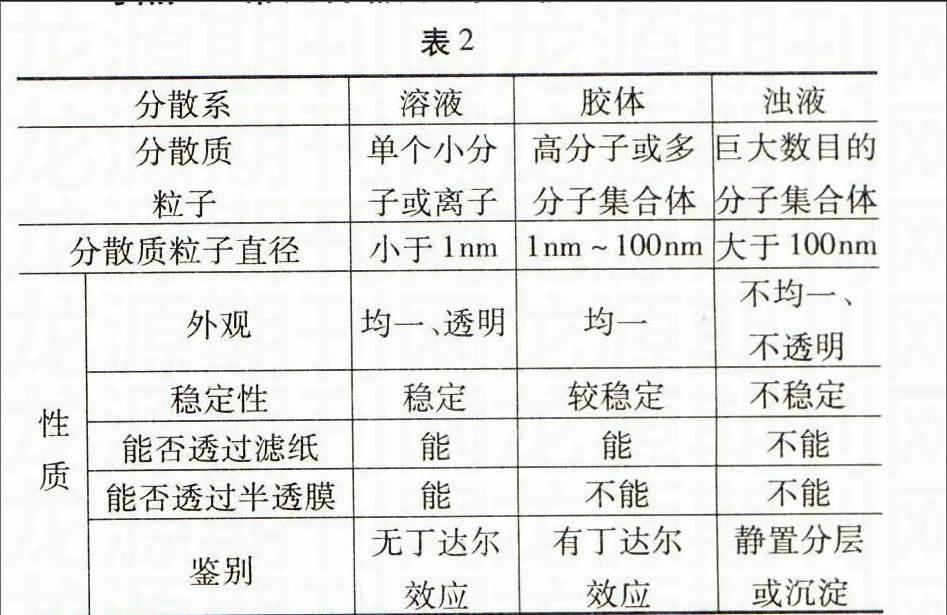
考点二:常见分散系的比较(见表2)
表2
分散系溶液胶体浊液
分散质粒子单个小分子或离子高分子或多分子集合体巨大数目的分子集合体
分散质粒子直径小于1nm1nm~100nm大于100nm
性质外观均一、透明均一不均一、不透明
稳定性稳定较稳定不稳定
能否透过滤纸能能不能
能否透过半透膜能不能不能
鉴别无丁达尔效应有丁达尔效应静置分层或沉淀
例3下列关于胶体和溶液的说法中,正确的是( )。
A.分散系的分类:
按照分散质微粒直径进行分类
B.溶液是电中性的,胶体是带电的
C.光线通过时,溶液产生丁达尔效应,胶体则无丁达尔效应
D.只有胶状物如胶水、果冻类的物质才能称为胶体
解析胶体是一种分散系,呈电中性,故B错误;光线通过时,溶液无丁达尔效应,胶体产生丁达尔效应,故C错误;胶体有像胶水、果冻类的液溶胶,也有像水晶、玛瑙类的固溶胶,还有像烟、雾类的气溶胶,故D错误。答案:A。
例4有关溶液和胶体的叙述正确的是()。
A.Fe(OH)3胶体和FeCl3溶液的本质区别为是否具有丁达尔效应
B.FeCl3溶液呈电中性,Fe(OH)3胶体带有电荷
C.纳米材料的粒子直径一般从几纳米到几十纳米,因此纳米材料是胶体
D.FeCl3溶液能使血液凝聚沉降
解析A项,胶体与溶液的本质区别是分散质粒子本身的大小,A错误;B项,胶粒可能带电,但胶体都呈电中性,B错误;C项,纳米材料只代表分散系中的粒子,缺少分散剂,从而无法形成胶体;D项,血液属于胶体,它与电解质溶液作用发生凝聚沉降,D正确。答案:D。
考点三:胶体的制备
Fe(OH)3胶体的制备:向沸水中逐滴加入饱和FeCl3溶液,继续煮沸至溶液呈红褐色,停止加热,即制得Fe(OH)3胶体,化学方程式为:
FeCl3+3H2O△Fe(OH)3(胶体)+3HCl
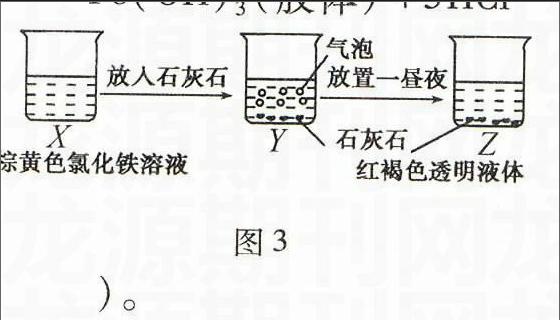
图3
例5某同学在实验室进行了如图3所示的实验,下列说法中错误的是( )。
A.利用过滤的方法,可将Z中固体与液体分离
B.X、Z烧杯中分散质相同
C.Y中反应的离子方程式为:
3CaCO3+2Fe3++3H2O2Fe(OH)3+3CO2↑+3Ca2+
D.Z中分散系能产生丁达尔效应
解析由于Fe3+水解,所以FeCl3溶液显酸性,加入石灰石后,与水解生成的H+反应,促进了Fe3+的进一步水解,最后得到Fe(OH)3胶体,反应的离子方程式为:
3CaCO3+2Fe3++3H2O2Fe(OH)3+3CO2↑+3Ca2+
X烧杯中分散质为FeCl3,Z烧杯中分散质为
Fe(OH)3胶粒和CaCl2,能产生丁达尔效应。答案:B。
考点四:胶体的性质
1.丁达尔效应:当可见光束通过胶体时,由于胶体粒子对光的散射作用,在胶体中出现一条光亮的“通路”的现象。
2.布朗运动:胶体中胶粒不停地做无规则运动。这种现象并非胶体独有的现象。
3.电泳现象:胶粒在外加电场作用下,能在分散剂里向阳极或阴极做定向移动,这种现象叫电泳。胶粒带电荷,但整个胶体仍是显电中性的。
例6下列现象不能用胶体知识解释的是()。
A.牛油与NaOH溶液共煮,向反应后所得溶液中加入食盐,会有固体析出
B.一支钢笔使用两种不同牌号的蓝黑墨水,易出现堵塞
C.向FeCl3溶液中加入Na2CO3溶液,会出现红褐色沉淀
D.在河水与海水的交界处,有三角洲形成
解析牛油是油脂,与NaOH溶液共煮后得到胶体,加入电解质发生聚沉,析出固体,A可以;墨水是胶体,不同品牌的墨水混合发生聚沉,B可以;Na2CO3溶液与FeCl3溶液发生水解相互促进反应生成Fe(OH)3沉淀,与胶体性质无关;D是胶体的聚沉。答案:C。
考点五:胶体的应用
如:皂化反应,制取肥皂过程涉及胶体的性质,皂化反应所得的混合体系属于胶体,加入NaCl析出固体称作盐析,盐析是可逆过程。
例7下列“化学与生活”的说法不正确的是()。
A.硫酸钡可用于钡餐透视
B.盐卤可用于制豆腐
C.明矾可用于水的消毒、杀菌
D.醋可用于除去暖水瓶中的水垢
解析硫酸钡难溶于水,不溶于酸,医疗上常用于钡餐透视,A正确;盐卤中的电解质可以使豆浆(胶体)聚沉,B正确;明矾可用于净水,但不能用于水的消毒、杀菌,C错误;水垢的主要成分是碳酸钙和氢氧化镁,故用醋可以除去暖水瓶中的水垢,D正确。答案:C。
跟踪训练:
1.下列说法中正确的是( )。
A.干冰、液态氯化氢都是电解质
B.Na2O2晶体中既含有离子键又含有共价键
C.Na2O、Fe2O3、Al2O3既属于碱性氧化物,又属于离子化合物
D.根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体
2.下列现象或变化过程与胶体的性质无关的是( )。
A.清晨森林中的道道光柱
B.夕阳下的晚霞
C.海水的淡化
D.明矾净水
3、生产生活中的许多现象或应用都与化学知识有关,下列现象或应用与胶体性质无关的是( )
A.将盐卤或石膏加入豆浆中,制成豆腐
B.一支钢笔使用两种不同型号的蓝黑墨水,易出现堵塞
C.泡沫灭火器中将Al2(SO4)3与NaHCO3两溶液混合后,喷出大量泡沫,起到灭火作用
D.清晨,人们经常能看到阳光穿过茂密的树木枝叶所产生的美丽景象
4、下列说法不正确的是( )
A.化学变化不产生新元素,产生新元素的变化不是化学变化
B.根据分散质粒子直径大小可以将分散系分为溶液、浊液和胶体
C.向25 mL沸水中逐滴加入2 mL FeCl3饱和溶液,继续煮沸至溶液呈红褐色,停止加热,可以制得Fe(OH)3胶体
D.某粒子的电子数等于质子数,则该粒子可能是一种分子或一种离子
5、2011年冬天,全国多个地区发生持续大雾天气,“PM2.5”数据监测纳入公众视野。“PM2.5”是指大气中直径小于或等于2.5微米的细小颗粒物,也称为可入肺颗粒物。下列有关说法中错误的是( )
A.雾属于胶体,能产生丁达尔现象 B.持续大雾天气给农业生产、交通运输等带来很大的影响
C.大雾的形成与汽车的尾气排放没有关系 D.空气中悬浮的细小颗粒物严重危害人体健康
跟踪训练参考答案:
1 B 解析:A选项干冰为非电解质,错误。B选项Na2O2的电子式为 ,正确。C选项Al2O3为两性氧化物,错误。D选项根据分散质直径大小分为溶液、浊液和胶体,错误。
2 C 解析:胶体的性质有:丁达尔效应、布朗运动、电泳现象、胶体的聚沉。清晨在森林中,空气和水蒸气等杂质构成的分散系中分散质的粒子直径在1~100 nm之间,构成了胶体,在阳光照射下会产生丁达尔效应,A正确;夕阳下的晚霞也是产生丁达尔效应现象,云属于胶体,B正确;明矾净水是铝离子水解生成了氢氧化铝胶体,胶体颗粒表面积比较大,具有比较强的吸附能力,D正确。
3 C 解析:C项泡沫灭火器中将Al2(SO4)3与NaHCO3两溶液混合后,发生了水解相互促进的反应,跟胶体的性质无关;A项将盐卤或石膏加入豆浆中,制成豆腐,因为豆浆是胶体,加入电解质会使胶体聚沉,制成豆腐;B项墨水是胶体,不同型号的蓝黑墨水,胶体粒子带的电荷相反,相互中和,使胶体聚沉;D项是胶体的丁达尔效应。
4 D 解析:分散质粒子直径的大小是区分溶液、浊液、胶体最本质的属性,B项说法正确;当粒子的电子数等于质子数时,粒子应为中性粒子,不可能为离子,D项说法不正确。
5 C 解析:空气中的水蒸气很容易在空气中的小颗粒(凝结核)上液化为小水滴,进而形成雾。城市大气中的可入肺颗粒物的主要来源是汽车尾气,尤其是柴油汽车尾气,它们可为雾的形成提供凝结核,故大雾的形成与汽车的尾气排放有关,C错。
(收稿日期:2015-01-10)
