浅谈高考中实验基础知识的考查
2015-07-13宋伟
宋伟


实验是化学的灵魂。化学实验是高考中考查的重头戏,无论是单科卷还是理科综合卷中化学实验知识的考查都会占很大的比重。高考中的实验考查主要分为三个部分:一是关于实验基础知识的考查,如中学常用的化学实验仪器的使用方法的考查;二是基本实验操作的考查,如中学化学中常见的物质分离和提纯方法的考查、中学化学中物质检验方法的考查以及中学化学中常见物质的实验室制备方法的考查;三是化学实验知识的应用考查,如在一些化学工业生产流程中对各个环节中的实验操作或实验方法的考查等。无论高考中的化学实验题从哪个角度或是用什么样的方法考查,都离不开化学实验中的基础知识,所以从高考考查的试题或是考查形式对我们进行高考的复习都会起到很重要的指导作用。本文拟就高考中化学实验基础知识的考查
进行总结。
一、中学化学常用仪器使用方法的考查
中学化学中除了试管、烧杯、锥形瓶、铁架台等是常见常用仪器,大部分学生都已熟悉其用法。但还有很多的常用仪器也是高考中考查的对象,是我们在高考复习中不可忽视的化学实验基础知识。
1.分离操作的仪器
分液漏斗用于分离两种互不相溶的液体的仪器,在使用时除了洗涤检漏外,还要注意在分液时要打开漏斗塞以达到平衡漏斗内外气体压强相等,从而使液体能顺利流出。蒸馏烧瓶和冷凝管是用于分离存在较大沸点差的互溶液体的仪器,其中蒸馏烧瓶在使用中要注意它是一种不能直接加热的仪器,在加热时需垫石棉网,在加热液体时要在蒸馏烧瓶中加入防止暴沸(或描述为液体沸腾时发生剧烈跳动)的碎瓷片;冷凝管在使用时要注意到冷却水的连接方法,即其导入冷水的方向是下口进水,而上口出水,这并不是对冷凝管本身的上下描述,而是从连接的装置中处于物理位置的上下的一种描述。
2.定量实验中的仪器
中学化学实验中的定量实验主要有两类:一是配制一定体积一定物质的量浓度的溶液中的容量瓶的使用,它只能用于配制溶液,在容量瓶的瓶壁上有三个量,包括规格、刻度线及使用温度,它不能加热包括不能用于溶解和稀释操作,也不能用于作反应容器等,并且在容量瓶上没有刻度而只有一条刻度线,所以在配制时只要发生了错误操作,一般来说也只能是倒掉重配;二是溶液浓度的测定实验——滴定实验,在实验中的主要仪器是酸式或碱式滴定管,它们在使用中除了要检漏洗涤外,还要注意到它们在装液前还需要进行润洗,也就是用待盛放的液体进行洗涤,这主要是防止洗涤完的滴定管壁上必然附着有水,如果直接装液则会使所装溶液的浓度变小而影响实验的结果,另外还要注意酸碱滴定管的构造的不同,其目的是让它们适用于盛放不同的液体,酸式滴定管用于盛放酸性及强氧化性的液体,而碱式滴定管一般只用于盛放碱性试剂。
例1下列有关仪器使用方法或实验操作正确的是( )。
A.洗净的锥形瓶和容量瓶可以放进烘箱中烘干
B.酸式滴定管装标准溶液前,必须先用该溶液润洗
C.酸碱滴定实验中,用待滴定溶液润洗锥形瓶以减小实验误差
D.用容量瓶配溶液时,若加水超过刻度线,立即用滴管吸出多余液体
解析A选项中的容量瓶是一种不能加热的仪器,只能在常温下使用,A不正确;C选项中的酸碱滴定实验中需要进行润洗的仪器是酸式滴定管和碱式滴定管,而锥形瓶是取一定量溶液进行反应的容器,如果润洗就会导致所取溶液的增多而带来实验的误差,C不正确;D选项中配制溶液时,如果加入的水超过了容量瓶的刻度线,加入的虽然是水,但一旦加入由于溶质的扩散,吸出的就不是水而是溶液,所以吸出会使部分溶质损失从而使所配的溶液浓度偏小,D不正确。
答案 B
二、中学化学实验基本操作的考查
中学化学实验的基本操作主要是物质分离提纯实验、物质的检验、溶液的配制、溶液浓度的滴定以及物质的制备和性质等实验中的一些基本操作。
1.物质分离提纯中的基本操作
物质分离提纯的方法主要有过滤、蒸馏、结晶、萃取分液等。在过滤实验中一定要注意的是“二低和三靠”;蒸馏操作中要注意蒸馏烧瓶和冷凝管的操作,注意温度计的位置应是在蒸馏烧瓶的支管口处,因为其控制的是进入冷凝管的蒸气的温度;在结晶时要注意有两种实验方法,一是用蒸发结晶,主要用于从溶液中析出溶解度较小的溶质,二是用冷却结晶,主要用于从溶液中析出溶解度随温度变化较大的溶质,它的前提是得到温度较高的浓溶液;再如萃取分液时的操作中萃取溶剂的选择条件(萃取溶剂不能与原溶剂互溶、溶质在萃取溶剂中的溶解度远大于在原溶剂中的溶解度)、分液时的操作中要注意下层液体从下口放出,而上层液体应从分液漏斗的上口倒出,等等。
2.物质性质、制备实验中的基本操作
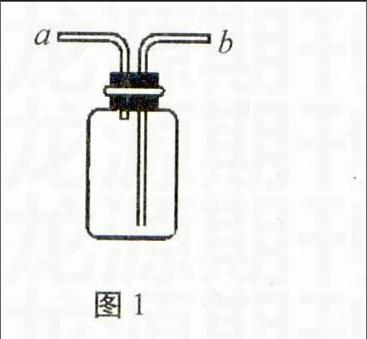
图1
物质的性质和制备实验中会涉及到许多的实验基本操作方法,比如在物质的加热实验中,如果用大试管加热固体时管口应向下略微倾斜,加热液体时试管口应向上略微倾斜,并且它们都要注意是夹在试管离口的1/3处等。再如实验中的洗气(除杂质、干燥、排液体收集气体以及排液体量气等)、收集气体等都可用同一个装置,如图1所示。如果是用于排空气法收集气体,收集密度比空气大的气体应是从b进气而从a排出空气,收集比空气密度小的气体应是从a进气而从b排出空气;如果是用于排液体收集气体,则应从a进气而从b排出液体来进行收集;如果是用于洗气而除杂及干燥等时应从b进气从a出气,等等。
例2下列图示实验正确的是( )。
解析A选项中过滤操作中应注意三靠,如玻璃棒应紧靠三层滤纸的一侧,A不正确;B选项中是通过加热碳酸氢钠固体来检验碳酸氢钠的稳定性实验,在加热固体时应使试管口略向下倾斜,B不正确;C选项中是用洗气的方法除去CO中的CO2,则在通入液体中时要注意是长管进气而短管出气,C不正确。
答案 D
三、物质检验中试剂选择的考查
物质的检验主要是针对溶液或是固体中存在的成分的确定。它所依据的标准是实验操作简便,现象很明显,得到的结论可靠的原则。所以在检验中试剂的选择及其加入的顺序都很重要。中学常见的几种离子的检验方法:氯离子用硝酸银和稀硝酸,看到的现象是生成了白色不溶液于稀硝酸的沉淀;硫酸根离子的检验不仅要选择正确的试剂,同时还要注意试剂加入的顺序,一般来说是先向溶液中加入稀盐酸,然后再向溶液中加入氯化钡,如果在加入氯化钡时产生了白色沉淀,则说明溶液中一定存在硫酸根离子;铵离子的检验是向溶液中加入强碱并微热,如果能产生一种能使湿的红色石蕊试纸变蓝的气体,则原溶液中一定含有大量的铵离子。
例3下列叙述Ⅰ和Ⅱ均正确并有因果关系的是( )。
解析A选项中是由于硝酸钾的溶解度随温度变化大,所以可用冷却结晶的方法除去硝酸钾中的氯化钠,A不正确;C选项中检验硫酸根离子应先加入盐酸再加入氯化钡,产生白色沉淀说明原溶液中存在硫酸根离子,硫酸钡不溶于水不溶于酸,B正确;C选项中氨气能进行喷泉实验是因为其极易溶于水,C不正确;D中的氢氧化钙是微溶物,能形成澄清石灰水,其浓度很小,不能形成较高浓度的氢氧化钙溶液。
答案 B
总之,在实验学习和复习中,我们要着力于实验基本知识,高考的考查中,总是高起点低落点,虽然题干是一个很新颖的工业流程,但在我们要完成的点却是一些中学化学实验中的主干的基本知识。“万仗高楼平地起”,只有有了扎实的基本功才能解决复习的问题。
(收稿日期:2014-09-10)
