离子液体制备碳氮硫共掺杂TiO2及其光催化性能的研究
2015-06-27陈久福钟俊波李建章程朝柱窦琳
陈久福,钟俊波,李建章,程朝柱,窦琳
(1.绿色催化四川省高校重点实验室,四川自贡643000;2.四川理工学院化学与制药工程学院,四川自贡643000)
离子液体制备碳氮硫共掺杂TiO2及其光催化性能的研究
陈久福1,2,钟俊波1,2,李建章1,2,程朝柱1,2,窦琳1,2
(1.绿色催化四川省高校重点实验室,四川自贡643000;2.四川理工学院化学与制药工程学院,四川自贡643000)
以1-乙基-3-甲基咪唑硫酸氢盐([EMIm]HSO4)离子液体为掺杂剂,采用溶胶-凝胶法制备碳、氮、硫共掺杂TiO2(CNS-TiO2)。用比表面孔隙仪、X射线衍射仪、扫描电镜、紫外-可见漫反射、X射线光电子能谱和表面光电压仪对制备的光催化剂进行了表征,以甲基橙为模拟污染物,在模拟太阳光照射下考察了光催化性能。结果表明:所制备的CNS-TiO2拥有更高的比表面和电荷分离速率,并对可见光有响应;CNS-TiO2的光催化活性是纯TiO2的3倍。
TiO2;离子液体;掺杂;光催化性能
引言
在光催化剂研究中,TiO2因具有无毒、化学稳定性强、价格便宜和催化活性强等特点而备受关注[1-2]。然而锐钛型TiO2较宽的禁带宽度(约3.2 eV)限制了它的实际应用。因为锐钛型TiO2只对紫外光有响应,而紫外光只占太阳光光谱的3%~5%[3],所以TiO2对太阳光的利用率很低。因此通过改性来提高TiO2的太阳光催化活性具有十分重要的理论和实际意义。
目前,研究改性TiO2的手段主要包括染料光敏化、离子掺杂、贵金属沉积和半导体复合,其中拓展TiO2对可见光有响应最有效的手段是离子掺杂,制备的光催化剂具有优异的光催化活性。自从Asahi R等[4]发现氮元素掺杂的TiO2薄膜对可见光有响应后,用非金属改性TiO2的研究得到迅速发展。目前研究者已经制备出多种非金属共同掺杂TiO2,包括N-S[5],C-N-S[6]和N-BF[7]等共同掺杂TiO2,研究结果都表明在可见光区非金属掺杂的TiO2有催化活性,且明显比纯TiO2的催化活性高。
离子液体由阴阳离子组成,能完全融入水溶液,因此它十分适合于溶胶-凝胶法[8],另外离子液体可以抑制TiO2微粒的快速生长,便于得到较小晶粒的催化剂,从而促进光催化作用[7]。本文以[EMIm]HSO4离子液体为掺杂剂,采用溶胶-凝胶法制备碳、氮、硫共掺杂TiO2,并用甲基橙为模拟污染物考察了改性后TiO2的光催化活性。
1 实验部分
1.1 仪器及主要试剂
SSA-4200比表面孔隙分析仪(北京彼奥德电子有限公司),TU-1901双光束紫外可见分光光度计(北京谱析通用仪器有限责任公司),DX-2600型X射线衍射仪(丹东方圆仪器有限公司),JSM-7500F扫描电子显微镜(日本电子株式会社),XSAM 800型X射线光电子能谱仪(英国Kratos公司),PhchemⅢ型光化学反应仪(北京纽比特科技有限公司)。实验用水均为二次去离子水,钛酸四丁酯、无水乙醇、冰乙酸和甲基橙(均为分析纯,成都科龙化工试剂厂),[EMIm]HSO4(纯度>99%,购买于中国科学院兰州化学物理研究所)。
1.2 催化剂的制备
称取21.6 g的钛酸四丁酯溶于50 mL无水乙醇中,在不断搅拌下形成溶液A;再称取占钛酸四丁酯2%质量的[EMIm]HSO4溶于40 mL去离子水中,在不断搅拌下加入15 mL冰乙酸形成溶液B;然后将A和B两种溶液混合并搅拌120 min,溶液形成凝胶后,置于100℃烘箱中干燥24 h得到前驱体,把研磨后的前躯体放入马弗炉中于550℃焙烧1 h得到CNS-TiO2粉体。纯TiO2的制备过程与上述相同,只是不加入[EMIm]HSO4离子液体。
1.3 光催化剂的活性测定
以甲基橙为模拟污染物,所有样品的活性都在PhchemⅢ型光化学反应仪测定。先在石英管中加入50 mg光催化剂和50 mL浓度为10 mg/L的甲基橙溶液,再用高氯酸或NaOH调节反应液,使其pH为7.0;然后在500 W氙灯下进行光照,间隔取样,经离心分离后取上清液在λ=460 nm测定甲基橙溶液的吸光度,甲基橙溶液浓度与吸光度的关系符合朗伯-比尔定律。所有数据测试3次取平均值。
1.4 样品的表征
采用SSA-4200比表面孔隙分析仪测定样品的比表面积和孔容大小,用X射线衍射仪测定样品的晶相结构,辐射源为Cu Kα,λ=1.5406 nm,电流25 mA,管压为40 kV,扫描速度3°/min,扫描范围20°-80°。采用JSM-7500F型扫描电子显微镜观察纳米粉体颗粒形貌。用TU-1901双光束紫外可见分光光度计测定样品的紫外-可见漫反射谱图,并以硫酸钡为参考。样品的X射线光电子能谱分析采用XSAM 800型光电子能谱仪,激发源为Mg KαX射线,电压12 kV,电流12 mA,电子结合能用C 1s峰(284.8 eV)校正。采用表面光电压仪测定催化剂的表面光电压。
2 结果与讨论
2.1 催化剂的表征
催化剂的XRD图谱如图1所示,与JCPDS卡片(No.89-4921)相比较,CNS-TiO2和TiO2都是锐钛相。另外CNS-TiO2的XRD图谱没有出现C-O、N-O和S-O的衍射峰,说明了C、N和S的含量很低,且高度分散[9]。与纯TiO2相比较,CNS-TiO2(101)晶面衍射峰宽化,这可能是阴离子掺入TiO2晶格导致。由Scherrer公式可计算出催化剂的平均晶粒尺寸:其中,D是催化剂的平均晶粒尺寸;λ是衍射角辐射的波长,并取λ=1.5406 nm;谢乐常数K=0.89;β为衍射峰半高宽,θ为该峰对应的衍射角。通过计算得出了CNSTiO2和TiO2的平均晶粒大小分别为13.4 nm和14.5 nm,这表明了在一定程度上非金属离子掺杂减小了TiO2的晶粒尺寸,有利于增加比表面,该结果可以从比表面参数结果得到印证。
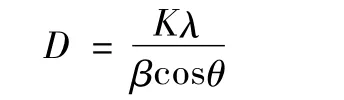
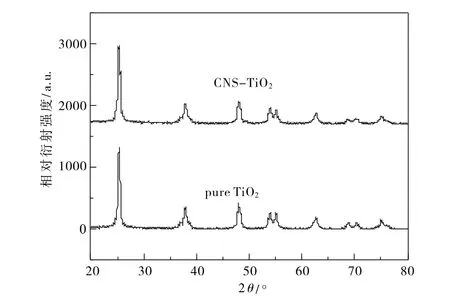
图1样品XRD图谱
所制备催化剂的比表面参数见表1,从表1可知,碳、氮、硫掺杂TiO2的比表面积和孔容增加,孔半径减小。这可能是原因离子液体抑制了TiO2的微粒快速生长,形成更小的晶粒和更多无规则的微粒,从而得到更高的比表面积和更大的孔容。众所周知,比表面积高的催化剂可以吸附更多的有机物参加反应,从而有助于提高其光催化活性。
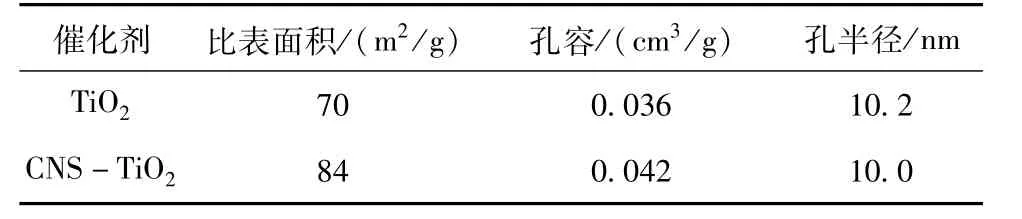
表1催化剂的比表面参数
图2是样品的SEM图,从图2可以看出,催化剂的形貌均是多孔无规则块状,但采用离子液体辅助制备的样品和纯TiO2形貌没有明显差异,结合光催化剂结果可知形貌不是影响光催化活性差异的主要因素。
催化剂在250-800 nm区间的紫外-可见漫反射图谱如图3所示。从图3可以看出样品在紫外光区域的吸收都很强,CNS-TiO2在400~500 nm可见区的吸收有所增强,对可见光产生响应,该结果也与SPS结果一致。
图4是CNS-TiO2样品C 1s的XPS图谱。从图4可知,C 1s在284.6 eV、286.0 eV和288.8 eV处存在3个峰,位于284.6 eV的峰是仪器表面的碳,而在286.0 eV和288.8 eV处的两个峰归属于C-O、C=O和C-N键[10],另外在288.8 eV处的峰归属于Ti-O-C结构[6]。在282 eV处没有观察到峰,这说明没有发生C取代氧形成Ti-C键[10],主要原因是样品在富氧下煅烧。CNS-TiO2样品N 1s的XPS图谱如图5所示,N在399.8 eV和401.6 eV处有2个强峰,它们分别归属于N 1s1/2和N 1s3/2[11],这可能是N元素掺入了TiO2的晶格,形成了Ti-O-N和O-Ti-N的结构形式[12]。图6是CNS-TiO2样品S 2p的XPS图谱,在169.5 eV处出现的峰源于样品里含有,这说明催化剂表面含有阴离子,而在168.4 eV处的峰则源于一部分S4+阳离子取代了部分Ti4+阳离子[13]。从以上分析结果可知,C、N和S都已掺入TiO2晶格。图7是样品在396~600 nm区间的表面光电压。从图7可知,CNS-TiO2样品出现了很强的表面光电压,而纯TiO2
几乎没有光电压产生,这说明碳、氮、硫的掺杂使得TiO2对可见光产生了响应。根据SPS测定原理,强SPS响应峰对应于高光生电子-空穴分离速率[14],由此可知,在可见光区CNS-TiO2比TiO2的光生电荷分离速率更高。这有利于提高催化剂活性,其结果与光催化活性测试结果一致。

图2样品SEM图
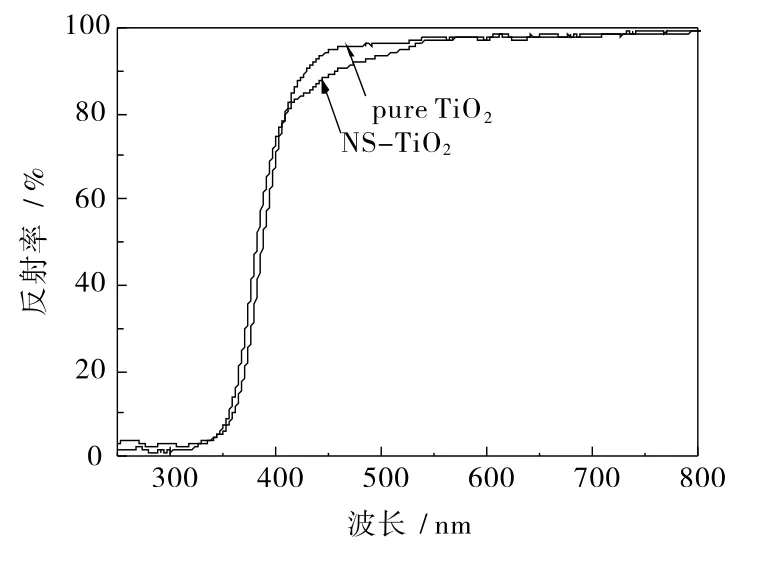
图3样品的紫外-可见漫反射图谱
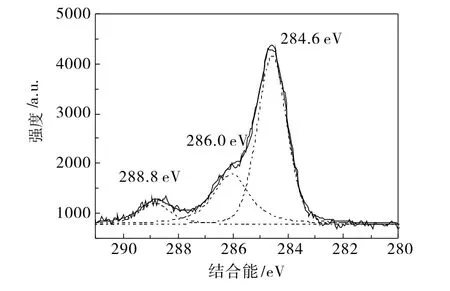
图4 CNS-TiO2样品的C 1s XPS谱图
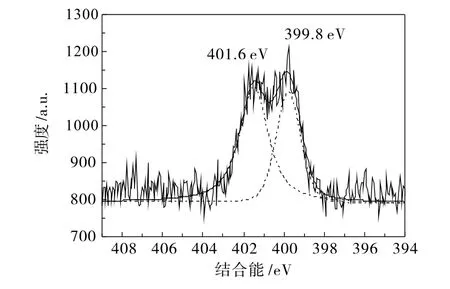
图5 CNS-TiO2样品的N 1s XPS谱图
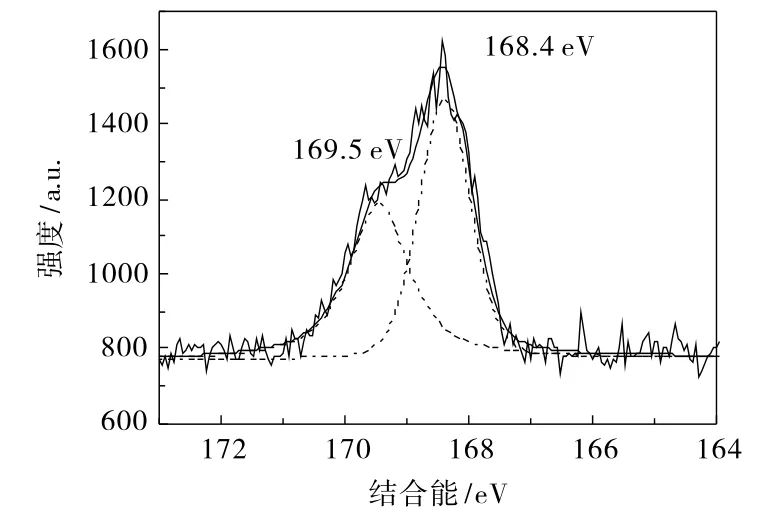
图6 CNS-TiO2样品的S 2p XPS谱图
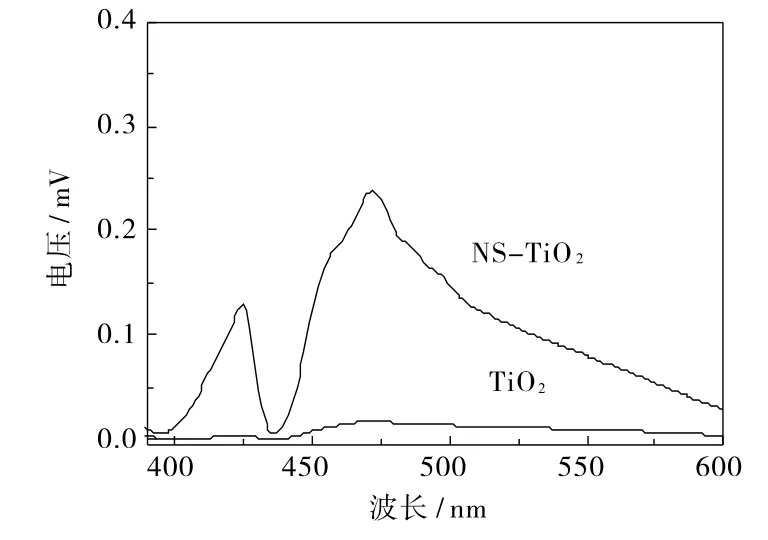
图7样品SPS谱图
2.2催化剂的光催化活性
图8是甲基橙浓度随时间变化的关系曲线。从图8可知,甲基橙光
催化反应符合一级动力学方程,其速率方程可表示为ln(C0/Ct)=kt,式中,C0为起始时刻甲基橙浓度,Ct为t时刻甲基橙溶液浓度,k表示反应速率常数。通过计算可以得出CNS-TiO2和TiO2催化甲基橙的光催化脱色速率常数k分别为0.606 h-1和0.204 h-1,表明碳、氮、硫掺杂的TiO2对甲基橙的光催化脱色速率常数显著提高,约为3倍。这说明碳、氮、硫共掺杂能显著提高TiO2的光催化活性。其主要原因是改性后的TiO2对可见光有响应,具有更高的比表面积和更高的电荷分离速率。
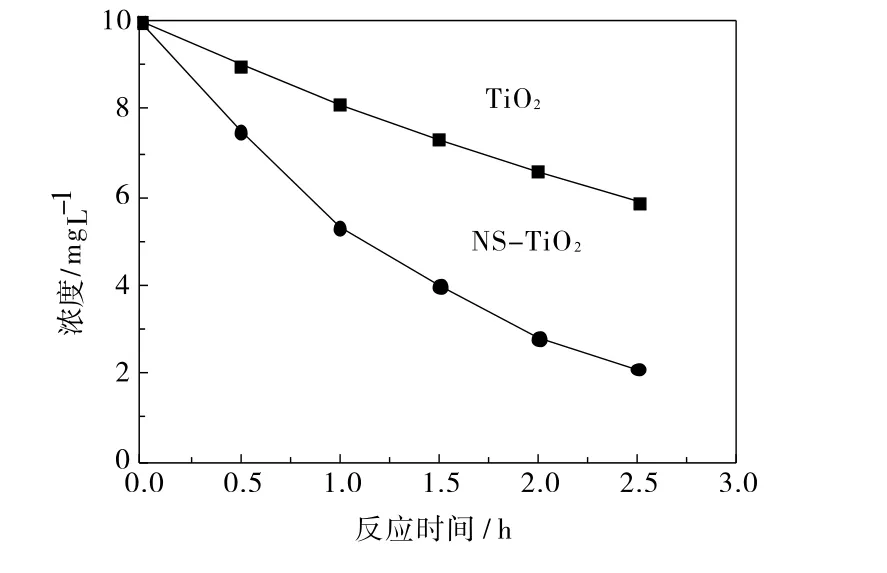
图8甲基橙浓度与光照时间曲线
3 结论
用[EMIm]HSO4离子液体为掺杂源,采用溶胶-凝胶法制备了碳、氮、硫共掺杂的TiO2,并用甲基橙为模拟污染物评价样品的太阳光光催化活性,其结果表明:
(1)碳、氮、硫共掺杂可以减小TiO2的晶粒大小,增加它的比表面积,从而提供更多的活性中心。
(2)碳、氮、硫共掺杂使TiO2对可见光产生响应,且提高了它的电荷分离速率。
(3)碳、氮、硫共掺杂TiO2对甲基橙的脱色率速率常数大约是纯TiO2的3倍,说明碳、氮、硫共掺杂能显著提高TiO2的光催化活性。
[1]Roy P,Berger S,Schmuki P.TiO2nanotubes:synthesis and applications[J].Angew.Chem.Inter.Edit.,2011,50(13):2904-2939.
[2]Liu Z,Zhang X,Nishimoto S,et al.Highly ordered TiO2nanotube arrays w ith controllable length for photoelectron-catalytic degradation of phenol[J].J.Phys.Chem.C, 2008,112(1):253-259.
[3]Tomkiew icz M.Scaling properties in photocatalysis[J]. Catal.Today,2000,58(2-3):115-123.
[4]AsahiR,Morikawa T,OhwakiT,et al.Visible-light photocatalysis in nitrogen-doped titanium oxides[J].Science,2001,293:269-271.
[5]Sano T,Mera N,Kanai Y,et al.Origin of visible-light activity of N-doped TiO2photocatalyst:behaviors of N and S atoms in a wet N-doping process[J].Appl.Catal. B-Environ.,2012,128:77-83.
[6]Zhang G,Zhang Y C,Nadagouda M,et al.Visible lightsensitized S,N and C co-doped polymorphic TiO2for photocatalytic destruction of microcystin-LR[J].Appl. Catal.B-Environ.,2014,144:614-621.
[7]Li F T,Wang X J,Zhao Y,et al.Ionic-liquid-assisted synthesis of high-visible-light-activated N-B-F-tri-doped mesoporous TiO2via a microwave route[J].Appl.Catal. B-Environ,2014,144:442-453.
[8]韩一丹,王凯,徐志坚,等.离子液体修饰溶胶-凝胶法制备介孔二氧化钛[J].硅酸盐学报,2009,40(9):1289-1293.
[9]Behpour M,A touf V.Study of the photocatalytic activity of nanocrystalline S,N-codoped TiO2thin films and powders under visible and sun light irradiation[J].Appl.Surf. Sci.,2012,258(17):6595-6601.
[10]Wang P,Yap P S,Lim T T.C-N-S tridoped TiO2for photocatalytic degradation of tetracycline under visiblelight irradiation[J].Appl.Catal.A-Gen.,2011,399(1-2):252-261.
[11]Cheng XW,Yu X J,Xing Z P.Synthesis and characterization of C-N-S-tridoped TiO2nano-crystalline photocatalyst and its photocatalytic activity for degradation of rhodamine B[J].J.Phys.Chem.Solids,2013,74(5):684-690.
[12]Rengifo-Herrera JA,Pierzchala K,Sienkiew icz A,et al. Abatement of organics and Escherichia coli by N,S co-doped TiO2under UV and visible light.Implications of the formation of singlet oxygen(1O2)under visiblelight[J].Appl.Catal.B-Environ.,2009,88(3-4):398-406.
[13]Xiao Q,Ouyang L,Photocatalytic photodegradation of xanthate over C,N,S-tridoped TiO2nanotubes under visible light irradiation[J].J.Phys.Chem.Solids,2011,72(1):39-44.
[14]Cheng X W,Yu X J,Xing Z P.One-step synthesis of visible active C-N-S-tridoped TiO2photocatalyst from biomolecule cysteine[J].Appl.Surf.Sci.,2012,258(19):7644-7650.
Study on the Photocatalytic Performance of C-N-S-codoped TiO2Prepared by Ionic Liquid
CHEN Jiufu1,2,ZHONG Jubo1,2,LIJianzhang1,2,CHENG Chaozhu1,2,DOU Lin1,2
(1.Green Catalysis Key Laboratory of Colleges in Sichuan Province,Zigong 643000,China;2.School of Chemistry and Pharmaceutical Engineering,Sichuan University of Science&Engineering,Zigong 643000,China)
The C-N-S-codoped TiO2(CNS-TiO2)is successfully prepared by the sol-gelmethod with 1-ethel-3-methylimdazolium hydrosulfate([EMIm]HSO4)ionic liquid as dopant.The synthesized photocatalysts is characterized by surface porositymeter,X-ray diffraction,scanning electron microscope,UV-Vis diffuse reflectance spectroscopy,X-ray photoelectron spectroscopy and surface photovoltage instrument.The photocatalytic performance of the samples is investigated by utilizing decolorization methyl orange aqueous solution as the simulation pollutants under simulated solar light irradiation.The results show that the as-synthesized CNS-TiO2has higher BET surface area and separation rate of charge and can response to visible light.The photocatalytic performance of CNS-TiO2is about3 times of that of pure TiO2.
titanium dioxide;ionic liquid;adulteration;photocatalytic performance
O64.4
A
1673-1549(2015)01-0012-05
10.11863/j.suse.2015.01.04
2014-12-11
绿色催化四川省高校重点实验室开放课题(LYJ14203;LZJ1301);四川理工学院研究生创新基金项目(Y2013025)
陈久福(1988-),男,四川遂宁人,硕士生,主要从事光催化方面的研究,(E-mail)cjf2171@163.com;李建章(1963-),男,教授,主要从事有机合成及有机催化方面的研究,(E-mail)lyl63@sina.com
