蒽醌法生产H2O2工作液的改进
2015-06-27方向晨贾立明刘全杰
刘 航,方向晨,贾立明,刘全杰
(1.辽宁石油化工大学 材料科学与工程系, 辽宁 抚顺 113001; 2.中国石化 抚顺石油化工研究院, 辽宁 抚顺 113001)
蒽醌法生产H2O2工作液的改进
刘 航1,2,方向晨2,贾立明2,刘全杰2
(1.辽宁石油化工大学 材料科学与工程系, 辽宁 抚顺 113001; 2.中国石化 抚顺石油化工研究院, 辽宁 抚顺 113001)
为了改进蒽醌法生产H2O2的由重芳烃(AR)和磷酸三辛酯(TOP)组成的工作液的氢效,考察了2-乙基蒽醌(2-EAQ)在添加邻甲基环己基醋酸酯(2-MCHA)或二异丁基甲醇(DIBC)的三组分工作液(AR+TOP+2-MCHA和AR+TOP+DIBC)中的溶解度,并分析了三组分工作液的密度、黏度、界面张力和H2O2的分配系数,从中选取了体积比为75∶20∶5的AR+TOP+2-MCHA和体积比为75∶5∶20的AR+TOP+DIBC 2种性能优异的工作液,采用微反装置评价了其氢效。结果表明,与两组分工作液相比,2-EAQ在三组分工作液中的溶解度得到了显著提高;与两组分工作液的氢效5.65 g/L相比,三组分工作液的氢效得到显著提高,分别达到12.53和11.31 g/L。
蒽醌法;邻甲基环己基醋酸酯;二异丁基甲醇;氢效
作为一种绿色化学品,双氧水广泛应用于织物和纸浆的漂白、化学合成、废水处理、电子行业和航天等领域,并且用量和使用范围逐年扩大[1]。目前,绝大部分双氧水由蒽醌法生产。将重芳烃(AR)和磷酸三辛酯(TOP)以75:25体积比制成混合溶剂,再溶解一定量的载体2-乙基蒽醌(2-EAQ)形成工作液,2-EAQ的溶解度为110 g/L;通过氢化、氧化、净化、浓缩以及后处理得到H2O2质量分数为27.5%的双氧水。该种工作液的氢效只有6 g/L左右。氢效低导致产量低,产品质量差,最主要的原因是工作液性能不够理想。笔者从这个角度出发,寻求合适的新型溶剂作为第三组分加入到原两组分溶剂体系,以改善工作液的性能。新型溶剂的选取原则:①蒽醌及氢蒽醌的溶解度要高;②H2O2在水与所选溶剂中的分配系数要高;③对氢化、氧化稳定,不水解;④沸点高、闪点高;⑤与水不互溶或互溶度低;⑥与水的密度差大;⑦廉价易得;⑧对催化剂的活性、选择性无影响;⑨与H2O2不反应[2]。根据以上9个原则和文献数据[3-4],选取邻甲基环己基醋酸酯(2-MCHA)和二异丁基甲醇(DIBC)2种溶剂作为新型工作液的第三组分。2-MCHA的抗水解性能好[5],这样可减少萃取过程中工作液的损失和对H2O2萃取液的污染[6]。在美国,DIBC产量的90%作为生产双氧水的溶剂[7]。将2-EAQ分别溶解于3种溶剂按一定比例混合制得的混合溶剂中,形成新型工作液体系,并从密度、黏度、界面张力、2-EAQ溶解度、H2O2的分配系数、反应氢效等方面进行比较,以选择性能良好的新型工作液体系。
1 实验部分
1.1 试剂和原料
2-乙基蒽醌(2-EAQ),萨恩化学技术(上海)有限公司产品;重芳烃(AR),江苏华伦化工有限公司产品;磷酸三辛酯(TOP),杭州大自然有机化工实业有限公司产品;邻甲基环己基醋酸酯(2-MCHA)、二异丁基甲醇(DIBC),东京化成工业株式会社产品;石英砂(10~20目、40~70目),天津市石英钟厂霸州市化工分厂产品;γ-Al2O3、蒸馏水、5.9%(质量分数)PdCl2溶液、H2,自制。
1.2 2-EAQ溶解度的测定
分别按V(AR)∶V(TOP)∶V(2-MCHA)为75∶20∶5、75∶10∶15和75∶5∶20,或V(AR)∶V(TOP)∶V(DIBC)为75∶20∶5、75∶10∶15和75∶5∶20配制几种混合溶剂。取相应体积的混合溶剂倒入三口烧瓶,再加入一定质量的2-EAQ,盖上瓶塞,置于25℃的水浴中,开动磁力搅拌。完全溶解后再向三口烧瓶中加入适量2-EAQ,根据其溶解速率调整每一次加入的量,直到2-EAQ不再溶解为止,记下此时消耗的2-EAQ的质量。由式(1)计算2-EAQ的溶解度。
S=me/VS
(1)
式(1)中,S为2-EAQ的溶解度,g/mL;me为溶解2-EAQ的质量,g;VS为混合溶剂的体积,mL。
1.3 工作液密度的测定
采用奥地利ANTON Passer公司DMA4500M型密度计,根据GB/T 1884-2000标准测量工作液密度。在20℃下,将工作液倒入温度大致相同的密度计量筒中,将密度计置于其中,静止。当温度达到平衡后,读取密度计刻度读数和工作液温度。用石油计量表将观察到的密度计读数换算成标准密度。
1.4 工作液黏度的测定
采用美国凯能公司CAV2100型黏度计,根据GB/T 265-1988标准测定工作液的运动黏度。在20℃下测定一定体积的工作液在重力下流过一个标定好的玻璃毛细管黏度计的时间,黏度计的毛细管常数与流动时间的乘积,即为该温度下工作液的运动黏度。
1.5 工作液界面张力的测定
在德国KRUSS公司K100型全自动表面张力仪上,采用板法界面张力测量法测定工作液层与水层之间的界面张力。向样品杯中装入样品杯体积80%的去离子水,置于主机样品台上,升高样品台,靠近板时停止,测定得到低密度液体的浮力;然后,清洗灼烧板待用;取出低密度液体,清洗样品杯后,倒入高密度液体,升高样品台,靠近板时停止;待高密度液体浸入板2 mm时,倒入低密度液体,直至液体完全浸没板,到达板的上边缘为止,此时数据即为工作液层与水层之间的界面张力。
1.6 H2O2分配系数的测定
取50 mL 30%质量分数的H2O2溶液置于三口烧瓶中,加入相同体积的工作液与其混合。将该三口烧瓶置于25℃的水浴锅中,搅拌30 min。将混合溶液转入分液漏斗中,静置90 min,分别取样分析工作液相和水相的H2O2浓度,按分配系数定义,由式(2)计算分配系数[8]。
D=cH2O/c
(2)
式(2)中,D为分配系数;cH2O和c分别为水相中和工作液相中H2O2的质量浓度,g/mL。
1.7 工作液性能的评价
采用微型固定床管式反应器进行加氢反应制备H2O2。反应管带有夹套,内径7 mm、高55 cm。H2和工作液由上口进入。催化剂是负载了Pd的Al2O3小球,Pd质量分数0.3%,小球直径0.4 mm,填充体积5 mL。在适宜条件下反应5 h,得到50 mL氢化液,然后通空气氧化,使其中的氢蒽醌全部反应生成H2O2。每次用20 mL去离子水分4次萃取所生成的H2O2[9],采用迷你数显折射仪测定萃取液中H2O2质量分数,称量萃取液质量并按式(3)计算氢效。
He=(wf·m)/V
(3)
式(3)中,He为氢效,g/mL;wf为萃取液中H2O2的质量分数,%;m为萃取液的质量,g;V为氢化液的体积,mL。
2 结果与讨论
2.1 第三组分加入对蒽醌法生产H2O2的混合溶剂工作液性能的影响
2.1.1 对2-EAQ溶解度的影响
2-EAQ在混合溶剂工作液中的溶解度是评价蒽醌法生产H2O2工作液性能的一个关键因素。2-EAQ在几种不同体积比的混合溶剂工作液中的溶解度列于表1。

表1 25℃下2-EAQ在几种不同混合溶剂工作液中的溶解度(S)
由表1可以看出,与两组分工作液相比,添加第三组分2-MCHA和DIBC后,2-EAQ的溶解度显著提高,且随第三组分体积分数的增大,2-EAQ的溶解度逐渐增加。
从理论上可以解释上述现象。2-EAQ和2-MCHA的分子结构示于图1。2-MCHA和2-EAQ分子中均含有C=O基团,C=O中的C原子是sp2杂化,它的3个sp2杂化轨道形成的3个σ键在同一平面上,键角120°,还余下的1个C原子p轨道和O的1个p轨道,与σ键所在的平面垂直,相互交盖形成π键。因此C=O双键是由1个σ键和1个π键组成。由于O原子的电负性大于C原子,因此C=O的π键一旦形成,即是极性的,电子云偏向O,这使得2-MCHA和2-EAQ分子都具有较大的偶极矩。由于溶剂化效应,这2种分子之间就会形成很强的偶极-偶极作用力。这是一种非专属性溶剂化的作用,偶极-偶极作用力会克服2-EAQ分子间比较弱的分子间作用力,使得2-EAQ分子被迅速溶解到溶剂中,增大了2-EAQ的溶解度。而且,2-MCHA极性很强,根据相似相溶原理,2-MCHA作为第3组分的加入形成的混合溶剂体系对2-EAQ的溶解性很强,增大了其溶解度。

图1 2-EAQ和2-MCHA分子结构式
DIBC的分子结构示于图2。DIBC的分子中有可以给出H+的OH基团,因此DIBC可以作为氢键给体,是质子型极性溶剂。2-EAQ分子中有2个C=O,其O上有孤对电子,是氢键受体,这样DIBC与2-EAQ分子间能够形成氢键。氢键是一种比较强的静电引力,比分子间作用力强,这使得2-EAQ分子通过扩散作用均匀地分散到溶剂中去,从而增加了2-EAQ的溶解度。同时DIBC有较强的极性,而2-EAQ也是极性分子,根据相似相溶原理,2-EAQ会更容易溶解在添加有DIBC的混合溶剂中。
图2 DIBC分子结构式
2.1.2 对工作液密度的影响
密度是评价一种工作液好坏的基本指标之一。工作液的密度与水的密度相差越大,萃取过程中与水分层程度越好。几种工作液的密度列于表2。

表2 20℃下不同混合溶剂工作液的密度(ρ)
由表2可以看出,随着第3组分加入量的增加,工作液密度逐渐增大。其中AR+TOP+2-MCHA体积比分别为75∶10∶15、75∶5∶20的工作液密度已经非常接近水的密度,对后续的萃取分离不利,不适合作为反应的原料;而AR+TOP+DIBC的工作液密度与两组分工作液相比增加不大,比较适合作为原料进行反应。
虽然课外科技活动是理论课堂的重要补充,对提高学生实践创新能力具有重要意义,教育部非常重视以学生课外科技活动为载体,提高学生实践创新能力,并于2012年起设立了“大学生创新创业计划项目”,各医药院校也设立了一系列各具特色的课外科技活动,但目前大学生课外科技活动中仍存在问题,影响了实施效果。
2.1.3 对工作液黏度的影响
黏度表征了工作液的循环流动性能,黏度越小,工作液循环流动越好。几种不同体积比混合溶剂工作液黏度数据列于表3。

表3 20℃下几种不同混合溶剂工作液的黏度(ν)
由表3看出,工作液的黏度也是随着第三组分加入量的增加而逐渐增大,其中,与两组分工作液相比,AR+TOP+2-MCHA工作液黏度整体较大,体积比为75∶20∶5的工作液黏度较为合适,而AR+TOP+DIBC的工作液黏度变化幅度较小,黏度值也较小,能够满足实验需要。
2.1.4 对工作液界面张力的影响
界面张力表征了工作液在萃取过程中与水层分离的难易程度,界面张力越大,越容易与水分层。几种不同混合溶剂工作液的界面张力数据列于表4。

表4 20℃下几种不同混合溶剂工作液的界面张力(γ)
由表4可以看出,几种工作液的界面张力随着第三组分加入量的增加而降低,但数值与两组分工作液接近,说明与水层分离能力较好。
H2O2在工作液中的分配系数反映了在萃取操作过程中H2O2在油相和水相之间的迁移能力和分离效能,分配系数越大,H2O2的迁移能力和分离效能越好,越容易被水萃取出来。H2O2在几种不同混合溶剂工作液中的分配系数列于表5。
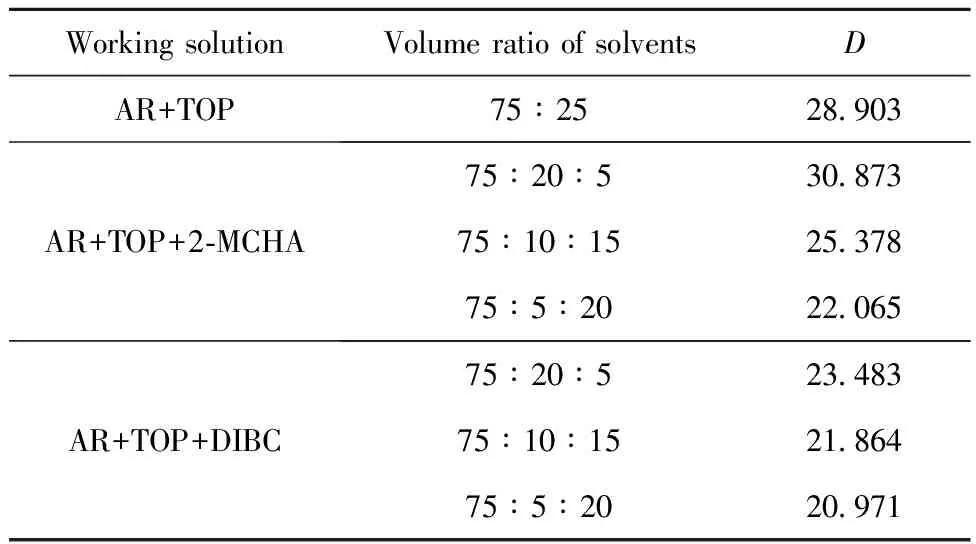
表5 25℃下H2O2在几种不同混合溶剂工作液中的分配系数(D)
由表5可以看出,H2O2在75∶20∶5 的AR+TOP+2-MCHA工作液中的分配系数最高,分配系数整体高于添加了AR+TOP+DIBC工作液。这是由于2-MCHA分子中的基团均是疏水基团,与H2O2分子相互排斥,使得H2O2分子容易被迁移和分离,因此分配系数较大;而DIBC分子中有1个羟基,羟基是比较强的亲水基团,与H2O2分子之间有一定的吸引力,使得在萃取时H2O2分子不容易被迁移和分离,因此分配系数较小。
2.3 3种不同混合溶剂工作液的氢效
工作液的氢效直接反映了工作液的整体性能。在保持氢化深度小于60%的情况下,氢效越高,表明工作液的氢化性能越好,单位体积工作液产出H2O2的量越大。综合以上几组实验结果,选择了2组性能较为优异的三组分工作液体系AR+TOP+2-MCHA(体积比75∶20∶5)和AR+TOP+DIBC(体积比75∶5∶20)作为考察氢效的对象,以AR+TOP工作液(体积比75:25)作为对比,考察第3组分的加入对工作液氢效的影响,结果列于表6。

表6 3种不同混合溶剂工作液的氢效(He)
由表6可以看出,添加了DIBC和2-MCHA的工作液的氢效比两组分工作液有了显著提升,并且添加了2-MCHA的工作液的氢效要比添加了DIBC的工作液的要高。这可以由DIBC和2-MCHA分子结构中的取代基对2-EAQ分子中C=O基的影响来解释。DIBC分子结构中有1个OH,其中的O原子电负性较强,使得电子云偏向O,H带正电,O带负电,从而产生较大偶极矩,是吸电子基团;2-MCHA分子中的-COOR基团中,O原子的电负性也比C原子的电负性要强,C带正电,O带负电,可产生较大偶极矩,也是吸电子基团。2-EAQ分子中C=O基的电子云偏向O,2种带有吸电子基团的溶剂加入后,使得2-EAQ分子中C=O基的电子云偏向O的程度加大,电子云分布发生畸变而产生极化效应;同时吸电子基团提高了2-EAQ的还原电势,其还原电势越高越容易被还原[10]。加氢反应时,H原子会优先进攻电子云分布比较密集的O原子,也就是加氢反应会更加倾向于发生在C=O基,使其加氢反应活性增大,加氢效率提高,同时DIBC和2-MCHA均对氢蒽醌有一定的溶解性能,这使得高度氢化成为可能,而不致于产生氢蒽醌和四氢氢蒽醌沉淀,因而可获得一种高产率H2O2的工作溶液[11]。而-COOR基团的吸电子能力要强于OH,对2-EAQ的极化效应更强,C=O基的加氢反应活性更大,因此加入2-MCHA后工作液的氢效也较加入DIBC的工作液的氢效要高。
3 结 论
蒽醌法生产H2O2的两组分混合溶剂工作液(重芳烃(AR)+磷酸三辛酯(TOP))中,加入第三组分邻甲基环己基醋酸酯(2-MCHA)或二异丁基甲醇(DIBC),显著提高了2-乙基蒽醌(2-EAQ)的溶解度,增加了工作液中有效蒽醌的含量。综合性能较好的三组分工作液体系为AR+TOP+2-MCHA(体积比75∶20∶5)和AR+TOP+DIBC(体积比75∶5∶20)。与两组分工作液相比,该2种三组分工作液的氢效分别增加了120%和100%,能够作为新型溶剂应用在H2O2生产中,以提高H2O2产量。
[1] 陈冠群, 周涛,曾平,等. 蒽醌法生产双氧水的研究进展[J]. 化学工业与工程,2006, 23(6):550-555. (CHEN Guanqun,ZHOU Tao,ZENG Ping,et al. Progress in production of hydrogen peroxide through anthraquinone[J]. Chemical Industry and Engineering,2006, 23(6):550-555.)
[2] 化工百科全书编委会. 化工百科全书[M]. 北京:化学工业出版社,1994:641.
[3] PRAUER J W, FALLS N. Production of hydrogen peroxide:US,2657980[P]. 1953-11-03.
[4] THURMAN E, BROWN C J. Method of making hydrogen peroxide: GB, 856420[P]. 1960-12-14.
[5] COINGT M. Improvement in or relating to the manufacture of hydrogen peroxide: GB, 1211572A[P]. 1968.
[6] 于剑昆. 醋酸甲基环己酯的合成及其在蒽醌法过氧化氢生产中的应用[J]. 化学推进剂与高分子材料. 2011,9(4):9-15. (YU Jiankun. The synthesis of methyl cyclohexanol acetate and its application in the production of hydrogen peroxide by anthraquinone[J]. Chemical Propellants & Polymeric Materials, 2011,9(4):9-15.)
[7] Toxicology/Regulatory Services,Inc. 4-Heptanol, 2,6-dimethyl- (Diisobutyl Carbinol;CAS RN 108-82-7) High production volume (HPV) chemical challenge test plan and data review. http://www.epa.gov/hpv/pubs/summaries/4hept26d/c15004rt3.pdf.2006-11-22/2013-09-22.
[8] 张国臣. 过氧化氢生产技术[M]. 北京:化学工业出版,2012: 110-111.
[9] 陈四海, 蔡志伟,龚凌,等. 四丁基脲代替磷酸三辛酯用于过氧化氢生产[J]. 石油化工, 2003,32(6):470-473. (CHEN Sihai,CAI Zhiwei,GONG Ling, et al. Tetrabutyl urea instead of trioctyl phosphate for the production of hydrogen peroxide[J]. Petrochemical Technology, 2003,32(6):470-473.
[10] 邢其毅,裴伟伟, 徐瑞秋,等. 基础有机化学[M]. 第三版. 北京:高等教育出版社,2005: 864.
[11] 叶道明. 双氧水生产中工作溶液的选择[J]. 无机盐工业,1999,31(1):26-27. (YE Daoming. Selection of working solution in the production of hydrogen peroxide[J]. Inorganic Chemicals Industry,1999, 31(1):26-27.)
Improvement of Working Solution for H2O2Production by Anthraquinone Method
LIU Hang1,2, FANG Xiangchen2, JIA Liming2, LIU Quanjie2
(1.DepartmentofMaterialsScienceandEngineering,LiaoningShihuaUniversity,Fushun113001,China;2.FushunResearchInstituteofPetroleumandPetrochemicals,SINOPEC,Fushun113001,China)
In order to improve the hydrogen efficiency of working solution containing two components of heavy aromatics(AR) and trioctyl phosphate(TOP) for H2O2production by anthraquinone method, the solubilities of 2-ethylanthraquinone(2-EAQ) in working solutions of AR+TOP added acetic acid (2-methylcyclohexyl) ester(2-MCHA) or 2,6-dimethyl-4-heptanol(DIBC) were measured. The density, viscosity, surface tension of AR+TOP+2-MCHA and AR+TOP+DIBC solutions, and the distribution coefficient of H2O2in these solutions were analyzed. The AR+TOP+2-MCHA and AR+TOP+DIBC solutions with the volume ratios of 75∶20∶5 and 75∶5∶20, respectively, were chosen as the working solutions, which possessed good properties for production of H2O2. Then their hydrogen efficiencies were evaluated in a microreactor. The results showed that compared with the AR+TOP working solution, whose hydrogen efficiency was 5.65 g/L, the hydrogen efficiencies of the two new working solutions were significantly improved, reaching 12.53 and 11.31 g/L, respectively.
anthraquinone method; acetic acid (2-methylcyclohexyl) ester; 2,6-dimethyl-4-heptanol; hydrogen efficiency
2013-11-07 第一作者: 刘航,男,硕士研究生,从事蒽醌法生产双氧水工作液方面的研究;E-mail:lhsdut@163.com
方向晨,男,教授级高级工程师,从事石油炼制加氢工艺及相关动力学方面的研究;E-mail:fangxiangchen.fshy@sinopec.com
1001-8719(2015)01-0072-06
TQ
A
10.3969/j.issn.1001-8719.2015.01.012
