H3PW12O40/SiO2高效催化Mannich反应合成β-氨基酮衍生物
2015-06-23陈慧媛徐玉林叶华林杨水金
陈慧媛,徐玉林,叶华林,杨水金
(湖北师范学院化学化工学院,稀有金属化学湖北省协同创新中心(湖北师范学院),湖北黄石435002)
H3PW12O40/SiO2高效催化Mannich反应合成β-氨基酮衍生物
陈慧媛,徐玉林,叶华林,杨水金
(湖北师范学院化学化工学院,稀有金属化学湖北省协同创新中心(湖北师范学院),湖北黄石435002)
在室温条件下,采用浸渍法合成的H3PW12O40/SiO2为催化剂,高效催化酮、芳香醛和苯胺的Mannich反应合成系列β-氨基酮衍生物.对新型催化剂H3PW12O40/SiO2的制备条件进行优化,系统地研究了H3PW12O40负载量、焙烧温度、活化时间对催化剂的影响.探讨了H3PW12O40/SiO2对酮、芳香醛和苯胺的Mannich反应的催化活性,系统地研究了反应温度、催化剂用量、反应物的摩尔比等因素对产物收率的影响.实验结果表明:在n(酮)∶n(芳香醛)∶n(苯胺)=1.5∶1.2∶1.0,催化剂的用量占反应物料总质量的8%,反应温度为20℃,反应时间为9 h的最佳条件下,β-氨基酮衍生物的收率在61.2%~77.0%之间.整个反应体系具有条件温和、操作简单、不污染环境和催化剂可重复回收利用等优点.①
H3PW12O40/SiO2;Mannich反应;β-氨基酮;催化
Mannich反应是合成β-氨(胺)基羰基化合物及其衍生物的重要有机反应.其反应产物β-氨基酮是有机合成中天然生物活性分子的中间体,在医药、农药、火药、染料、涂料等方面有着广泛的用途[1-4].传统合成β-氨基酮的工艺条件是在盐酸的催化下进行的,但是这种传统的方法存在腐蚀性较强、污染环境、后处理困难等缺点[5].近几年也有文献报道,Mannich反应可用稀土金属盐[6]、过渡金属盐[7]、氨基磺酸[8]、离子液体[9]、Yb(OTf、NaBAr4F[11]、相转移催化剂季铵盐[12]等来催化.虽然这些催化技术相对成熟,但是这些方法均存在许多缺点,诸如催化剂较昂贵、催化剂用量较大、催化效率不高、分离困难等.因此,寻找一类新的催化活性高、环保型的催化剂成为人们追求的目标.
杂多酸又称多金属氧酸盐(Polyoxometalates,简写为POMs),对其开发研究日益受到人们关注[13].因杂多酸具有独特的酸性、“准液相”行为、较高的催化活性和选择性、对设备的腐蚀性低、反应条件温和等优点,近年来在催化研究领域中受到研究者们的广泛重视.其中磷钨酸是由杂原子P和配位原子W以一定的结构通过氧原子配位桥联组成的含氧多元酸,兼具强酸性和氧化还原性,同时具有催化活性高、稳定性好、可调变性等优点,对环境无污染,是一种多功能的新型绿色催化剂,具有广阔的研究价值和应用前景.
但磷钨酸易溶于水,分离和回收困难.SiO2具有大的比表面积和规则的孔结构,常用作载体.本研究以SiO2为载体,将磷钨酸负载于SiO2上催化环己酮或苯乙酮、芳香醛和苯胺合成系列的β-氨基酮衍生物,反应通式如Scheme 1所示.
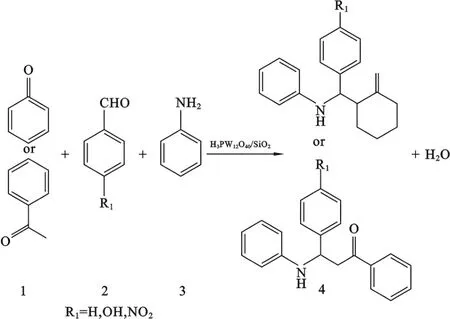
Scheme 1β-氨基酮衍生物的合成路径
1 实验部分
1.1 主要仪器和试剂
1.1.1 主要仪器粉末衍射分析用DADVANCE型X-射线衍射仪(德国布鲁克公司产),石墨单色器滤波,用铜靶Kɑ1辐射,在管电流40 mA,管电压40 kV的条件下测定,扫描范围5°~70°;Nicolet 5700型红外拉曼光谱仪(美国尼高力公司产)KBr压片法;1H NMR用Varian Mercury 300型核磁共振仪测定,TMS为内标;MS使用Finnigan LCQ Advantage MAX质谱仪测定;X-4数字显示显微熔点测定仪(上海隆拓仪器设备有限公司);电子天平(北京赛多利斯仪器系统有限公司);PKW-Ⅲ型电子节能控温仪.
1.1.2 主要试剂苯甲醛、对羟基苯甲醛、对硝基苯甲醛、环己酮、苯乙酮、苯胺、饱和NaHCO3、正硅酸乙酯、无水乙醇、浓氨水均为分析纯,磷钨酸(自制),实验用水均为去离子水.
1.2 H3PW12O40/SiO2催化剂的制备方法
1.2.1 SiO2的制备将无水乙醇、H2O和浓氨水按照n(C2H5OH)∶n(H2O)∶n(浓氨水)=8∶4∶1的比例配制混合溶液.在室温下搅拌混合均匀后,将一定量的正硅酸乙酯慢慢滴加到混合溶液中,搅拌半小时,形成乳白色液体.然后静置半小时,将溶液装入离心管进行离心,沉淀用蒸馏水、乙醇交替洗涤3次,烘干,研磨后即可得SiO2白色粉末.
1.2.2 浸渍法制备H3PW12O40/SiO2将一定量的H3PW12O40·xH2O溶解于20 mL的蒸馏水中,准确加入定量的SiO2,在室温下混合搅拌12 h.所得悬浮液经蒸干后,在马弗炉中以一定的温度煅烧一定时间,研碎即可得到催化剂H3PW12O40/SiO2.
1.3 β-氨基酮衍生物的合成在50 mL圆底烧瓶中按一定计量比加入苯甲醛、环己酮、苯胺及一定量的催化剂和无水乙醇,在室温下磁力搅拌,反应一段时间后有大量固体析出,抽滤,产物经饱和NaHCO3洗涤后,过滤得到粗产物,在粗产物中加入一定量的无水乙醇加热,使粗产物尽可能的溶解,然后趁热过滤,滤液经室温冷却后结晶,得到纯产品.
2 结果与讨论
2.1 催化H3PW12O40/SiO2表征
2.1.1 催化剂的IR光谱H3PW12O40和H3PW12O40/SiO2的红外谱图如图1所示.
由图1可知,H3PW12O40(a)的特征峰为1 082.2,985.6,898.4和802.6 cm-1,表明其具有Keggin型结构.另外在1 659.1 cm-1有弱的吸收峰,其为水的弯曲振动峰,说明此化合物中含有结晶水.而在(b),(c),(d)中,负载后H3PW12O40(a)在898.4 cm-1处的特征峰迁移至951.3 cm-1,1 082.2和985.6 cm-1处与SiO2的特征峰重合,在1 079.2 cm-1处表现为一宽峰,但802.6 cm-1的特征峰仍保留,说明H3PW12O40/SiO2中H3PW12O40仍保留Keggin型结构.
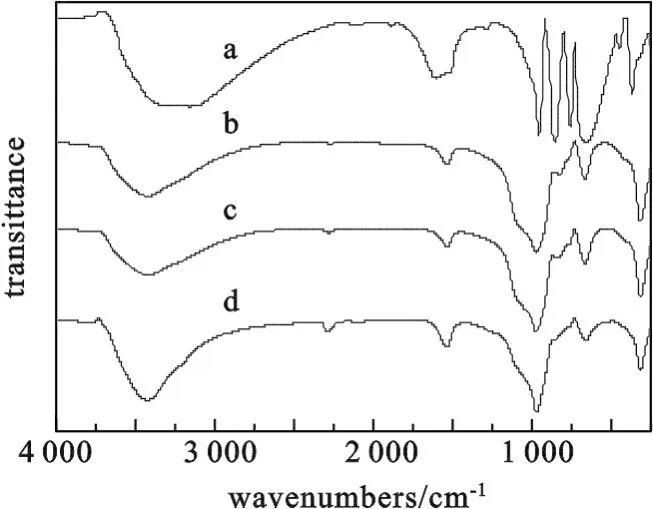
图1 H3PW12O40(a),20%H3PW12O40/SiO2(b),30% H3PW12O40/SiO2(c)和40%H3PW12O40/SiO2(d)的IR谱图
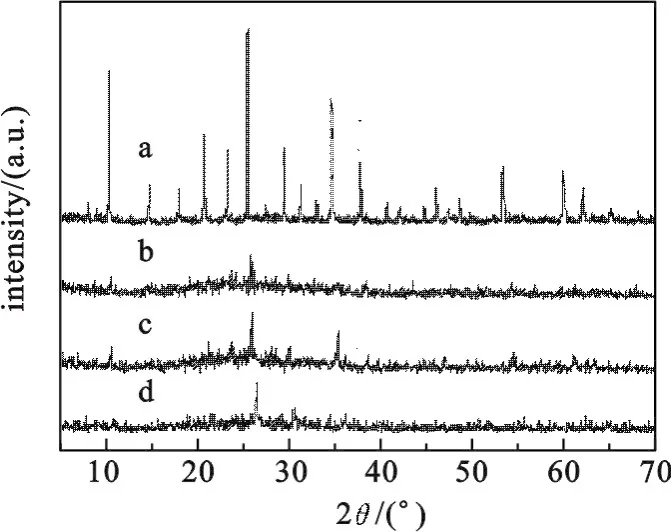
图2 H3PW12O40(a),20%H3PW12O40/SiO2(b),30% H3PW12O40/SiO2(c)和40%H3PW12O40/SiO2(d)的XRD谱图
2.1.2 催化剂的XRD谱H3PW12O40和H3PW12O40/SiO2的XRD光谱图如图2所示.
由图2可知,H3PW12O40(a)的特征衍射出现在10°,21°,25°,30°和35°左右,这为Keggin型结构的特征衍射峰.而在(b),(c),(d)中,H3PW12O40/SiO2只在25°左右出现一个宽峰,H3PW12O40的衍射峰消失,表明H3PW12O40均匀分布在二氧化硅表面上,没有出现聚合现象.
2.2 催化剂H3PW12O40/SiO2制备条件的优化采用合成2-(1-苯胺基)苯甲基-环己酮为探针反应,探针反应条件为:固定环己酮为20 mmol,苯胺20 mmol,苯甲醛20 mmol,催化剂的用量为8%(占反应物料总质量的百分含量),无水乙醇用量为10 mL,反应时间为9 h.
2.2.1 H3PW12O40负载量的优化固定催化剂的活化时间4 h,焙烧温度为200℃,改变H3PW12O40负载量,考察H3PW12O40负载量对催化剂催化活性的影响,实验结果见表1.
由表1可知,随着H3PW12O40负载量的增大,产物的收率先开始增大,后随H3PW12O40负载量的增大产物收率反而降低.当H3PW12O40负载量为30%时,催化剂催化活性达到最高,故确定适宜的H3PW12O40负载量为30%.
2.2.2 焙烧温度的优化固定催化剂的活化时间4 h,H3PW12O40的负载量为30%,改变焙烧温度,探讨焙烧温度对催化剂催化活性的影响,实验结果见表2.

表1 H3PW12O40负载量对催化剂活性的影响

表2 焙烧温度对催化剂活性的影响
由表2可知,随着焙烧温度的升高,产物的收率先开始增大,后随焙烧温度的升高收率反而下降.当焙烧温度为100℃时,催化剂催化活性达到最高,故确定适宜焙烧温度为100℃.
2.2.3 活化时间的优化确定催化剂的焙烧温度为100℃,H3PW12O40的负载量为30%,改变活化时间,探讨活化时间对催化剂催化活性的影响,实验结果见表3.
由表3可知,随着活化时间的延长,产物的收率先增大后降低.当活化时间为4 h时,催化剂催化活性达到最高,故确定适宜活化时间为4 h.
由以上实验结果表明,催化剂H3PW12O40/SiO2的最优制备条件是:H3PW12O40/SiO2负载量为30%,焙烧温度为100℃,活化时间为4 h.
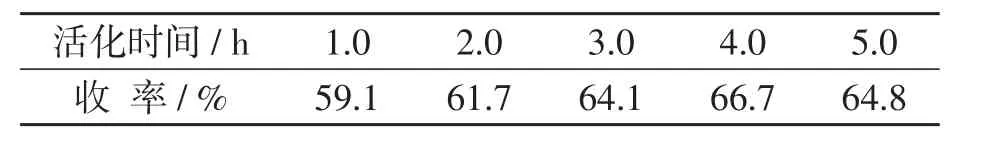
表3 活化时间对催化剂活性的影响
2.3 反应条件的优化
2.3.1 催化剂用量对反应的影响以苯甲醛(20 mmol)、环己酮(20 mmol)和苯胺(20 mmol)作为反应底物,10 mL乙醇为溶剂,H3PW12O40/SiO2为催化剂,反应9 h,对三组分Mannich反应的条件进行优化.催化剂的用量对反应收率的影响结果见表4.
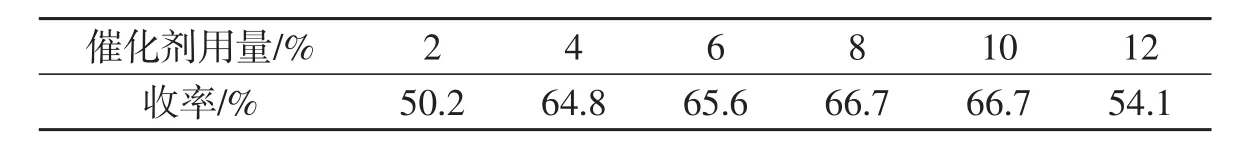
表4 催化剂用量对收率的影响
由表4分析可知,随着催化剂用量的增加,得到的Mannich反应的收率先呈上升的趋势.用量为8%时,收率达到66.7%;继续增加催化剂用量,收率反而下降.所以选择催化剂最适宜用量为8%.
2.3.2 反应物的配比对收率的影响确定催化剂的适宜用量后,进一步考察了反应物的摩尔比对反应收率的影响,结果见表5.

表5 反应物的摩尔对收率的影响
由表5可知:当n(环己酮)∶n(苯甲醛)∶n(苯胺)=1.5∶1.2∶1.0时,产品的收率最高,因此确定n(环己酮)∶n(苯甲醛)∶n(苯胺)为1.5∶1.2∶1.0.
2.3.3 反应温度对收率的影响确定了催化剂用量和三组分摩尔比以后,进一步考察了反应温度对反应收率的影响,其结果见表6.
表6结果表明,高温不利于Mannich反应进行,反应温度过高时,反应体系颜色加深,TLC跟踪表明有副产物生成.在20℃时产品收率最高,因此确定理想反应温度为20℃.
2.3.4 催化剂重复使用反应完后回收催化剂,经过滤、洗涤、活化后重复使用.在最优反应条件下,以环己酮(30 mmol)、苯甲醛(24 mmol)和苯胺(20 mmol)作为反应底物,探索了催化剂重复使用过程中的催化效率,其结果见表7.结果发现:催化剂重复使用4次,产品的收率依次为:77.0%,63.9%,56.2%和42.2%.催化效率有降低的趋势,其主要原因可能是由于重复使用多次以后,磷钨酸部分脱落,引起催化效率降低.但催化剂重复利用4次后,收率仍有42.2%,说明该催化剂具有一定的催化效果.具有回收再利用的优点,克服了传统催化剂难以回收利用,污染环境的缺点.
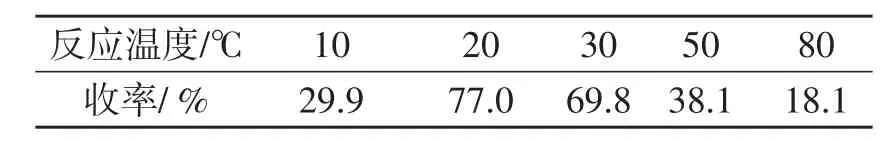
表6 反应温度对收率的影响

表7 催化剂重复使用次数对收率的影响
2.3.5 反应底物对收率的影响以最优化的反应条件,在20℃时,8%的H3PW12O40/SiO2为催化剂,对不同的酮(30 mmol)、芳香醛(24 mmol)和苯胺(20 mmol)在10 mL的乙醇中反应9 h,其反应结果见表8.
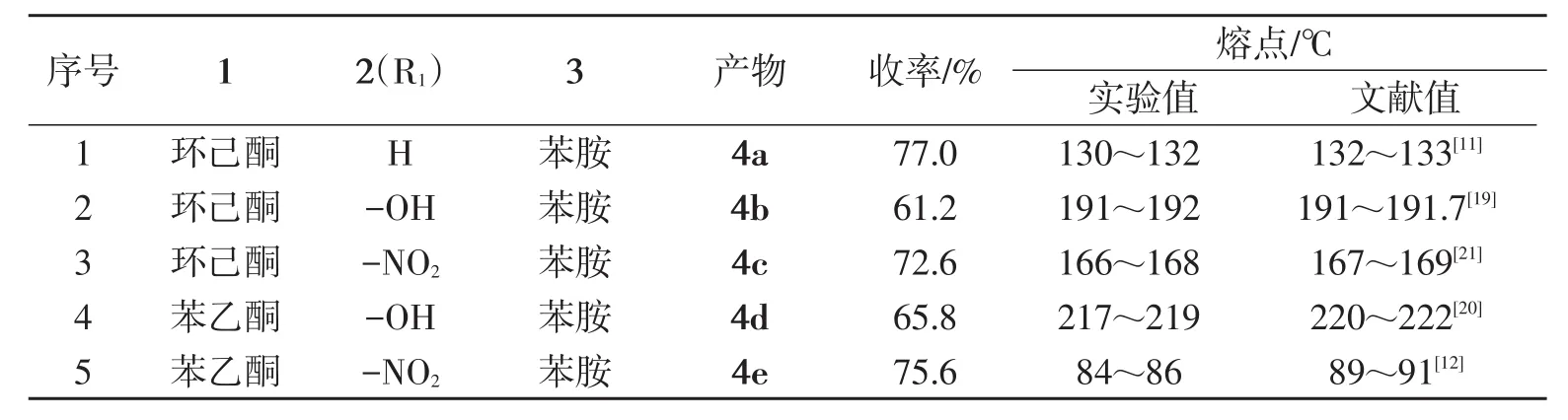
表8 H3PW12O40/SiO2催化合成不同的β-氨基酮衍生物
由表8可知:H3PW12O40/SiO2对合成β-氨基酮衍生物具有良好的催化效果,5种β-氨基酮衍生物的收率在61.2%~77.0%之间.
2.3.6 产品的IR光谱分析对5种β-氨基酮衍生物进行了IR分析,其特征吸收峰数据见表9.
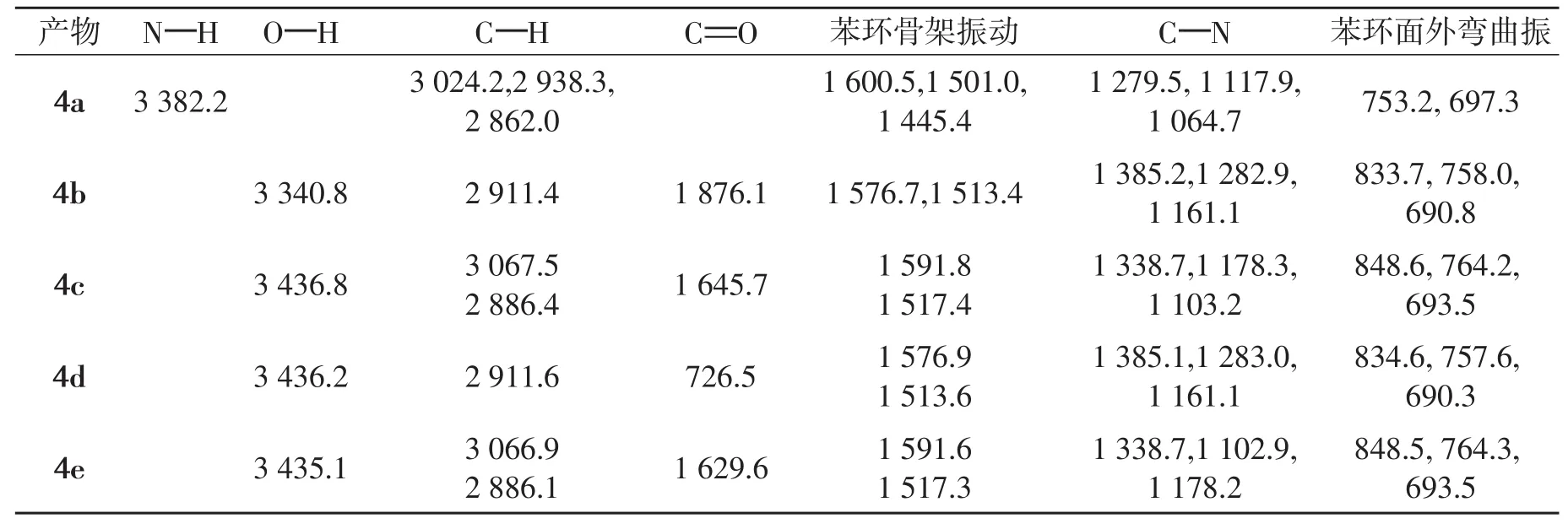
表9 β-氨基酮衍生物的IR特征吸收峰数据表
由表9可知,其IR特征吸收峰数据与其结构和文献一致,符合要求.
2.3.7 产品的质谱分析对所合成的2-(1-苯胺基)苯甲基-环己酮进行质谱分析,其结果见图3.

图3 2-(1-苯胺基)苯甲基-环己酮的MS图
由图3可知:m/z:280.02为[M+1]+,结合目标产物分子式可知,所合成的2-(1-苯胺基)苯甲基-环己酮与目标产物的相对分子质量是一致的,所合成的化合物符合要求.
对2-(1-苯胺基)苯甲基-环己酮进行核磁氢谱和碳谱分析,由1H NMR(CDCl3,300 MHz)δ:1.26~2.5 (m,9H,CH2),2.77(s,1H,CH),4.61(s,1H,NH),6.5~7.5(m,10H,ArH);13C NMR δ:23.59,24.80,26.96,27.84,28.59,31.25,41.72,42.36,113.72,114.02,117.63,126.94,127.45,128.31,128.94,129.01,141.42,211.32,212.94可知,该数据与其结构和文献数据一致,符合要求.
3 结论
综上所述,在H3PW12O40/SiO2的最优条件下,酮、芳香醛和苯胺进行的三组分“一锅法”Mannich反应,合成β-氨基酮衍生物的适宜条件是:当反应温度为20℃、反应物摩尔比为:n(环己酮)∶n(苯甲醛)∶n(苯胺)=1.5∶1.2∶1.0,催化剂的用量占反应物料总质量的8%,溶剂为无水乙醇,反应时间为9 h,5种β-氨基酮衍生物的收率在61.2%~77.0%之间.使用H3PW12O40/SiO2作催化剂具有价廉易得,对环境无污染,可回收利用的优点.该方法为β-氨基酮衍生物的合成提供了新的途径,具有良好的应用前景.
[1]万道正.曼尼希反应和曼尼希碱化学[M].北京:科学出版社,1986:1-455.
[2]惠斌,孟娜,陈凤凰,等.离子液体中的Mannich反应研究[J].化学试剂,2006,28(6):323-325.
[3]路军,白银娟,米春喜,等.浅谈曼尼奇反应及其在有机合成中的应用[J].大学化学,2000,15(1):29-32.
[4]Sheela J,Navita K,Deepak K,et al.Synthesis and in vitro study of novel mannich bases as antibacterial agents[J].Bioorg Med Chem Lett,2005,15(1):221-226.
[5]Yi L,Lei H S,Zou J H,et al.The Mannich reaction between aromatic ketones,aromatic aldehydes and aromatic amines[J]. Synthesis,1991(9):717-718.
[6]Dai Y,Li B D,Quan H D,et al.CeCl3·7H2O as an efficient catalyst for one-pot synthesis of β-amino ketones by threecomponent Mannich reaction[J].Chin Chem Lett,2010,21(1):31-34.
[7]Wang R,Li B G,Huang T K,et al.NbCl5-Catalyzed one-pot Mannich-type reaction:three component synthesis of β-amino carbonyl compounds[J].Tetrahedron Lett,2007,48(12):2071-2073.
[8]Zeng H Y,Li H,Shao H W.One-pot three-component Mannich-type reactions using sulfamic acid catalyst under ultrasound irradiation[J].Ultrasonics Sonochemistry,2009,16(6):758-762.
[9]Li J Z,Peng Y Q,Song G H.Mannich reaction catalyzed by carboxyl-functionalized ionic liquid in aqueous media[J].Catal Lett,2005,102(3/4):159-162.
[10]王利民,韩建伟,盛佳,等.无溶剂条件下Yb(OTf)3催化的亚甲基化合物和醛的Knoevenagel反应[J].有机化学,2005,25(5):591-595.
[11]Chang C T,Liao B S,Liu S T.Mannich-type reactions in a colloidal solution formed by sodium tetrakis(3,5-trifluoromethylphenyl)borate as a catalyst in water[J].Tetrahedron Lett,2006,47(52):9257-9259.
[12]Shen W,Wang L M,Tian H J.Quaternary ammonium salt gemini surfactants containing perfluoroalkyl tails catalyzed onepot Mannich reactions in aqueous media[J].Fluorine Chem,2008,129(4):267-273.
[13]杨水金,喻莉,王雨飞,等.H4SiW6Mo6O40/SiO2在H2O2催化氧化环己酮合成己二酸中的应用[J].湖北大学学报:自然科学版,2013,35(1):123-127.
[14]王恩波,胡长文,许林.多酸化学导论[M].北京:化学工业出版社,1998:1-204.
[15]邢烨.杂多酸催化有机反应的研究[D].乌鲁木齐:新疆大学,2008:8-9.
[16]张富民.杂多化合物催化剂的制备及其催化性能[D].南京:南京工业大学,2006:19-20.
[17]许林,胡长文,王恩波.杂多酸型催化剂的研究进展[J].石油化工,1997,26(9):632-638.
[18]李瑞波,徐贵潭.杂多酸催化剂应用研究进展[J].牡丹江师范学院学报,2007,59(3):25-27.
[19]韩波,祁国庆,魏清渤,等.Keggin型硅钨酸高效催化一锅法合成β-氨基酮衍生物[J].化学试剂,2012,34(8):753-755.
[20]王敏,梁艳,宋志国,等.温和条件下对甲基苯磺酸铝高效催化一锅法合成β-氨基酮衍生物[J].有机化学,2010,30(2): 295-298.
[21]张豪,黄云云,赵尖斌,等.三氟甲磺酸铜催化的Mannich反应合成β-氨基酮的研究[J].广东化工,2012,39(12):59-60.
[22]吴璇,李维思,李振江.氨基磺酸催化的Mannich反应合成β-氨基酮[J].化学试剂,2008,30(4):277-279.
[23]宋志国,梁艳,王敏.苯磺酸铝催化苯乙酮、芳香醛和芳香胺合成β-氨基酮衍生物[J].化学研究与应用,2010,22(11): 1462-1466.
[24]Manoj B G,Paula S B,Alexandre V,et al.A facile synthesis of cysteine-ferrite magnetic nanoparticles for application in multicomponent reactions-a sustainable protocol[J].RSC Advances,2012,2(15):6144-6149.
[25]Hanzlik R P,Leinwetter M.Reactions of epoxides and carbonyl compounds catalyzed by anhydrous copper sulfate[J].J Org Chem,1978,43(3):438-440.
[26]吕宝兰,付德英,杨水金.分子筛MCM-48负载磷钨酸催化合成苯甲醛乙二醇缩醛[J].湖北师范学院学报,2010,30 (2):9-13.
[27]Najmodin A,Lalleh T,Mohammad R S.Highly efficient one-pot three-component Mannich reaction in water catalyzed by heteropoly acids[J].Organic Letters,2006,8(10):2079-2082.
[28]Matsshita Y,Yasuda S.Reactivity of a condensed-type lignin model compound in the Mannich reaction and preparation of cationic surfactant from sulfuric acid lignin[J].Journal of Wood Science,2003,49:166.
[29]雷皇书,林晓梅,王宁,等.芳香胺的Mannich反应研究[J].西南师范大学学报,1995,20(1):44-48.
[30]陈君丽,解正峰,邢烨.水相中磷钨酸催化苯乙酮、芳香醛和芳香胺的Mannich反应[J].有机化学,2011,31(10):1714-1718.
(责任编辑 胡小洋)
Efficient one-pot synthesis of β-amino ketone derivatives catalyzed by H3PW12O40/SiO2
CHEN Huiyuan,XU Yulin,YE Hualin,YANG Shuijin
(College of Chemistry and Chemical Engineering,Hubei Normal University,Hubei Collaborative Innovation Center for Rare Metal Chemistry(Hubei Normal University),Huangshi 435002,China)
A new environmental friendly catalyst,H3PW12O40/SiO2was prepared by impregnation method. The catalyst exhibited excellent catalytic activities for the synthesisis of β-amino ketone derivatives via Mannich reaction of ketones,aromatic aldehydes and aromatic amines.The preparation conditions of the catalyst were conducted a comprehensive optimization.The effects of reaction on the yield of β-amino ketone were investigated and the optimum conditions were determined as follows:n(ketones)∶n(aromatic aldehydes)∶n (aromatic amines)=1.5∶1.2∶1.0,the mass ratio of the catalyst to total reactant was 8%,the reaction temperature was 20℃,and the reaction time was 9 h.The yield of the product was up to 61.2%77.0%.The results show that the reaction catalyzed by H3PW12O40/SiO2has advantages of mild reaction conditions,simple operation,easy isolation and the catalyst can be recycled.
H3PW12O40/SiO2;Mannich reaction;β-amino ketone;catalyst
TQ426.91
A
10.3969/j.issn.1000-2375.2015.05.018
1000-2375(2015)05-0492-06
投稿日期:2015-01-28
2013年国家级大学生创新创业训练计划项目(201313256001)和湖北师范学院本科生科研项目(2014ZD31)资助
陈慧媛(1993-),女,本科生;杨水金,通信作者,教授,E-mail:yangshuijin@163.com
