富锂锰基固溶体材料研究进展
2015-06-19许国峰王念贵樊勇利
许国峰,王念贵,樊勇利
(中国电子科技集团公司第十八研究所,天津300384)
富锂锰基固溶体材料研究进展
许国峰,王念贵,樊勇利
(中国电子科技集团公司第十八研究所,天津300384)
锰基固溶体材料是Li2MnO3和LiMO2复合结构的新型锂离子电池正极材料,具有比容量高、热稳定性好、电压高、能量密度大及对环境友好等优点,被视为下一代锂离子电池正极材料的理想之选。同时该材料存在首次效率低、倍率性能差、低温性能差等缺点,有许多新的合成方法和技术值得进一步探索,使其满足实用化要求。从结构、合成及改性等三方面综述了Li2MnO3·(1-)LiMO2的研究进展。
正极材料;层状固溶体;结构;合成方法;改性
在混合动力汽车和纯电动汽车中,动力电池是电动汽车的核心部件。动力电池主要包括铅酸电池、氢镍电池和锂离子电池。与铅酸电池和氢镍电池相比,锂离子电池有着比容量高、能量密度大、循环次数多、无环境污染等优点,将成为未来电动汽车使用的主要动力电池。智能手机、电动汽车以及电网储能对锂离子电池的比容量、能量密度和循环性能的要求越来越高。目前市场化的正极材料钴酸锂、锰酸锂、尖晶石结构锰酸锂、橄榄石结构磷酸铁锂以及镍钴酸锂等,均不能满足产品对高容量和低成本的要求。具有比容量高、热稳定性好、循环性能良好、充放电压范围宽且价格低廉、对环境友好等优点的富锂锰基电池材料吸引了国内外专家学者的深入研究。Li2MnO3·(1−)LiMO2因材料中含有大量的Mn元素,而Co元素相对较少,所以材料的价格较低,安全性相对较高,被视为下一代锂离子电池正极材料的理想之选。
1 结构
鉴于Li2MnO3与层状LiMO2晶体结构具有较好的兼容性,研究者一直致力于合成能够在结构上“匹配”的“层状-层状”Li2MnO3·(1−)LiMO2。合成的富锂材料Li2MnO3· (1−)LiMO2(0<<1,M=Mn、Co、Ni)含有两种组分Li2MnO3(也可表示为Li[Li1/3M2/3]O2)和LiMO2,可以看做是LiMO2和Li2MnO3按一定比例形成的固溶体化合物,或者说是LiMO2中的M部分取代了Li[Li1/3M2/3]O2中的Li+和Mn4+而形成的固溶体化合物。而Mn4+不变,主要起稳定晶体结构的作用。
Li2MnO3中的O与M层中的Li和Mn构成八面体结构,而锂层中的结构为四面体结构,Li2MnO3的电化学活性比较低,具有石盐结构,属于单斜晶系,空间群为C2/m,与α-NaFeO2层状结构相似。其中的Fe被Li及过渡金属离子(Ni、Co及Mn)取代,而Na被Li取代[1]。Li层与过渡金属层被紧密堆积的O原子层分开。α-NaFeO2层状结构的氧离子呈立方紧密堆积,大部分Li+占据四面体位构成Li层,仅有少部分Mn4+和Li+共同占据八面体位构成的M层,每个Li+被最近的6个Mn4+所包围形成局部团簇LiMn6的结构[2],属于六方晶系,R-3m空间群,Li占据3 a位,过渡金属占据3 b位,其中过渡金属Ni与Mn的化合价分别为+2与+4价[3]。Li2MnO3和LiMO2(M=Co,Ni,Mn)的层状结构如图1所示[4]。
2 合成
目前制备富锂固溶体多采用溶胶-凝胶法及共沉淀法等,利用增加廉价的锂和锰,形成富锂高锰型化合物,降低正极材料的制备成本,并达到改善正极材料电化学性能的目的。
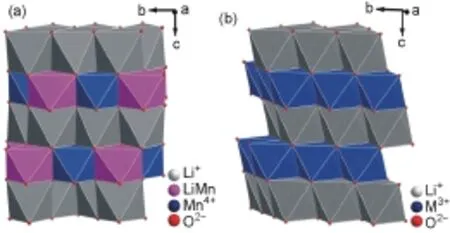
图1 Li2MnO3(a)和LiMO2(M=Co,Ni,Mn)(b)的层状结构
2.1 共沉淀法
共沉淀法是目前最常用的合成方法。简单来说就是先通过共沉淀得到氢氧化物共沉淀前驱体,然后将共沉淀前驱体与锂盐混合均匀,最后经过高温处理后制得产物。共沉淀法可使几种过渡金属离子在溶液中充分接触,基本上能达到原子级水平,使样品的形貌易于形成规则球形,粒径分布均匀,从而保证最终的产物电化学性能稳定。
Christopher S.Johnson等[5]利用共沉淀法,将Ni、Co、Mn的硝酸盐混合溶液缓慢滴加入LiOH溶液中,以NH4OH调节pH至11,在50℃下得到Ni、Co、Mn的混合氢氧化物沉淀,过滤干燥后,将混合氢氧化物与计量比的LiOH混合,首先在300~500℃下烧结3~6 h,随后在800~1 000℃下煅烧3~5 h。得到的Li2MnO3·(1-)LiMn0.333Ni0.333Co0.333O2(0臆臆0.7)当=0.3,在2.0~4.6 V,0.05 mA/cm3下,比容量达到250 mAh/g。Lee等[6]采用碳酸盐共沉淀法合成了前驱体(Ni0.25Mn0.75)CO3,将其与LiOH·H2O混合并在900℃下煅烧20 h得到Li-[Li0.2Ni0.2Mn0.6]O2。在20 mA/g、2.0~4.6 V下,电极材料首次放电比容量为265 mAh/g,经50次循环后保持在244 mAh/g左右。
尽管采用该方法可以获得容量较高的产品,但其控制参数较多,操作流程较长,因此在一定程度上限制了该材料的工业化生产。如果能在固相反应中通过恰当的手段使得上述三种金属元素也能达到较高水平的均匀混合,则可以大大简化工艺流程,降低成本,并同时提高操作的重复性。
2.2 固相合成法
固相法成本低,产率高,制备工艺简单,广泛用于粉体材料的制备,也常用于制备锂离子电池的正极材料。
Numata等[7]通过固相法将反应物锂、钴和锰的碳酸盐在900、1 000℃煅烧20 h得到Li2MnO3·(1−)LiCoO2,在1 mA/cm2、3.0~4.3 V、=0.1时,表现出较好的循环稳定性,比容量为140 mAh/g。Yu等用低温固相法制备了0.65 Li[Li1/3-Mn2/3]O2·0.35 Li(Ni1/3Co1/3Mn1/3)O2材料,在2.5~4.6 V范围以100 mA/g电流充放电,首次放电比容量为97 mAh/g,但是经25次循环后放电比容量可达到229 mAh/g,50次循环后放电比容量保持在216 mAh/g。Yu等还利用低热固相法制备锰基固溶体正极材料Li[Li0.167Mn0.583Ni0.25]O2,在2.5~4.6 V以100 mA/g进行充放电循环时,最高比容量可达234 mAh/g,且随着循环次数的增加,容量呈现上升的趋势[8]。
固相反应温度较高,烧结时间长,极易造成缺锂的现象,使化学计量偏移的程度加大;且固相反应受反应物固体比表面积、反应物间接触面、生成物相的成核速率以及通过生成物相的离子扩散速率等因素的影响,故合成材料的均一性较差,难以充分反应得到纯相。
2.3 溶胶-凝胶法
溶胶-凝胶法即将反应物溶解在水中,经一系列步骤先形成溶胶,通过蒸发等手段将溶胶转化成具有一定结构的凝胶。它具有反应温度低,可容纳不溶性组分或不沉淀性组分,反应易控制,合成的材料化学均匀性好、粒径分布窄、纯度高等优点,是制备富锂正极材料的重要方法。
S.H.Kang等[9]利用溶胶-凝胶法,以锂、镍、钴和锰的醋酸盐为原料,连续搅拌下加入乙醇酸,调节pH=7.5,在70~80℃下蒸发,直至得到粘性的透明胶体,将胶体在500℃下烘12 h,球磨后于900℃下烧结12 h。得到0.5 Li2MnO3·0.5 Li-(x=0,0.012,0.06,0.125,0.25和0.5),在0.1 mA/cm、2.0~4.6 V、=0.5时,首次放电比容量为208 mAh/g,30次循环后比容量为163 mAh/g。王绍等[10]以过渡金属乙酸盐和乙酸锂为原料,柠檬酸为螯合剂,通过溶胶-凝胶法结合高温煅烧法制备了锂离子电池富锂锰基正极材料Li2MnO3· (1-)Li[Ni1/3Mn1/3Co1/3]O2,结果表明:=0.5时,在900℃下煅烧12 h得到颗粒均匀细小的层状Li2MnO3·(1-)Li-[Ni1/3Mn1/3Co1/3]O2材料,并具有良好的电化学性能,在室温下以20 mA/g的电流密度充放电,2.0~4.8 V电位范围内首次放电比容量高达260 mAh/g,循环40次后放电比容量为244.7 mAh/g,容量保持率为94.12%。Kim等[11]以葡萄糖、PVA为溶胶-凝胶剂合成Li2MnO·3(1-)LiCoO2,电化学性能研究表明在100 mA/g、2.0~4.6 V时,Li[Li0.2Co0.4Mn0.4]O2经过50次循环之后的放电比容量为180 mAh/g,容量保持率高达94%。
3 改性
富锂型固溶体正极材料由于其较高的克容量备受关注。就目前而言,该材料仍存在一些不足:第一,富锂相材料在第一周循环中结构会有一个较明显的改变,在之后的循环过程中结构仍然在持续地变化[12-14];第二,富锂材料倍率性能差;从反应机理可以看出,在首次充电过程中,部分Li+以Li2O的形式脱出,但在放电过程中却不能重新嵌入,从而使不可逆容量增大,首次充放电效率降低[15];第三,高充电电压会引起电解液分解,使得电解液酸度提高,破坏材料表面,严重影响了材料本身的结构稳定性,使得循环性能不够理想。因此在实际使用中,需要对材料进行各种改性,以保持材料结构、容量、电压稳定,提高电极材料的电导率与离子扩散能力,减少材料本身与电解液的接触面积,抑制电极材料与电解液之间的副反应等。目前的改性方法主要有表面修饰、晶格掺杂、酸处理等。
3.1 表面修饰
为了提高循环过程中材料的稳定性,可以给材料包覆金属氧化物、氟化物和磷酸盐等,包覆在富锂锰基固溶体材料表面的过渡金属化合物本身大多是电化学惰性物质,能够有效减少活性物质与电解液的反应,抑制首次充电结束时氧空位的消失。同时,部分过渡金属离子在退火处理过程中还会进入母体材料的晶格,起到稳定结构的作用,从而提高循环过程中材料的稳定性。
邓胜男等[16]将制得的Li1.2Mn0.54Ni0.13Co0.13O2材料搅拌到硝酸铝溶液中,在连续搅拌、80℃水浴的情况下,将氟化铵溶液缓慢滴加到上述溶液中,蒸发水分,干燥后,在氮气气氛下的管式炉中400℃煅烧5 h,得到AlF3包覆的材料。当充放电倍率为28 mA/g时,首次放电比容量245 mAh/g,首次充放电效率为78%;当充放电倍率为566 mA/g时,首次放电比容量为159 mAh/g;循环50次后,放电比容量仍然达到141 mAh/g。Sun-Ho Kang等[17]采用溶胶-凝胶法合成了包覆LiNiPO4的0.5 Li2MnO3·0.5 LiNi0.44Co0.25Mn0.031O2材料,2.0~4.6 V,0.1 mA/cm2,首次放电比容量260 mAh/g。首次效率为87%,在充放电循环过程中,比容量稳定在250 mAh/g,1下比容量也可稳定在200 mAh/g,综合性能明显优于未包覆处理的材料。
一般认为通过表面包覆实现表面改性的作用是利用包覆材料电化学惰性物质对电解液中酸性物质的抗腐蚀作用,通过减小电解质与活性材料之间的接触面积,减少电解液对电极材料表面的腐蚀,抑制首次充电结束时氧空位的消失,提高了载流子的扩散速率,改善了电极材料倍率性能。并且部分过渡金属离子在退火处理过程中还会进入母体材料的晶格[18],起到稳定结构的作用,进而改善材料的电化学性能。
3.2 体相掺杂
唐爱东等[19]将适量的铬、锰和锂的硝酸盐按摩尔比溶于一定量的水中混合均匀,连续搅拌下加入柠檬酸,形成均匀透明的溶液,加热蒸发直至最终形成凝胶。将凝胶在120℃下烘干,得到前驱体,将前驱体放入微波马弗炉,于950℃恒温10 h,冷却得到目标产物。在25℃、2.5~4.5 V,14 mA/cm2进行恒流充放电测试发现,材料最高放电比容量可达22l mAh/g,循环10次后比容量为180 mAh/g。Park等[20]通过溶胶-凝胶法合成了掺铝的富锂材料(=0~0.1),分析表明Al掺杂提高了材料结构的稳定性,具有较高的放电比容量;当=0.06时,在2.5~4.6 V范围内、0.4 mA/cm2电流下,材料首次放电比容量达到210 mAh/g。Jiao等[21]亦用溶胶-凝胶法合成掺杂Cr的富锂材料经研究,掺杂Cr能降低富锂材料的电化学阻
抗,从而改善了富锂锰基正极材料的容量和倍率性能。
3.3 酸处理
富锂正极材料需要充电到高电压活化之后才可以获得高比容量,首次充电过程中的脱锂脱氧是一个不可逆过程,加上高电位下电解液与电极之间发生的副反应,对材料作酸处理,可以从Li2MnO3相中除去Li2O并同时活化Li2MnO3相,减小首次循环过程中不可逆容量损失。
Thackeray等研究发现,在1 mol/L的HNO3溶液中浸泡富锂正极材料可以将其首次库仑效率由82%提升到90%,但材料的循环性能变得更差。因为酸处理破坏了富锂材料的表面结构,导致循环性能变差。所以在实际应用中,表面酸处理并不是一种有效的改性方法。
3.4 其他改性
将富锂材料与缺锂的锂离子载体复合,复合后,那部分不可逆脱出的锂离子嵌入到这部分缺锂锂离子载体中,从而降低了不可逆容量。
Manthiram等[22]将富锂材料与V2O5、LiV3O8和Li4Mn5O12按一定比例混合得到复合材料,不仅可以将首次不可逆容量降低至零,还提高了材料的放电容量。Gao等[23]将Li[Li0.2-Mn0.54Ni0.13Co0.13]O2材料与不同比例的V2O5混合成复合材料,当混合物中的V2O5含量达到11%(质量分数)时,首次不可逆容量基本不损失,并且首次放电比容量达到300 mAh/g,在0.05、25次循环后比容量为220 mAh/g。
4 总结与展望
层状锰系衍生物具有合成简单、成本低、电化学性能好等优点,其中富锂锰基固溶体材料有可能成为未来电动汽车用的新型高比能锂离子电池正极材料。如果能解决其大电流充放电能力、结构稳定性、首次不可逆容量以及电解液侵蚀等问题,寻求适合商业生产的合成方法,层状富锂锰基固溶体必将使锂离子电池的发展跨入一个新的时代。
[1]KOYAMA Y,TANAKA I,NAGAO M,et al.First-principles study on lithium removal from Li2MnO3[J].Journal of Power Sources, 2009,189(1):798-801.
[2]LU Z,BEAULIEU L Y,DONABERGER R A,et al.Synthesis,structure,and electrochemical behavior of Li[Ni Li1/3-2x/3Mn2/3-x/3]O2[J]. Journal of the Electrochemical Society,2002,149(6):A778-A791.
[3]SHAJU K M,SUBBA R G V,CHOWDARI B V R.Performance of layered Li(Nil/3Col/3M n1/3)O2as cathode for Li-ion batteries[J].Electrochim Acta,2002,48:145-151.
[4]THACKERAY M M,KANG S H,JOHNSON C S,et al.Li2MnO3-stabilized LiMO2(M=Mn,Ni,Co)electrodes for lithium-ion batteries[J].J Mater Chem,2007,17:3112-3125.
[5]JOHNSON C S,LI N C,LEFIEF C,et al.Synthesis,characterization and electrochemistry of lithium battery electrodes:Li2MnO3· (1-)LiMn0.333Ni0.333Co0.333O2(0臆臆0.7)[J].Chem Mater,2008,20: 6095-6106.
[6]LEE D K,PARK S H,AMINEB K,et al.High capacity Li[Li0.2Ni0.2-Mn0.6]O2cathode materials via a carbonate co-precipitation method [J].Journal of Power Sources,2006,162(2):1346-1350.
[7]NUMATA K,SAKAKI C,YAMANAKA S.Synthesis and characterization of layer structured solid solutions in the system of Li-CoO2-Li2MnO3[J].Solid State Ionics,1999,117(3/4):257-263.
[8]于凌燕,仇卫华,连芳,等.锂离子电池正极材料Li[Li0.167Mn0.583-Ni0.25]O2的合成与性能研究[J].电化学,2008,14(2):135-139.
[9]KANG S H,KEMPGENS P,GREENBAUM S,et al.Interpreting the structural and electrochemical complexity of 0.5 Li2MnO3· 0.5 LiMO2electrodes for lithium batteries(M=Mn0.5-Ni0.5-Co2x,0臆臆0.5)[J].J Mater Chem,2007,17:2069-2077.
[10]王昭,吴锋,苏岳锋,等.锂离子电池正极材料Li2MnO3·(1-)Li-[Ni1/3Mn1/3Co1/3]O2的制备及表征[J].Acta Phys Chim Sin,2012, 28(4):823-830.
[11]KIM J M,TSURUTA S,KUMAGAI N.Electrochemcial properties of Li[Co Li(1/3-/3)Mn(2/3-2/3)]O2(0臆臆1)solid solutions prepared by poly-vinyl alcohol(PVA)method[J].Electrochem Commun,2007,9(1):103-108.
[12]GU M,BELHAROUAK I,ZHENG J,et al.Formation of the spinel phase in the layered composite cathode used in Li-ion batteries[J]. ACS Nano,2013,7(1):760-767.
[13]JOHNSON C S,LI N,LEFIEF C,et al.Synthesis,characterization andelectrochemistry of lithium battery electrodes:Li2MnO3· (1-)LiMn0.333Ni0.333Co0.333O2(0臆臆0.7)[J].Chemistry of Materials,2008,20:6095-6106.
[14]GU M,GENG A,BELHAROUAK I,et al.Nanoscale phase separation cation ordering,and surface oxygen vacancy formation in pristine Li1.2Ni0.2Mn0.6O2for Li-ion batteries[J].Chem Mater,2013,25 (11):2319-2326.
[15]KIKKAWA J,AKITA T,TABUCHI M.Real-space observation of Li extraction/insertion in Li1.2Mn0.4Fe0.4O2positive electrode material for Li-ion batteries[J].Electrochem Solid-State Lett,2008,11: A183-A186
[16]邓胜男,施志聪,郑隽,等.正极材料Li1.2Mn0.54Ni0.13Co0.13O2的表面包覆改性研究[J].电源技术,2012,36:4.
[17]KANG S H,THACKERAY M M.Enhancing the rate capability of high capacity xLi2MnO3·(1-)LiMO2(M=Mn,Ni,Co)electrodes by Li-Ni-PO4treatment[J].Electrochemistry Communications,2009(11):748-75l.
[18]吴晓彪,董志鑫,郑建明,等.锂离子电池正极材料Li[Li0.2Mn0.54-Ni0.13Co0.13]O2的碳包覆研究[J].厦门大学学报,2008,47(增刊):224-227.
[19]唐爱东,黄可龙.掺铬层状锰酸锂衍生物的制备与表征[C]//中国储能电池与动力电池及其关键材料研讨会论文集.长沙:中国储能电池与动力电池及其关键材料研讨会,2005.
[20]PARK S H,SUN Y K.Synthesis and electrochemical properties of layered Li[Li0.15Ni(0.275–x/2)AlxMn(0.575–x/2)]O2materials prepared by sol-gel method[J].J Power Sources,2003,119/121:161-165.
[21]JIAO L F,ZHANG M,YUAN H T,et al.Effect of Cr doping on the structural,electrochemical properties of Li[Li0.2Ni0.2-x/2Mn0.6-x/2-Crx]Ox(=0,0.02,0.04,0.06,0.08)as cathode materials for lithium secondary batteries[J].J Power Sources,2007,167(1):178-184.
[22]GAO J,KIM J,MANTHIRAM A.Eliminating the irreversible capacity loss of high capacity layered Li[Li0.2Mn0.54Ni0.13Co0.13]O2cathode by blending with other lithium insertion hosts[J].J Power Sources,2009,191(2):644-647.
[23]GAO J,KIM J,MANTHIRAM A,et al.High capacity Li[Li0.2Mn0.54-Ni0.13Co0.13]O2-V2O5composite cathodes with low irreversible capacity loss for lithium ion batteries[J].Electrochem Commun, 2009,11(1):84-86.
Research progress of Li-rich Mn-based layed solid-solution series cathode material
XU Guo-feng,WANG Nian-gui,FAN Yong-li
The solution material was a novel Li-ion battery anode material based on the composite structure between Li2MnO3and LiMO2.High capacity,good thermal stability,high voltage,high energy density,eco-friendliness and low cost were its advantages.It was regarded as the ideal of the next generation of lithium ion battery anode materials. But there were some shortcomings of the materials,such as lower first discharge efficient,worse rate property and low temperature property.Some new synthesis methods and technology were needed to be improved to meet the requirementsofpracticalapplication.Thestructure,synthesisandimprovementofperformanceofthe Li2MnO3·(1-)LiMO2were reviewed.
cathode materials;layed solid-solution;structure;synthesis mechanism;improvement of performance
TM 912
A
1002-087 X(2015)03-0620-04
2014-09-28
许国峰(1981—),男,安徽省人,学士,主要研究方向为锂离子电池正极材料。
