N-乙酰基神经氨酸标准物质的研制*
2015-06-15李莹席兴军周晓晶初侨林楠王尉张经华
李莹,席兴军,周晓晶,初侨,林楠,王尉,张经华,
(1.北京工业大学生命科学与生物工程学院,北京 100124;2.北京市理化分析测试中心,有机材料检测技术与质量评价北京市重点实验室,北京 100089; 3.中国标准化研究院,北京 100191)
N-乙酰基神经氨酸标准物质的研制*
李莹1,席兴军3,周晓晶2,初侨3,林楠2,王尉2,张经华1,2
(1.北京工业大学生命科学与生物工程学院,北京 100124;2.北京市理化分析测试中心,有机材料检测技术与质量评价北京市重点实验室,北京 100089; 3.中国标准化研究院,北京 100191)
采用半制备液相色谱法制备N-乙酰基神经氨酸标准物质。分别以UV,IR,MS和NMR方法对N-乙酰基神经氨酸标准物质进行定性分析,以高效液相色谱方法进行均匀性检验和稳定性检验,经F检验表明在置信区间为95%的范围内测定结果稳定。与国内8家资质合格的实验室进行联合定值,计算出不确定度结果。N-乙酰基神经氨酸标准物质的定值结果为98.63%,置信水平为95%时的扩展不确定度为0.098 6%(k=2)。该N-乙酰基神经氨酸标准物质可用于有关食品检测方法的校正。
N-乙酰基神经氨酸;标准物质;均匀性;稳定性;不确定度
N-乙酰基神经氨酸(N-acetylneuraminic acid,NANA,结构式见图1)是唾液酸家族中最常见的一种[1]。
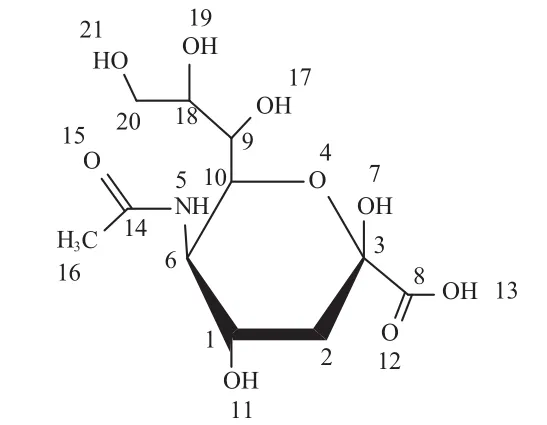
图1 N-乙酰基神经氨酸结构式
唾液酸是一族神经氨酸的氮或氧基取代的衍生物,是一个含有9个碳原子并具有吡喃糖结构的酸性氨基糖,系统命名为5-氨基-3,5-二脱氧-D-甘油-D-半乳壬酮糖。5号碳上不同的连接基团构成了不同的唾液酸衍生物,最主要的两种唾液酸为5-乙酰氨基-3,5-二脱氧-D-甘油-D-半乳壬酮糖(N-乙酰神经氨酸)和3-脱氧-D-甘油-D-半乳壬酮糖(KDN),其它唾液酸均由这两种衍生而成[2-5]。
唾液酸广泛存在于动物组织和体液中[6],是糖蛋白、低聚糖和糖脂的重要成分。N-乙酰基神经氨酸能使唾液产生光滑的感觉,通过改变粘液的流体阻力充当免疫调节剂,以及在大脑和神经系统的产生和发育中发挥非常重要的作用[7]。此外,N-乙酰基神经氨酸是一种天然的营养成分,在燕窝[8-9]、鹿茸[10]、鸡蛋[11-12]、奶粉[13-14]等食品中含量较高,且已经作为一种营养辅助剂加入到婴幼儿配方奶粉中。经查新,国内外未发现N-乙酰基神经氨酸标准物质,为了满足相关产品分析检测、质量控制工作的需求,保证检测结果的准确性、可比性和溯源性,结合标准物质的国际发展趋势[15],笔者制备了N-乙酰基神经氨酸标准物质。
1 实验部分
1.1 主要仪器与试剂
半制备高效液相色谱系统:LC-6AD型,日本岛津公司;
高效液相色谱仪:LC-20A型,日本岛津公司;
旋转蒸发仪:EYELA-OSB-2100型,东京理化器械株式会社;
冷冻干燥机:ALPHR1-2 LD plus型,德国CHRIST公司;
紫外可见分光光度计:UV-1800型,日本岛津公司;
傅立叶变换红外-近红外光谱仪:Spectrum 400型,美国珀金-埃尔默公司;
核磁共振谱仪:Bruker 400 MHz,德国Bruker公司;
超高分辨飞行时间质谱仪:UHR-TOFmaXis 4G型,德国Bruker公司;
甲醇:色谱纯,美国Thermo Fisher公司;
超纯水:默克密理博Milli-Q Integral 3纯水机生产。
1.2 半制备色谱条件
色谱柱:SHIM-PACK PREP-ODS(H)·KIT柱(250 mm×20 mm,5 μm);流动相:乙腈-0.1%磷酸(1∶9);流量:7 mL/min;柱温:30℃;运行时间:11 min;检测波长:203 nm。
1.3 标准物质样品制备
取N-乙酰基神经氨酸粗提品适量溶解于超纯水溶剂中,充分溶解后经半制备液相色谱系统分离纯化,收集目标峰馏分,进行旋蒸后冷冻干燥,最终获得纯度大于98%的高纯度化合物。经定性分析后,分装在干净、干燥的2 mL棕色样品瓶中,于4℃冷藏。
1.4 定性分析方法
经紫外光谱、红外光谱、质谱和核磁共振波谱分析,对N-乙酰基神经氨酸进行定性。
紫外光谱测定使用紫外-可见分光光度计,以乙腈为背景溶剂,于0~400 nm下波长扫描,得到紫外光谱图。
红外光谱测定使用傅立叶变换红外-近红外光谱仪,采用KBr压片法得到红外光谱图。
质谱测定使用超高分辨飞行时间质谱仪,在正、负离子模式下测定,扫描范围(m/z):100~1 000。
核磁共振波谱测定使用400 MHz核磁共振谱仪,氘代试剂为DMSO-d6(含TMS),25℃条件下得到氢谱和碳谱。
1.5 纯度定值分析方法
采用高效液相色谱技术测定标准物质纯度,并通过8家实验室协作对本标准物质进行定值。从不同HPLC洗脱条件、不同色谱柱等多方面对所制备样品的纯度进行定值。
1.5.1 不同色谱柱条件
采用两根C18色谱柱Waters XTerraRP C18柱(150 mm×4.6 mm,5 μm)和Waters Atlantis HILIC Silica柱(150 mm×4.6 mm,5 μm),在相同的流动相、不同流动相配比的条件下测定N-乙酰基神经氨酸标准物质纯度。
(1)Waters XTerra RP C18柱的色谱条件
流动相:乙腈-0.1%磷酸(1∶9),流量为1.0 mL/min;柱温:30℃;运行时间:20 min;检测波长:203 nm。
(2)Waters Atlantis HILIC Silica柱的色谱条件
流动相:乙腈-0.1%磷酸(95∶5),流量为1.0 mL/min;柱温:25℃;运行时间:20 min;检测波长:203 nm。
1.5.2 不同流动相条件
流动相:甲醇-0.1%磷酸(8∶2)与乙腈-0.1%磷酸(95∶5),流量均为1.0 mL/min;柱温:30℃;运行时间:20 min;检测波长:203 nm。
1.5.3 定值色谱条件
色 谱 柱:Waters Atlantis HILIC Silica柱(150 mm×4.6 mm,5 μm);流动相:乙腈-0.1%磷酸(95∶5),流量为1 mL/min;柱温:25℃;运行时间:20 min;检测波长:203 nm。
此方法为最终定值确定方法,为了保证定值结果的准确度,8家定值单位均采用此方法进行定值。
2 结果与讨论
2.1 定性分析
分别采用UV,IR,MS和NMR方法对N-乙酰基神经氨酸进行定性。
UV(CH3OH):波长为203 nm,谱图见图2;MS:m/z310.1129[ M+H]+,谱图见图3;308.0992[M-H]+,谱图见图4。1HNMR(400 MHz,DMSO-d6):δ1.70(t,J=11.8 Hz,1H,3-H),1.89(s,3H,12-H),1.99(q,J=4.9 Hz,1H,3'-H),3.18(d,J=1.0 Hz,1H,10-H),3.29(dd,J=10.9 Hz,J=6.8 Hz,1H,15-H),3.50(ddd,J=2.2 Hz,J=6.8 Hz,J=9.0 Hz,1H,14-H),3.51(d,J=8.4 Hz,1H,1-H),3.61(dd,J=10.9 Hz,J=2.2 Hz,1H,15'-H),3.74(dd,J=10.6 Hz,J=1.0 Hz,1H,6-H),3.83(dd,J=4.9 Hz,J=11.8 Hz,1H,2-H),8.04(d,J=8.4 Hz,1H,9-H)谱图见图5;13CNMR(400 MHz,DMSO-d6):δ53.50,66.19,39.97,95.13,70.82,171.76,69.64,172.26,23.04,70.29,64.09,谱图见图6;IR(KBr压片)波数(cm-1):3 339(νN-H),2 933 (ν-C-H),1 722(νC=O),1 654(νC=O酰 胺 ),1 122(νC-O-C),1 024(νC-O),谱图见图7。

图2 紫外光谱图

图3 正离子模式质谱图

图4 负离子模式质谱图
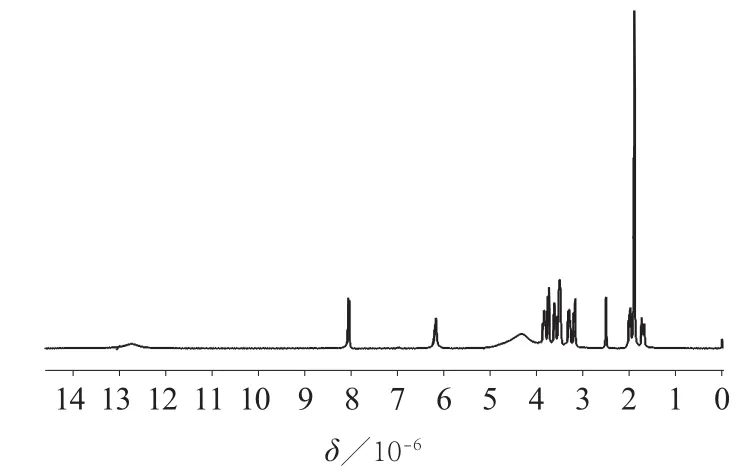
图5 N-乙酰基神经氨酸核磁共振氢谱图
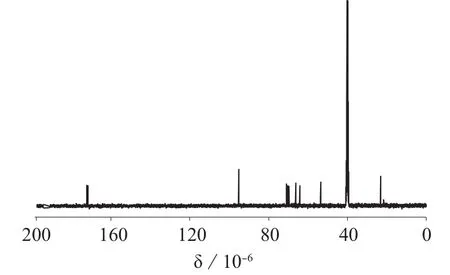
图6 N-乙酰基神经氨酸核磁共振碳谱图

图7 N-乙酰基神经氨酸红外光谱图
综合文献数据及与数据库对比[16],确定本样品为N-乙酰基神经氨酸。
2.2 定值方法
2.2.1 检测波长的确定
采用高效液相色谱配备检测器为SPD-M20A二极管阵列检测器,进行全波长扫描后生成三维光谱图见图8,根据三维光谱图确定N-乙酰基神经氨酸的最佳吸收波长。由图8可知,N-乙酰基神经氨酸的最佳检测波长为203 nm。

图8 N-乙酰基神经氨酸标准物质三维图谱
2.2.2 色谱柱选择
分 别 选 择 Waters XTerra RP C18柱 (150 mm×4.6 mm,5 μm)和Waters Atlantis HILIC Silica柱(150 mm×4.6 mm,5 μm)进行比较,C18柱对N-乙酰基神经氨酸的保留效果较差,而HILIC Silica亲水色谱柱对N-乙酰基神经氨酸的保留效果较好,最终选择规格为150 mm的HILIC Silica色谱柱作为定量分析色谱柱。
2.2.3 流动相选择
选用甲醇-0.1%磷酸、乙腈-0.1%磷酸两组流动相进行比较,试验结果表明,甲醇-0.1%磷酸流动相对N-乙酰基神经氨酸的分离效果较差;乙腈-0.1%磷酸水流动相的分离效果较好,峰型理想,故选择乙腈-0.1%磷酸(95∶5)作为定值实验流动相。
2.2.4 检测器比较
对岛津蒸发光散射检测器ELSD-LTⅡ和岛津二极管阵列检测器(DAD)进行比较,结果表明,二极管阵列检测器信号响应较好,且为实验室常用检测器,最终确定检测器为二极管阵列检测器。
2.3 均匀性检验
根据JJG 1343-2012《 标准物质定值的通用原则及统计学原理的要求》[17],对标准物质进行均匀性检验。采用的是随机顺序重复测量的方法,从分装后200瓶样品中随机抽取20瓶样品。抽取的样品瓶号按照正序、倒序、乱序的方式测量3次,结果见表1、表2。
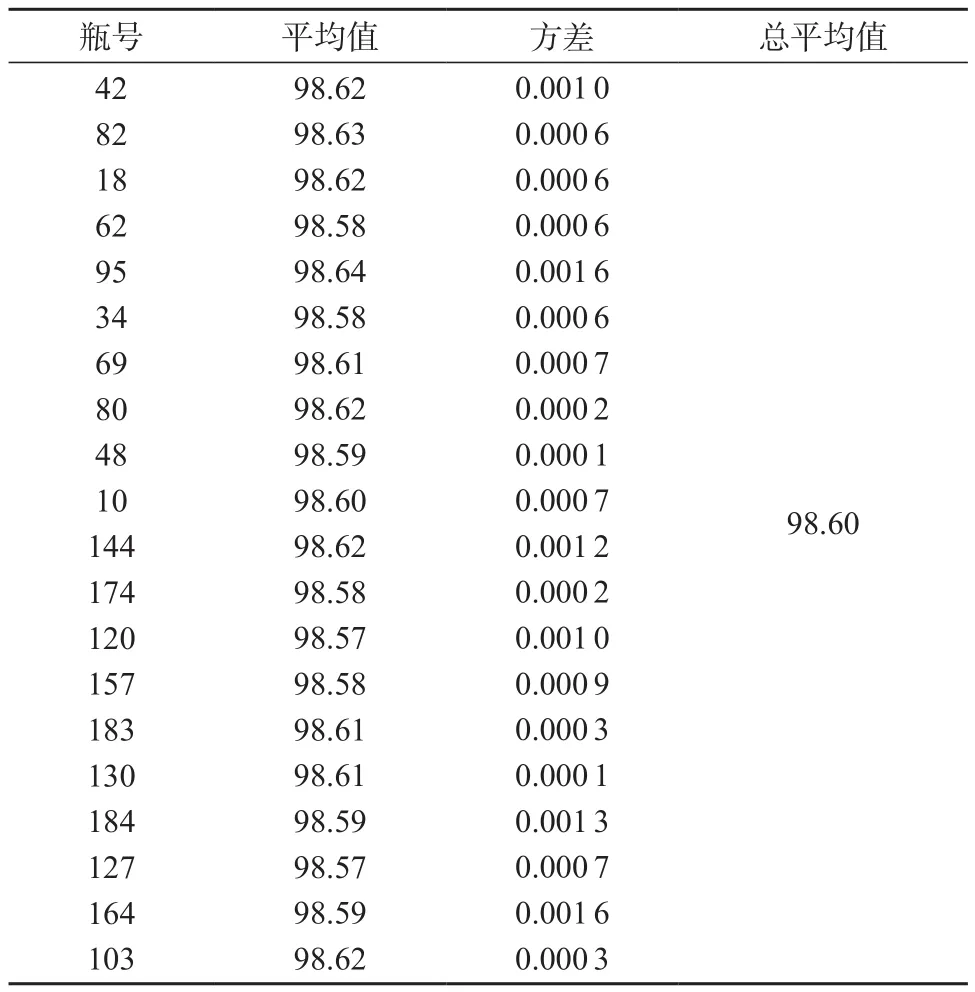
表1 N-乙酰基神经氨酸均匀性检验的测量数据(n=3) %

表2 N-乙酰基神经氨酸均匀性研究方差分析结果
查F临界值表,得F0.05(19,40)=2.03,计算得F=MS瓶间/MS瓶内=1.99<F0.05(19,40),表明本标准物质是均匀的。
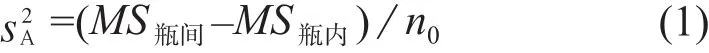
式中:n0=3。
瓶间标准偏差sbb是该方差的平方根:sbb=sA=0.015 5。
重复性标准偏差sr由MS瓶内开平方求得,sr=0.027。
2.4 稳定性考察
标准物质的稳定性考察按先密后疏的原则,分别在第0,1,3,6个月进行稳定性检测。笔者以6个月为期,对制备的N-乙酰基神经氨酸标准物质在不同时间段条件下进行稳定性试验,结果见表3。
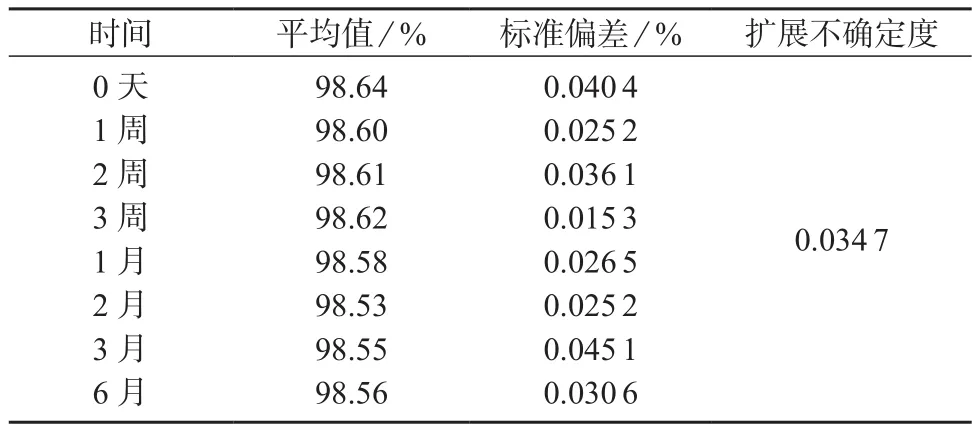
表3 N-乙酰基神经氨酸稳定性检验结果
通过对表3数据进行分析,采用直线作为经验模型,观察斜率值是否有显著变化,以此对标准物质的稳定性变化进行预测。斜率β1按式(2)计算:

式中:β1——回归系数,即直线斜率;
xi——第i个时间点;
yi——第i个时间点的检测值;
n——稳定性测量次数,n=8。
直线上某点的标准偏差:
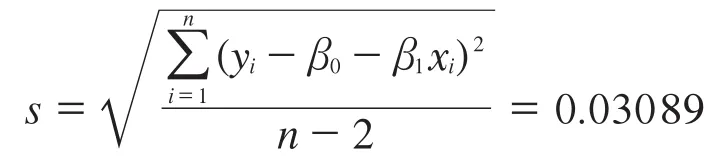
与斜率相关的不确定度s(β1):

自由度为n-2,P=0.95(95%置信水平)的分布因子t=2.441,由于|β1|<t0.95,n-2·s(β1),故斜率是不显著的,因而未观测到该样品的不稳定性。6个月(T=6)的长期稳定性的不确定度:us=s(β1)·T=0.034 7%。
上述结果表明N-乙酰基神经氨酸标准物质在6个月内未观测到明显的不稳定性。更长时间的稳定期将根据持续不断的检测结果进行确定。
2.5 定值结果
本标准物质定值按照JJG 1343-2012 标准要求,通过多个实验室协作实验定值,参加定值的实验室有8家,每个实验室测定2个单元,每个单元测量3次,提供6次独立重复测量数据。所有实验室选择方法是经过多次试验总结的方法,且各个实验室实验方法一致。定值数据及其方差分析结果分别见表4、表5。
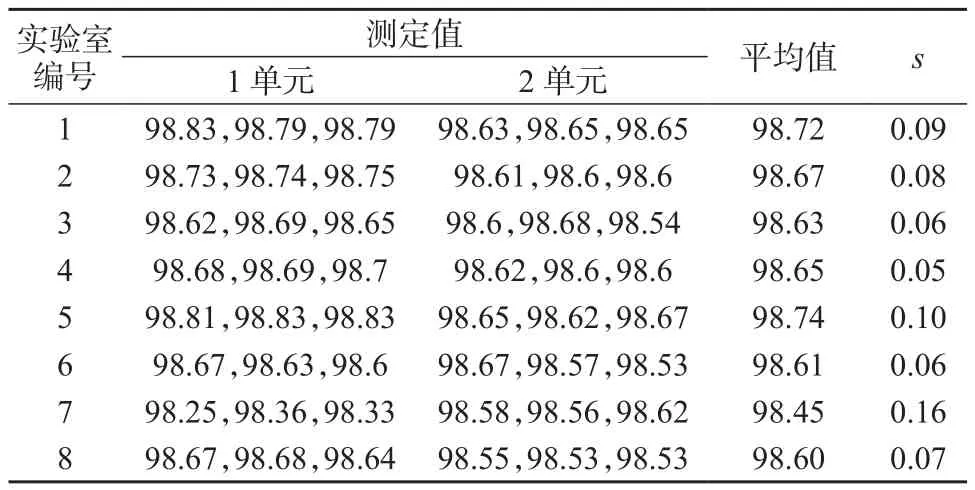
表4 N-乙酰基神经氨酸HPLC纯度定值结果 %


式中:sL2——每次测量瓶内方差,;
m——参加实验室数目;
sr2——m次测量瓶间方差,sr2=s22;
n——定值实验室测量结果数目。
2.6 不确定度评定结果
不确定度由三部分组成:标准物质的不均匀性引入的不确定度;标准物质的不稳定性引入的不确定度;标准物质的定值过程引入的不确定度。
均匀性引入的不确定度ubb=sbb=0.015 5%。
稳定性引入的不确定度:本标准物质稳定性研究时间为6个月,故其不确定度us=s(β1)·T=0.034 7%。
合成标准不确定度u:
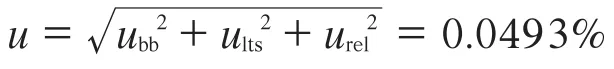
扩展不确定度U=ku=0.098 6%,k=2。
2.7 定值结果表达
N-乙酰基神经氨酸纯度标准物质定值结果为98.63%,扩展不确定度为0.098 6%(k=2)。
3 结论
研制了N-乙酰基神经氨酸标准物质,采用波谱法进行定性分析,采用液相色谱法进行均匀性检验及稳定性考察,考察结果根据统计学方法进行判定,符合标准物质均匀性与稳定性的要求。对定值结果的不确定度进行了评定,确保用户在不同时间、不同空间,使用不同包装的该种标准物质时,所使用的量值及不确定度准确可靠,对于N-乙酰基神经氨酸的准确测定具有重要意义。该标准物质可满足含有N-乙酰基神经氨酸相关食品的分析检测、质量控制工作的需求,为其检测结果的准确性、可比性和溯源性提供技术支撑和量值溯源保证。
[1] Juneja L R,Koketsu M,Nishimoto K,et al. Large-scale preparation of sialic acid from chalaza and egg-yolk membrane[J]. Carbohydr Res,1991,214(1): 179-186.
[2] Yeşilyurt B,şahar U,Deveci R. Determination of the type and quantity of sialic acid in the egg jelly coat of the sea urchin paracentrotus lividus using capillary LC-ESI-MS/MS[J]. Molecular Reproduction and Development,2015,82(2): 115-122.
[3] Wang Q,Wang B,Ma M,et al. A Sensitive and selective fluorimetric method of quick determination of sialic acids in egg products by lectin-CdTe quantum dots as manoprobe[J]. Journal of Food Science,2014,79(12): C2434-C2440.
[4] Aminoff D. Methods for the Quantitative estimation ofN-acetylneuraminic acid and their application to hydrolysates of sialomucoids[J]. Biochem J,1961,81: 384-392.
[5] Schauer R,Kamerling J P. Chapter 11-chemistry,biochemistry and biology of sialic acids[J]. New Comprehensive Biochemistry,J Montreuil J F G V,Elsevier,1997,29,Part B: 243-402.
[6] Fernando S F,Woonton B W. Quantitation ofN-acetylneuraminic (sialic) acid in bovine glycomacropeptide (GMP)[J]. Journal ofFood Composition and Analysis,2010,23(4): 359-366.
[7] Tao F,Zhang Y,Ma C,et al. Biotechnological production and applications ofN-acetyl-d-neuraminic acid:current state and perspectives[J]. Applied Microbiology and Biotechnology,2010,87(4): 1 281-1 289.
[8] 侯向昶,朱丽萍,刘春生,等.超高效液相色谱-串联质谱法测定燕窝中唾液酸的含量[J].现代食品科技,2013(7): 1 706-1 709.
[9] 靳颖华.液相色谱法测定燕窝中唾液酸含量研究[J].中国医药导刊,2011(6): 1 071-1 072.
[10] 吕秀琇,李刚,薛冬桦,等.液相色谱法测定鹿茸中唾液酸含量[J].食品科学,2010(12): 215-218.
[11] 张昂,陆启玉,王留留.鸡蛋中唾液酸含量的测定[J].农产品加工(学刊),2010(4): 69-70.
[12] Li H,Fan X. Quantitative analysis of sialic acids in Chinese conventional foods by HPLC-FLD[J]. Open Journal of Preventive Medicine,2014,4(2): 57-63.
[13] 解鸿蕾,李春,刘宁.超高效液相色谱-串联四极杆质谱法分析婴儿乳粉中的唾液酸[J].色谱,2013,31(8): 781-785.
[14] 冯君,李宏基,韩立强,等.高效液相色谱法测定奶粉中唾液酸的含量[J].中国乳品工业,2008(6): 62-64.
[15] 张庆合,卢晓华,阚莹,等.化学测量相关领域标准物质现状与趋势[J].化学试剂,2013,35(10): 865-870.
[16] Klepach T,Zhang W,Carmichael I,et al.13C-1H and13C-13C NMR j-couplings in13C-labeledN-acetyl-neuraminic acid: correlations with molecular structure[J]. The Journal of Organic Chemistry,2008,73(12): 4 376-4 387.
[17] JJF 1343-2012 标准物质标准样品定值的一般原则和统计方法[S].
英科学家开发新技术用蜜蜂检测空气污染状况
据英国《每日电讯报》报道,不久前,英国科学家们开发出环境检测新技术,利用附着在蜜蜂身上的颗粒物来检测空气质量,其原理是根据蜜蜂身上附着的污染颗粒物,寻找这些粒子的源头,这样大大缩小了污染源存在的可能范围。
英国自然博物馆一项最新研究发现,蜜蜂的身体和翅膀上有较强的静电,因此他们能吸附各种微小的环境污染颗粒物。利用这一发现,科学家们开始利用蜜蜂检测空气污染状况。
传统的空气质量观测站只能固定地观测附近空气中微粒的数量。与此相反,一只蜜蜂每天能绕着蜂巢在四周飞行大约2 500 m。也就是说,空气质量观测者能通过观察附着在蜜蜂身上的颗粒物,获得方圆2 500 m内污染颗粒物种类的数据。确定了空气中污染物的种类,科学家就能从污染物出发,再进一步缩小污染源可能存在的范围。
(中国分析计量网)
石墨烯传感器可让小分子“现形”
尽管科学家因为石墨烯无与伦比的属性而对其青睐有加,但迄今为止,其实际应用仍然乏善可陈。不过,瑞士洛桑联邦理工学院(EPFL)生物纳米系统实验室和西班牙光子科学研究所的科学家们在最新一期的《科学》杂志上宣称,他们利用石墨烯独特的光学和电子学属性,研制出了一种具有超高灵敏度的分子传感器,可以探测蛋白质或药物小分子的详细信息。
在红外吸收光谱学这种标准的探测方法中,光被用来激活分子。不同分子的振动不同,借由这种振动,分子会显示其存在甚至表现自己的“性格”。这些“蛛丝马迹”可在反射光中“读出”。但在探测纳米大小的分子时,这一方法的表现差强人意。因为照射分子的红外光子的波长约为6 μm,而目标分子仅几个纳米,很难在反射光中探测到如此微小分子的振动。
于是石墨烯受命于危难之间。研究合作者丹尼尔·罗德里戈解释道,如果让石墨烯拥有合适的几何形状,就能将光聚焦在其表面上的某个特定点上,并“倾听”附着其上的纳米分子的振动。他说:“通过使用电子束轰击并使用氧离子蚀刻,使石墨烯表面形成一些纳米结构。当光到达时,纳米结构内的电子会振荡,产生的‘局域表面等离子体共振’可将光聚集在某个点上,与目标分子的尺度相当,因此能探测纳米大小的结构。”
除此之外,这一过程也能揭示组成分子的原子键的属性。研究人员称,当分子振动时,连接不同原子的原子键会产生多种振动,不同振动之间的细微差别可提供与每个键的属性以及整个分子的健康状况有关的信息。为了找出每个原子键发出的“声音”从而确定所有的频率,需要用到石墨烯。在实验中,研究人员对石墨烯施加不同的电压,让其“调谐”到不同的频率,从而能“阅读”其表面上的分子所有振动情况,而使用目前的传感器无法做到这一点。研究人员海蒂斯·奥特格说:“我们让蛋白质附着在石墨烯上,并用这一方法,得到了分子全方位的信息。”
(分析仪器网)
国家煤化工产品质量监督检验中心成立
从国家认监委官网获悉,新疆维吾尔自治区质监局依托自治区产品质量监督检验研究院筹建的“国家煤化工产品质量监督检验中心(新疆)”已按要求通过了国家认监委组织的“三合一”评审和授权,并经质检总局组织的专家组验收合格,分级评定为B级。国家质检总局、国家认监委批准国家煤化工产品质量监督检验中心(新疆)正式成立。
近年来,新疆自治区产品质量监督检验研究院能源、煤化工产品质量检验技术发展迅速,人员、设备及检测检测量增加迅速,在自治区质监局领导的指示和相关处室指导帮助下,经过中心全体人员一年多的辛勤努力,国家煤化工产品质量监督检验中心(新疆)终于正式成立,为方便企业、服务地方经济发展及检验业务的顺利发展提供了坚实的技术保障。
(中国分析计量网)
Development of N-acetylneuraminic Acid Certified Reference Material
Li Ying1, Xi Xingjun3, Zhou Xiaojing2, Chu Qiao3, Lin Nan2, Wang Wei2, Zhang Jinghua1,2
(1. College of Life Science and Bio-engineering, Beijing University of Technology, Beijing 100124, China; 2. Beijing Center for Physical and Chemical Analysis, Beijing Key Laboralory of Detection Technology & Quality Evaluation of Organic Material, Beijing 100089, China; 3. China National Institute of Standardization, Beijing 100191, China)
N-acetylneuraminic acid certified reference material was separated by semi-preparation HPLC. The qualitative analysis ofN-acetylneuraminic acid was identified by UV, IR, MS and NMR spectrum. The inspection of uniformity and stability were carried out by HPLC. The results examined byF-test statistical methods were stable in the confidence interval of 95%. The combined measurement was executed with 8 qualified laboratory rooms and the uncertainty value was counted at the same time. The purity ofN-acetylneuraminic acid certified reference material was 98.63% with the expanded uncertainty of 0.098 6%(k=2) in the confidence interval of 95%.N-acetylneuraminic acid certified reference material can be used for food detection methods of calibration.
N-acetylneuraminic acid; certified reference material; uniformity; stability; uncertainty
O652.3
:A
:1008-6145(2015)05-0001-06
10.3969/j.issn.1008-6145.2015.05.001
*创新工程Ⅲ-1(PXM2015_178305_000003)
联系人:李莹;E-mail: yingli816@sina.com
2015-08-10
