多中心间的协同性决定队列生物样本的一致性
2015-06-08吴美琴吴宇航赵丽周光迪赵莎莎王伟业
吴美琴,吴宇航,赵丽,周光迪,赵莎莎,王伟业
作为转化医学、个体化医学和精准医学研究领域必不可少的宝贵资源,生物样本的价值在于其本身既有疾病相关个体特异的临床信息,又可以通过一系列生物技术手段获得实验室的实验信息。比如对肿瘤的遗传基因分型以及高风险的遗传标志(基因型体质、风险家族史等)多方位的分析,再结合相应患者的临床表现(基因型与表现型的符合性与特异性)和生活习惯(如环境暴露相关的致病风险因子)等信息可以对疾病发生的相关性做更加全面、可靠的分析,其结果可为临床治疗提供任何实验室研究或临床观察分析所不可能提供的依据[1]。
随着人们对医学生物样本价值认识的提高以及各方面的投入和支持,以医院为主体的众多生物样本库迅速建立,加上疾病种类和资源丰富等特点,与欧美国家相比,我国在较短的时间内积累了大量的生物样本资源。队列研究是病因学研究的重要方法,是将某一特定人群按是否暴露于某可疑因素或暴露程度分为不同的亚组,追踪观察两组或多组成员结局(如疾病)发生的情况,比较各组之间结局发生率的差异,从而判定这些因素与该结局之间有无因果关联及关联程度的一种观察性研究方法。而该类研究近年来在国内也得到迅速发展,积累了大量的样本资源,相应的队列样本库建设也随之发展起来[2]。与以医院为主体建设的生物样本库相比,队列生物样本库的特点就是样本资源大多来源于多个不同的样本收集点(单个中心的队列项目除外)。目前我国样本库发展还处于初期建设阶段,建设和发展水平和规范程度,技术人员掌握的技术能力差异性大,随之带来相互之间的关键问题表现在两个方面:一是样本从收集到制备的异质性(sample heterogeneity);二是统一制定的工作流程在各样本中心的执行一致性不易做到,再加上队列研究有比较长期的随访,一些小的差异性可能会随着样本收集面广和时间长逐步放大,变得更加显著。因此如何管理多中心的样本库建设和样本收集之间的一致性是多中心队列生物样本资源面临的挑战。多中心队列生物样本库为了使各中心的样本资源保持一致性,除通常制定一系列相关的标准操作规范(standard operation protocol,SOP)和系统性培训相关工作人员外,目前存在的主要问题是:首先,协调中心如何系统化监控和跟踪各中心的工作流程,就是多中心之间的协同性;其次,如何根据各中心的实际情况,权衡现实工作中SOP 的必要性和可行性,使得 SOP 得以在各中心都能够真正被使用;再次,如何建立一套质量保证(quality assurance,QA)评估流程并对各中心的实际操作进行评估;最后,对于已经不能避免以及解决不了的问题,怎么处理?这些问题导致的样本异质性是目前多中心队列研究面临的棘手问题——即多中心队列研究能否兼顾生物样本资源和相关数据信息的数量和质量。
环境与儿童健康教育部和上海市重点实验室在上海市卫生计生委的资助下从 2012年开始在整个上海市开展多中心的出生队列研究,截至目前,已经有 6 家单位参与本项目。在国内,想要和国外很多多中心队列研究一样,在规定时间内将新鲜采集的样本集中到一个中心(或协调中心)处理,人、财、物等多方面的可行性都不强。故本项目在设计上采用了折中的办法——将新鲜的样本先在各中心处理、分装和暂存,然后定期运送回新华医院生物样本库长期储存。本文接下来将详细描述项目组如何协调不同中心之间的工作流程和管理方式,探讨如何进行多中心队列研究协同管理的模式,希望能在一定程度上为相关、相似生物样本库建设和管理者提供思路和方向。
1 方法
1.1 协同管理的方法
1.1.1 信息化管理 采用协调中心的生物样本库信息化管理系统对各中心的样本库进行工作流程的协同管理,各中心采用统一的模板对样本生命周期相关信息进行详细记录,更好地监控各中心生物样本留取的整个过程。
1.1.2 质量保证评估 在项目实施过程中为了监控各中心对统一制定的 SOP 的执行力和执行率,项目组编制了《队列研究监查访视报告》,对各中心的样本库进行不定期的监查访视。
1.1.3 SOP 的制定和修改 除了让各中心遵循协调中心统一制定的 SOP 外,项目组还根据信息化管理和质量保证评估得到的各中心信息的比较结果和访视过程中直接发现的问题进行决策,对 SOP 范围内能够解决的问题,及时通知相关中心进行改正;对执行力不强的 SOP,启动相应的变更程序,及时修改和精简,使得各中心都能够按照统一的SOP 来操作。

表1 样本采集、接收、处理时间记录数据集
1.1.4 问题记录 各中心对已经存在的并且没有办法解决的问题及时记录下来,汇总到协调中心,协调中心通过信息化管理系统注释到所对应的样本上面。
1.2 统计方法
采用 IBM SPSS Statistics 19.0 对各协作单位相关信息进行比较;其余图表使用 Microsoft Office 2007 进行制作。
2 结果
2.1 生命周期相关信息记录和系统化管理
各个协作中心通过使用统一的生物样本信息导入模板,除记录生物样本的基础临床信息以外,对各样本留取过程时间进行了详细的记录,由此协调中心生物样本库得到了各中心样本库样本保存过程的信息资料。如表1 所示,模板中记录样本离体到进入冻存状态所经历的各个阶段的时间记录格式。协调中心将收集到的各中心的相关信息通过数据集的形式添加到样本上面,图1 是信息化管理系统中时间记录数据集的注释的内容;通过记录,项目组可以清楚知道各个中心样本离体后每个环节时间耽搁的长短,便于明确责任,寻找问题,进而解决问题,提高工作效率和水平。
同时项目组对各中心样本的运输环节也进行了详细记录和管理。所有的样本运输过程由专业的冷链物流运输公司操作,将各中心的样本统一运送到新华生物样本库储存,运输全程实行温度监控,实时记录运输过程中的温度。如图2所示是 2015年3月26日上午 2 个小时左右的运输过程的温度监控记录,由图可知整个过程的温度控制稳定,一直保持在 –80℃左右。样本接收人员可以通过核对温度监控记录和样本运输单上的时间,协同管理各中心样本运输过程中样本的温度。
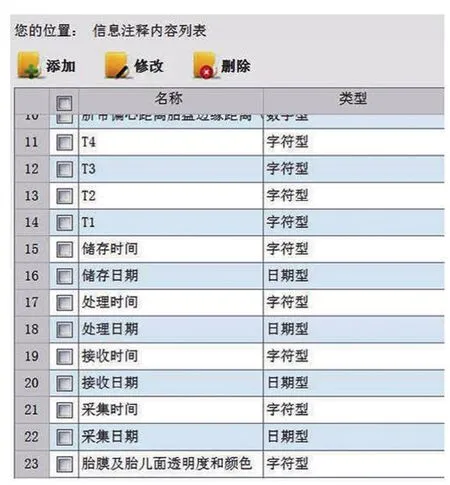
图1 生物样本库信息化管理系统中时间记录数据集的注释
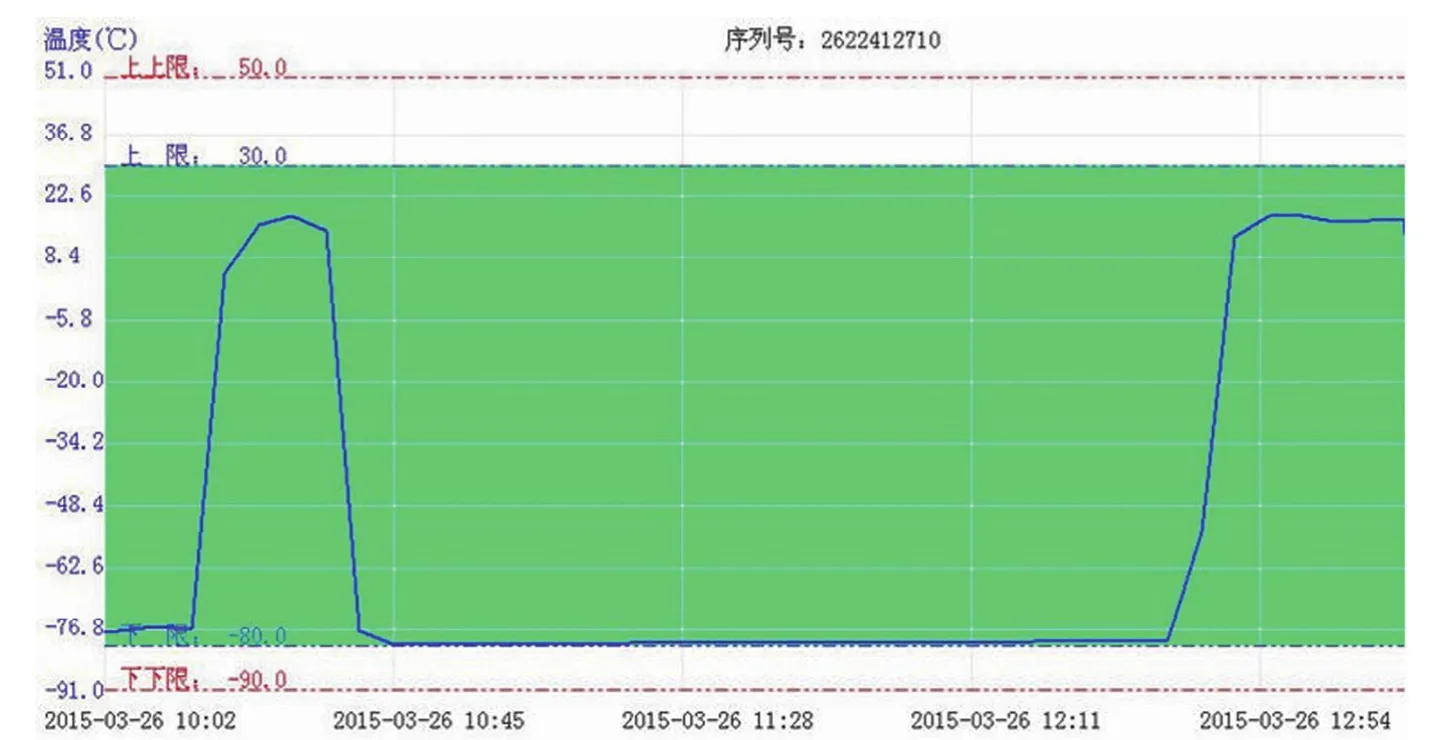
图2 出生队列生物样本运输温度监控记录
2.2 队列研究监查访视报告
主要监控内容包括样本采集和转运、样本处理和保存、样本信息记录、样本运输以及随访过程中的失访率等。如图3 呈现了队列研究监查访视报告的部分内容,可以看出该被访视中心存在的问题很多,项目组需要对这些问题及时、逐一进行处理和解决,否则该中心在这种情况下采集和处理的样本和其他中心的会有差异,影响样本的整体质量。

图3 队列研究监查访视报告部分截图
2.3 各中心相关信息的比较结果
监查访视和样本生命周期信息记录的目的是能够从中整理、统计、总结得到项目实施过程中存在的问题,以便于寻找解决问题的方法,使得各中心能够协同参与项目。图4是我们按照样本采集时各个点的时间记录,选取了两家医院的某一个月份中的胎盘样本的数据,经统计分析得到的图。通过对胎盘采集、运送和处理时间比较,很容易发现医院 B的样本离体后送到样本库所经过的时间(T1)和样本库收到样本到样本开始处理所经过的时间(T2)特别长,即分娩后胎盘没有及时送到样本库,样本送达样本库后,样本库工作人员没有及时处理,从而导致医院 B 的胎盘从离体到入库的时间(T4)特别的长。
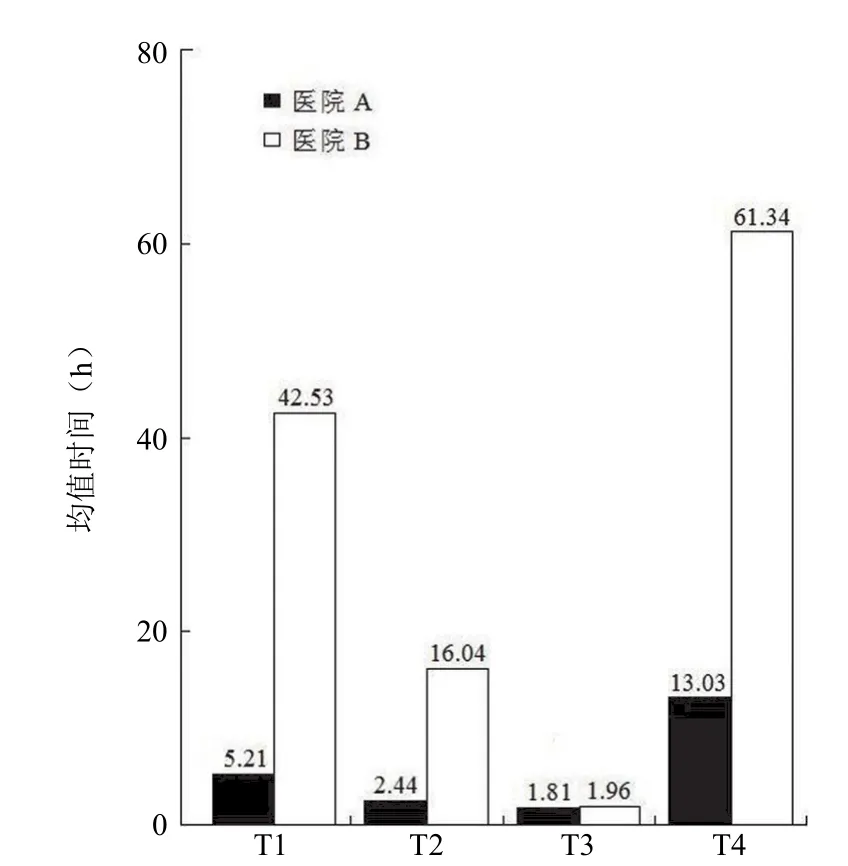
图4 医院 A、B 胎盘样本采集、运送和处理时间的比较
2.4 问题处理方法
首先针对如上述的医院 A、B 胎盘样本采集、运送和处理时间的比较之类问题,在原来 SOP 范围内能够解决的,项目组工作人员将此情况及时反映给医院 B 的样本监察员,由他去医院 B 实地查看以发现问题:是分娩后样本采集人员没有及时通知运送人员,还是样本运送人员没有及时运送胎盘;另外,什么原因导致样本操作人员没有及时处理胎盘?是每天样本库需要处理的样本太多,需要增加该医院的样本操作人员,还是其他的原因。原因明确后,按照胎盘处理的 SOP 督促和改进医院 B 的胎盘收集的整个流程。图5 显示的是医院 B 在改进方案前后各阶段时间的比较,很容易看出该医院在 T1、T2 时间的控制上有了很大的进步,总时间 T4 由原来的 61.34 h,缩减到 38.69 h,当然和医院 A 的 13.03 h 相比,还有待进一步的改进。以此螺旋式改进提高的方法,逐步达到各个研究机构的协同管理。另外我们的统计结果还显示出一个很好的结果,就是医院 A 和医院 B 所有的 T3,即胎盘处理所花费的时间体现了一致性,都在 2 小时左右,这表明样本库工作人员在对各个中心样本库操作人员的培训上是成功的。

图5 医院 B 改进前后胎盘样本采集、运送和处理时间的比较

表2 胎盘、脐带处理标准化操作程序版本变更记录
其次,对于访视过程中发现的 SOP 执行力低,即 SOP的操作性不强的问题,项目组对 SOP 进行修改、精简,使得 SOP 在各个中心都得以实施。例如在项目实施过程中由于各协作单位日分娩量、预算以及分娩流程上的硬性规定等的限制,我们对胎盘采集处理的 SOP 经过了多次的修改。表2 是项目实施过程中胎盘 SOP 版本变更记录。从表中可以看到生物样本库需要如何采集保存何种疾病的何种类型的生物样本及其信息资源这个问题没有统一的固定模式和标准答案,像队列研究这种以项目为导向的样本库,需要根据项目的需求和自身情况来决定,关键目的是需要各个中心都能执行所制定的 SOP。
最后,对已经存在的,没有办法解决的问题应及时记录下来。如前面监查访视报告中所描述的“样本采集后运送到样本库过程中没有使用冰袋”,这是已经发生的事情,对于发现和改正之前所收集的样本我们没有好的办法将这种状态进行改进,但是也不能因为这个失误,就将该中心之前收集的样本做销毁处理,最佳的处理办法就是将样本的这些信息都详细记录下来,以便于今后数据统计分析时查看。
3 讨论
多中心队列研究生物样本收集非常突出的问题就是各中心生物样本收集的一致性,而如何在分散的各中心统一管理样本采集、处理、分装、暂存、运输以及数据的收集等协调中心没有办法直接干预的过程是保证各中心样本质量一致性的关键。这也充分体现了分析前变量(pre-analytical factors)对样本质量的巨大影响。而本项目采用了各中心都能够接受的简便易行的方法,对样本在各中心经历的生命周期中的不同阶段进行记录、追踪和比较,以保证各中心在样本处理各阶段的一致性。生物样本库的基本要求除了样本取材的准确性、样本质量的可控性以及建设、运转标准化外,相关信息的完整性和可跟踪性也是其不可或缺的部分[3]。对于队列研究而言,其信息的完整性是建立在可跟踪性得以实现的基础上的,如果对研究对象没有很好地跟踪随访,就会导致其信息的缺失和不完整,最后分析结果出现难以预料的偏差。生物样本库信息化管理系统在该问题的解决过程中起到了关键作用。
生物样本是不可再生的宝贵资源,而样本质量是整个样本库的核心,除了制定一系列的 SOP 以保证样本采集、处理、分装、运输、保存等过程的规范性,从而保证各样本的质量,SOP 制定后操作人员遵循度才是最关键的。如果写归写,做归做,制定的 SOP 就会成为一纸空文,没有任何意义。对于国内比较新兴的多中心出生队列研究来说,由于样本的操作不能像国外一样,在样本离体后 24 h 内送到统一的中心进行处理,而是需要在各家参与单位的样本库进行直接处理,这就更加大了 SOP 执行率的判断难度。如何知晓统一培训后的各中心样本库工作人员对 SOP 的执行率,项目组采取了定期对项目各中心样本库监查访视的办法,这样很容易发现各个中心对 SOP 的遵循情况和各中心间的差异。如图3 监查访视报告中提到的尿液分装前需要用电动移液器进行混匀操作,尿液处理的 SOP 中是明确写明和要求——“尿液用移液管反复吸吹 15 次,将尿液混匀”。这是很容易做到的,但是在实际操作中各个中心的执行率是不同的,有 7 次,10 次,12 次……,即使是同一个操作人员,在处理不同捐献者的尿液时,吸吹的次数也不一样。这样的差异虽然很小,但是从科学研究严谨的态度出发,样本量达到一定数目,是会造成统计学上的差异。如果没有监查访视,项目组不可能及时发现这些问题,更谈不上及时解决和改正。没有这些预防性的措施来改进样本的质量,而是等到样本收集完成后依靠某一个检测指标的测定来对样本进行质量控制,就为时已晚,没有补救措施。而各中心操作上的参差不齐,将会严重影响样本本身的质量。
不论是样本生命周期中相关信息的记录,还是质量保证评估,目的都是为了及早发现问题,解决问题,最终目标是使得各中心收集回来的样本和数据趋于一致,从而达到协同管理各中心样本库的目的。并且项目组认为采取这样的管理模式是可行的,也是可信的。在胎盘样本各阶段时间记录来看,新生儿的出生时间是准确无误的;胎盘送到样本库的时间也是可信的,因为运送人员和接收人员需要同时签字;样本入库时间是样本库信息化管理系统记录的,没有办法改变;样本开始处理的时间受到样本入库时间的限制,同时样本处理的时间基本是固定不变的。由此逻辑,项目组设定了此方法,该方法不仅仅是为了找到问题出在哪里,也不是责备和惩罚出错之人,而是从错误中学到知识,以便从能够优化改进的地方入手,逐步使各中心都向着所有中心都能实现的目标努力,提高样本整体质量。
而对于相关信息分析得出的结果,项目组会根据实际情况采取不一样的方法来协同各中心。主要的解决办法不外乎①及时改进:操作过程中一些细节且各中心都能很容易做到的,最好方式是各中心都朝着统一的 SOP 来努力,使得各中心在操作上保持一致性。②精简 SOP:SOP 不是越严格越好。SOP 内容的可行性和科学性直接关系到实验数据的质量和完整性,也只有在实际使用过程中不断地对 SOP 的可行性及科学性进行优化,SOP 才更完善,更符合自己的实际情况,提高各中心样本库的遵从性,更好地确保样本的质量和随访数据的完整性。如项目组就胎盘处理的 SOP 经过了多个版本的修订,最终精简和降低要求,使得这个 SOP在参与项目的各个中心样本库都可行。最早制定胎盘 SOP前,我们查阅和参考了国际上已经开展的队列研究对其处理的方法,但发现不尽相同:如英国的 ALSPAC 研究是将整个胎盘浸泡在福尔马林中处理后室温保存[4];而丹麦的奥胡斯出生队列研究是没有保存胎盘样本,而仅保存了 2 管1 ml 的脐带组织于冻存管中[5]。本项目在多个中心开展,各个中心的招募流程和诊疗程序会因为各医院的规定而有所不同,使得在胎盘的采集和处理上统一处理的难度加大。所以在制定第一版时,项目组经过再三讨论,才将总的目标确定下来,后面的修改是在原来版本基础上的简化。这样的修订在整理项目实施过程中还有很多,胎盘处理 SOP 的修订只是其中的一个例子。③记录实情:SOP 版本的修订可以改善新版本 SOP 实施后的样本质量,但是由于参与本项目的各中心不是同一时间参与的,所以会经历不同版本的SOP。即最先参与的中心可能使用了所有版本的 SOP,而后面参与进来的,也许只使用了后面两个版本的 SOP。这些信息都必须记录下来,一旦样本检测后遇到难以解释的结果,可以查询这些记录,可以探讨是不是不同版本 SOP操作引起的。同时通过这些分析前变量的记录,为今后使用正规的样本预分析标准规范(standard PREanalytical code,SPREC)系统奠定一定基础,可以通过批量导入后进行代码解析[6]。这也是协同管理多中心生物样本库的方法之一。对于记录下来的信息,可在统计分析时作为混杂因素进行分层分析或控制变量。
队列研究和生物样本库建设是转化医学的两大研究资源,协同管理多中心队列研究中各生物样本库的建设将为今后的研究提供更加高质量的样本和更加可靠的数据信息,也将加大各方面数据的整合和多平台的合作,实现合理高效利用样本资源,实现资源共享,从而促进转化医学的发展。
[1]Ragin C, Park JY.Biospecimens, biobanking and global cancer research collaborations.Ecancermedicalscience, 2014, 8:454.
[2]Xiong WY, Lü J, Guo Y, et al.Overview on the practice and characteristics of large prospective cohort studies.Chin J Epidemiol,2014, 35(1):93-96.(in Chinese)熊玮仪, 吕筠, 郭彧, 等.大型前瞻性队列研究实施现况及其特点.中华流行病学杂志, 2014, 35(1):93-96.
[3]Dong ED, Hu H, Yu WH.A fundamental role of biobank in biomedical research.Scientia Sinica (Vitae), 2015, 45(4):359-370.(in Chinese)董尔丹, 胡海, 俞文华.生物样本库是生物医学研究的重要基础.中国科学: 生命科学, 2015, 45(4):359-370.
[4]Fraser A, Macdonald-Wallis C, Tilling K, et al.Cohort profile: the avon longitudinal study of parents and children: ALSPAC mothers cohort.Int J Epidemiol, 2013, 42(1):97-110.
[5]Mortensen LM, Bech BH, Nohr EA, et al.Data resource profile: the Aarhus birth cohort biobank (ABC biobank).Int J Epidemiol, 2013,42(6):1697-1701.
[6]Betsou F, Lehmann S, Ashton G, et al.Standard preanalytical coding for biospecimens: defining the sample PRE analytical code.Cancer Epidemiol Biomarkers Prev, 2010, 19(4):1004-1011.
