自动化在生物样本库中的应用现状
2015-06-08明星周学迅
明星,周学迅
为了将基础医学研究的成果充分应用到临床疾病诊治中,近年来,转化医学和精准医学的概念逐渐兴起,作为有望成为跨越这个鸿沟的桥梁,生物样本库如雨后春笋般地出现在全国各地,科研工作者也把目光投向生物样本库的标准化建设以及随之而来的价值发掘上[1]。然而,生物样本库普遍存在样本数量少、样本数据不完整、质量不达标等现象,严重地影响了相关研究结果的可靠性[2-3]。因此,高效地获取和存储质量合格、数据完整的生物样本,并更有效地为医学研究服务,便成为生物样本库行业发展的关键。随着技术的不断革新,解决上述问题的方法不断被探索出来,这其中最重要之一就是“自动化”。“自动化”能最大效率地提高样本制备质量,降低交叉污染,提高样本准备和处理速度,可追踪溯源从而降低出错风险[4]。“自动化”因其更统一、规范、高效的特点,成为了生物样本库的下一个发展方向。本文旨在介绍自动化在生物样本库中的应用现状,希望能为同行起到借鉴作用。
1 自动化样本前处理
液体样本,尤其是血液样本,因其广泛的应用价值,成为了最普遍收集的生物样本。血液一般被分离成血浆、血清、白膜层或外周血单个核细胞(peripheral blood mononuclear cells,PBMCs)等组分,再进行进一步核酸提取或直接进行分装储存。每一个冻存管上面都有唯一的识别码,并用样本管理系统(managing system for inventory,MSI)控制其在冰箱的位置。血液样本的前处理很复杂,手工操作模式已经不能满足高通量、多步骤的样本处理所需要的高效性、准确性及安全性,液体样本前处理工作站的诞生解决了这个难题。
现在广泛应用的样本前处理工作站有 Freedom Evo200®(Tecan,瑞士)液体样本前处理工作站、MicroLab®STAR(Hamilton,瑞士)全自动液体处理工作站等(图1)[5]。有些系统内有条码识别装置,可扫描获取采血管及冻存管对应的信息,精确分装。整合于部分系统内的离心机能够实现样本的全自动装载、平衡和离心,可以根据样本处理的具体需要,设定离心时间、温度和速度。可高通量、自动化完成整个样本制备流程。该系统能识别离心后采血管中的白膜层和分离胶层,并自动将不同组分分装至不同的目标管中。白膜层的回收率比传统的吸取法提高了将近一倍,达 95%以上[6]。在离心转速、时间、分离液和冻存方法一样的情况下,手动和自动的方法获取 PBMCs 并进行冻存后复苏细胞的活性的比较,结果无差异[7]。自动化完成乏味的白膜层和PBMCs 移液处理,可解放实验室劳动力。对于开展生物液体样本液相色谱-质谱分析的样本库而言,全自动液体处理工作站还可以用来做分析前的液体处理[8]。

图1 MicroLab® STAR(Hamilton,瑞士)全自动液体处理工作站,可进行自动加样、试剂分配、移液和分装
样本储存的成分越单一,稳定性越强。相较于直接冻存,尽早地对血液或组织进行核酸提取再加冷冻保护剂的储存方法能最大程度地保护核酸。高质量的核酸提取决定下一步实验如基因测序、基因芯片、实时定量聚合酶链式反应等结果的可靠性[4]。手动的核酸提取方法的原理是有机溶剂抽提法,获取的纯度,浓度较低,受人为操作影响较大,一致性差。另外,提取过程繁琐,工作量繁重,且提取过程会造成健康伤害。最初的自动化核酸提取法是滤膜分离,相较于最新的磁珠分离法,提取的产量和纯度有限,长片段提取效果差,试剂不开放,使用成本高,磁珠分离法具有能提取微量样本,试剂开放,方便使用等优点(表1)。
如今,核酸提取设备的种类繁多,该如何挑选呢? 我们总结了国内外应用较普遍的自动化核酸提取仪并比较了通量、样本体积及所需时间(表2)。
Kim 等[9]比较了三种常用的自动化核酸提取设备提取的患者咽拭子的核酸,并用 RT-PCR 进行呼吸道病毒的核酸验证。他们发现,不同的系统对不同的核酸具有不同的特异性和敏感性,所以样本库应该根据自身特色,如样本种类,目的核酸等选择自动核酸提取设备。自动化核酸提取系统的发展趋势是:通量逐渐加大,提取时间持续缩短。比如,面向大型样本库的自动化核酸提取系统 Kingfisher Flex(Thermo Fisher,美国)和 Chemagic 360®(PerkinElmer,美国)等,在 30~60min 内最多实现 96 个样本的核酸提取,后者用 12 孔道适配器时样本体积达到 10 ml。国产的iAUTOMAG®(百泰克)、TGuide M16/M48®(天根)等仪器以最大通量工作时,单样本的处理体积达到 2 ml 以上。

表1 不同核酸提取方法的比较

表2 国内外应用较普遍的自动化核酸提取仪的通量、所需时间以及最大处理体积的比较
样本的热缺血/冷缺血时间、反复冻融次数、储存时间等都跟样本的质量息息相关。在标准化采集储存的前提下,仍需要定期进行质量检查。质量不达标的样本需要及时出库销毁,腾出储存空间,有助于样本库的良性运转。对于样本库管理人员而言,对不同的样本,需要选择对应可信的质量控制方法。自动化全覆盖的质控工作平台能轻松解决质控的难题。传统的核酸质控依靠电泳后的条带以及紫外分光光度计测量的浓度和纯度,目前广泛应用的 2100 Bioanalyzer®生物分析仪(Agilent,美国)结合了电泳和流式细胞仪的检测方法,可以对 DNA、RNA、蛋白及细胞进行纯度、浓度、数量等的检测,产生高质量的质控数据,操作过程简单,真正用一个平台解决多样本样本库质控的难题[10]。
新一代样本库的概念中,强调数据的质量及完整性[11]。传统的样本数据获得是依靠人工从医疗机构医院医疗信息系统(hospital information system,HIS)、医院检验信息系统(laboratory information system,LIS)、医院影像传输系统(picture archiving and communication system,PACS)中摘抄。现如今,MSI 与这些系统无缝对接,使得患者信息自动被抓取,节省了劳动力的同时保证数据的可靠性及安全性。还有一些小型自动化装置,包括自动旋盖、自动封盖、自动排序、整板读码装置及对应的预置识别码的冻存管,可以辅助液体样本前处理工作站,使整个样本前处理成为一条自动化链。
2 自动化存储和出库
理论上来说,样本储存的温度越低,越接近离体时的状态[12]。对于短期储存,可以选择 –20℃自动化存储系统,对于战略性收集的样本,因储存时间较长,普遍应用 –80℃及 –196℃自动化存储系统。
德国国家队列(German national cohort,GNC)自 2014年10月1日正式启动项目以来,在 18 个分中心的同步收集下,短短八个月,收集的样本量达到 170 万,平均每日入库 2000 个样本,包括全血、血清、血浆、红细胞、RNA、尿液、唾液、鼻黏膜分泌物以及粪便,与样本同时收集的还有每个受试者完整的健康档案,样本库运转压力非常大。为了最大限度地保护如此庞大且宝贵的资源,GNC样本库将 2/3 的基线样本及后续的随访样本都存储在德国环境健康中心的自动化生物样本库中,该中心配有全球唯一的百万级双系统(–80℃和 –196℃)(LiCONiC,列支敦士登)自动化样本库,剩下 1/3 的基线样本则将存储在各个本地的研究中心并用于本地分析和作为备份存储[13]。
LiCONiC 公司的自动化智能存储系统是目前很多大型样本库的选择,德国的格赖夫斯瓦尔德大学医学院开展的名为“格赖夫斯瓦尔德对个性化医疗的探索”的队列样本库[14]及瑞典隆德大学生物样本库[15]等也应用不同型号的 LiCONiC自动化存储系统,智能化地解决大量样本的入库、储存及出库问题。
英国国家样本库作为一个大型前瞻性研究的样本库,调查遗传因素、环境暴露以及生活方式在中老年群体的重大疾病的发病过程中所起的作用。依照异地备份的原则,总共1500 万份分装的样本将分别存储在 2 个相对独立的样本库中:其中 950 万份样本存储在 –80℃自动化储存系统中[4],剩下的 550 万份存储在 –180℃手动操作液氮存储系统中[16]。
图2 以 Biolix STC(LiCONiC,列支敦士登)–80℃自动化智能存储系统为例,展示了自动化存储系统的基本架构。自动化存储系统有以下三个基本工作模块:样品接收(或输出),样本输送,样本存入(或出库)。组成的硬件包括接收区、输送机械臂、低温储存区(冰箱或液氮罐),均接受样本管理软件传达的指令。国内样本库的自动化存储概念还处于萌芽阶段,生物芯片上海国家工程中心等机构已率先开始试点使用,自动化存储现象的普及只是时间问题。
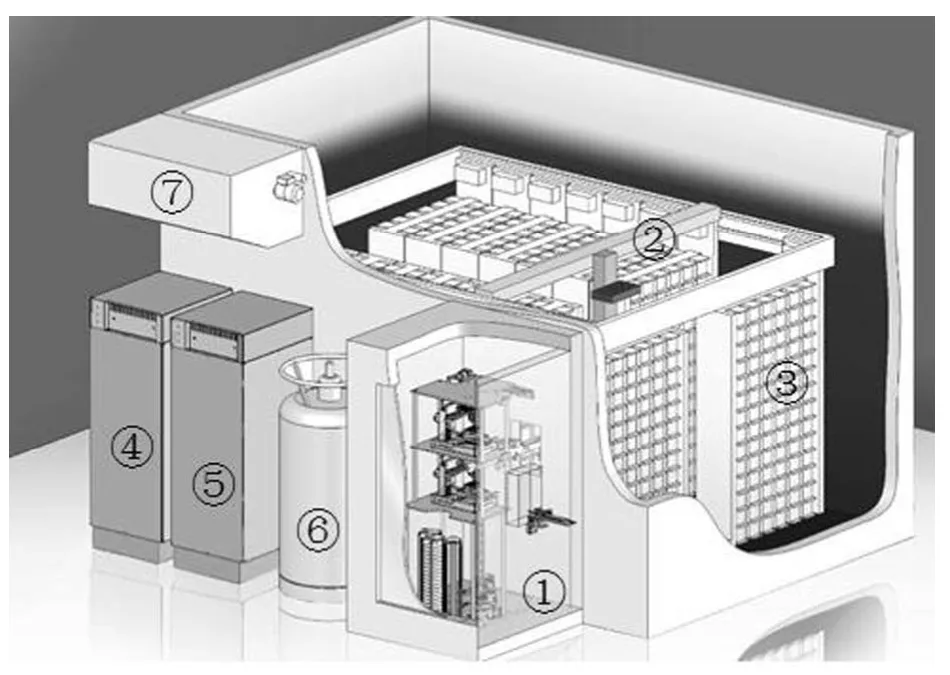
图2 自动化存储系统的基本架构(①样本接收区;②输送机械臂;③样本储存区;④、⑤冷却系统;⑥液氮后备制冷系统;⑦空气干燥器)
3 小结
由于大规模样本库项目样本存储周期长,附加信息量大,样本来源多中心化等因素,往往承载了巨大的价值。样本库的自动化建设和实施可保证样本被高效管理的同时确保信息的绝对可追溯性,尽可能地杜绝人为差错。自动化使得样本存取准确化、存储环境的高质量化和流程的科学化都得到了显著的提高,可以极大地促进我国生物样本库行业的科学管理和资源共享,为各项重大科研课题研究做贡献。然而,样本库的自动化依然处于刚刚起步的阶段,自动化设备费用高昂,一般规模的样本库无法应用。我们期待,在不久的将来,随着技术的革新,自动化设备的成本能降低,又或者,各个分中心的样本由具有自动化处理及储存能力的第三方协助统一储存并管理,用较小的成本达到高质量储存的目的。
[1]Végvári A, Welinder C, Lindberg H, et al.Biobank resources for future patient care: developments, principles and concepts.J Clin Bioinforma, 2011, 1(1):24-34.
[2]Massett HA, Atkinson NL, Weber D, et al.Assessing the need for a standardized cancer HUman Biobank (caHUB): findings from a national survey with cancer researchers.J Natl Cancer Inst Monogr,2011, 2011(42):8-15.
[3]LaBaer J.Improving international research with clinical specimens: 5 achievable objectives.J Proteome Res, 2012, 11(12):5592-5601.
[4]Peakman T, Elliott P.Current standards for the storage of human samples in biobanks.Genome Med, 2010, 2(10):72.
[5]Welinder C, Jönsson G, Ingvar C, et al.Establishing a Southern Swedish Malignant Melanoma OMICS and biobank clinical capability.Clin Transl Med, 2013, 2(1):7.
[6]Mathay C, Ammerlaan W, Betsou F.Automatic buffy coat extraction:methodology, feasibility, optimization and validation study.Biopreserv Biobank, 2012, 10(6):543-547.
[7]Hamot G, Ammerlaan W, Mathay C, et al.Method validation for automated isolation of viable peripheral blood mononuclear cells.Biopreserv Biobank, 2015, 13(3):152-163.
[8]Zhang J, Wei S, Ayres DW, et al.An automation-assisted generic approach for biological sample preparation and LC-MS/MS method validation.Bioanalysis, 2011, 3(17):1975-1986.
[9]Kim Y, Han MS, Kim J, et al.Evaluation of three automated nucleic acid extraction systems for identification of respiratory viruses in clinical specimens by multiplex real-time PCR.Biomed Res Int, 2014,2014:430650.
[10]Miyagi Y.Sample quality control through the depository and distribution of cancer-related human materials: experience of kanagawa cancer research & information association (KCRIA).Rinsho Byori, 2015, 63(1):111-118.
[11]Nakamura A, Osonoi T, Terauchi Y.Relationship between urinary sodium excretion and pioglitazone-induced edema.J Diabetes Investig,2010, 1(5):208-211.
[12]Hubel A, Spindler R, Skubitz AP.Storage of human biospecimens:selection of the optimal storage temperature.Biopreserv Biobank,2014, 12(3):165-175.
[13]German National Cohort (GNC) Consortium.The German National Cohort: aims, study design and organization.Eur J Epidemiol, 2014,29(5):371-382.
[14]Grabe HJ, Assel H, Bahls T, et al.Cohort profile: Greifswald approach to individualized medicine (GANI_MED).J Transl Med, 2014,12:144.
[15]Malm J, Lindberg H, Erlinge D, et al.Semi-automated biobank sample processing with a 384 high density sample tube robot used in cancer and cardiovascular studies.Clin Transl Med, 2015, 4(1):67-74.
[16]Elliott P, Peakman TC, UK Biobank.The UK Biobank sample handling and storage protocol for the collection, processing and archiving of human blood and urine.Int J Epidemiol, 2008, 37(2):234-244.
