唑来膦酸治疗绝经后妇女骨质疏松的不良反应分析
2015-06-01张建丰施松青
袁 耀,张建丰,施松青
唑来膦酸治疗绝经后妇女骨质疏松的不良反应分析
袁 耀a,张建丰b,施松青a
目的 观察唑来膦酸治疗绝经后妇女骨质疏松的安全性。方法 对90例绝经后骨质疏松患者给予5 mg唑来膦酸注射液,观察用药后1个月内不良反应的发生情况,根据是否发生不良反应将患者分为发生组及未发生组,对不良反应发生的影响因素进行Logistic回归分析。结果 90例患者用药后发热、头痛、肌肉痛、关节痛、白细胞减少、轻微肾功能损害的发生率分别为21.11%、14.44%、11.11%、13.33%、4.44%、2.22%,总发生率为45.56%;发生组与未发生组骨钙素水平、钙剂、骨吸收抑制剂、内分泌调节药物使用率比较差异有统计学意义(P<0.05);Logistic回归分析显示使用内分泌调节药物(OR=0.71,P<0.05)是不良反应发生的危险因素,使用钙剂(OR=0.83,P<0.05)、骨吸收抑制剂(OR=1.23,P<0.05)是不良反应发生的保护性因素。结论 唑来膦酸治疗绝经后骨质疏松患者的不良反应发生率较高,但程度较轻,辅之以钙剂、骨吸收抑制剂治疗可减少不良反应。
骨质疏松;绝经后;唑来膦酸;毒副反应
0 引言
唑来膦酸是新一代双磷酸盐制剂,是目前临床抑制骨吸收能力最强的药物[1],在骨质疏松的治疗中受到广泛关注。国外研究证实,对骨质疏松患者静脉注射唑来膦酸疗效显著,其安全性及耐受性良好。但是注射用唑来膦酸进入我国的时间尚短,临床缺乏注射用唑来膦酸治疗绝经后骨质疏松患者安全性的系统评价。本文调查90例绝经后骨质疏松患者使用唑来膦酸注射液治疗后不良反应的发生情况,分析唑来膦酸的安全性,现报道如下。
1 资料与方法
1.1 一般资料 选择2012年6月至2014年6月在本院就诊的绝经后骨质疏松患者90例。入选标准:①符合《骨质疏松骨折诊疗指南》中相关诊断标准[2];②绝经年限≥1年;③无唑来膦酸过敏史;④签署知情同意书。排除标准:①合并严重心、肝、肾等疾病;②伴有甲状腺、甲状旁腺、骨髓瘤、维生素D缺乏症或其他骨代谢疾病;③脊柱或髋部畸形影响骨密度测量者;④未给予唑来膦酸治疗前即出现不良反应者。年龄54~73岁,平均(66.48±7.32)岁;32例合并骨质疏松骨折,19例合并乳腺疾病。
1.2 治疗方法 90例患者均给予唑来膦酸注射液(江苏正大天睛药业,国药准字:H20041346)静脉注射治疗。先给予患者250 mL生理盐水静点充分水化,再给予含5 mg的唑来膦酸100 mL静脉输注,输注时间>30 min,输注完成后再给予250 mL生理盐水静点充分水化,在此过程中嘱患者饮用500 mL以上温开水。输注完成后3 d内严密监测患者体温、脉搏、血压及尿量变化,及时发现不良反应。
在给予唑来膦酸前,53例服用钙剂(碳酸钙D3口服,600 mg/d;阿尔法D3胶丸口服,0.25 μg/d),持续治疗1个月以上。48例服用骨吸收抑制剂,其中20例口服阿仑膦酸钠,70 mg/次,1次/周;12例口服盐酸雷洛昔芬,60 mg/次,1周/次;17例给予鲑鱼降钙素针剂治疗,50 IU/次,1次/d。持续治疗1个月以上。19例合并乳腺疾病患者给予内分泌药物治疗,即给予弗隆口服,2.5 mg/d,1次/d,持续治疗1个月。
1.3 调查方法 参考文献[1,3-5]总结唑来膦酸注射液治疗后的常见不良反应,包括发热、血小板减少、白细胞减少、流感样症状、头痛、肌肉痛、肌肉痉挛、关节痛、肾功能损害、血尿、尿蛋白、心律失常等。采用门诊随访或电话调查的方式,统计给予唑来膦酸注射液治疗1个月内患者上述不良反应发生情况。根据是否发生不良反应将90例患者分为发生组与未发生组,对治疗前血清钙、骨钙素、骨密度、合并骨折、使用钙剂、使用骨吸收抑制剂、使用内分泌调节药物等对不良反应的影响进行Logistic回归分析。
1.4 检测方法
1.4.1 骨密度测量 治疗前采用Ostecore 2型双能X线检测仪(美国GE公司)测量髋关节整体、桡近端1/3、腰椎L1~4、股骨颈等部位骨密度值。测量前均校正检测仪器性能,确保变异系数在1%以内。峰值骨量源自仪器储存的中国成年女性骨量数据。
1.4.2 血清钙、骨钙素检测 治疗前取患者晨起空腹静脉血5 mL,3 000 r/min离心处理10 min,取上层血清。采用日立7180生化分析仪(日本日立公司)测定血清钙水平;采用放射免疫法测定骨钙素水平,试剂盒购于英国IDS公司。
1.5 统计学方法 采用SPSS 17.0软件包对数据行统计学分析,单因素分析采用χ2检验,多因素分析采用非条件Logistic 回归分析。P<0.05为差异有统计学意义。
2 结果
2.1 不良反应发生情况 给予唑来膦酸注射液治疗1个月内,90例患者均未发生心律失常、肾功能障碍等严重不良反应。不良反应均为一过性,经简单处理即可好转。其中发热19例、头痛13例、肌肉痛10例、关节痛12例、白细胞减少4例、轻微肾功能损害2例,发生率分别为21.11%、14.44%、11.11%、13.33%、4.44%、2.22%,共计41例患者发生不良反应,总发生率为45.56%。
2.2 不良反应单一因素分析 发生组41例,未发生组49例。两组治疗前血清钙、骨密度水平、合并骨折率比较差异无统计学意义(P>0.05),而骨钙素水平及使用钙剂、骨吸收抑制剂、内分泌调节药物率比较差异有统计学意义(P<0.05),见表1。
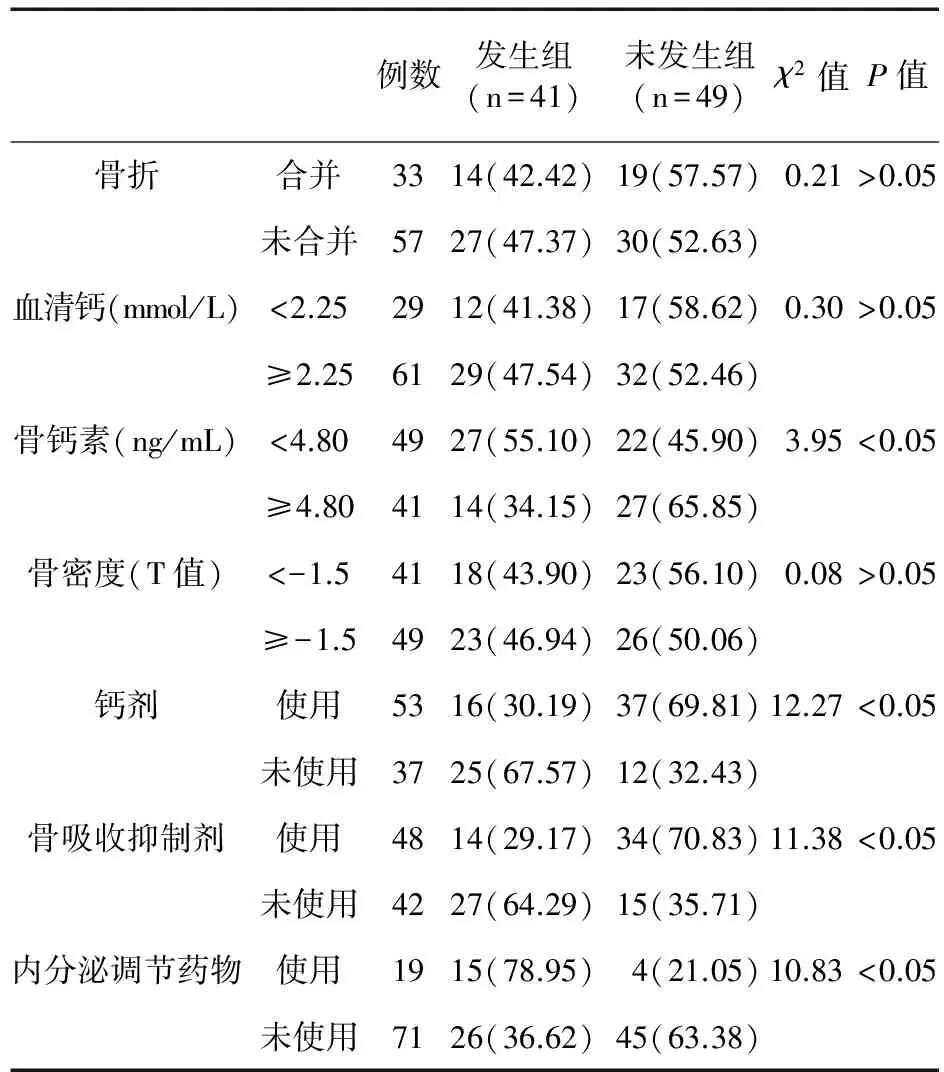
表1 不良反应发生的单因素分析(例,%)
2.3 不良反应发生的多因素分析 以上述4个有统计学意义的因素作为自变量,以是否发生不良反应作为因变量,采用非条件多因素Logistic回归分析,结果显示使用内分泌调节药物是不良反应发生的危险因素,使用钙剂及骨吸收抑制剂是不良反应发生的保护性因素,见表2。

表2 不良反应发生的多因素Logistic回归分析
3 讨论
骨质疏松是绝经后妇女常见疾病,易引发骨痛、身材变矮、畸形及骨折等,给绝经后妇女生活带来严重影响。据统计,我国50岁以上妇女骨质疏松患病率高达50%,而骨质疏松症患者骨折后有80%以上致残,1年内死亡率高达10%~50%[6]。双膦酸盐类药物是目前临床治疗骨质疏松最有效的药物。1年静脉注射1次唑来膦酸使患者的治疗依从性及治疗效果大大提高。国内外临床实践表明,唑来膦酸注射液治疗绝经后骨质疏松可显著提高患者骨密度,降低骨折发生风险[1,3,7]。
国外研究报道,静脉注射唑来膦酸对普通骨质疏松患者的安全性及耐受性良好,部分患者仅出现轻微的头晕、胃肠道不适等不良反应[7]。然而研究针对的是普通骨质疏松患者,对于绝经后骨质疏松患者的用药安全性报道较少。近年我国不断有唑来膦酸注射液用药后引起发热、关节痛、肌肉痛、低钙性抽搐及心律失常等病例报道。杨毅等[8]报道,对绝经后骨质疏松患者给予唑来膦酸注射液治疗后,急性发热、关节痛、骨痛发生率分别为20.74%、15.34%、12.76%。Kachnic等[4]给予2例绝经后骨质疏松患者唑来膦酸注射液治疗,用药10~13 d后出现轻微肾损害,发生率为1.12%。本研究中,无1例发生心律失常、肾功能障碍等严重不良反应,发热、头痛、肌肉痛、关节痛、白细胞减少、轻微肾功能损害的发生率分别为21.11%、14.44%、11.11%、13.33%、4.44%、2.22%,略高于上述报道,可能与本研究样本量较小有关。共计41例患者发生不良反应,总发生率为45.56%。虽然不良反应总发生率较高,但均为一过性反应,不需过多处理即可好转,与徐万龙等[9]报道基本相符。提示唑来膦酸治疗绝经后骨质疏松不良反应发生率较高,但均较轻微。
掌握唑来膦酸不良反应发生的相关因素有助于制定相应的防治措施。Rossini等[5]研究认为,唑来膦酸注射液治疗骨质疏松症,其独特的双氮结构对破骨细胞的关键酶及骨吸收有明显的抑制作用,在短期内会导致血清钙水平降低,进而引发头痛、关节痛、肌肉痛等不良反应。权朋勃等[10]研究报道,采用唑来膦酸治疗前,患者血清钙水平或骨钙素水平较低,可增加头痛、关节痛及发热等不良反应发生率。本研究中,发生组与未发生组血清钙水平比较差异无统计学意义(P>0.05),但发生组骨钙素水平较低(P<0.05)。Logistic回归分析显示骨钙素水平与不良反应发生之间无明显相关性。袁宏等[11]研究认为,骨密度较低的患者骨转化率高,唑来膦酸优先被转运到骨形成或吸收部位,沉积到骨表面而被破骨细胞摄取,对骨吸收的抑制作用较强,在短期内血清钙水平下降会更明显,进而导致不良反应发生率增加。Spiegel 等[12]也得到相同的结论,骨密度较低的患者骨转化率较高,唑来膦酸可抑制甲醛戊酸途径,增加香叶焦磷酸的累积,促进大量炎性因子释放,引起发热、白细胞异常等不良反应[13]。但本研究结果显示,骨密度高低并不影响不良反应的发生,与上述两项研究有所差异,其原因有待进一步研究。
骨量减少、骨微结构破坏是骨质疏松的发病机理。内分泌调节药物是乳腺增生、乳腺癌治疗的主要药物,其长期用药易引起骨质流失,导致骨钙素、血清钙等的流失[14],在一定程度上影响唑来膦酸的疗效,也增加了不良反应发生率。Logistic回归分析显示,治疗前应用内分泌调节药物是唑来膦酸引发不良反应的危险因素。因此,临床在对骨质疏松患者给予唑来膦酸治疗前,应适当调整内分泌调节药物的使用剂量及时间,降低不良反应发生率。
本研究结果表明,治疗前补充钙剂、骨吸收抑制剂,可降低唑来膦酸引发的不良反应的发生率。Logistic回归分析显示,使用钙剂(OR=0.83,P<0.05)、骨吸收抑制剂(OR=1.23,P<0.05)是不良反应发生的保护性因素,这与聂海等[15]研究报道基本相符。唑来膦酸引发不良反应的主要机制是其在抑制破骨细胞与骨吸收的同时使血清钙水平下降。适当补充钙剂及骨吸收抑制剂可预防血清钙下降,降低不良反应发生率[16]。
综上所述,对绝经后骨质疏松患者给予唑来膦酸治疗,不良反应发生率较高,但程度较轻,辅之以钙剂、骨吸收抑制剂治疗可减少不良反应。
[1] Freitas-Neto CA,De Oliveira Fagundes WB,Ribeiro M Jr,et al.Unilateral Uveitis with Vitreous Haze Following Zoledronic Acid Therapy for Osteoporosis[J].Semin Ophthalmol,2013,22(29):68-80.
[2] 中华医学会骨科学分会.骨质疏松骨折诊疗指南[J].中华骨科杂志,2008,28(10):875-878.
[3] 赵志,李昭程,刘扬.唑来膦酸治疗骨转移肿瘤疼痛的临床观察[J].中华全科医学,2012,4(4):518-519.
[4] Kachnic LA,Pugh SL,Tai P,et al.randomized phase III trial to evaluate zoledronic acid for prevention of osteoporosis and associated fractures in prostate cancer patients[J].Prostate Cancer Prostatic Dis,2013,16(4):382-386.
[5] Rossini M,Zanotti R,Viapiana O,et al.Zoledronic Acid in Osteoporosis Secondary to Mastocytosis[J].Am J Med,2014,3(19):9340-9343.
[6] 陆琳松,旭合热提·吾提库尔,哈巴西·卡肯,等.唑来膦酸对维吾尔族绝经后妇女骨质疏松性骨折骨代谢指标的影响[J].中国骨科临床与基础研究杂志,2013,5(3):138-142.
[7] 罗政,吴炜戎,蔡晓燕,等.唑来膦酸治疗绝经后骨质疏松症后急性发热反应的临床特点[J].广东医学,2014,35(6):928-930.
[8] 杨毅,李蓬秋,鲜杨,等.唑来膦酸治疗女性绝经后骨质疏松所致急性发热临床分析[J].中国骨质疏松杂志,2013,19(1):58-60.
[9] 徐万龙,钟慧琴,王利,等.唑来膦酸对维、汉族绝经后骨质疏松妇女骨密度的影响[J].中国医药导刊,2013,15(5):816-817.
[10]权朋勃,王明礼,郭得辛,等.注射型唑来膦酸与阿仑膦酸钠治疗绝经后骨质疏松症的临床比较[J].中国妇幼保健,2014,29(8):1283-1285.
[11]袁宏,陆琳松,钟惠琴,等.唑来膦酸对骨质疏松患者全髋关节置换术后假体周围骨密度的影响[J].中华关节外科杂志(电子版),2014,7(3):278-285.
[12]Spiegel R,Nawroth PP,Kasperk C.The effect of zoledronic acid on the fracture risk in men with osteoporosis[J].J Endocrinol Invest,2014,37(3):229-232.
[13]Khajuria DK,Razdan R,Mahapatra DR.The combination therapy with zoledronic acid and propranolol improves the trabecular microarchitecture and mechanical property in an rat model of postmenopausal osteoporosis[J].J Osteoporos,2014,22(30):56-60.
[14]桂程丽,陈芸,程彩涛.密固达治疗骨质疏松症临床分析[J].实用药物与临床,2012,15(11):760-761.
[15]聂海,彭超,郝杰,等.唑来膦酸预防绝经妇女骨质疏松性骨折的meta分析[J].第二军医大学学报,2011,32(9):985-990.
[16]张玲谦.唑来膦酸治疗老年骨质疏松患者不良反应的预防方法[J].中国医药,2013,8(11):1615-1616.
Investigation and analysis of toxicity caused by zoledronic acid in the treatment of postmenopausal women with osteoporosis
YUAN Yaoa,ZHANG Jian-fengb,SHI Song-qinga
(a.Department of Orthopedics,b.Department of Radiology,The People′s Hospital of Yuyao City,Yuyao 315400,China)
Objective To investigate the toxicity caused by zoledronic acid in postmenopausal women with osteoporosis.Methods 90 postmenopausal women with osteoporosis were treated with 5 mg zoledronic acid,the occurrence of adverse reactions within a month were observed,then patients were divided into toxicity group (group T) and no toxicity group (group N) depending on whether adverse reactions occured or not,Logistic regression analysis was carried out for the related factors of toxicity.Results The incidences of fever,headache,muscle pain,joint pain,neutropenia,mild renal impairment were 21.11%,14.44%,11.11%,13.33%,4.44% and 2.22%,the total incidence rate was 45.56%.There were significant differences in the osteocalcin levels,calcium,bone resorption inhibitors,endocrine regulation drug use between the 2 groups (P<0.05).Logistic regression analysis showed that the endocrine regulation drugs use (OR=0.71,P<0.05) was the risk factor for adverse reactions,while the use of calcium (OR=0.83,P<0.05) and bone resorption inhibitors (OR=1.23,P<0.05) were the protective factors.Conclusion Zoledronic acid has a high incidence of toxic reactions in the treatment of postmenopausal women with osteoporosis,while the degree of the toxicity is light,supplement with calcium and bone resorption inhibitors could reduce the toxicities.
Osteoporosis;Postmenopausal;Zoledronic acid;Toxicity
2014-07-15
余姚市人民医院a.骨科,b.放射科,浙江 余姚 315400
10.14053/j.cnki.ppcr.201502024
