口蹄疫灭活疫苗基础研究
2015-05-30李培林等
李培林等

摘 要:口蹄疫灭活疫苗目前仍然是控制口蹄疫的主要手段。随着悬浮工艺和纯化工艺的改进,使口蹄疫灭活疫苗的质量有很大的提高,但基础研究也不容忽视。本文主要探讨影响种毒制备的一些因素,包括细胞状态、接毒量的改变及毒液保存条件对种毒质量的影响。基本得出如下结论:第一,细胞状态会影响收毒时间的变化,同时一定程度上也会影响LD50毒价的变化;第二,接毒含量增高,收获时间缩短,而低剂量、正常剂量接毒传代试验均能获得合格的种毒支系,适宜地改变接毒量有助于提高种毒质量;第三,不论是4 ℃冷藏保存,还是-20 ℃冷冻保存,随着保存时间的延长,毒价均有不同程度的损失,而且4 ℃保存的毒液下降率明显低于-20 ℃保存方式。因此,上述因素在生产中要细化研究,对提高种毒质量起到指导意义。
关键词:BHK-21细胞;口蹄疫灭活疫苗;种毒制备;质量控制
中图分类号:S855.3 文献标识码:A 文章编号:1001-0769(2015)09-0028-03
口蹄疫是由口蹄疫病毒(FMDV)引起偶蹄动物的一种急性、热性、高度接触性传染病,严重危害畜牧业的发展[1,2]。OIE将该病列为A类家畜传染病之首,而我国农业部也把该病列为第一类防控疫病。对于口蹄疫的防控,目前仍以灭活疫苗为主。此项措施在我国重大疫情中发挥巨大防治作用。
对于口蹄疫疫苗生产企业,质量的提高、产品创新以及员工素质提高是企业发展的动力。因此,疫苗质量提高离不开工艺革新以及基础方面的优化研究。工艺革新是疫苗制备企业的硬件系统,由企业的综合实力决定。而基础研究主要包括:种细胞的驯化与筛选、种毒的优化制备以及抗原纯化等相关研究[3,4]。从种毒制备人员的自身素质讲,筛选制备出良好的种毒,不仅给疫苗前端解决了问题,而且也给后端工艺带来可喜的成果。因为种毒质量好坏、抗原含量高低,直接影响口蹄疫抗原中的有效成分,而且关系到疫苗的免疫效果。在生产中获得一支理想的种毒支系,不仅给生产人员带来方便,而且也给企业带来很大的经济收益。因此,制苗毒株的选择及质量的提高是疫苗生产的首要问题[5]。
筛选优质的种毒需要有正确的操作方法,更需要掌握影响种毒质量的一些因素。目前,影响贴壁种毒因素主要有细胞贴壁状态、维持液的酸碱度、接毒量、最佳收获时间、检验周期、种毒保存时间以及种毒传代路线及无菌观念等,上述因素均能影响种毒毒价及质量效果。因此,本次试验主要探讨影响种毒质量的一些因素,并进行分析与总结,从而通过过程控制,调整传代条件、保存方法,筛选出毒价稳定、146S高的基础种毒,从而保障种毒质量,提高企业竞争力。
1 材料与方法
1.1 材料
1.1.1 仪器与设备
二氧化碳培养箱(Thermo 8000 WJ);生物安全柜(HFsafe-1200型);倒置显微镜清(OLMPUS);4 ℃平温冰箱;-20 ℃卧式冷冻冰柜;温室、生物细胞转瓶机、细胞观察台;超低温冰箱(Thermo ULT1386-3-V41)、移液器、恒温震荡培养箱等仪器。以上设备均由金宇保灵生物药品有限公司提供。
1.1.2 BHK-21细胞
由金宇保灵生物药品有限公司提供,分种传代一般按1∶3~1∶4进行操作,加入营养液,置37 ℃培养箱中培养。营养液配制按本公司的配液SOP进行操作。
1.1.3 O型口蹄疫基础种毒
由金宇保灵生物药品有限公司质量检验部提供FMDV基础种毒,由车间领取并由专人管理。
1.2 方法
1.2.1 BHK-21细胞贴壁状态对种毒的影响
按常规细胞传代的方法,将细胞复苏传代后,将同批培养24 h、48 h、53 h、72 h、96 h细胞,每瓶细胞换液,加入病毒维持液100 mL,同时每个培养时间组下设两个重复,分别按5 %~8 %的接毒量接毒,接毒完成后置二氧化碳培养箱37 ℃培养6 h~8 h观察,病变达到90 %时收获病毒冷冻保存后混勻测病毒含量。
1.2.2 改变接种比例对筛选种毒的影响
选同批48 h、72 h培养阶段的BHK-21细胞,细胞换液,加病毒维持液100 mL,一组以7 %~8 %的接毒量接毒,另一组以1 %接毒量接毒,置二氧化碳培养箱37 ℃培养6 h~8 h观察,病变达到90 %时收获病毒冷冻保存后混匀测病毒含量,连续传代3次。
1.2.3 不同保存方式对种毒质量的影响
通过测毒结果筛选出毒价高和毒价低的种毒,然后分别将上述两种种毒,进行4 ℃平稳保存和-20 ℃冷冻保存,保存期限为7月,经过测毒结果分析计算不同时间毒价的损失率,毒价损失率=(原样毒价-不同时间段的毒价)/原样毒价,记录结果。
1.2.4 LD50测定
用pH值为7.6~7.8的细胞维持液将待测各批次种毒样品进行10倍系列稀释,取10-7、10-8、10-9 3个稀释度,每个稀释度颈背部皮下接种2~3日龄乳鼠4只,设对照2只,每只注射0.2 mL,接种后观察7 d,根据发病死亡乳鼠数按Reed-Muench法计算LD50。
2 结果与分析
2.1 BHK-21细胞贴壁状态对种毒因素的影响
细胞培养24 h、48 h、53 h、72 h、96 h后分别按5 %~8 %的接毒量接毒收获毒和LD50情况,具体详见表1与图1。
由表1图1可知,随着BHK-21细胞培养时间的延长,即细胞从24 h到96 h的过程中,细胞表现基本形成单层、致密单层、脱落等现象的发生。因此,选择不同培养时间段的细胞,对筛选种毒支系有一定的影响,从上述数据分析可知,细胞培养时间与收毒时间存在一定的相关性,从LD50毒价分析可知,毒价上升的阶段对应的是细胞48 h~72 h培养阶段。
2.2 改变接种比例对筛选种毒的影响
7 %~8 %正常剂量组与1 %低剂量组种毒传代收毒情况具体情况详见表2与表3。
从表2可知,按7 %~8 %种毒含量,连续传3代,种毒LD50基本在7.5~8.0范围内变化,说明按7 %~8 %正常含量接毒,可以得到理想的种毒支系。而且可以保证抗原的正常生产。从收毒时间分析,随着代次的增加,收毒时间逐渐在缩短,而细胞颗粒饱满时间基本稳定在8.5 h~11.5 h 范围内。
从表3低剂量组数据分析可知,以1 %种毒含量进行接毒传代,种毒LD50基本在7.0~8.0范围内变化,而且通过收毒时的观察,SY001 F10代毒价不合格,通过后续连续传代,收毒时间缩短毒价升高,可以初步证明,用低剂量接毒方法可以盲传两到三代,毒价基本趋于合格。说明这种传代方法可以达到生产的要求,而且这种工艺有一定的可行性。经表2与表3对比分析可知,正常剂量组与低剂量组种毒传代方式最大的不同,种毒含量高收毒时间快,种毒含量低收毒时间慢,即种毒含量的多少与收毒时间呈一定的正相关性,测毒结果与细胞病变情况,两种方式基本一致。
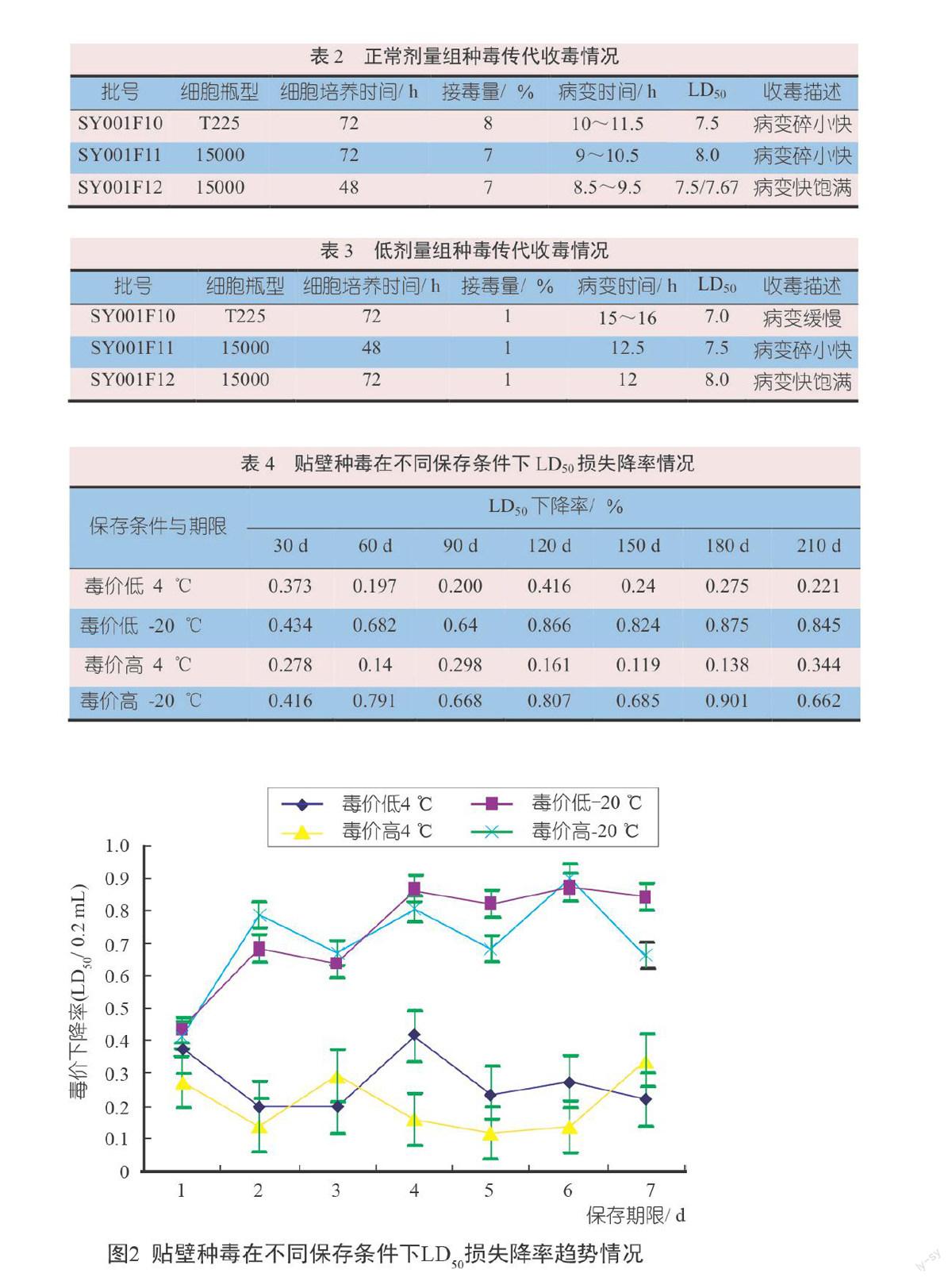
2.3 贴壁种毒不同保存方式对种毒质量的影响
从表4、图2可知,不论是4 ℃平稳保存和还是-20 ℃冷冻保存,随着保存时间的延长,毒价匀有不同程度的损失;从保存条件分析,4 ℃保存的毒液下降率明显低于-20 ℃保存方式。从毒价高低分析可知,在大部分保存时间内,在 4 ℃下保存,高毒价的下降率明显低于4 ℃低毒价的下降率,而-20 ℃保存方式也有上述规律,这就说明,保存方式和毒价高低影响贴壁种毒的质量。
3 讨论
3.1 BHK-21细胞贴壁状态及传代稳定性对筛选种毒质量的影响
细胞培养时间、分种比例、细胞营养液以及不同种类的血清与添加量,均能影响贴壁细胞状态与形态。而本次试验在固定分种比例、营养液以及血清因素同时,只考虑细胞培养时间对筛选种毒支系的影响,旨在探讨细胞培养时间与种毒质量的关联性。在实际工作中,细胞状态是指细胞的致密程度、融合率及细胞肉眼观察情况状。细胞状态影响收毒时间的变化,同时也一定程度上影响LD50毒价的变化。一般情况下,不同培养阶段BHK-21细胞,细胞的致密度与薄厚度不一致;在接毒量一致的情况下,细胞培养时间会影响CPE收获时间,从而间接地影响毒价。在实际工作中,尽量选择细胞形态好,培养时间在48 h~72 h细胞进行接毒,同时在工作中加无菌观念意识,在一定程度上,利于筛选优质的种毒。
3.2 不同的接种比例对筛选种毒的影响
在细胞状态良好,细胞培养时间一定的情况下,贴壁种毒接毒含量增高,收获时间缩短,反之亦然。经报道,接毒量高低直接影响病毒繁殖周期,细胞病变快慢直接影响细胞维持液的酸碱度及营养物质的消耗快慢,这些因素的变化会直接影响完整病毒粒子的情况。通过本次试验结果可知,低剂量、正常剂量接毒传代试验均能获得合格的种毒支系。因此,在实践中,适宜地改变接毒量有助于提高种毒毒价。所以,在种毒传代中多注意上述问题。
3.3 贴壁病毒液的不同保存条件对种毒质量
的因素的影响
在口蹄疫灭活疫苗制备过程中,不可避免地要将基础种毒、抗原灭活液、成品苗进行保存,选择适宜的保存条件和储备方法,对疫苗质量的提高有一定的指导意义。大量资料报道表明[6],冷链系统是口蹄疫苗的主要储存和运输方式,可见如何有效地保存疫苗终端产品也是疫苗质量提高的关键。本次试验证明,不论是 4 ℃平稳保存和还是-20 ℃冷冻保存,随着保存时间的延长,毒价匀有不同程度的损失,而且4 ℃保存的毒液下降率明显低于-20 ℃保存方式,本次结果与一些报道有所差距。经查阅资料分析有如下原因所致,因為在保存口蹄疫抗原或毒液时,大部分采用的是缓冲体系来保存,在4 ℃或 -20 ℃保存条件下,-20 ℃保存条件下更容易使缓冲体系酸碱度发生变化,从而使毒液中的完整病毒粒子更容易降解,影响口蹄疫病毒质量。
4 结语
综上所述,疫苗制备过程是一个系统过程,本次试验只是从种毒方面初步探讨了,细胞培养时间的变化、接毒量的变化以及毒液保存条件的改变对贴壁种毒质量的影响,基本得出如下结论细胞状态、保存时间是影响口蹄疫种毒质量的关键。因此,在实际工作中细化这方面的研究,对口蹄疫疫苗质量的提高会有一定的指导意义。□□
参考文献:(6篇,略)
