氯虫苯甲酰胺、氟苯虫酰胺在不同水体中降解特性
2015-05-28孟志远陈小军陆春良
孟志远,王 平,陈小军,陆春良,陈 思,任 莉
(扬州大学 园艺与植物保护学院,江苏 扬州 225009)
农药的水解是决定农药在环境中转归、消失的重要途径,是农药登记和环境安全性评价中必不可少的参数,研究农药水解具有重要的环境学意义。因此,开展农药水解化学转化研究,对开发新农药,安全、合理使用农药,防治污染,保护生态环境,都具有重要的理论意义和现实意义。
氯虫苯甲酰胺、氟苯虫酰胺是新型杀虫剂,主要用于防治蔬菜、水果、水稻和棉花等作物上的鳞翅目害虫;它们对成虫和幼虫都有较好的活性,而且作用速度快、持效期长。由于作用机理独特,因此与传统杀虫剂没有交互抗性;对节肢类益虫安全,适宜于害虫综合治理和害虫抗性治理[1-6]。目前关于氯虫苯甲酰胺、氟苯虫酰胺的研究主要集中在药剂部分水果、蔬菜或土壤介质中的残留,制剂有效成分分析等[7-17];还未见有关氯虫苯甲酰胺、氟苯虫酰胺在不同水体环境条件下的降解动态和安全性评价的研究报道,本文选用不同pH值的缓冲溶液和不同的自然水体,研究氯虫苯甲酰胺、氟苯虫酰胺在不同水体下的光解动态,为评价氯虫苯甲酰胺、氟苯虫酰胺水体中残留状况提供科学依据。
1 材料与方法
1.1 仪器与试剂
高压汞灯:上海亚明飞亚灯管厂;85-2型恒温磁力搅拌器:上海司乐仪器有限公司产品;pH计(PB-10)、BS210S型电子天平:德国Sartorius公司;SB-1000型旋转蒸发器,日本Eyela公司;THZ-82A型振荡机,江苏富华仪器有限公司。
氯虫苯甲酰胺标准品(w=99.0%):美国Chemservice公司提供;氟苯虫酰胺标准品(w=98.52%):Fluka公司提供;甲醇、乙腈(色谱纯):美国Tedia公司;无水硫酸镁(A.R)、氯化钠(A.R);天津化学试剂厂;试验用蒸馏水经0.22μm的微孔滤膜过滤后使用。
1.2 缓冲溶液的配制
不同酸碱度的缓冲液采用重蒸水配制。采用0.05 mol/L的邻苯二甲酸钠、0.025 mol/L的混合磷酸钠和0.01 mol/L的硼砂混合,加入重蒸水后混合均匀,调节溶液的 pH 值依次为4.00、6.86和9.18,待试验用。
1.3 不同水体的采集
所有采集水样分别过中速定性滤纸和0.22μm微孔滤膜后冷藏备用;重蒸水为实验室自制。不同水体的物理参数如表1。
1.4 试验方法
1.4.1 在不同缓冲溶液中的水解试验 在250 mL已灭菌的锥形瓶中加入氯虫苯甲酰胺或氟苯虫酰胺母液(2.5 mL),再加入已配制好的缓冲溶液,使溶液的总体积为100 mL,溶液中氯虫苯甲酰胺或氟苯虫酰胺的最终浓度均为10μg/mL。取10 mL具塞试管,分别准确吸取5 mL的10μg/mL氯虫苯甲酰胺或氟苯虫酰胺水溶液于每支试管中。把试管置于(25±1)℃的培养箱中,定期(0 h、1,3,5,7,9,14,21,28,35 d)采集水样 5 mL,每处理重复 3 次。采集后向溶液分别加入3×5mL二氯甲烷,振荡,提取,合并有机相,经氮气浓缩吹干,乙腈定容到2mL,待检测分析各处理中氯虫苯甲酰胺或氟苯虫酰胺的含量,检测方法参考文献[18-19]。
1.4.2 不同水体的光解试验 在250 mL烧杯中加入氯虫苯甲酰胺、氟苯虫酰胺贮备液(2.5 mL),再加入采自不同地方的水,定容使溶液的总体积为100 mL,此时溶液中氯虫苯甲酰胺、氟苯虫酰胺的最终浓度均为10μg/mL。将装有反应溶液的烧杯移入装有300W高压汞灯的光解箱中进行光照,开启磁力搅拌仪、冷却水和通风扇,反应温度控制在(25±1)℃,定期(0 h、1,3,5,7,9,14,21,28,35 d)采集水样,同时设置黑暗对照,具塞试管中黑暗贮藏。经处理后检测分析不同处理中氯虫苯甲酰胺或氟苯虫酰胺的含量,每处理重复3次。

表1 不同水体的物理参数Tab.1 Properties of different waters
1.5 计算
氯虫苯甲酰胺或氟苯虫酰胺的水解或光解反应动力学方程按一级动力学方程计算:

式中:T1/2为降解半衰期,K为降解速率常数,C0为氯虫苯甲酰胺或氟苯虫酰胺的初始浓度,Ct为t时刻氯虫苯甲酰胺或氟苯虫酰胺的残存浓度。
2 结果与分析
2.1 氯虫苯甲酰胺、氟苯虫酰胺在水体中的添加回收率
水体中氯虫苯甲酰胺的添加回收率分别为82.72%~95.97%,变异系数分别为0.29%~4.00%;水体中氟苯虫酰胺的添加回收率分别为86.15%~95.26%,变异系数分别为0.82%~4.74%(表2)。结果表明,各样本的添加回收率和变异系数在允许范围内,符合农药残留分析的要求。
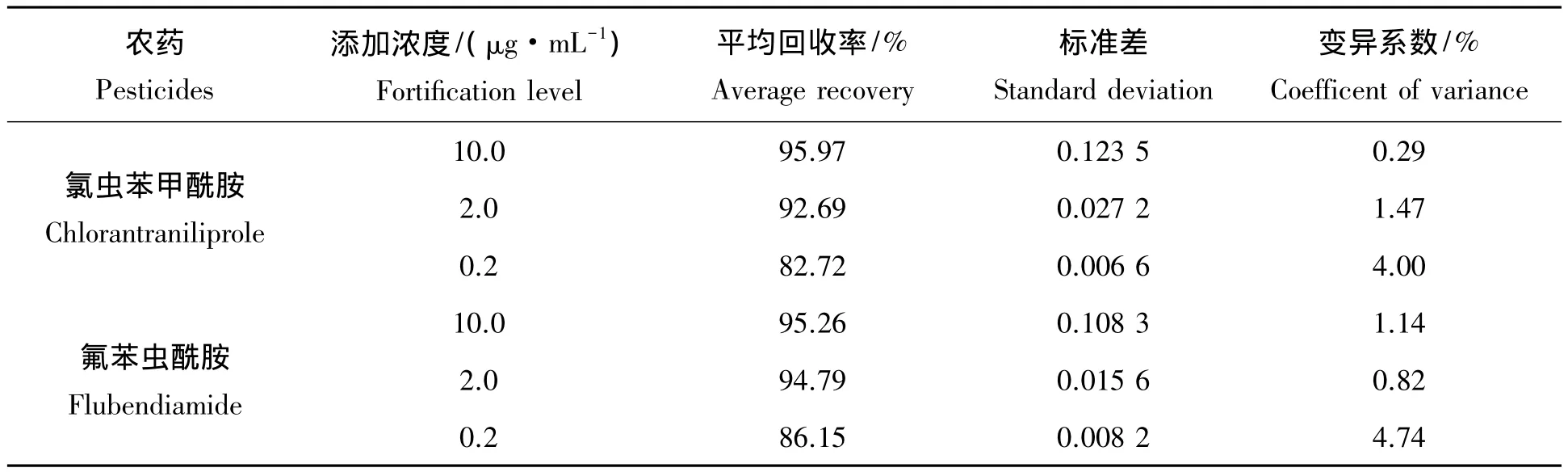
表2 氯虫苯甲酰胺和氟苯虫酰胺在水体中的添加回收率(n=3)Tab.2 The recoveries of ch lorantraniliprole and flubendiam ide from the water

表3 不同缓冲溶液中氯虫苯甲酰胺的降解动力学参数Tab.3 Different degradation kinetic parameters of chlorantraniliprole in different buffer solutions
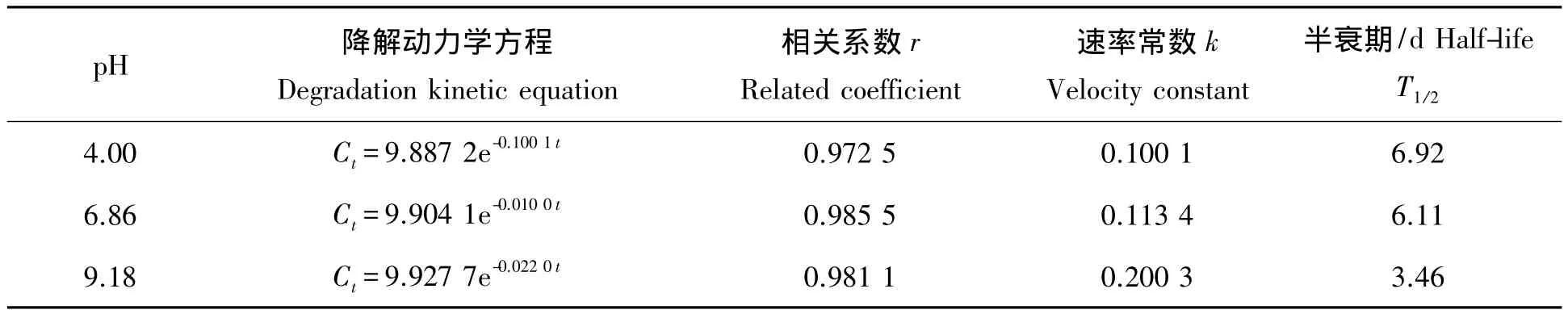
表4 不同缓冲溶液中氟苯虫酰胺的降解动力学参数Tab.4 Different degradation kinetic parameter of flubendiam ide in different buffer solutions
2.2 氯虫苯甲酰胺、氟苯虫酰胺在不同缓冲溶液中的水解
氯虫苯甲酰胺在缓冲溶液中的光解半衰期是 pH 4.00>pH 6.86>pH 9.18,分别为 7.53,7.12,3.89 d(表 3)。氟苯虫酰胺在不同缓冲溶液中的光解半衰期是 pH 4.00>pH 6.86>pH 9.18,分别为 6.92,6.11,3.46 d(表 4)。
2.3 氯虫苯甲酰胺、氟苯虫酰胺在不同水体中的光解
氯虫苯甲酰胺、氟苯虫酰胺在五种类型水中分别进行光解,水溶液中氯虫苯甲酰胺、氟苯虫酰胺的残留浓度均随着光照时间的延长而下降,水解反应符合一级动力学方程。氯虫苯甲酰胺、氟苯虫酰胺在不同自然水体中的光解半衰期由长到短依次是重蒸水、稻田水、水库水、地表水和湖水,氯虫苯甲酰胺的半衰期分别为 4.46,4.07,3.95,3.85,3.55 d(表 5);氟苯虫酰胺的半衰期分别为 3.95,3.74,3.30,3.05,2.96 d(表 6)。
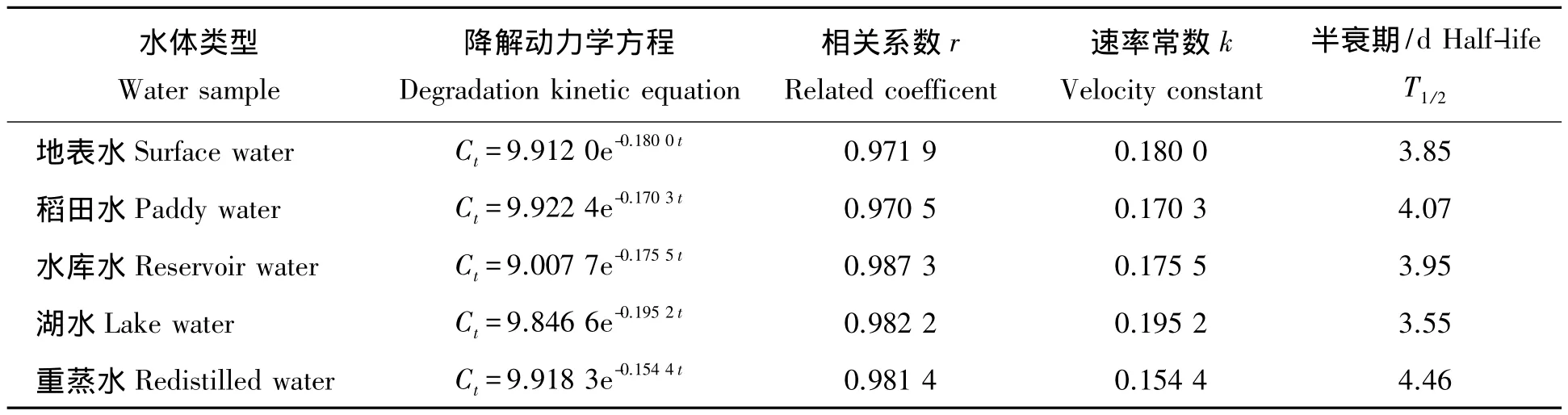
表5 不同水体下氯虫苯甲酰胺的降解动力学参数Tab.5 Different degradation kinetic parameters of chlorantraniliprole in different aquatic environm ents
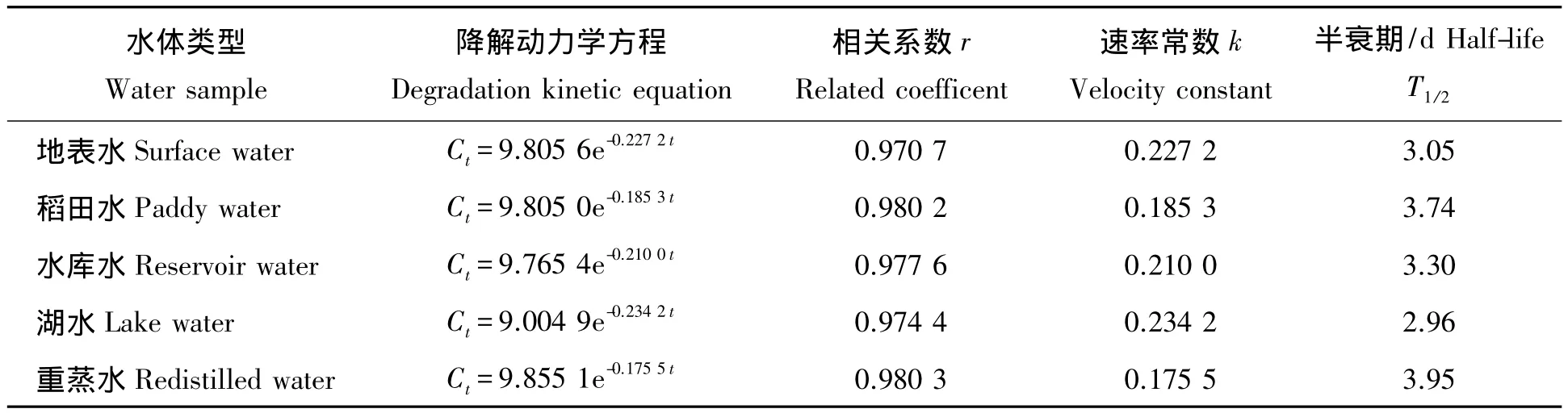
表6 不同水体下氟苯虫酰胺的降解动力学参数Tab.6 Different degradation kinetic parameters of flubendiam ide in different aquatic environments
3 结论与讨论
研究表明氯虫苯甲酰胺、氟苯虫酰胺在水溶液中的降解均遵循一级动力学规律,且降解速率随溶液pH值的变化而变化,光解率随pH值的增加而增大;在高压汞灯照射下,氯虫苯甲酰胺、氟苯虫酰胺在5种不同自然水体中的光解半衰期由长到短依次是重蒸水、稻田水、水库水、地表水和湖水。
一般说来,水溶液的pH值对农药的水解具有一定的影响,农药在水体中的水解动态中,杀虫剂较杀菌剂、除草剂和植物生长调节剂易于发生水解,部分农药可以在pH值为8~9的溶液中水解[20]。溶液的pH值每增加一个单位,水解反应速率将可能增加10倍左右[21]。本研究发现水溶液中氯虫苯甲酰胺、氟苯虫酰胺的降解动态均遵循一级动力学规律,且降解速率随溶液pH值的变化而变化,光解率随pH值的增加而增大。这与相关的文献报道农药在水体中的降解速率与溶液pH值成正相关,pH值越高,降解越快的观点一致[22-25]。
导致氯虫苯甲酰胺、氟苯虫酰胺在不同类型水中光解速度差异的原因可能与水体pH值对氯虫苯甲酰胺、氟苯虫酰胺的存在形态以及水中所含其它物质对光能的吸收与传导影响有关,河水和井水含有较少的有机物质,而无机成分较多,对农药光解的影响复杂,在此种情况下,pH值高的溶液可能更有利于氯虫苯甲酰胺、氟苯虫酰胺光解;纯水中不含其它物质,对光的吸收传导阻碍作用小,但在纯水中农药降解主要为直接光解,反应速度较慢;而稻田水中则含有较为丰富的腐殖质等其它物质,在一定的光波长范围内,对光的吸收与传导产生掩蔽效应,从而使氯虫苯甲酰胺、氟苯虫酰胺的光致降解受阻,光解速度减慢。
[1]Lahm G P,Selby T P,Freudenberger JH,et al.Insecticidalanthranilic diamides:a new class of potent ryanodine receptor activators[J].Bioorganic & Medicinal Chemistry Letters,2005,15(22):4898-4906.
[2]Lahm GP,Cordova D,Barry JD.New and selective ryanodine receptor activators for insect control[J].Bioorganic and Medicinal Chemistry,2009,17(12):4127-4133.
[3]TohnishiM,Nakao H,Furuya T,et al.Flubendiamide,a new insecticide characterized by its novel chemistry and biology[J].PestManagment Science,2005,30:354-360.
[4]柴宝山,林丹,刘远雄,等.新型邻甲酰氨基苯甲酰胺类杀虫剂的研究进展[J].农药,2007,46(3):148-153
[5]柴宝山,杨吉春,刘长令.新型邻苯二甲酰胺类杀虫剂的研究进展[J].精细化工中间体,2007,37(1):1-8
[6]Hoffmann E J,Vandervoort C,Wise JC.Curative activity of insecticides against plum curculio(Coleoptera:Curculionidae)in tartcherries[J].Journal of Economic Entomology,2009,102(5):1864-1873.
[7]Caboni P,Sarais G,Angioni A,et al.Liquid chromatography-tandem mass spectrometric ion-switching determination of chlorantraniliprole and flubendiamide in fruits and vegetables[J].Journal of Agricultural and Food Chemistry,2008,56(17):7696-7699.
[8]步海燕,欧晓明,马俊凯,等.高效液相色谱法测定水体中的氯虫酰胺残留量[J].光谱实验室,2008,25(6):1230-1234.
[9]徐妍,战瑞,马超,等.30%噻虫嗪·氯虫苯甲酰胺悬浮剂高效液相色谱分析[J].农药,2009,48(7):494-495.
[10]秦冬梅,秦旭,孙扬,等.氟虫双酰胺在土壤和白菜中的高效液相色谱分析[J].农药,2009,48(10):755-756.
[11]王广成,吴春先,高立明,等.氯虫苯甲酰胺悬浮剂的高效液相色谱分析[J].农药,2009,48(4):267-269.
[12]Grant J,Rodgers C A,Chickering CD,et al.Determination of chlorantraniliprole residues in crops by liquid chromatography coupled with atmospheric pressure chemical ionization mass spectrometry/mass spectrometry[J].Journal of AOAC International,2010,93(4):1293-1301.
[13]Mohapatra S,Ahuja A K,Deepa M,etal.Persistence and dissipation of flubendiamide and des-iodo flubendiamide in cabbage(Brassica oleracea Linne)and soil[J].Bulletin of Environmental Contamination and Toxicology,2010,85(3):352-356.
[14]秦冬梅,秦旭,徐应明,等.土壤和番茄中氯虫苯甲酰胺的残留检测与消解动态研究[J].农业环境科学学报,2010,29(5):858-863.
[15]刘金凤,朱国念,丁伟,等.超高效液相色谱-串联质谱法分析氟虫双酰胺在稻田生态系统中的消解动态[J].农药学学报,2011,13(3):310-313.
[16]陈小军,王萌,范淑琴,等.QuEChERS前处理结合HPLC-MS/MS法分析氯虫苯甲酰胺在甘蓝和土壤中的残留[J].中国农业科学,2012,45(13):2636-2647.
[17]Chen X J,CuiH R,Fan SQ,etal.Systemicity of chlorantraniliprole in velvetleaf(Abutilon theophrasti)[J].Journal of AOAC International,2013,96(1):1-6.
[18]陈小军,费春,樊丽萍,等.氯虫苯甲酰胺在大豆植株中的内吸传导特性[J].中国农业科学,2011,44(11):2276-2283
[19]Chen X J,Lu C L,Fan SQ,et al.Determination of residual flubendiamide in the cabbage by QuEChERS-high performance liquid chromatography-tandem mass spectrometry[J].Bulletin of Environmental Contamination and Toxicology,2012,89(5):1021-1026.
[20]欧晓明.农药在环境中的水解机理及其影响因子研究进展[J].生态环境,2006,15(6):1352-1359.
[21]刘维屏.农药环境化学[M].北京:化学工业出版社,2006:165-195.
[22]田芹,周志强,江树人,等.毒死蜱在环境水体中降解的研究[J].农业环境科学学报,2005,24(2):289-293.
[23]Dang Q,HirozumiW Junghun O.Effect of pH on the degradation of imidacloprid and fipronil in paddy water[J].Journal of Pesticide Science,2013,38(4),223-227.
[24]Justina E U Crispin JH.Effects of Dissolved Water Constituents on the Photodegradation of Fenitrothion and Diazinon[J].Water Air Soil Pollut,2012,223:655-666.
[25]Georgia G Evaggelia I.Investigation of photodegradation and hydrolysis of selected substituted urea and organophosphate pesticides in water[J].Environmental Science and Pollution Research,2011,18:949-957.
