2009—2013年全国抗结核药物敏感性试验熟练度测试分析
2015-05-20宋媛媛赵冰夏辉赵雁林
宋媛媛 赵冰 夏辉 赵雁林
·论著·
2009—2013年全国抗结核药物敏感性试验熟练度测试分析
宋媛媛 赵冰 夏辉 赵雁林
目的 评价和分析2009—2013年全国抗结核药物敏感性试验(简称“药敏试验”)熟练度测试结果,改善我国结核病实验室药敏试验能力。 方法 2009—2013年对全国有能力开展药敏试验的省级、地市级508个结核病实验室每年寄发30株Mtb菌株进行8种抗结核药物[异烟肼(H)、链霉素(S)、乙胺丁醇(E)、利福平(R)、卡那霉素(Km)、阿米卡星(Am)、卷曲霉素(Cm)、氧氟沙星(Ofx)]的药敏试验熟练度测试,药敏试验方法采用WHO推荐的基于罗氏培养基的比例法。共计收到508个实验室报告的一线抗结核药物药敏试验熟练度测试结果,445个实验室报告的二线抗结核药物药敏试验熟练度测试结果。结果统一由国家结核病参比实验室进行比对。评价指标为敏感度、特异度、重复性和一致性。2009—2013年各指标差异采用卡方检验,变化趋势采用Cochran-Armitage趋势检验,以P<0.05为差异有统计学意义。结果 对于各个药物总敏感度、总特异度、总重复性和总一致性的范围是:H:91.88%~97.62%、92.01%~98.33%、86.55%~95.27%和91.40%~97.60%;S:88.79%~94.14%、87.59%~91.36%、77.37%~93.13%和88.20%~92.45%;E:66.24%~85.17%、83.22%~97.87%、63.46%~89.76%和75.78%~90.80%;R:78.54%~96.34%、96.19%~98.07%、79.11%~95.66%和90.72%~97.21%;Km:81.12%~95.46%、95.35%~98.86%、94.12%~96.84%和90.23%~97.77%;Am:93.14%~98.94%、96.16%~99.00%、93.52%~97.94%和95.59%~98.19%;Cm:52.45%~95.68%、89.68%~97.85%、89.48%~92.99%和89.08%~95.61%;Ofx:84.75%~94.38%、96.21%~98.90%、88.01%~94.41%和93.01%~96.90%。除S的总特异度、Km和Cm的总重复性每年差异无统计学意义外(χ2值分别为8.49、4.1和7.78,P值均>0.05),各个药物的总敏感度每年差异有统计学意义(H:χ2=134.76;S:χ2=44.12;E:χ2=266.22;R:χ2=256.35;Km:χ2=197.46;Am:χ2=12.16;Cm:χ2=433.50;Ofx:χ2=47.38,P值均<0.05);其他各个药物的总特异度每年差异有统计学意义(H:χ2=67.69;E:χ2=439.39;R:χ2=16.61;Km:χ2=94.97;Am:χ2=52.96;Cm:χ2=139.51;Ofx:χ2=11.66,P值均<0.05);其他各个药物的总重复性每年差异有统计学意义(H:χ2=61.82;S:χ2=127.15;E:χ2=246.49;R:χ2=180.03;Am:χ2=21.65;Ofx:χ2=28.49,P值均<0.05);各个药物的总一致性每年差异有统计学意义(H:χ2=162.05;S:χ2=36.58;E:χ2=369.11;R:χ2=152.30;Km:χ2=233.69;Am:χ2=32.55;Cm:χ2=168.79;Ofx:χ2=36.97,P值均<0.05)。除Am、Cm的总敏感度,Ofx的总特异度,Km、Am、Cm的总重复性逐年趋势检验无统计学意义外(Z值分别为0.46、0.99、-0.30、-0.85、0.09和-0.27,P值均>0.05),其他各个药物总敏感度呈逐年提高趋势,趋势检验有统计学意义(H:Z=-11.06;S:Z=-6.39;E:Z=-12.39;R:Z=-11.17;Km:Z=-12.60;Ofx:Z=-4.40,P值均<0.05);其他各个药物总特异度呈逐年提高趋势,趋势检验有统计学意义(H:Z=-3.85;S:Z=-2.14;E:Z=-12.30;R:Z=-3.31;Km:Z=-5.05;Am:Z=-5.43;Cm:Z=-8.90,P值均<0.05);其他各个药物总重复性呈逐年提高趋势,趋势检验有统计学意义(H:Z=-5.36;S:Z=-9.11;E:Z=-7.76;R:Z=-8.52;Ofx:Z=-3.44,P值均<0.05);各个药物总一致性呈逐年提高趋势,趋势检验有统计学意义(H:Z=-10.95;S:Z=-5.95;E:Z=-11.87;R:Z=-9.70;Km:Z=-14.11;Am:Z=-3.32;Cm:Z=-5.71;Ofx:Z=-3.40,P值均<0.05)。结论 开展熟练度测试工作是提高药敏试验能力的有效方法,对于提高我国结核病实验室药敏试验能力具有很大贡献。长期连续的做好实验室内部质量控制并开展药敏试验培训和熟练度测试工作可使全国结核病实验室药敏试验能力逐年提高。
分枝杆菌, 结核; 微生物敏感性试验; 敏感性与特异性
结核病耐药率是结核病防治工作中的一项有价值指标,为此1994年WHO与国际防痨和肺病联合会(The Union)制定了全球结核病耐药性监测规程,其目的是可以对从世界各国收集的耐药监测信息进行有效的比较和分析,从而获得全球结核病耐药数据,有效控制耐药结核病。可靠的抗结核药物敏感性试验(简称“药敏试验”)是获得准确可比的耐药数据的前提条件,因此,WHO与国际防痨和肺部疾病联合会同年在全球正式成立了跨国结核病参比实验室,作用是对实施结核病耐药性监测(调查)工作的国家提供技术援助和质量控制[1]。
从1996 年至今我国22个省(直辖市、自治区)参加了WHO开展的耐药监测工作, 省级结核病参比实验室同时接受了药敏试验培训和跨国结核病参比实验室的药敏试验熟练度测试。为进一步评估全国结核病实验室药敏试验能力, 并对耐药结核病诊断提供质量保证,2005年我国逐步对部分省级结核病实验室开展比例法的药敏试验熟练度测试。从2008 年开始正式在全国范围内进行比例法的药敏试验熟练度测试,在进行药敏试验操作前实验室工作人员都接受了系统的培训。现将2009—2013年全国抗结核药物药敏试验熟练度测试结果进行分析。
材料和方法
一、参与实验室
2009—2013年共计收到508个实验室报告的一线抗结核药物药敏试验熟练度测试结果,445个实验室报告的二线抗结核药物药敏试验熟练度测试结果。每年参与药敏试验熟练度测试的实验室数量见表1。
二、Mtb菌株来源
熟练度测试菌株由30株Mtb菌株构成,其中10株为重复株。菌株来源于我国香港跨国结核病参比实验室,测试时间为4个月。每年给省、地市级实验室发放的测试菌株中耐药菌株数见表2。
三、菌株准备及运输
将Mtb接种于2 ml含罗氏培养基的冻存管中,按照《可感染人类的高致病性病原微生物菌(毒)种或样本运输管理规定》[2]采用航空或陆路的运输方式进行菌株运输。
四、药敏试验方法
所有实验室都采用基于固体罗氏培养基的比例法进行药敏试验,在培养基中各药物终浓度分别为异烟肼(H)0.2 μg/ml、链霉素(S)4 μg/ml、乙胺丁醇(E)2 μg/ml、利福平(R)40 μg/ml、卡那霉素(Km)30 μg/ml、阿米卡星(Am)30 μg/ml、卷曲霉素(Cm)40 μg/ml、氧氟沙星(Ofx)2 μg/ml。个别实验室根据药物浓度自行配制培养基,国家结核病参比实验室统一配发Sigma公司药物纯粉,并告知各药物效价。大多数实验室采购符合要求浓度的商品化培养基。
五、数据分析
分析药敏试验熟练度测试结果的敏感度、特异度、重复性和一致性。各指标含义解释如下:(1)敏感度:实验室检出的耐药菌株占真正耐药菌株数的百分率,反映实验室检出真正耐药的能力;(2)特异度:实验室检出的敏感菌株占真正敏感菌株数的百分率,反映实验室检出真正敏感的能力;(3)重复性:实验室检出正确的重复菌株数占真正重复菌株数的百分率,反映技术员误差或者实验室系统误差;(4)一致性:实验室检出正确结果菌株数占总菌株数的百分率,反映实验室整体检测能力。其中一致性是评价实验室药敏试验能力的重要指标。药敏试验合格的实验室H、R、Km、Am、Cm、Ofx的一致性应达到90%;S和E的一致性应达到80%。国家结核病参比实验室收集药敏试验测试结果并统一与标准结果进行比对。2009—2013年各指标差异比较采用R×2表资料卡方检验,P<0.05认为差异有统计学意义。各指标值变化趋势采用Cochran-Armitage 趋势检验,P<0.05认为差异有统计学意义。2009—2013年总敏感度、总特异度、总重复性和总一致性含义举例说明:2009年H总敏感度指标计算方法是将2009年参与药敏试验的30个实验室H药物的敏感度指标的分母(每个实验室真正耐药菌株数)进行加和,分子(每个实验室检出耐药菌株数)进行加和,分子除以分母×100%得出。
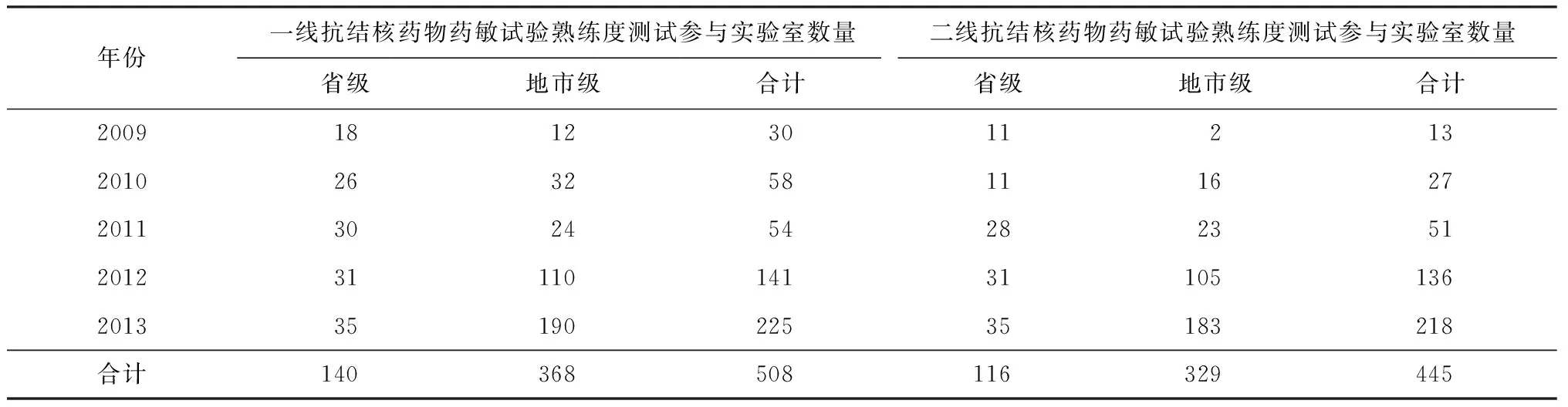
表1 2009—2013年省、地市级室验室参与一、二线抗结核药物药敏试验熟练度测试情况(个)

表2 2009—2013年30株测试菌株中耐不同药物菌株数
注 H=异烟肼;S=链霉素;E=乙胺丁醇;R=利福平;Km=卡那霉素;Am=阿米卡星;Cm=卷曲霉素;Ofx=氧氟沙星
六、质量控制
(1)国家结核病参比实验室为每个实验室准备的菌株都有一套独立编号,以保证盲法对各个实验室进行测试。(2)国家结核病参比实验室统一时间段通过陆路或航空方式按照国家规定进行菌株运输工作。(3)国家结核病参比实验室统一规定药敏试验方法及各药物浓度。(4)国家结核病参比实验室统一配发Sigma公司药物纯粉,并告知各药物效价。(5)参加测试的实验室统一将最终药敏试验结果(敏感或耐药)报告给国家结核病参比实验室。各实验室进行药敏试验熟练度测试的同时需做一株Mtb标准菌株H37Rv进行对照试验。
七、伦理学解释
此研究不涉及人体试验,不需要伦理学审查,在药敏试验过程中患者信息不公开。
结 果
一、2009—2013年药敏试验熟练度测试结果分析
图1为2009—2013年药敏试验熟练度测试的总敏感度、总特异度、总重复性、总一致性的折线图,表3为不同药物2009—2013年药敏试验熟练度测试总敏感度、总特异度、总重复性、总一致性的差异性检验和趋势性检验值,对各个药物的各个指标结果分别分析如下。
H 2009—2013年药敏试验熟练度测试结果总敏感度范围是91.88%~97.62%,总特异度范围是92.01%~98.33%,总重复性值范围是86.55%~95.27%,总一致性范围是91.40%~97.60%,5年中各指标差异有统计学意义(P<0.01)。2010年各指标值最低。各指标呈逐年提高趋势,趋势检验有统计学意义(P<0.01)。
S 2009—2013年药敏试验熟练度测试结果总敏感度范围是88.79%~94.14%,总特异度范围是87.59%~91.36%,总重复性范围是77.37%~93.13%,总一致性范围是88.20%~92.45%,5年中除特异度外各指标差异均有统计学意义(P<0.01)。2009年和2010年重复性值明显偏低,分别为79.19%、77.37%。各指标呈逐年提高趋势,趋势检验有统计学意义(P<0.05)。
E 2009—2013年药敏试验熟练度测试结果总敏感度范围是66.24%~85.17%,总特异度范围是83.22%~97.87%,总重复性范围是63.46%~89.76%,总一致性范围是75.78%~90.80%,5年中各指标差异均有统计学意义(P<0.01)。2011年总特异度、总重复性、总一致性最低。2013年总敏感度、总特异度、总一致性值最高。各指标呈逐年提高趋势,趋势检验有统计学意义(P<0.01)。
R 2009—2013年药敏试验熟练度测试结果总敏感度范围是78.54%~96.34%,总特异度范围是96.19%~98.07%,总重复性范围是79.11%~95.66%,总一致性范围是90.72%~97.21%,5年中各指标差异均有统计学意义(P<0.01)。2010年总敏感度、总重复性、总一致性最低。2013年各指标值最高,各指标呈逐年提高趋势,趋势检验有统计学意义(P<0.01)。
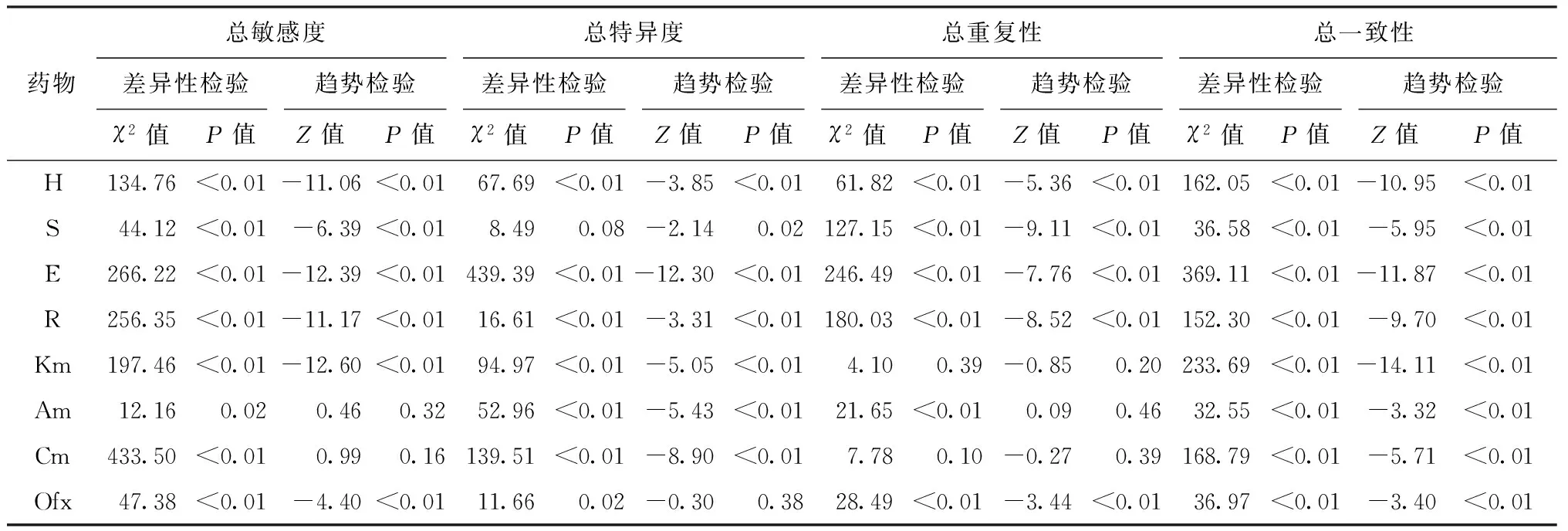
表3 不同药物2009—2013年药敏试验熟练度测试总敏感度、总特异度、总重复性、总一致性的差异性检验和趋势性检验结果
注 H=异烟肼;S=链霉素;E=乙胺丁醇;R=利福平;Km=卡那霉素;Am=阿米卡星;Cm=卷曲霉素;Ofx=氧氟沙星
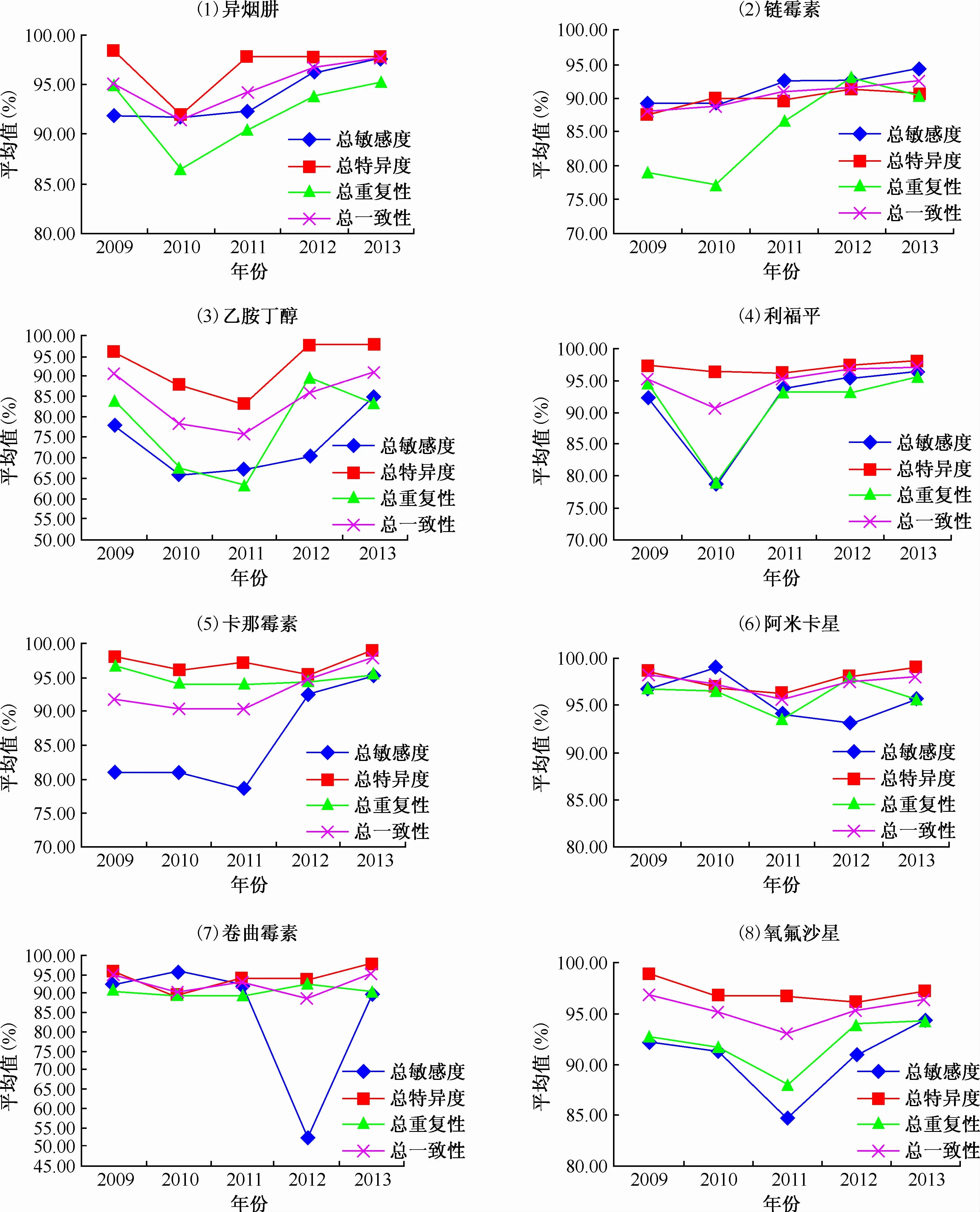
图1 2009—2013年药敏试验总敏感度、总特异度、总重复性和总一致性结果
Km 2009—2013年药敏试验熟练度测试结果总敏感度范围是81.12%~95.46%,总特异度范围是95.35%~98.86%,总重复性范围是94.12%~96.84%,总一致性范围是90.23%~97.77%,5年中除总重复性外各指标差异均有统计学意义(P<0.01)。总一致性、总敏感度、总特异度呈逐年提高趋势,趋势检验有统计学意义(P<0.01)。
Am 2009—2013年药敏试验熟练度测试结果总敏感度范围是93.14%~98.94%,总特异度范围是96.16%~99.00%,总重复性范围是93.52%~97.94%,总一致性范围是95.59%~98.19%,5年中各指标差异均有统计学意义(P<0.05)。总一致性和总特异度呈逐年提高趋势,趋势检验有统计学意义(P<0.01)。
Cm 2009—2013年药敏试验熟练度测试结果总敏感度范围是52.45%~95.68%,总特异度范围是89.68%~97.85%,总重复性范围是89.48%~92.99%,总一致性范围是89.08%~95.61%,5年中除总重复性外各指标差异均有统计学意义(P<0.01)。2012年Cm的总敏感度最低。总一致性和总特异度呈逐年提高趋势,趋势检验有统计学意义(P<0.01)。
Ofx 2009—2013年药敏试验熟练度测试结果总敏感度范围是84.75%~94.38%,总特异度范围是96.21%~98.90%,总重复性范围是88.01%~94.41%,总一致性范围是93.01%~96.90%,5年中各指标差异均有统计学意义(P<0.05)。2011年总敏感度、总重复性、总一致性值最低。总一致性、总重复性、总敏感度呈逐年提高趋势,趋势检验有统计学意义(P<0.01)。
二、2009—2013年药敏试验熟练度测试一致性情况分析
在2009—2013年药敏试验熟练度测试工作中,参与一线抗结核药物药敏试验的实验室数量是508个;参与二线抗结核药物药敏试验的实验室数量是445个,但由于其中9个实验室没有报告Cm的药敏试验结果,因此Cm一致性结果为436个。不同药物一致性结果在不同范围内的实验室数量见表4。
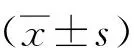
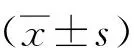
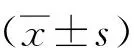
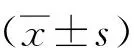
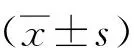
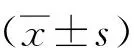
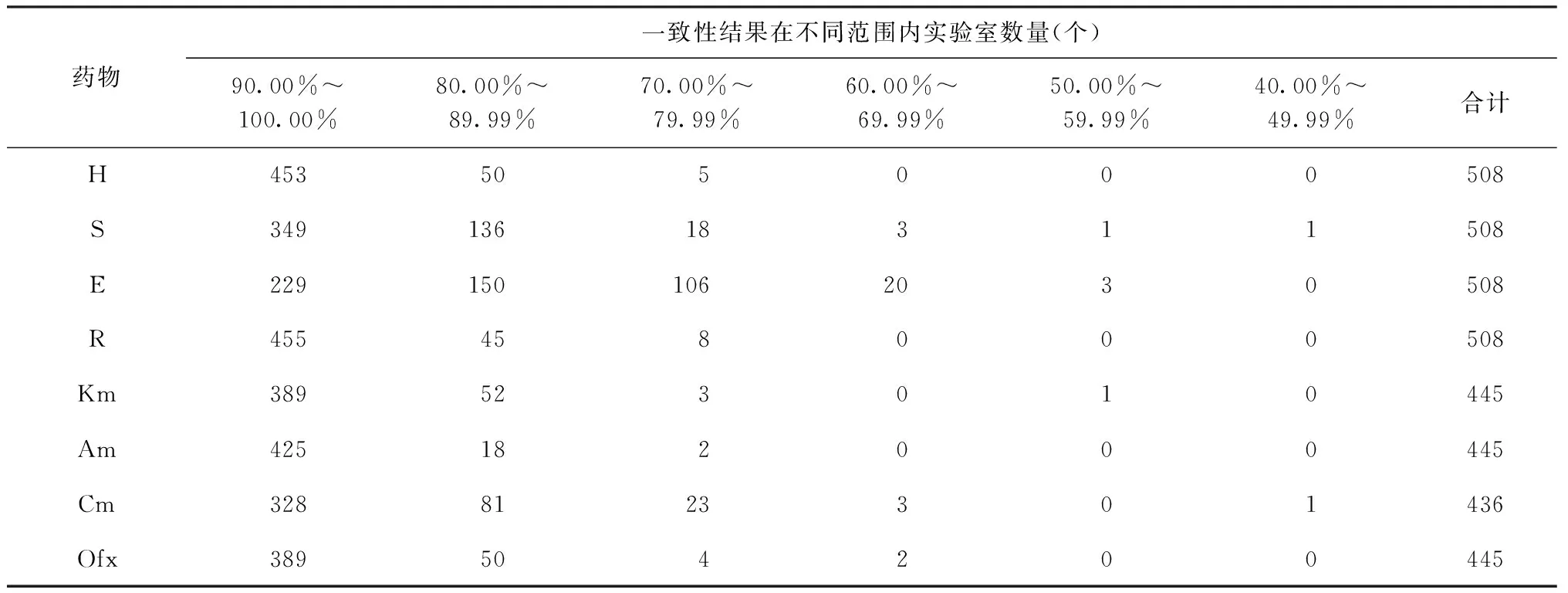
表4 2009—2013年不同药物一致性结果在不同范围内的实验室数量
注 H=异烟肼;S=链霉素;E=乙胺丁醇;R=利福平;Km=卡那霉素;Am=阿米卡星;Cm=卷曲霉素;Ofx=氧氟沙星
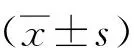
讨 论
药敏试验结果的差异性取决于实验人员操作的准确性及培养基中所需药物的浓度和效价[3]。因此药敏试验实验室内部质量控制至关重要,国际上有些国家熟练度测试结束后都会集中开会讨论药敏试验失败原因并查找试验中出现的问题,以达到提高质量的目的[4-6]。目前,我国药敏试验熟练度测试结束后,对于不合格的实验室是通过电话询问查找失败原因。因此,建议每年全国结核病参比实验室主任会议增加对药敏试验熟练度测试工作的总结与交流,以更好地提高我国实验室药敏试验的质量。为达到更好的实验室内部质量控制,在开展药敏试验熟练度测试之前国家结核病参比实验室推荐各实验室使用基于固体罗氏培养基的比例法进行药敏试验,并推荐了各种药物浓度。对于自己配置培养基的实验室,国家结核病参比实验室统一配发Sigma公司生产的药物纯粉,并告知各药物效价。
图1表现出在2009年各指标值相比其他年较高,一方面这与其中7个省级结核病参比实验室都参与过WHO开展的耐药监测工作,并多次参与其开展的药敏试验熟练度测试工作有关[7-10];另一方面2009年参加熟练度测试的实验室中省级实验室参加的比例较高(60.00%,18/30),省级实验室药敏试验的经验非常丰富,因此各个指标值比较高。总体看来,2009—2013年各指标数值呈逐年提高趋势,反映了全国结核病实验室药敏试验能力逐年提高。说明各个实验室经过连续的药敏试验熟练度测试后积累了一定经验,并且在这几年中随着在全国开展耐药监测工作,以及中国全球基金结核病项目、中华人民共和国卫生部-盖茨基金会结核病防治合作项目等工作,各个实验室接受培训和督导的机会增加,为提高实验室能力奠定了基础。另外国家结核病参比实验室菌株接收、传代、发放工作更趋于完善,也是各项指标逐年提高的重要保证。
在2012年Cm的总敏感度为52.45%,这与菌株设置(耐药/敏感)有关,在2012年耐Cm药物的菌株数为3株,如果有1株耐药检出错误,则敏感度为66.67%(2/3),这无形中降低了Cm的检出敏感度。因此,也提示组织药敏试验熟练度测试的实验室在准备测试菌株时除了要注意菌株的稳定性外,对于耐药菌株的数量也应引起重视,WHO和国际防痨和肺病联合会推荐测试菌株中每种药物应包含50%的耐药菌株[11]。
一致性是评价实验室药敏试验能力的重要指标[4],从2009—2013年一致性结果中看出,各个药物仍然有不同程度的不合格比例,其中S和Am不合格比例较低,E和Cm不合格比例较高,其他4种药物不合格比例在10.43%~12.58%之间。一方面这可能与S合格线设置较低,Cm合格线设置较高有关。另外,药物的不稳定性可能造成培养基中药物终浓度不准确,药敏试验过程中实验人员比浊1麦氏浓度不准确、接种量控制不好、判读结果方法掌握不好也是造成不合格的重要原因。这提示需要审视设置合格线是否科学合理,并且需要连续不断加强实验室内部质量控制及督导培训工作。
据文献 [4-5,12-13]报道,各一线药物的一致性合格线一般设定为:H为89%~95%、R为90%~95%、S和E为80%~90%。对于2009—2013年各药物的总一致性都达到了我国最初设定的合格线;如果对最初设定的合格线进行改进,按照Laszlo等[13]提到的“一般设定合格线应在总一致性的基础上减去一个标准差”,则根据2009—2013年总一致性、标准差通过计算得出:H、S、E、R、Km、Am、Cm、Ofx的一致性合格线分别为90.93%、84.70%、76.37%、90.84%、90.06%、93.70%、85.61%、90.21%。如果按此合格线看,E和Cm的不合格比例会减少。总体看各个药物的合格线与最初设定的数值差别不大,因此在今后的熟练度测试工作中可继续使用我国最初设定的合格线,即H、R、Km、Am、Cm、Ofx的一致性应达到90%,S和E的一致性应达到80%。本研究没有讨论关于设定重复性、敏感度、特异度各指标合格线的过程,但方法也类似于设定一致性合格线的过程。由于每年的菌株数和重复数是固定的,因此笔者建议一致性和重复性的合格线每年可以固定。但是,由于每年耐药菌株数不同,因此敏感度和特异度的合格线应该根据当年做药敏试验熟练度测试>3次且能力较稳定的实验室各指标所得总体值减1个标准差来定。
另外,我国大陆目前测试菌株均来自我国香港跨国结核病参比实验室,在时间上有一定局限性。为了更好、更快地提高我国省级、地市级结核病实验室药敏试验能力,我国大陆将来应是朝着自己制备药敏试验熟练度测试菌株的方向发展,需要对此做进一步研究。
提高结核病实验室药敏试验能力不是通过简单的督导、培训或者短期内1~2次的药敏试验熟练度测试就能实现的,连续开展药敏试验培训和熟练度测试可以使全国结核病实验室药敏试验能力得到逐年提高。因此,需要长期、连续地做好实验室内部质量控制,并开展药敏试验培训和熟练度测试工作,以达到质量的持续提高。
志谢 感谢全国省级、地市级结核病实验室对全国抗结核药物药敏试验熟练度测试工作的支持和辛勤工作!
[1] World Health Organization.Guidelines for surveillance of drug resistance in tuberculosis.WHO/TB/94.178. Geneva: WHO, 1994.
[2] 中华人民共和国卫生部.可感染人类的高致病性病原微生物菌(毒) 种或样本运输管理规定.中华人民共和国卫生部公报, 2006,2:1-6.
[3] Kim SJ. Drug-susceptibility testing in tuberculosis: methods and reliability of results. Eur Respir J,2005,25(3):564-569.
[4] Jou R,Chiang CY,Yu CY,et al. Proficiency of drug susceptibility testing forMycobacteriumtuberculosisin Taiwan. Int J Tuberc Lung Dis,2009,13(9):1142-1147.
[5] Shulgina MV,Malakhov VN,Hoffner SE,et al.Results of the external quality assessment ofMycobacteriumtuberculosisdrug susceptibility testing in Russia, 2005—2007. Int J Tuberc Lung Dis,2009,13(10):1294-1300.
[6] Wu MH,Chiang CY,Deng YM,et al.Proficiency of drug susceptibility testing forMycobacteriumtuberculosisin Taiwan, 2007—2011. Int J Tuberc Lung Dis,2013,17(1):113-119.
[7] World Health Organization.The WHO/IUATLD global project on anti-tuberculosis drug resistance surveillance. WHO/TB/97.229.Geneva:World Health Organization,1997.
[8] World Health Organization.The WHO/IUATLD global project on anti-tuberculosis drug resistance surveillance. WHO/CDC/TB/2000.278.Geneva:World Health Organization,2000.
[9] World Health Organization.The WHO/IUATLD global project on anti-tuberculosis drug resistance surveillance.WHO/HTM/TB/2004.343. Geneva: World Health Organization,2004.
[10] World Health Organization. The WHO/IUATLD global project on anti-tuberculosis drug resistance surveillance. WHO/HTM/TB/2008.394.Geneva: World Health Organization,2008.
[11] Van Deun A,Wright A,Zignol M,et al. Drug susceptibility testing proficiency in the network of supranational tuberculosis reference laboratories. Int J Tuberc Lung Dis, 2011,15(1):116-124.
[12] Bai GH,Kim SJ,Chang CL.Proficiency analysis of drug susceptibility testing by national-level tuberculosis reference laboratories from 1995 to 2003. J Clin Microbiol,2007,45(11):3626-3630.
[13] Laszlo A,Rahman M,Espinal M,et al. Quality assurance programme for drug susceptibility testing ofMycobacteriumtuberculosisin the WHO/IUATLD Supranational Reference Laboratory Network: five rounds of proficiency testing, 1994—1998. Int J Tuberc Lung Dis,2002,6(9):748-756.
(本文编辑:范永德)
Analysis of anti-tuberculosis drug susceptibility proficiency test 2009—2013 in China
SONG Yuan-yuan, ZHAO Bing, XIA Hui, ZHAO Yan-lin.
National Tuberculosis Reference Laboratory, National Center for Tuberculosis Control and Prevention, Chinese Center for Disease Control and Prevention,Beijing 102206, China
ZHAO Yan-lin, Email: zhaoyanlin@chinatb.org
Objective To evaluate and analyze the results of nationwide anti-tuberculosis drug susceptibility proficiency testing from 2009 to 2013, and improve the capability of tuberculosis laboratories in China. Methods Natio-nal tuberculosis reference laboratory issued 30Mycobacteriumtuberculosisisolates for the DST to each participating laboratories yearly from 2009 to 2013. The laboratories performed DST for isoniazid(H), streptomycin(S), ethambutol(E), rifampicin(R), kanamycin(Km), amikacin(Am), capreomycin(Cm) and ofloxacin (Ofx) using the proportion method in Löwenstein-Jensen medium, the World Health Organization guideline was strictly followed. All 508 laboratories participated the proficiency testing and reported the results of first line DST, and 445 laboratories reported the results of second line DST. The reported results were checked and compared with the judicial results by national tuberculosis reference laboratory. The evaluation index is sensitivity, specificity, reproducibility and efficiency. The Chi-square test was be used to analyze the results, and the Cochran-Armitage trend test was be used to describe the trend results, significant difference was defined asP<0.05. Results The overall value of sensitivity, specificity, reproducibility and efficiency for each drug was respectively as following: H: 91.88%-97.62%, 92.01%-98.33%, 86.55%-95.27% and 91.40%-97.60%;S: 88.79%-94.14%, 87.59%-91.36%, 77.37%-93.13% and 88.20%-92.45%;E:66.24%-85.17%, 83.22%-97.87%, 63.46%-89.76% and 75.78%-90.80%;R: 78.54%-96.34%, 96.19%-98.07%, 79.11%-95.66% and 90.72%-97.21%;Km: 81.12%-95.46%, 95.35%-98.86%, 94.12%-96.84% and 90.23%-97.77%;Am: 93.14%-98.94%, 96.16%-99.00%, 93.52%-97.94% and 95.59%-98.19%;Cm:52.45%-95.68%, 89.68%-97.85%, 89.48%-92.99% and 89.08%-95.61%;Ofx: 84.75%-94.38%, 96.21%-98.90%, 88.01%-94.41% and 93.01%-96.90%. Except for the specificity of S, reproducibility of Km and Cm was not statistically significant difference between each year(χ2value of 8.49, 4.1, 7.78, respectively,P>0.05),the difference of overall sensitivity for each drug between each year was statistically significant(H:χ2=134.76;S:χ2=44.12;E:χ2=266.22;R:χ2=256.35;Km:χ2=197.46;Am:χ2=12.16;Cm:χ2=433.50;Ofx:χ2=47.38,P<0.05); the difference of overall specificity for other drug between each year was statistically significant(H:χ2=67.69; E:χ2=439.39;R:χ2=16.61;Km:χ2=94.97;Am:χ2=52.96;Cm:χ2=139.51;Ofx:χ2=11.66,P<0.05);the difference of overall reproducibility for other drug between each year was statistically significant(H:χ2=61.82;S:χ2=127.15;E:χ2=246.49;R:χ2=180.03;Am:χ2=21.65;Ofx:χ2=28.49,P<0.05); the difference of overall efficiency for each drug between each year was statistically significant(H:χ2=162.05;S:χ2=36.58;E:χ2=369.11;R:χ2=152.30;Km:χ2=233.69;Am:χ2=32.55;Cm:χ2=168.79;Ofx:χ2=36.97,P<0.05). While, except for the overall sensitivity of Am and Cm, the overall specificity of Ofx and the overall reproducibility of Km, Am and Cm(Z value of 0.46, 0.99, -0.30, -0.85, 0.09 and -0.27, respectively,P>0.05), the overall sensitivity for other drug showed a trend of increase by year (H:Z=-11.06;S:Z=-6.39;E:Z=-12.39;R:Z=-11.17;Km:Z=-12.60;Ofx:Z=-4.40,P<0.05);the overall specificity for other drug showed a trend of increase by year(H:Z=-3.85;S:Z=-2.14;E:Z=-12.30;R:Z=-3.31;Km:Z=-5.05;Am:Z=-5.43;Cm:Z=-8.90,P<0.05); the overall reprodu-cibility for other drug showed a trend of increase by year(H:Z=-5.36;S:Z=-9.11;E:Z=-7.76;R:Z=-8.52;Ofx:Z=-3.44,P<0.05);the overall efficiency for each drug showed a trend of increase by year (H:Z=-10.95;S:Z=-5.95;E:Z=-11.87;R:Z=-9.70;Km:Z=-14.11;Am:Z=-3.32;Cm:Z=-5.71;Ofx:Z=-3.40,P<0.05). Conclusion Proficiency testing was an efficient method to improve the capacity and performance of DST, PT has made a great contribution to increase the ability of DST in Chinese TB laboratory network, and continuously conducting the laboratory internal quality control and carrying out personnel training to perform proficiency testing could increase the laboratory capabilities of DST year by year.
Mycobacteriumtuberculosis; Microbial sensitivity tests; Sensitivity and specificity
10.3969/j.issn.1000-6621.2015.02.007
102206 北京,中国疾病预防控制中心结核病预防控制中心 国家结核病参比实验室
赵雁林,Email:zhaoyanlin@chinatb.org
2014-08-17)
