Sysmex血凝仪在冷沉淀质量检测中的应用
2015-05-10秦艳兰叶柱江何子毅
秦艳兰,叶柱江,何子毅
(东莞市中心血站,广东 东莞523930)
冷沉淀制品含FⅧ 、纤维蛋白原、血管性血友病因子、和纤维结合蛋白。临床上主要用于血友病A、血管性血友病及纤维蛋白原、因子XⅢ或纤维结合蛋白量的减少或质的缺陷引起出血的患者,期望通过补充外源性的凝血因子达到止血的目的
[1]。目前冷沉淀产品的质量检测主要是依靠全自动血凝仪,由于血凝仪检测的凝血因子Ⅷ属因子活性或时间检测,定量参数较少,检测项目的影响因素多,再加上试验未标准化,缺乏国际公认的标准品和参考方法,其影响因素具有特殊性。当其启动因子被某些因素激活后,就会发生一系列连锁反应,导致检测结果的极大误差。为了保证检测质量,在每一次检测时确保仪器性能处于良好状态显得至关重要。为了探讨本血站现有的采供血模式所制备的冷沉淀的质量是否符合 《全血及成分血质量要求》(GB18469-2012),在确保仪器性能良好的状态下检测了97份冷沉淀产品,对其中的因子Ⅷ 、纤维蛋白原含量进行了检测和分析,现将其结果报道如下。
1 材料与方法
1.1 评价样品 西门子公司正常定值血浆 (批号503174)Ⅷ含量:靶值 100%,范围80%~120%;纤维蛋白原(Fg)含量:靶值2.4g/L,范围 1.9~2.9g/L;低值定值血浆(批号509946)Ⅷ含量:靶值31%,范围23%~39%;纤维蛋白原(Fg)含量:靶值1.0g/L,范围0.6~1.4g/L。
1.2 抽检样品 献血服务科按《献血者健康检查要求》(GB18467-2011)采集自愿无偿献血者血液,抗-HCV、HBsAg、抗-HIV、梅毒抗体和转氨酶(ALT)检测合格,成分制备组用虹吸法制备的冷沉淀。
1.3 仪器与试剂 Sysmex血凝仪CA-500 (日本),活化部分凝血活酶时间测定试剂 (APTT批号R2011),乏Ⅷ因子血浆 (批号 546572),CaCl2试剂(批号 R3001), Fg 试剂(批号 R3003),定标血浆 Ⅷ因子含量97%,Fg含量2.45g/L(批号503227A)试剂全部为西门子公司出品,在实验过程中严格按试剂说明书操作。
1.4 方法
1.4.1 精密度评价 根据NCCLSEP15-A文件对精密度评价的要求,批内精密度:取一个正常水平的定值质控血浆和一个低值水平的定值质控血浆,复溶后按仪器的操作规程连续重复分别测定Ⅷ和Fg20次,计算平均值(x),标准差(SD)及变异系数(CV),CV<5%为精密度符合要求。批间精密度 :取复溶后的正常水平的定值质控血浆和低值水平的定值质控血浆,每天上午下午各测定1次,连续10d,分别计算其平均值(x),标准差(SD)及变异系数(CV),判断标准CV<5%为批间精密度符合要求。
1.4.2 准确度评价 取一个正常水平的定值质控血浆和一个低值水平的定值质控血浆,分别测定Ⅷ和Fg含量,在血凝仪上重复检测 20次 ,分别计算其均值然后和各自的靶值进行比较观察其一致性、其偏差是否在允许范围内[2]。
1.4.3 标准曲线的建立 在确认仪器的精密度和准确度符合要求的情况下,用定标血浆按仪器要求和操作说明书制作以X轴为活性(浓度),Y轴为凝固时间(反应速度)的标准曲线。
1.4.4 室内质控图的建立和应用 在本实验室常规条件下,对同一批号正常水平的定值质控血浆按操作说明书分别连续测定其Ⅷ和Fg20次,获取Ⅷ和Fg二组数据,分别计算其均值x和标准差SD,以此数据建立Ⅷ和Fg质控框架图。在以后的样品检测中用该质控品随样品一同检测,并将测得的质控值点入质控框架图中,检测结果进入质控状态,凡超过2SD的数据为告警;超过3SD的数据为失控,本次实验需进行重做[3]。
1.4.5 冷沉淀中的凝血因子Ⅷ、纤维蛋白原质量标准 根据GB18469-2012《全血及成分血质量要求》:来源于 400ml全血:。1.4.6统计学方法 采用SPSS统计学软件进行数据分析,数据以“均数±标准差”(x±s)表示。
2 结果
2.1 精密度评价结果 Sysmex全自动血凝仪(型号CA-500)检测正常水平的定值质控血浆和低值水平的定值质控血浆其批内精密度见表1。所测得的两个水平的血浆批内和批间CV值均<5.0%。

表1 Sysmex血凝仪批内和批间精密度(n=20)
2.2 准确度评价结果 根据NCCLS(美国临床和实验室标准协会)的要求,Ⅷ因子和Fg总允许误差<10%。检测两个定值血浆结果与各自靶值相比,偏差均在允许误差范围内。
2.3 冷沉淀FⅧ、Fg检测结果见表2、表3。
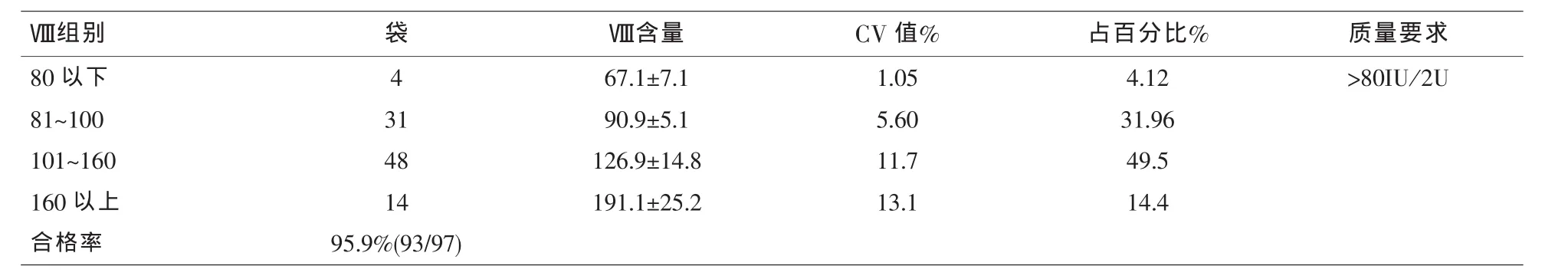
表2 冷沉淀制品FⅧ含量(n=97)
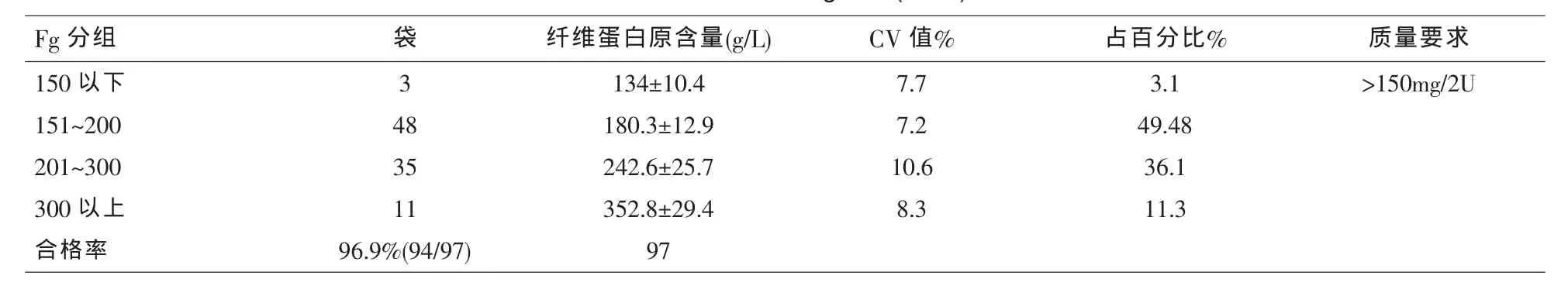
表3 冷沉淀制品Fg含量(n=97)
3 讨论
为了保证血液产品质量确保输血安全有效,按照《血站技术操作规程》(2012版)的要求及《全血及成分血质量要求》(GB18469-2012),每月对冷沉淀制品FⅧ因子和纤维蛋白原进行质量监测。为了准确反映冷沉淀制品的质量,在进行质量检测时为了得到准确可靠的结果,检测仪器的性能须处在最佳状态。
Sysmex血凝仪是用于监测冷沉淀质量的专用仪器,Fg定量检测方法Clauss法是WHO推荐的参考方法[5];Clauss法的原理是在标本中加入过量凝血酶,使Fg转变成纤维蛋白而凝固,Fg的含量与出现凝固的时间呈负相关,能直接反应Fg在冷沉淀中的含量。
尽管厂家已经提供了仪器性能的初步参数,但由于地区、人种、实验室之间的差异,特别是某些试剂制备、批号改变后性能会有显著改变,各实验室引进使用前应重新评估,按照NCCLS有关文件要求进行评估。本次结果显示,该仪器两个项目正常和异常水平的质控品批内和批间的精密度均<5%,具有良好的精密度,检测稳定性好;准确度高,系统误差小,检测结果准确可靠,与其它品牌血凝仪检测结果可比[6]。
仪器除了日常保养和特殊维护外,在分析检测前,下面的一些因素也要考虑:试剂从冰箱拿出室温恒定后再复溶,试剂复溶时水或稀释剂加量一定要准确,并混合均匀,放置 5~10min后再将试剂预温,复溶后的试剂应在试剂规定的稳定期使用,否则会影响实验结果;试剂杯混入灰尘,有可能堵塞吸样针,影响仪器的吸液量,反应杯进入灰尘会影响结果的判读。在更换试剂批号后,应重新用定标品建立标准曲线以保证检测的准确性。每次检测时,用正常水平的定值质控血浆和低值水平的定值质控血浆与样品同行检测。该质控品最好使用与试剂同一厂家,有的进行了自制凝血质控品用于室内质控的研究[7]。影响检验结果质量的因素是多方面的,这些检验前的分析直接影响检验的质量,是保证检测质量的前提[8]。
本次实验结果显示,97袋冷沉淀中Ⅷ含量低于质量标准(80IU)的有4袋、占4.12%;合格的有93袋,FⅧ含量多集中在81IU到160IU之间,占81.5%,160IU以上的占14.4%合格率为95.9%。Fg含量低于质量标准(150mg)的有3袋,占3.1%;合格的有94袋,含量多集中在151mg到300mg之间,占85.58%,300mg以上的有11袋占11.3%。通过抽检了解到冷沉淀FⅧ因子含量及纤维蛋白原含量均有不合格情况存在,抽检的97袋冷沉淀总合格率(90/97)为92.8%,有7.2%的不合格率。本次实验的冷沉淀是用虹吸法制备,虹吸法在原料新鲜冰冻血浆融化过程中,部分冷沉淀不能形成大的凝聚团块或絮状,无法聚集吸附在中央未融化的冰碴上或袋壁上,有部分散在的细小冷沉淀由于虹吸作用直接流到另一冷上清转移空袋中,另外,由于虹吸法制备冷沉淀时,原料血浆融化的速度不一致,部分血浆融化为少量冷不融物的时间较为集中,工作人员来不及取出部分冷沉淀袋,致使袋内的少量冷不融物继续融化,甚至完全融化而直接流入冷上清的转移袋内[9]。冷沉淀中的Ⅷ是一种极不稳定的凝血因子,受到制备程序的影响很容易失去活性,为获得较高活性的FⅧ,控制新鲜冰冻血浆融化时温度和融化时间很重要,融化血浆时,温度必须控制在4℃左右,超过8℃则冷沉淀将复溶,回收率降低[10]。
采用Sysmex血凝仪对冷沉淀制品中FⅧ因子和Fg进行监测,并加强了对采血、成分制备、贮存及运输全过程的全面质量监督,能有效地控制了新鲜冰冻血浆、冷沉淀制品的质量,保证了合格、安全有效的血液制品应用于临床。
[1]付涌水,钱开诚,陆志刚,等.临床输血[M].北京:人民卫生出版社,2013:43-44.
[2]许小英,于海涛,周存敏,等.某型号全自动血凝分析仪的性能评价[J].国际检验医学杂志,2012,33(11):1361-1362.
[3]郑怀竟.临床免疫学检验质量保证[M].北京:北京医科大学中国协和医科大学联合出版社,1995:51-54.
[4]中华人民共和国卫生部,中国国家标准化管理委员会.GB18469-2012.全血及成分血质量要求[S],2012:12.
[5]熊立凡.临床检验基础[M].第3版.北京:人民卫生出版社,2006:93.
[6]彭赛亮,梁小亮,尹向飞.ACLTOP血凝仪两种方法相结合检测纤维蛋白原的分析[J].实验与检验医学2012,30(3):271-273.
[7]王琳,王笔金.自制凝血质控品用于室内质控的研究[J].实验与检验医学,2009,27(4):428-429.
[8]张国强,陶振东,邹雪,等.ThrombolyzerCompactX全自动血凝仪常见故障及处理[J].实验与检验医学,2012,30(4):416-417.
[9]蒋燕,陈宝葵,林敏诗.快速融化离心法与虹吸法制备冷沉淀的质量评价[J].江苏大学学报(医学版),2012,22(2):167-168.
[10]李炜华,漆云霞.冷沉淀制备过程中的关键因素探讨[J].现代检验医学杂志,2011,26(6):156-157.
