气体发生剂产气燃料研究进展
2015-05-10史大昕孙克宁李加荣
张 凯, 史大昕, 张 奇, 孙克宁, 李加荣
(1. 北京理工大学化工与环境学院, 北京 100081; 2. 化学电源与绿色催化北京市重点实验室, 北京 100081)
1 引 言
气体发生剂又称产气剂,是指燃烧后能够产生大量冷气体的各种物质[1]。气体发生剂一般由产气燃料、氧化剂、燃烧调节剂、抗爆剂等构成,其主要成分是产气燃料和氧化剂,前者确保燃爆时能够提供所需的最大供气量,后者确保燃爆时燃烧充分,因此它们是气体发生剂的主要成分。
气体发生剂在军事和民用领域应用广泛。在军事中,主要用于火箭、导弹的推进、灭火装置以及飞机驾驶员座椅弹射等; 民用中,则主要应用于汽车安全气囊、救生筏和飞机安全滑梯的快速充气[2]以及果蔬保鲜[3]等。
传统的气体发生剂主要以叠氮类气体发生剂为主,但由于叠氮类气体发生剂自身毒性较大,对环境影响不利,已经难以满足当今世界对气体发生剂的要求。因而新型的绿色环保气体发生剂越来越受到研究人员的重视,成为当今气体发生剂的研究重点。新型气体发生剂的产气燃料应具有含氮量高、产气量大、热稳定性好、高能钝感、燃烧产物无毒和绿色环保等优点。目前,新型气体发生剂的产气燃料的研究主要包括唑类、胍类和嗪类等高氮含能化合物。其中,唑类化合物主要包含1,2,4-三唑类化合物、1,2,4-三唑酮类化合物、5-氨基四唑、双四唑盐、偶氮四唑盐和吡唑类化合物; 胍类化合物主要有硝基胍、硝酸胍及其衍生物; 嗪类化合物主要包括三嗪类化合物和四嗪类化合物。尽管新型气体发生剂在实际应用中取得了一定的进展,但仍有许多领域尚未得到开发利用,因而具有广阔的研究前景。
本文就气体发生剂的主要部分——产气燃料的国内外研究进展进行综述,为进一步研究新型气体发生剂提供参考。
2 叠氮类
叠氮类气体发生剂是人类应用最早、最普遍的一类气体发生剂,该类气体发生剂以碱金属叠氮化物为产气燃料,以金属氧化物、硝酸盐和高氯酸盐为氧化剂,有时还加入冷却剂、粘合剂等调节剂,目的在于提高其稳定性和工艺性能,所用的叠氮化物主要有NaN3、LiN3、KN3和NH4N3等。与其他碱金属叠氮化物相比,NaN3具有诸多优点[2],如稳定性好,在410 ℃左右仍不分解,且感度比其他碱金属叠氮化物都低; 点火容易、低燃温、高燃速、低成本; 燃烧后产生的气体主要是氮气,对人体无毒害。因此从安全和经济等方面综合考虑,几乎所有叠氮类气体发生剂均选择NaN3作为主要产气燃料。目前,叠氮化钠类气体发生剂已被广泛应用于许多领域,尤其是汽车安全气囊应用较多。
NaN3不足之处[2,4]主要表现在: (1)是一种剧毒物质,0.05 g 进入人的肠胃即能引起剧烈心跳,随之昏迷; 0.05 g 以上则会引起死亡,因此生产过程必须有严格的防毒措施; (2)存在因分解或燃烧而引起火灾的危险; (3)其与氧化剂反应会产生有毒成分,对人体有害; (4)燃烧后残渣较多; (5)存在回收难、易泄露等环保问题。因此,自20世纪90年代以来,人们就开始积极研发无毒、环保、性能优异的新型气体发生剂来代替传统的叠氮类气体发生剂,且其性能要达到产气量大、燃速快、燃烧温度低、热稳定性好以及绿色环保等优点。
目前, 新型气体发生剂的产气燃料研究主要集中在唑类、胍类和嗪类等高氮化合物为产气燃料的研究方面。
3 唑类
唑类含能化合物是20世纪七八十年代初开始研究的一类高能量密度物质。许多唑类高氮含能化合物具有较高的正生成焓、高产气量、燃烧无烟或少烟和气体产物多为氮气等优点,且对人体无毒害。这种高能量密度和低毒的特性符合当前气体发生剂领域所追求的高性能、绿色、环保等要求,将会成为今后的研究重点[5]。
3.1 三唑类化合物
三唑类含能化合物是研究较早的一类产气燃料,主要包括1,2,4-三唑类化合物和1,2,4-三唑酮类化合物[6]。
3.1.1 1,2,4-三唑类化合物
1,2,4-三唑类产气燃料的典型代表是3,5-二硝基-1,2,4-三唑铵盐(ADNT)和5,5′-二硝基-3,3′-偶氮基-1-氢-1,2,4三唑(DNAT)。前者在20世纪80年代初,由美国Los Alamos国家实验室首次合成出来[7],该物质的含氮量为47.72%。在此基础上Pevzner M S[8]和我国学者朱朝阳等[9]先后报道了3-氨基-5-硝基-1,2,4-三唑(ANTA) 及5,5′-二硝基-3,3′-偶氮基-1-氢-1,2,4三唑(DNAT)的合成(Scheme 1)。其中DNAT的含氮量为55.12%,密度为1.88 g·cm-3,生成焓446.45 kJ·mol-1 [9],是一种性能良好的高氮含能化合物。

Scheme 1 Synthesis of ANTA[7]and DNAT[9]
3.1.2 1,2,4-三唑酮类化合物
3-硝基-1,2,4-三唑-5-酮(NTO)及其盐是非常有价值的含能、高成气化合物。尽管NTO自身酸性较大(pKa=3.67),但其许多盐已经作为含能氧化剂和气体发生剂的产气燃料组分[10](Scheme 2)。
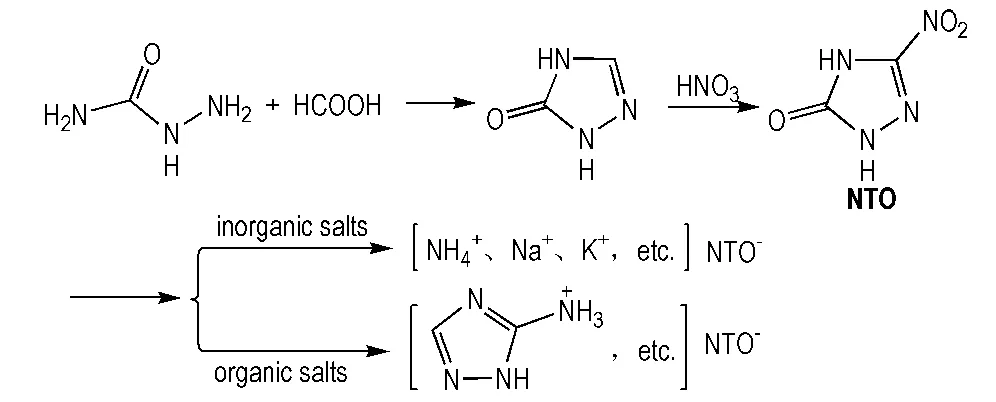
Scheme 2 Synthesis of NTO and its salts[10]
3.2 四唑类
3.2.1 5-氨基四唑及其离子型化合物

1991年,美国科学家Poole[12]发明了一种新型气体发生剂,该气体发生剂以5-氨基四唑为产气燃料,并加入了Sr(NO3)2、NaNO3作为氧化剂和SiO2添加剂,有效地提高了产气量。1993 年Lund 等[13]以5-氨基四唑为原料,加入过渡金属Zn 和Cu,合成得到5-氨基四唑过渡金属盐,再加入传统的氧化剂,该配方气体发生剂燃烧产生的N2含量很高,适用于汽车安全气囊和其他充气设备的快速充气。
5-氨基四唑的制备多采用Stolleet法[14],即叠氮化钠和硝酸在水溶液中反应生成的叠氮酸与双氰胺成环反应生成5-ATZ(Scheme 3)。
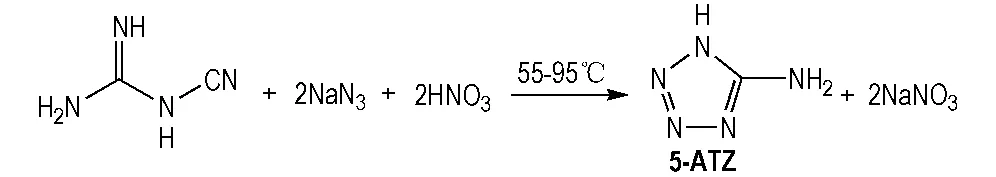
Scheme 3 Synthesis of 5-ATZ by Stolleet method[14]
Stolleet法虽然工艺简单、收率较高,但合成过程中会产生剧毒叠氮酸,对人体危害很大。2003年,Himo F等[15-16]利用易得的双氰胺和叠氮化钠为原料,在ZnBr2催化下合成5-氨基四唑(Scheme 4)。此法工艺简单、催化剂廉价、产品收率高,避免了Stolleet法中剧毒中间体叠氮酸的产生。
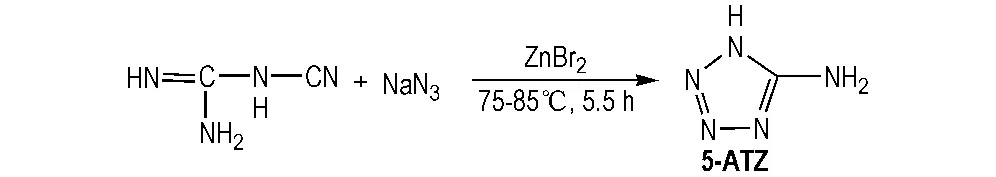
Scheme 4 Synthesis of 5-ATZ by the improving way[15-16]
以5-氨基四唑为起始原料合成的5-氨基四唑二硝胺盐的性能更优(Scheme 5)[17],该物质既具有较高的含氮量(58.33%),又具有较好的氧平衡(5.52%),在气体发生剂中有较好的发展潜力。

Scheme 5 Synthesis of 5-Aminotetrazole dinitramide amine salt[17]
3.2.2 双四唑类化合物
3.2.2.1 5,5′-肼基-双四唑
5,5′-肼基-双四唑(HBT)的晶体密度(XRD实测)为1.841 g·cm-3,含氮量高达83.3%,是目前已知的含氮量最高的气体发生剂之一。该物质的其它产气性能也不错,如爆速为9463 m·s-1、爆压(计算值EXPLO5code)为36.7 GPa、冲击波感度(BAM methods)>30 J[18]。此外,该物质的燃烧速度较快,是一种性能优良的高氮含能化合物,可作为气体发生剂中的产气燃料。HBT的合成主要以5-氨基四唑为原料,经过偶氮反应和还原反应合成(Scheme 6)。
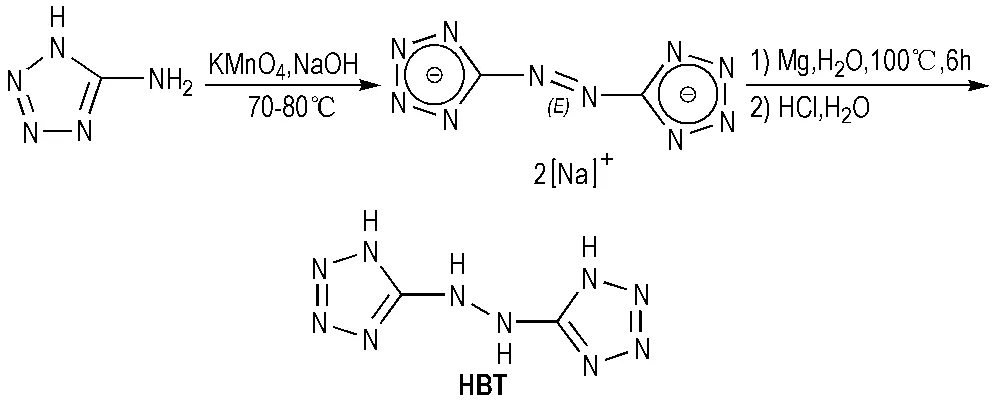
Scheme 6 Synthesis of HBT[18]
3.2.2.2 双四唑钾盐
双四唑钾盐结构与联苯相似,具有芳香性,含氮量为52.34%。双四唑钾盐熔化分解点为434.06 ℃,撞击感度:H50>50 cm,I50>49 J(97.99 N落锤,50 cm落高,爆炸百分数为0%)[19]。较高的热稳定性、吸湿性小并且制取方便以及较高燃速等优点,使其在气体发生剂方面的应用具有一定的优势。此外,该盐受亚硝酸钠、氯化钴、硝酸锶的影响可催化降低其分解温度,提高了其实用的可能性。该盐的合成先由叠氮化钠、氰化钠、二氧化锰和硫酸铜在酸性条件下反应生成双四唑锰盐,然后与碳酸钾加热回流反应,得到双四唑钾盐(Scheme 7)。

Scheme 7 Synthesis of bitetrazole potassium[19]
3.2.3 偶氮四唑非金属盐
若将偶氮基引入四唑分子结构中,既可以提高化合物的氮含量,也可以增加化合物的生成焓,使其具有更好的热稳定性。此外,偶氮四唑非金属盐的感度较低且不吸湿,是一类性能优异的产气燃料[20]。
已经研究的这类盐主要包括偶氮四唑铵盐(AZT)、偶氮四唑二胍(GZT)和偶氮四唑三氨基胍(TAGZT)等,它们的合成[5,21-22]均采用5-氨基四唑为原料,通过碱性氧化法将5-氨基四唑氧化为偶氮四唑钠盐水合物(SZT),然后分别与氯化铵,硝酸胍(GN),三氨基胍(TAGN)反应,生成AZT,GZT,TAGZT的产率均达到80%以上(Scheme 8)。
AZT、GZT和TAGZT热稳定性好,其中GZT 燃烧少烟,AZT 和TAGZT 燃烧无烟且无残渣,在气体发生剂领域有着不错的应用前景。
3.3 吡唑类化合物
吡唑类化合物用作产气燃料的典型化合物包括1,4-二氨基-3,6-二硝基吡唑[4,3-C]并吡唑(LLM-119)和4-氨基-3,5-二硝基吡唑(LLM-116)等。其中LLM-119的合成[23-24]是以乙酰丙酮为起始物多步转化合成所得,总产率约为21% (Scheme 9)。LLM-119的含氮量为49.12%,晶体密度为1.845 g·cm-3,DSC热分解峰温为253 ℃,标准生成焓114 kJ·mol-1,H50为24 cm,对摩擦和静电钝感[23]。
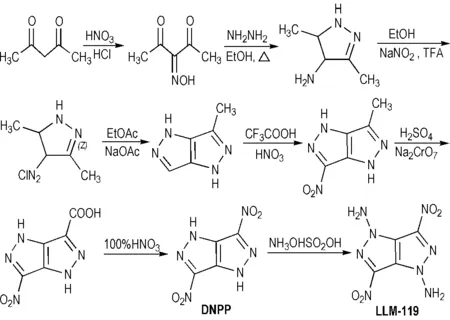
LLM-116的含氮量为40.70%,实测密度为1.900 g·cm-3,能量为HMX的90% ,H50为165 cm,分解温度为178 ℃[23]。其特点是能量较高、感度非常低、具有较好的氧平衡。其合成是在2001年由美国Livermore国家实验室的Schmidt 等[25]首先完成(Scheme 10)。
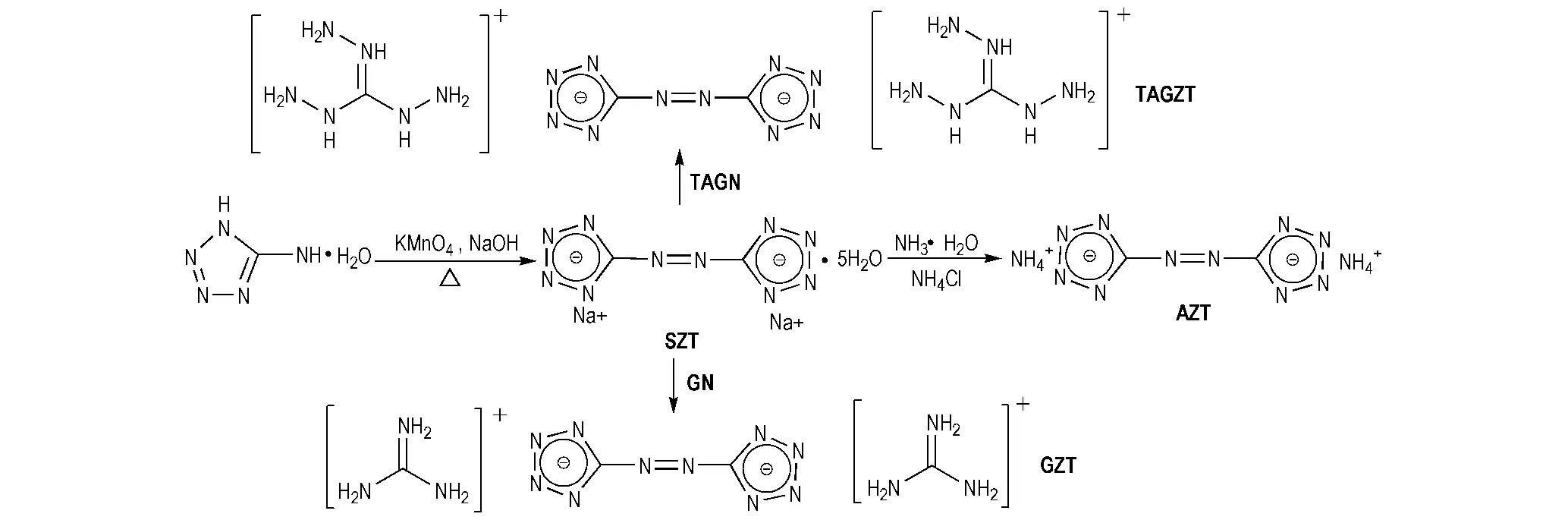
Scheme 8 Synthesis of AZT、GZT and TAGZT[5,21-22]
表1 AZT、GZT、TAGZT的性能[22]
Table 1 Properties of AZT、GZT and TAGZT

compoundTm.p./℃ρ/g·cm-3ΔHθf/kJ·mol-1H50/cmD/m·s-1p/GPaAZT>2001.530+443.5 21.4760018.7GZT>2401.538+409.6 >320710015.5TAGZT196-1971.602+1074.3 25905029.2
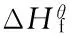
Scheme 9 Synthesis of LLM-119[23]

Scheme 10 Synthesis of LLM-116[25]
2007年,汪营磊等[26]报道了改进的亲核取代氢(VNS) 反应合成LLM-116。其转化是以1,3-二硝基吡唑为原料,经热重排、氨气中和得到3,5-二硝基吡唑铵盐,然后酸化得到3,5-二硝基吡唑。以三甲基肼碘化物(TMHI) 作为异常亲核取代氢(VNS) 反应试剂,在叔丁醇钾催化下与3,5-二硝基吡唑进行VNS反应制得4-氨基-3,5-二硝基吡唑(Scheme 11)。
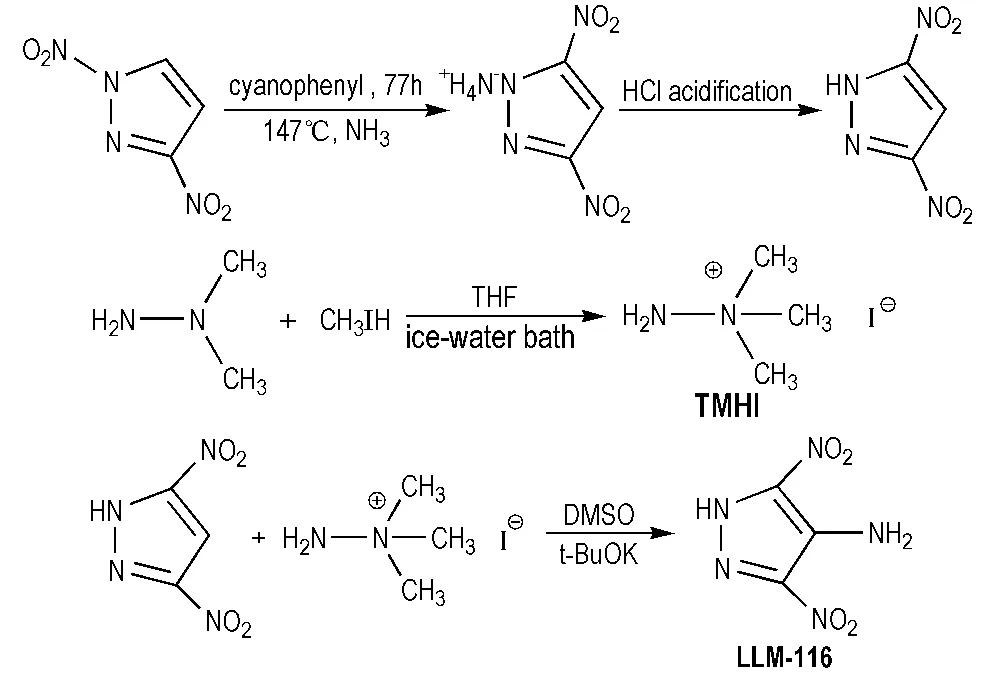
Scheme 11 Synthesis of LLM-116 by the improving way[26]
四唑类高氮含能化合物及其胺盐、肼盐和胍盐等物质,大部分具有高含氮量和高生成焓的特性,多是安定性较好的化合物,具有较高的能量和较好的爆炸性能。
4 胍类
胍类气体发生剂的产气燃料主要包括硝酸胍(GN)及其衍生物和一些胍盐。这类气体发生剂同样具有产气量大、产生的气体无毒、热稳定性好及原料易得等优点[27-31]。
胍类气体发生剂中应用最为广泛的是硝酸胍型气体发生剂。硝酸胍的含氮量为45.9%,在高温下分解并爆炸。硝酸胍作为气体发生剂产气燃料具有三大优点[32]: (1)产气量高; (2)产生的气体毒性很低; (3)产生的气体温度较低,因此硝酸胍在气体发生剂等方面的应用具有一定的优势。但该类气体发生剂存在燃速较低的缺点,且产气率较低,通常只有70%~80%。
以GN为主要燃料的气体发生剂,通常采用碱式硝酸铜(BCN)作为主氧化剂,硝酸锶(SrNO3)、高氯酸铵(AP) 、高氯酸钾(KP)等作为副氧化剂,有时还会加入5-ATZ等含氮有机物作为副燃料。该类型配方的优点是燃烧稳定、燃温较低、产生的有害气体较少,具有较高的热稳定性[32]。2005年,Ivan V.Mendenhall等[33]研究发现,在以GN为燃料,BCN为氧化剂的发生剂配方中,加入氢氧化氨基四唑的金属盐能够在有效地提高配方燃速的同时不降低产气效率; 2006年,Autoliv公司[34-35]研究发现,在GN/BCN配方中,加入质量分数1%~10% AP或碱金属高氯酸盐,能够获得0.03 mol·g-1的气体产率,并且BCN能够吸收高氯酸盐分解产生的HCl,有效地减少了有害气体的产生。
表2 GN型气体发生剂的性能[32]
Table 2 Performances of GN-based gas generant

formulationmassfractionCN/BCN/Cu(CH2N5)OH/Al2O3u/mm·s-1nρ/g·cm-3AB45.26/33.22/20.02/1.5045.97/52.53/0/1.5016.7613.210.430.542.051.91
Note:uis burning rate(under 6.9 MPa),nis burning rate pressure exponent,ρis density.
比较好的胍类产气燃料是三氨基硝酸胍(TAGN),其氮含量为58.68%,有很好的热稳定性,与其他推进剂和炸药组分有较好相容性,使用前可长期储存而不变质[36-37]。TAGN的合成方法主要有双氰胺法、氰胺钙法、氰胺法和硝酸胍法[36-40],其中硝酸胍法工艺简单,操作简便,产率较高。2006年,徐松林等[41]对传统硝酸胍法进行了改进,即以硝酸胍为起始原料,渐次与肼反应分别生成氨基硝酸胍(AGN)、二氨基硝酸胍(DAGN)和TAGN (Scheme 12)。
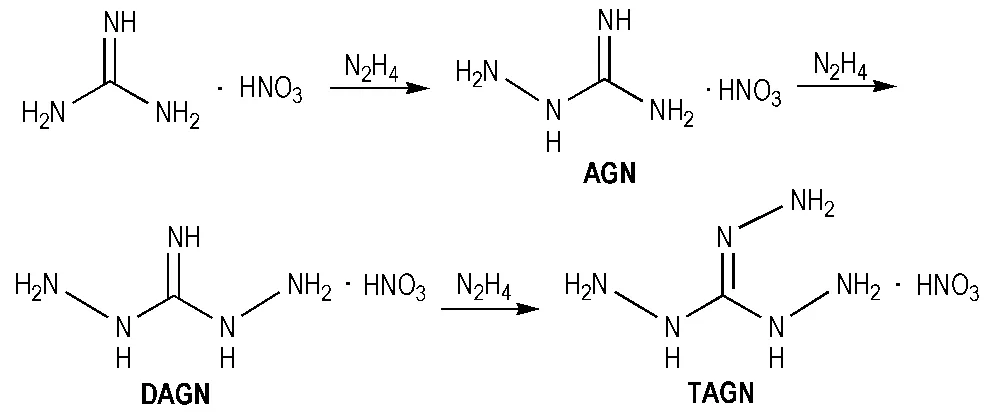
Scheme 12 Synthesis of AGN、DAGN and TAGN[41]
胍可接受质子,其与含能酸性唑类化合物结合成离子型化合物。此类化合物制备简单、产气量大,在气体发生剂中有很好的发展前景。例如: 5-氨基四唑胍盐(GA)的含氮量为77.78%,其热稳定性和感度适中,产气量大,适用于气体发生剂中的产气燃料。2003年,Neutz等[42]以5-氨基四唑和碳酸胍为原料合成GA,产率达到95%(Scheme 13)。
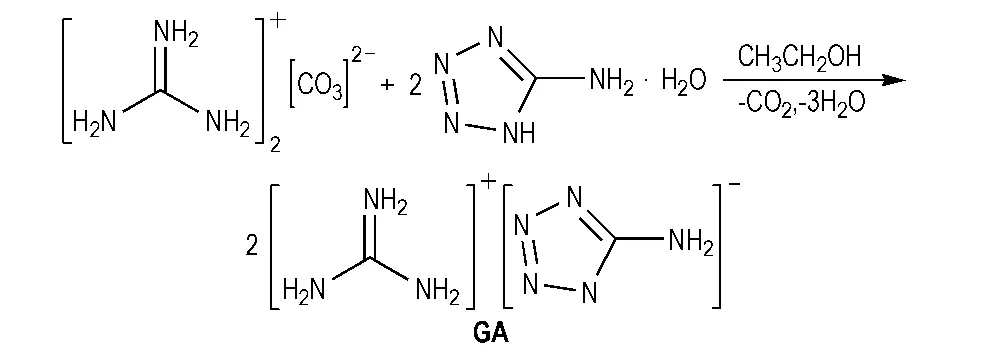
Scheme 13 Synthesis of GA[42]
胍类产气燃料中产气性能最好的是N-脒基脲二硝酰胺盐(FOX-12)。该化合物含氮量为46.9%,氧平衡为-19.14%,是一类氧平衡和产气量非常均衡的自供氧型气体发生剂。它的密度为1.755 g·cm-3,熔化分解点为204 ℃,DSC热分解峰温213 ℃; 其能量高于TATB,爆速可达8210 m·s-1,感度和热稳定性优于RDX,是一类不吸湿、低感度、化学稳定性好、含氮量高的新型含能化合物,用于气体发生剂时还具有燃温低、燃速高、产生的气体无毒等优点,可替代毒性高、稳定性差的叠氮类气体发生剂; 加之其不溶于冷水,制备简便、价格低廉,因此可广泛用于推进剂、气体发生剂和钝感炸药中[43]。FOX-12的合成[43]是将硫酸脒基脲溶于水中,加热至60 ℃左右再加入二硝酰胺铵(ADN)饱和溶液,反应1 h ,室温冷却,过滤干燥即得到FOX-12(Scheme 14)。
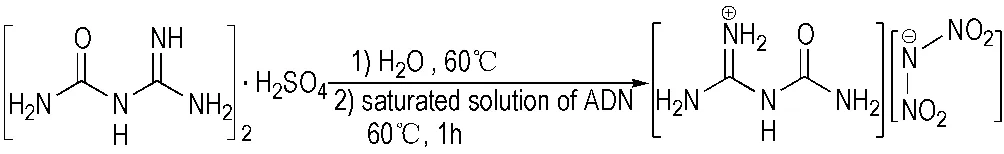
Scheme 13 Synthesis of FOX-12[43]
胍类产气燃料是一类高性能的产气燃料,与其它类产气燃料相比,胍类产气燃料因为其产气量大和原料易得的特点,已经被广泛应用军事和民用领域。
5 嗪类
目前,嗪类气体发生剂的产气燃料主要包含三嗪类化合物和四嗪类化合物。嗪类高氮含能化合物是近年来国内外研究较多的一类高氮化合物,其特点是热稳定性较好且冲击感度、摩擦感度较低[44]; 同时分子结构中的高氮、低碳氢含量不仅使其产气量大、燃烧产物少烟或无烟,而且还可使其更容易达到较好的氧平衡[45]。
5.1 三嗪类化合物
三嗪类化合物氮原子数较多,通常以三嗪环为母体,发生取代反应取代母体中的氢原子,生成一系列的三嗪类化合物。如2-硝亚胺基-5-硝基-六氢化-1,3,5-三嗪(NNHT)是一种重要的三嗪类含能化合物,其含氮量为44.74%,密度为1.88 g·cm-3,熔点为207 ℃; NNHT分子结构中既含有硝基,又含有氨基,分子间和分子内皆可形成氢键,其突出的特点是感度低,NNHT撞击感度为89 cm[46]。1990年,Huang D S等[47]首先合成了NNHT; 1998年,Cliff M D等[48]以甲醛、特丁胺和硝基胍为原料,经过Mannich 缩合反应和氯离子催化硝解反应得到NNHT(Scheme 15)。
2007年,张海昊等[46]在Matthew D. Cliff合成方法的基础上,采用工业硝酸代替纯硝酸硝解2-硝亚胺基-5-特丁基-六氢化-1,3,5-三嗪(NBHTA),不仅提高了收率,而且优化了硝解反应条件,使操作更简单,成本更低。2011年,李永祥等[49]报道了合成NNHT的新方法,该方法以硝基胍、乌洛托品和浓盐酸为原料,第一步通过成环反应生成中间产物NIHT·HCl,第二步通过硝化中间产物生成目标产物NNHT; 中间产物的收率可达到78.3%,目标产物的总收率可达到64.3%(Scheme 16)。
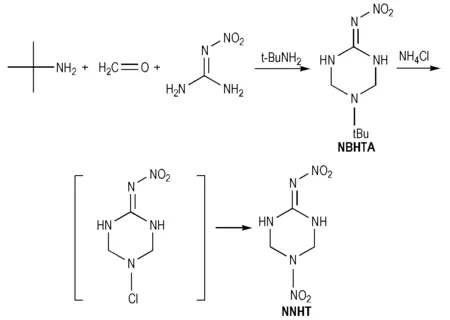
Scheme 15 Synthesis of NNHT[47]
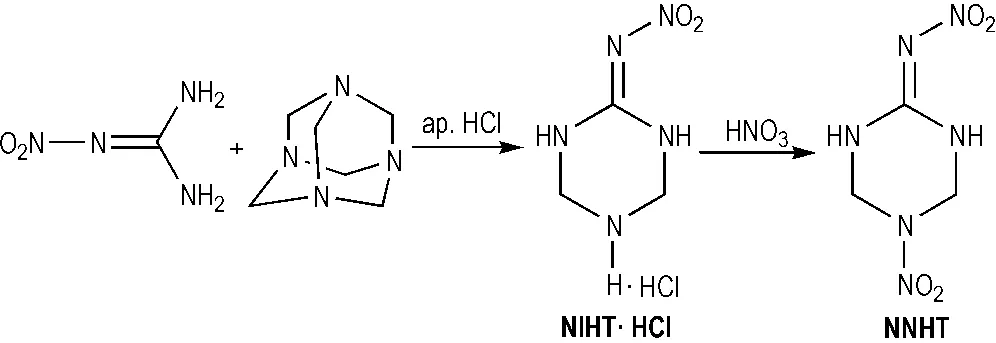
Scheme 16 Synthesis of NNHT[49]
尽管三嗪类化合物稳定性通常较低,但采用偶氮桥将两个三嗪类化合物连接起来形成大的共轭体系可以有效地改善稳定性,如氮含量达到79.55%的4,4′,6,6′-四叠氮基偶氮-1,3,5-三嗪(TAAT),其稳定性较好、分解温度较高、摩擦感度较低,生成热高达2171 kJ·mol-1[6]。M. Huynh等[50]报道TAAT的合成是4,4′,6,6′-四氯-二氢-偶氮-1,3,5-三嗪在乙睛中与水合肼反应得4,4′,6,6′-四肼基-二氢-偶氮-1,3,5-三嗪,接着在NaNO2/HCl作用下发生叠氮化反应,最后在CHCl3/H2O 混合溶剂中经氯气氧化脱氢得到TAAT(Scheme 17)。
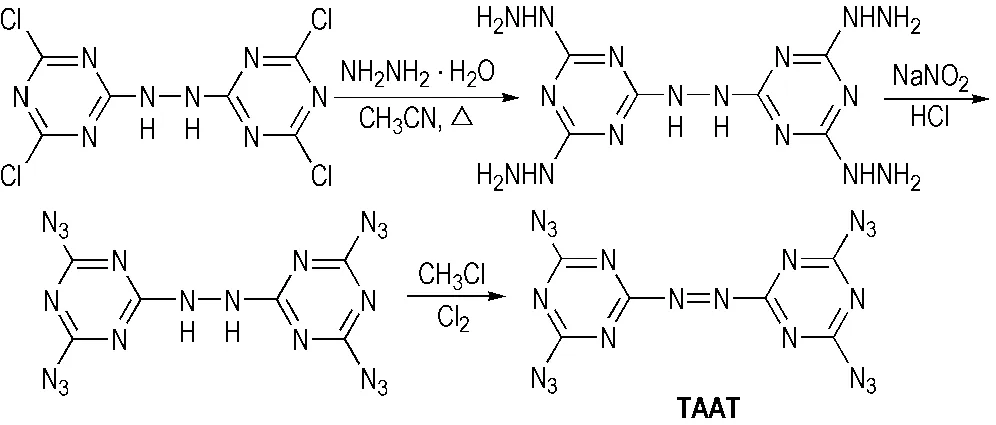
Scheme 17 Synthesis of TAAT[50]
5.2 四嗪类化合物
四嗪类高氮含能化合物是近年来国内外研究较多的一种新型含能化合物,具有生成焓较高、热稳定性好和感度较低等特点[51]。四嗪类化合物中具有气体发生剂应用潜力的主要有3,6-双(1-氢-1,2,3,4-四唑-5-氨基)-1,2,4,5-四嗪(BTATz)、3,3′-偶氮基-双(6-氨基-1,2,4,5-四嗪(DAAT)、3,6-二氨基-1,2,4,5-四嗪-1,4-二氧化物(LAX-112或DATZO2)、3,6-二肼基-1,2,4,5-四嗪(DHT)等[51]。其中DATZO2是不含氧化基团硝基的芳香杂环含能化合物,氮含量58.33%,生成焓164 kJ·mol-1,密度1.834 g·cm-3,H50为179 cm,是四嗪类低感度含能化合物[52-54]。2001年,Hiskey等[54]率先合成了DATZO2; 2005年,阳世清等[55]介绍了一种合成DATZO2的方法: 以3,6-对(3,5-二甲基吡唑)-1,2,4,5-四嗪(BT)为起始物,经两步反应制得3,6-二氨基-1,2,4,5-四嗪-1,4-二氧化物(Scheme 18),其中BT[54]的合成先以水合肼和硝酸胍为原料合成TAGN,TAGN与乙酰丙酮的成环反应合成3,6-双(3,5-二甲基吡唑)-1,2-二氢-1,2,4,5-四嗪(BDT),BDT氧化脱氢制得的BT(Scheme 19)。 3,6-二肼基-1,2,4,5-四嗪(DHT)及其盐是一类高氮杂环含能化合物,具有高含氮量、高能量、低特征信号和燃烧无残渣、无污染等优点,有望成为叠氮化钠的替代物而被用于汽车安全气囊中[56]。DHT的合成[57]也以BT为前体,经过亲核取代反应制得(Scheme 20)。
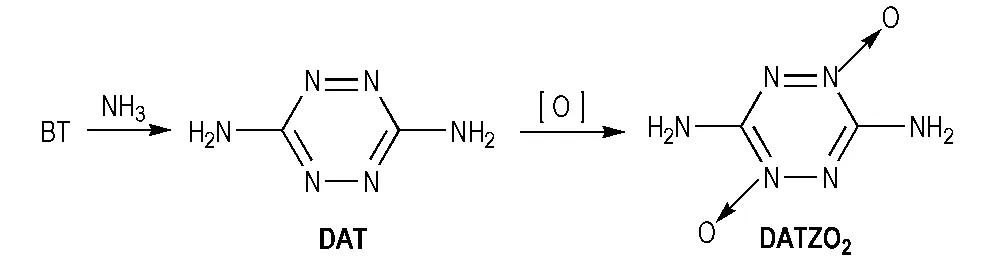
Scheme 18 Synthesis of DATZO2[55]
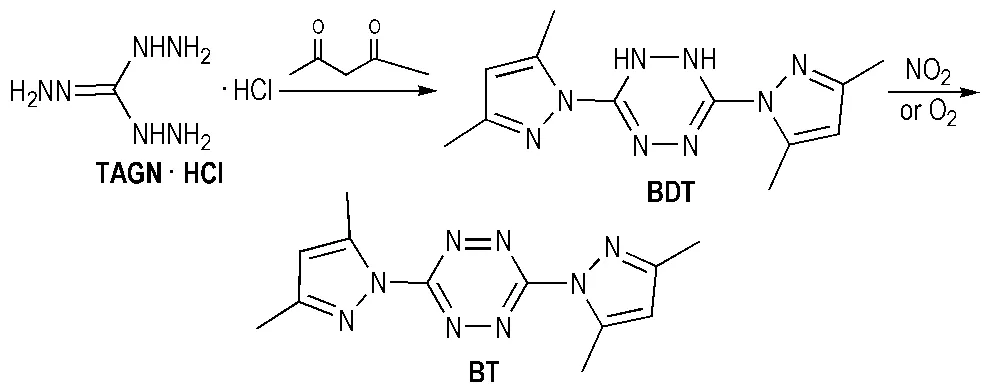
Scheme 19 Synthesis of BT[54]
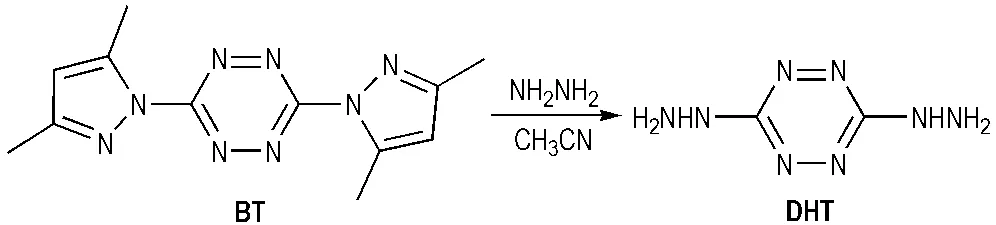
Scheme 20 Synthesis of DHT[57]
2002年,Hiskey等[58]研究DHT时合成出了DAAT。2006年,徐松林等[59]在此基础上,以BT为起始物,经亲核取代、氧化脱氢、氨解和水解等四步反应,合成了高含氮量的3,3′-偶氮基-双(6-氨基-1,2,4,5-四嗪(DAAT)(Scheme 21)。DAAT为深红色粉末,溶于二甲基亚砜(DMSO)、N-甲基吡咯烷酮(NMP)、N,N-二甲基甲酰胺(DMF)和环丁砜,不溶于水; DAAT的含氮量为76.36%,密度为1.84 g·cm-3,生成焓为862 kJ·mol-1,撞击感度H50为70 cm(HMX 25cm),对静电和摩擦钝感; 真空安定性测试结果为0.29 mL·g-1,DSC 峰温320 ℃[59]。DAAT具有较高的氮含量、较好的热稳定性和较高的能量等优点,适用于气体发生剂的产气燃料。
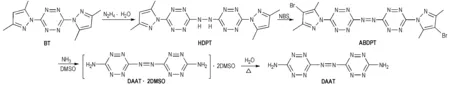
Scheme 21 Synthesis of DAAT[59]
3,6-双(1-氢-1,2,3,4-四唑-5-氨基)-1,2,4,5-四嗪(BTATz)是包含四嗪环和四唑环的高氮含能化合物,氮含量为79.03%,爆速为7520 m·s-1,生成焓为883 kJ·mol-1,DSC起始分解点264℃,其热稳定性较好且摩擦感度低[60]。其合成可以先用氯气氧化DHT 得到对氯四嗪,再与5-氨基四唑钠盐反应得到BTATz(Scheme 22)[61]; 也可以BT为起始反应物,与5-氨基四唑在高温下反应,制得BTATz(Scheme 23)[62]。
以嗪类高氮含能化合物为主要成分的气体发生剂,具有燃烧速度快、成气量大、燃烧温度低、有害气体少等特点,其综合性能较传统的非叠氮化钠基气体发生剂有了明显提高。

Scheme 22 Synthesis of BTATz[61]
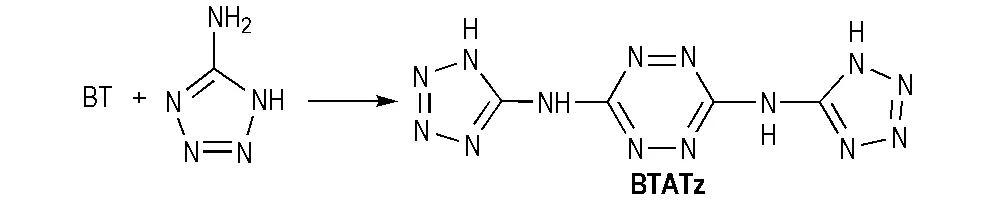
Scheme 23 Synthesis of BTATz[62]
6 其他类化合物
一些高氮含能材料因为自身良好的热稳定性和产气性能,也可用作气体发生剂中的产气燃料[4]。
6.1 六硝基六氮杂异伍兹烷(CL-20)
CL-20是具有笼型多环硝胺结构的一个高能量密度化合物,含氮量为38.4%,标准生成焓为415.5 J·mol-1,DSC 峰温245~254 ℃,爆速可达9000 m·s-1,热稳定性也较好,缺点是机械感度稍高; CL-20 耐热特性低于HMX,与RDX 接近,作为耐热炸药及气体发生剂组分较为安全可靠[4]。1987年,Nielsen[63-64]首次合成了CL-20(Scheme 24),后人在此基础上不断改进。2000年,王才等[65]使用一锅法以四乙酰基二苄基六氮杂异伍兹烷为原料, 经亚硝解脱苄再硝解合成CL-20,反应收率可达82%以上,纯度达98%。
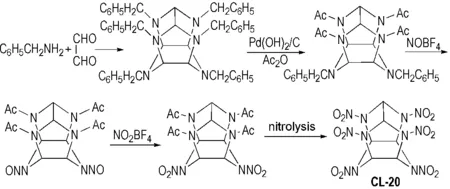
Scheme 24 Synthesis of CL-20[63-64]
2005年,Daoud等[66-67]提出了以CL-20为产气燃料,硝酸铵为氧化剂,聚己酸内酯为黏合剂的气体发生剂配方,此气体发生剂燃烧安全,燃烧后生成的气体产物为H2O、N2和CO2,绿色环保,燃烧温度低于322 K,且燃烧后无残渣,是一种性能非常突出的气体发生剂。
6.2 偶氮二胍二硝酸盐
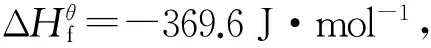
早在1892年,Thiele[68]就对AZODN 作了简单介绍,并使用高锰酸钾溶液作为合成AZODN的催化剂。整个过程虽然不需要外界加热,但引入了金属杂质,得到的的产物纯度不高。2000年,Lundstrom等[69]改进了上述合成方法,通过氨基硝酸胍(AGN)与70%的硝酸反应得到AZODN(Scheme 25)。
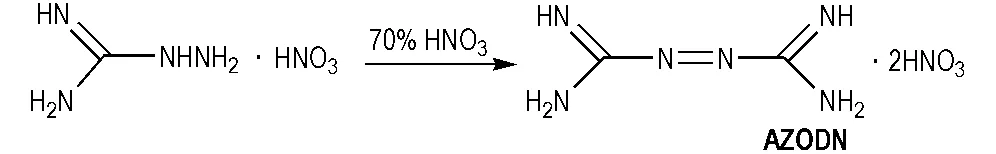
Scheme 25 Synthesis of AZODN[69]
2004年,Wheatley 等[70]对以AZODN 为产气燃料的气体发生剂进行了研究,指出AZODN、AgNO3和KNO3的共熔物,可用作燃烧辅助剂帮助点燃推进剂或气体发生剂。同时高氧平衡的AZODN也可作为氧化剂,是未来新型气体发生剂产气燃料的代表。
6.3 呋咱类化合物
呋咱类化合物的母体结构为五元氮氧杂环,是一个含能基团,其环内存在活性氧,可形成“潜硝基”内侧环结构[71],因此呋咱类化合物的密度和氧平衡普遍高于四嗪类和四唑类化合物,但热稳定性较差[19]。此外,呋咱类化合物分子结构中含有大量的C—N、CN键和NN键,使其具有如下优点[72]: (1)标准生成焓高; (2)氮氧含量高; (3)能量密度高; (4)具有芳香性,分子热力学稳定性较好; (5)熔点较低等。这类化合物具有高能量密度、高标准生成焓、高氮含量等优异性能,因此有望在气体发生剂领域得到重要应用。
二氨基呋咱(DAF)是制备呋咱含能材料的前体化合物,以DAF为基本结构单元,可合成得到上百种呋咱含能化合物[73]。通常,DAF的合成大多经历三步[74]: 即先从乙二醛制得乙二肟,再制得二氨基乙二肟(DAG),再由高压釜制得DAF。该过程不仅步骤繁琐,且温度不易控制。2006年,雷晴等[73]报道了一种更简单且易于制备的方法: 由乙二醛只需两步即可制得DAF(Scheme 26)。
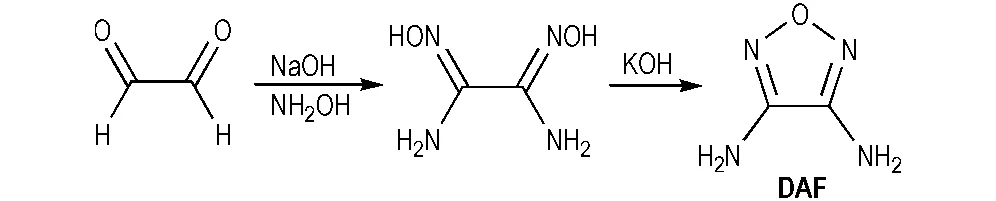
Scheme 26 Synthesis of DAF[73]
1981年,俄罗斯科学家Solodyuk等[75]首先以DAF为原料合成3,3′-二氨基-4,4′-氧化偶氮呋咱(DAAF)。DAAF为橙黄色粉末,含氮量约为52.83%,密度为1.88 g·cm-3,标准生成焓为+2986 kJ·mol-1,熔点250 ℃,热分解峰温252 ℃,生成热443 kJ·mol-1,爆速为9500 m·s-1,爆压29.9 GPa[6]。2002年,M. Hiskey等[76]用H2O2/H2SO4氧化DAF生成3,3′-二氨基氧化偶氮呋咱(DAOAF) ,再用醋酸和锌还原DAOAF 生成3,3′-二氨基-4,4′-氢化偶氮呋咱,接着通过与空气接触的甲醇溶液氧化成二氨基偶氮二呋咱(DAAF)。2013年,吴敏杰等[77]介绍了DAOAF的一种合成新方法: 以3,4-二氨基呋咱为原料,经过中间体3-氨基-4-甲酰胺基呋咱或3,4-二甲酰胺基呋咱合成DAOAF(Scheme 27),改进了以往的方法中存在的以3,4-二氨基呋咱为反应物,在浓硫酸或甲基硫酸中氧化的反应时间长,温度控制严格,产率低等缺点。DAOAF是一种含能化合物,含氮量为45.65%,DNOAF 的标准生成焓(计算值)为640 kJ·mol-1,密度1.91 g·cm-3,熔点100~112 ℃,H50为7.04 cm,根据Kamlet方程计算爆速9390 m·s-1,爆压40.5 GPa,具有优良的耐热性和稳定性[23]。
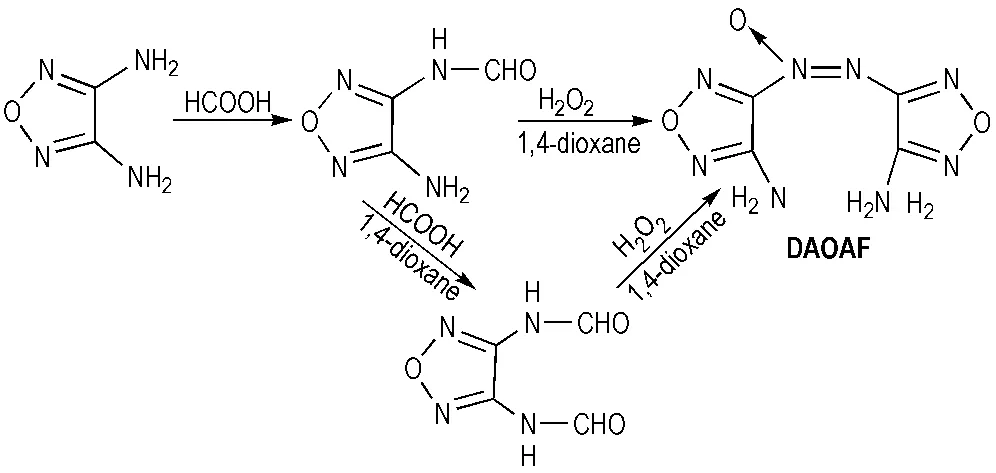
Scheme 27 Synthesis of DAOAF[77]
2003年,Blomquist 等[78]对推进剂用作气体发生剂中的产气燃料进行了研究,研究表明,3-硝胺-4-硝基呋咱羟胺(HANNF),是一类较好的产气燃料(Scheme 28)。Blomquist等人认为以HANNF为产气燃料的气体发生剂具有很大的发展潜力。
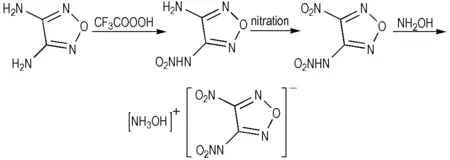
Scheme 28 Synthesis of HANNF[78]
7 前景展望
高产气量、高燃速、低燃温、无毒环保、热稳定性好、工艺性能好等特点,已经成为当今社会对气体发生剂的普遍要求,也必将成为今后气体发生剂的研究方向。叠氮类气体发生剂虽然成本低廉,但其本身具有毒性,存在许多环保难题,已经不能满足人们对气体发生剂的要求; 唑类、胍类、嗪类等气体发生剂无毒环保,并且具有很好的产气性能,是今后气体发生剂的研究重点。唑类、胍类和嗪类产气燃料本身具有产气量大、燃速快、燃温低和高氮无毒等优点,如果在唑类、胍类或嗪类产气燃料分子中引入含氧基团或含氧离子,使其更容易达到较好的氧平衡,进一步提高其产气性能,那么在气体发生剂领域将会有很好的发展前景,特别是在汽车安全气囊上的应用。
目前,含上述产气燃料的气体发生剂大多还停留在实验室阶段,还未大规模生产应用。今后的研究应进一步研究产气燃料的合成方法,优化其性能,尽快实现工业化生产。此外,应在理论研究的基础上,设计出性能优良、价格便宜、绿色环保的气体发生剂配方,早日将其应用到实际的生产和生活中。
参考文献:
[1] 张盛榜. 气体发生剂浅谈[J].火炸药,1980,5(7): 43-46.
[2] 王宏社, 杜志明. 烟火型气体发生剂研究进展[J].含能材料,2004,12(6): 376-380.
WANG Hong-du, DU Zhi-ming. Progress in Gas Generating Pyrotechnic Composition[J].ChineseJournalofEnergeticMaterials(HannengCailiao), 2004, 12(6): 376-380.
[3] 钟梅.瓜果保险技术的研究与应用[D]. 乌鲁木齐: 新疆大学,2006.
ZHONG Mei. Study and Application of the Techniques of Fruits preservation[D]. Wulumuqi: Xinjiang University, 2006.
[4] 雷永鹏, 阳世清, 徐松林, 等. 新型气体发生剂用非叠氮化合物可燃剂研究进展[J]. 化学推进剂与高分子材料, 2006, 4(6): 20-24.
LEI Yong-peng, YANG Shi-qing, XU Song-lin, et al. Research Progress of Non-Azide Fuel for New Gas Generant[J].ChemicalPropellants&PolymericMaterials. 2006, 4(6): 20-24.
[5] 徐松林, 阳世清, 岳守体. 偶氮四唑类高氮含能化合物的合成及表征[J]. 火炸药学报, 2005, 28(3): 52-54.
XU Song-lin, YANG Shin-qing, YUE Shou-ti. Synthesis and Characterization of High-Nitrogen Energetic Compounds Derived from Azotetrazolate[J].ChineseJournalofExplosives&Propellants, 2005, 28(3): 52-54.
[6] 李来才, 蔡皖飞, 张姝. 多氮含能材料的研究概述[J]. 四川师范大学学报, 2011, 34(5): 729-739.
LI Lai-cai, CAI Yuan-fei, ZHANG Shu. Review on Poly-Nitrogen Energetic Materials[J].JournalofSichuanNormalUniversity, 2011, 34(5): 729-739.
[7] Fowler M S, Benziger T M, Cady H H, et al. Castable ideal composite explosives containing ammounium nitrate[R]. Los Alamos Scientific Laboratory Report:LA-7398-MS. 1978.
[8] Pevzner M S, Kulibabina T N, Povarova N A, et al. Nitration of 5-amino-1,2,4-triazole and 5-acetamino-1,2,4-triazole by acetylinitrate and nitronium salt[J].KhimiyaGeterotsiklicheskikhSoedinenii, 1979 (8): 1132-1135.
[9] 朱朝阳, 曹一林, 孙忠祥, 等. 5,5′-二硝基-3,3′-偶氮基-1-氢-1,2,4-三唑(DNAT)的合成和性能研究[J]. 固体火箭技术, 2008, 31(5): 501-503.
ZHU Chao-yang, CAO Yi-lin, SUN Zhong-xiang, et al. Investigation on synthesis and properties of 5,5′-dinitro-3,3′-azo-1-hydro-1,2,4-triazole(DNAT)[J].JournalofSolidRocketTechnology, 2008, 31(5): 501-503.
[10] 李加荣. 3-硝基-1,2,4-三唑酮-5盐的研究概述[J]. 含能材料, 1999, 7(1): 12-15.
LI Jia-rong. A Review on 3-Nitro-1,2,4-Triazole-5-One Salts[J].ChineseJournalofEnergeticMaterials(HannengCailiao), 1999, 7(1): 12-15.
[11] 李芳, 杜志明. 氨基四唑含能化合物研究进展[J]. 化工进展, 2011, 30(11): 2481-2485.
LI Fang,DU Zhi-ming. Progress in energetic aminotetrazole compounds[J].ChemicalIndustryandEngineeringProgress. 2011, 30(11): 2481-2485.
[12] Poole D R. Azaide-free gas generant composition with easily filterable combustion products[P]. US: 5035757,1991.
[13] Edwards W W, Lund G K, Shaw III G C, et al. Non-azide gas generant formulation, method, and apparatus[P]. US:5197758,1993.
[14] Murotani M, Mura H , Takeda M , et al. Process for producing 5-aminotetrazole[P]. EP:669325,1994.
[15] Himo F, Demko Z P, Noodleman L, et al. Why is tetrazole formation by addition of azide to organic nitriles catalyzed by zinc(II) salts[J].JAmChemSoc, 2003, 125(33): 9983-9987.
[16] Himo F, Demko Z P, Noodleman L, et al. Mechanisms of tetrazole formation by addition of azide to nitriles[J].JAmChemSoc, 2002,124(41): 12210-12216.
[17] GAO Hai-xiang, Jean′ne M Shreeve. Azole-Based Energetic Salts[J].ChemicalReviews, 2011, (111): 7377-7436.
[18] 周小清,马卿,张晓玉,等.5,5′-肼基-双四唑的合成与性能[J].含能材料, 2011(3): 361-362.
ZHOU Xiao-qing, MA Qing, ZHANG Xiao-yu, et al. Synthesis and Properties of 5,5′-hydrazine-bitetrazole[J].ChineseJournalofEnergeticMaterials(HannengCailiao), 2011(3): 361-362.
[19] 周小清, 马卿, 张晓玉, 等. 5,5′-肼基-双四唑的合成与性能[J]. 含能材料, 2011(3): 361-362.
ZHOU Xiao-qing, MA Qing, ZHANG Xiao-yu, et al. Synthesis and Properties of 5,5′-hydrazine-bitetrazole[J].ChineseJournalofEnergeticMaterials(HannengCailiao), 2011(3): 361-362.
[20] 阳世清, 徐松林, 黄亨健, 等. 高氮化合物及其含能材料[J]. 化学进展, 2008, 20(4): 526-537.
YANG Shi-qing, XU Song-lin, HUANG Heng-jian, et al. High Nitrogen Compounds and Their Energy Materials[J].ProgressinChemistry, 2008,20(4): 526-537.
[21] Hammer A, Hiskey M, Holl G, et al. Azidoformamidinium and guanidinium 5,5 prime-azotetrazolate salts[J].ChemistryofMaterials, 2005, 17(14): 3784-3793.
[22] 徐松林, 阳世清. 偶氮四唑非金属盐类含能材料的合成与性能研究[J]. 含能材料, 2006,14(5), 377-380.
XU Song-lin, YANG Shi-qing. Synthesis and Properties of High-nitrogen Energetic Compounds Based on Azotetrazolate Nonmetallic Salts[J].ChineseJournalofEnergeticMaterials(HannengCailiao), 2006,14(5): 377-380.
[23] 阳世清, 徐松林, 雷永鹏. 氮杂环含能化合物的研究进展[J]. 含能材料, 2006, 14(6): 475-484.
YANG Shi-qing, XU Song-lin, LEI Yong-peng. Synthesis and Characterization of High-Nitrogen Energetic Compounds Derived from Azotetrazolate[J].ChineseJournalofEnergeticMaterials(HannengCailiao), 2006, 14(6): 475-484.
[24] Vinogradov V, Dalinger I, Shevelev S. N-Amination of pyrazoles: a general approach[J].MendeleevCommun, 1993, 3(3): 111.
[25] Schmidt R D, Lee G S, Pagoria P F, et al. Synthesis and properties of a new explosive 4-amino-3,5-dinitro-1H-pyrazole (LLM-116)[R]. Report UCRL-ID-148510, 2001.
[26] 汪营磊, 张志忠, 王伯周, 等. VNS反应合成LLM-116[J]. 火炸药学报, 2007, 30(6): 20-23.
WANG Ying-lei, ZHANG Zhi-zhong, WANG Bo-zhou, et al. Synthesis of LLM-116 by VNS Reaction[J].ChineseJournalofExplosives&Propellants, 2007, 30(6): 20-23.
[27] Barnes M W, Mendenhall Ivan V, Taylor R D. Alkail metal perchlorate-containing gas generants[P]. US:0016529A1,2006.
[28] Mendenhall I V, Smith R G. Micro-gas generation[P]. US:0217894,2008.
[29] Mendenhall I V, Lund G K. Gas generating compositions having glass fibers[P]. US:0116384,2010.
[30] Tkholdings Inc. Gas generant compositions. WO,054530[P], 2008.
[31] Khandhadia P S, Burns S P. Thermally stable nonazide automotive airbag propellants[P]. US:6306232, 2001.
[32] 关兵峰, 姚俊, 王小强. 新能源汽车安全气囊用气体发生剂研究进展[J]. 化学推进剂与高分子材料, 2012, 10(3): 17-22.
GUAN Bing-feng,YAO Jun, WANG Xiao-qiang. Research Progress in Gas Generants for Airbag of New Energy Source Automobile[J].ChemicalPropellants&PolymericMaterials, 2012, 10(3): 17-22.
[33] Mendenhal Ivan V,Taylor Robert D. Burn rate enhencemete via metal aminotetrazole hydroxides. US:20050098246[P],2005.
[34] 巴尼斯M W, 门登豪I V, 泰勒R D. 含有高氯酸铵的气体发生剂. 中国:1826301A[P],2006.
[35] 巴尼斯M W, 门登豪I V, 泰勒R D. 含有碱金属高氯酸盐的气体发生剂. 中国:101065340A[P],2007.
[36] Jean P Picard. Process for preparation of triaminoguanidine anditssalts. US:3813439[P],1974.
[37] Eugene F Rothgery. Process for producing triaminoguanidine nitrate and the high melting point product so produce. US:4800232[P],1989.
[38] Daniel R Satrinan, Verona N J. Preparationoftriaminoguanidine compounds from dicyandiamide. US:3285958[P],1966.
[39] Vernon E Haury, Simi Valley. Method of producing triaminoguanidinenitrate. US:3950421[P],1976.
[40] Kerry L Wagaman, Chester F Clark. Method of producing triaminoguanidinenitrate. US:5041661[P],1991.
[41] 徐松林, 阳世清. 三氨基硝酸胍的放大合成工艺及表征研究[J]. 化学推进剂与高分子材料, 2006, 4(3): 33-35.
XU Song-lin, YANG Shi-qing. Enlargement Synthesis Technology and Characterization of Triaminoguanidinium Nitrate[J].ChemicalPropellants&PolymericMaterials, 2006, 4(3): 33-35.
[42] Neutz J, Grosshardt O, Schaufele S, et al. Synthesis, Characterization and Thermal Behaviour of Guanidinium-5-aminotetrazolate(GA)-A New Nitrogen-Rich Compound[J].Propellants,Explosives,Pyrotechnics, 2003, 28(4): 181-188.
[43] 杨通辉, 何金选, 张海林. N-脒基脲二硝酰胺盐(FOX-12)的合成与表征[J]. 含能材料, 2004, 12(1): 36-37.
YANG Tong-hui, HE Jin-xuan, ZHANG Hai-lin. Synthesis and Characterization of FOX-12[J].ChineseJournalofEnergeticMaterials(HannengCailiao), 2004, 12(1): 36-37.
[44] 黄清华.四嗪及其衍生物的合成[D].南京:南京理工大学2010.
HUANG Qing-hua. Synthesis of tetrazine and its derivatives[D]. Nanjing: Nanjing Institute of Technology, 2010.
[45] 薛金强, 尚丙坤, 王伟. 四嗪类高氮分子及离子含能化合物的研究进展[J]. 化学推进剂与高分子材料, 2011, 9(4): 91-98.
XUE Jin-qiang, SHANG Bing-kun, WANG Wei. Research Situation and Development Trends of Degradable Polyurethane Materials[J].ChemicalPropellants&PolymericMaterials, 2011, 9(4): 91-98.
[46] 张海昊, 王伯周, 刘愆. 2-硝亚胺基-5-硝基-六氢化-1,3,5-三嗪(NNHT)的合成[J]. 火炸药学报, 2007, 30(6): 48-53.
ZHANG Hai-hao, WANG Bo-zhou, LIU Qian. Synthesis of 2-Nitroinino-5-nitrohexahydro-1,3,5-triazine (NNHT)[J].ChineseJournalofExplosives&Propellants, 2007, 30(6): 48-53.
[47] Huang D S, Rindone R R. High energy insensitive cyclic nitramines[P]. US:4937340, 1990.
[48] Cliff M D, Dagley I J, Parker R P. Synthesis of 2-nitroimino-5-nitro hexahydro-1,3,5-triazine[J].Propellants,Explosives,Pyrotechnics, 1998, 23(3): 179-181.
[49] 李永祥, 王建龙, 王艳红, 等. 一种合成2-硝亚胺基-5-硝基-六氢化-1,3,5-三嗪(NNHT)的新方法[J]. 有机化学, 2011,3 1(2): 256-259.
LI Yong-xiang, WANG Jian-long, WANG Yan-hong, et al. A Novel Synthetic Method of 2-Nitroimino-5-nitro-hexahydro-1,3,5-triazine (NNHT)[J].ChineseJournalofOrganicChemistry, 2011, 31(2): 256-259.
[50] Hyunh M, Hiskey M, Ernest L, et al.Polyazido high-nitrogen compounds: hydrazo-and azo-1,3,5-trizine[J].AngewChemIntEd, 2004, 43(37): 4924-4928.
[51] 周阳, 龙新平, 王欣, 等. 高氮含能化合物的研究新进展[J]. 含能材料, 2006, 14(4): 315-320.
ZHOU Yang, LONG Xin-ping, WANG Xin, et al. Review on High-Nitrogen Energetic materials[J].ChineseJournalofEnergeticMaterials(HannengCailiao), 2006, 14(4): 315-320.
[52] Hans-Heinrich Licht, Helmut Ritter. New energetic materials from triazoles and tetrazine[J].EnergeticMaterials,1994,12: 223-235.
[53] Hiskey M A, Chavez D, Naud D L. Insensitive high-nitrogen compounds[J]. NTIS, No: DE-2001-776133, 2001.
[54] Huynh M H V, Hiskey M A, Chavez D E, et al. Synthesis, characterization, and energetic properties of diazido heteroaromatic high-nitrogen CN compound[J].JournaloftheAmericanChemicalSociety, 2005, 127(36): 12537-12543.
[55] 阳世清, 徐松林. 3,6-二氨基-1,2,4,5-四嗪-1,4-二氧化物的合成与表征[J]. 含能材料, 2005, 13(6): 362-364.
YANG Shi-qing, XU Song-lin. Synthesis and Characterization of 3,6-Diamino-1,2,4,5-tetrazine-1,4-dioxide[J].ChineseJournalofEnergeticMaterials(HannengCailiao), 2005,13(6): 362-364.
[56] 潘劼, 何金选, 陶永杰. 3,6-二肼基-1,2,4,5-四嗪及其盐的合成与表征[J]. 含能材料, 2006, 14(2): 116-117.
PAN Jie, HE Jin-xuan, TAO Yong-jie. Synthesis and Characterization of 3,6-Dihydrazine-1,2,4,5-tetrazine and its Energetic Salts[J].ChineseJournalofEnergeticMaterials(HannengCailiao), 2006, 14(2): 116-117.
[57] 何冬梅, 程广斌, 吕春绪. 四嗪类高氮含能化合物的合成与表征[J]. 火炸药学报, 2010, 33(5): 8-11.
HE Dong-mei, CHENG Guang-bin, LV Chun-xu. Synthesis and Characterization of High-nitrogen Energetic Compounds Derived from Tetrazine[J].ChineseJournalofExplosives&Propellants, 2010, 33(5): 8-11.
[58] Hiskey M A, Chavez D E, Naud D. Preparation of 3, 3′-azobis (6-amino-1, 2, 4, 5-tetrazine), US: 6342589[P], 2002.
[59] 徐松林, 阳世清, 张炜, 等. 3,3′-偶氮-(6-氨基-1,2,4,5-四嗪)的合成及性能研究[J]. 化学通报, 2006(9): 685-689.
XU Song-lin, YANG Shi-qing, ZHANG Wei, et al. Study on the Synthesis and Performance of 3,3′-Azobis(6-amino-1,2,4,5-tetrazine)[J].Chemistry, 2006(9): 685-689.
[60] 岳守体, 阳世清. 3,6-双(1-氢-1,2,3,4-四唑-5-氨基)-1,2,4,5-四嗪的合成及其性能[J]. 含能材料, 2004, 12(3), 155-157.
YUE Shou-ti, YANG Shi-qing.Synthesis and Properties of 3,6-bis(1H-1,2,3,4-tetrazol-5-yl-amino)-1,2,4,5-tetrazine[J].ChineseJournalofEnergeticMaterials(HannengCailiao), 2004, 12(3): 155-157.
[61] Chavez D , Hiskey M. 1,2,4,5-Tetrazine based energetic materials[J].JournalofEnergeticMaterials, 1999, 17: 357-377.
[62] David E, Chavez D, Hiskey M. 3,3′-Azobis( 6-amino-1,2,4,5-tetrazine): A novel high nitrogen energetic material[J].AngewChemIntEd, 2000, 39(10): 1791-1793.
[63] Nielsen A T, Chan M L, Kraeutle C K. Polynitro-polyazacaged explosives, Part 7, NWC TP7200[R]. China Lake: Navel Weapons Center, 1989.
[64] 王昕, 彭翠枝. 国外六硝基六氮杂异伍兹烷的发展现状[J]. 火炸药学报, 2007, 30(5): 45-48.
WANG Xin, PENG Cui-zhi. Development of Hexanitrohexaazaisowurtzitane at abroad[J].ChineseJournalofExplosives&Propellants, 2007, 30(5): 45-48.
[65] 王才, 欧育湘, 陈博仁. 六硝基六氮杂异伍兹烷的一锅合成[J]. 北京理工大学学报, 2000, 20(4): 521-523.
WANG Cai, OU Yu-xiang, CHEN Bo-ren. One-pot Synthesis of Hexanitrohexaazaisowurtzitane[J].JournalofBeijingInstituteofTechnology, 2000, 20(4): 521-523.
[66] Daoud Sami. Dual-stage gas generator utilizing eco-friendly gas generant formulation, US: 6877435[P], 2005.
[67] Daoud Sami. Dual-stage gas generator utilizing eco-friendly gas generant formulation for military applications: US 6918340[P], 2005.
[68] 雷永鹏, 阳世清, 徐松林, 等. 钝感高能材料N-脒基脲二硝酰胺盐的研究进展[J]. 含能材料, 2007, 15(3): 289-293.
LEI Yong-peng, YANG Shi-qing, XU Song-lin, et al.Progress in Insensitive High Energetic MaterialsN-Guanylurea-dinitramide[J].ChineseJournalofEnergeticMaterials(HannengCailiao), 2007, 15(3): 289-293.
[69] Norman H, Lundstrom, Aaron J, et al. Pyrotechnic gas generant composition including high oxygen balance fuel, US: 6093269[P], 2000.
[70] Wheatley, Brian K, Greso, et al. Gas generant compositions exhibiting low autoignition temperatures and methods of generating gases therefrom: US 6673172[P],2004.
[71] 李战雄, 唐松青. 氧化呋咱衍生物的合成研究进展[J]. 含能材料, 2006, 14(1): 77-79.
LI Zhan-xiong, TANG Song-qing. Review on the Synthesis of Furoxan Derivatives[J].ChineseJournalofEnergeticMaterials(HannengCailiao),2006,14(1): 77-79.
[72] 高莉, 杨红伟, 伍波, 等. 五种呋咱衍生物的新法合成[J]. 含能材料, 2013, 21(2): 226-229.
GAO Li, YANG Hong-wei, Wu Bo, et al. New Synthetic Route of Five Furazan Derivatives[J].ChineseJournalofEnergeticMaterials(HannengCailiao), 2013, 21(2): 226-229.
[73] 雷晴, 陶永杰, 何金选. 偶氮呋咱和氧化偶氮呋咱的合成及表征[J]. 固体火箭技术, 2006, 29(5): 354-357.
LEI Qing, TAO Yong-jie, HE Jin-xuan. Synthesis and Characterization of Azofurazan and Azoxyfurazan[J].JournalofSolidRocketTechnology, 2006, 29(5): 354-357.
[74] 李占雄. 呋咱和氧化呋咱系含能化合物的合成、结构及性能研究[M]. 北京: 北京理工大学出版社, 2001.
[75] Solodyuk G D, Boldyrev M D, Gidaspov B V, et al. Oxidation of 3,4-diaminofurazan by peroxide reagents[J].ZhurnalOrganicheskoiKhimii, 1981, 17(4): 861-865.
[76] Hiskey M, Chavez D, Bishop R, et al. Use of 3,3′-diamino-4,4′-azoxyfurazan and 3,3′-diamino-4,4′-azofurazan as insensitive high explosive materials, US: 6358339[P], 2002.
[77] 吴敏杰, 陈树森, 金韶华, 等. 一种合成3,3′-二氨基-4,4′-氧化偶氮呋咱的新方法[J].含能材料, 2013, 21(2): 273-275.
WU Min-jie, CHEN Shu-sen, JIN Shao-hua, et al. A New Method to Synthesize 3,3′-Diamino-4,4′- azoxyfurazan(DAOAF)[J].ChineseJournalofEnergeticMaterials(HannengCailiao),2013, 21(2): 273-275.
[78] Blomquist, Harold R. Monopropellant smokeless gas generant materials[P]. US 6513834,2003.
