髂静脉支架植入后髂腔静脉连接部流场分布的PIV测试
2015-05-10张喜成奚斌黄才安陈兆雷徐淼潘广锐李晓强
张喜成 奚斌 黄才安 陈兆雷 徐淼 潘广锐 李晓强
·介入技术·
髂静脉支架植入后髂腔静脉连接部流场分布的PIV测试
张喜成 奚斌 黄才安 陈兆雷 徐淼 潘广锐 李晓强
目的 通过粒子图像测速技术(particle image velocimetry,PIV)测试髂静脉支架植入后对髂腔静脉连接部流场的影响。方法 制作髂腔静脉连接部的物理模型,利用甘油水溶液作为循环液,金属氧化颗粒作为示踪粒子,利用PIV技术对流场进行测试。结果 支架植入前,双侧髂静脉分腿的液体汇入下腔静脉后主流动方向基本位于中轴线,植入左髂静脉支架并覆盖对侧的髂静脉开口后,双侧髂静脉汇合后的液体主流动方向右偏移,流速无明显降低,未见到明显的涡流产生。 结论 髂静脉支架植入后覆盖对侧的髂静脉开口,PIV测试未见流速明显改变及明显涡流,表明裸支架植入后完全覆盖对侧髂静脉开口对局部流场影响较小。
髂静脉; 裸支架; 粒子图像测速技术
髂静脉受压综合征(Iliac vein compression syndrome, IVCS)是导致下肢深静脉血栓形成(DVT)和下肢慢性静脉功能不全的重要原因[1],腔内治疗是其首选治疗方法,多选择球囊扩张和支架植入术[2]。为避免支架植入后的移位及再狭窄,较多文献认为支架的前端需要部分或全部进入下腔静脉[3],如此覆盖对侧髂静脉的网状支架是否会造成血液回流障碍或血栓形成?目前研究多为回顾性临床研究,还缺乏前瞻性研究和相关的实验研究。
粒子图像测速技术(particle image velocimetry,PIV)是一种检测流场状态的可视化技术,近年也逐渐被应用于心血管系统的流场测试。本实验采用PIV技术对髂静脉的流场进行测试,观察支架植入前后的局部流场变化。
材料与方法
一、影像学资料的收集及数据测定
收集我院2008年5月—2013年11月行髂静脉CT静脉成像(CTV)检查的病例共100例,男56例,女44例,平均(43.2±7.6)岁。测量双髂静脉与下腔静脉之间的夹角,彩色多普勒测定50例健康人群的髂静脉血液流速、髂腔静脉直径,将这些数据进行归一化处理后制作下腔静脉、髂静脉的体外物理模型。
二、体外物理模型制作
采用模具灌注成型的玻璃管状模型,为倒“Y”型结构,该管状模型的的几何要求:下腔静脉、左右髂总静脉位于同一平面内,截面均为圆形。根据流动的相似性原理,以及为满足该实验中PIV测试所需的要求,本实验中的模型建立按照所测直径,依照1.2∶1的比例来制作髂腔静脉连接部的物理模型。
三、PIV测试的相关仪器设备
本实验中所进行的PIV测试,在扬州大学水利科学与工程学院的水利动力工程实验室进行,本实验所采用的PIV设备,为北京立方天地科技发展有限责任公司的MicroVec3 PIV系统,包括激光光源系统(DM3-4M350)、自相关/互相关摄像机(SMCCDB660)、同步器(MicroPulse 725)以及图像采集及分析处理系统(MicroVec3软件系统)。
四、PIV测试方法
1.测试装置的安装:本实验采用的主要循环装置如下:①髂静脉、下腔静脉连接部的玻璃管状模型;②循环储水箱,用于储存实验所用液体,通过软管连接玻璃的血管模型的上游和下游;③用于调节液体流速的流量计,可随时调节流体的流速;④用于驱动流体循环的动力泵,可将水箱的液体泵入玻璃管模型中;⑤用于检测流场相关信息的PIV系统。将制成的玻璃管状模型浸入装有甘油水溶液的玻璃水槽中固定,目的是减少激光照射产生的光线二次折射。下端两个髂静脉分腿分别通过2个软管与循环储存水箱内的循环动力泵连接,中间连接测定流速的流量计;通过循环动力泵的作用可以将水槽中的液体泵经两分腿进入玻璃管状模型,然后再从上方的下腔静脉主管以软管连接回流入水箱中。如此可保证储水箱中的水位维持稳定。
2.循环液及示踪粒子:为模拟黏度与血液相似的非牛顿流体特性,本实验循环液制作如下:将纯净水放置沉淀48 h后,取上层纯净水50 L,加入化学纯甘油17.5 L,该溶液密度ρ=1.1×103㎏/m3,黏度μ=3.75 mPa·s。本实验中循环流体的示踪粒子选用金属氧化颗粒,直径500 nm。该循环测试装置以及PIV测试设备的组成连接见图1。

图1 髂腔静脉连接部模型的流场测试示意图
3.PIV的实验过程:本研究重点为双髂静脉汇合部和下腔静脉远端的流场流速变化,故只对该部位的垂直平面进行PIV测量。搭建好实验平台,对测试系统反复调试,校准激光的片源,使其正好投照双髂静脉、下腔静脉分叉平面,CCD相机固定于片光源与模型中轴正交的前方约100 cm位置,保持CCD相机与检测区域同一水平。启动循环动力泵,使水槽中的流体经下端两个分腿进入模型。因流动的相似性原理,本实验中髂静脉流速调整为20 cm/min,调整激光片光源脉冲频率为50 Hz,每个脉冲能量为350 mj;CCD相机调整为12bit级灰度识别示踪粒子,采样频率为260帧/秒,记录所测区域流体的流动规律和PIV粒子图像,将图像信号传递到计算机处理系统。本实验测试项目分别为管状模型在支架植入前后的髂腔静脉连接部的流场变化情况。血管支架植入方法:从左侧髂静脉分腿中植入血管支架12 mm×80 mm(Maris,美敦力医疗有限公司,美国),支架前端完全进入下腔静脉、并完全覆盖对侧的髂静脉开口,见图2。
结 果
1.模型制作相关数据:根据所测得的髂、下腔静脉直径,按照1.2∶1的比例,本研究中所制模型的髂静脉直径为14 mm,腔静脉直径为22 mm。双侧分腿的夹角设计为70°,其中右髂腔静脉夹角为25°,左髂腔静脉夹角为45°。
2.支架植入前的流场测试情况:正常髂腔静脉流场测试情况的流速图与流线图见图3、4,从图中可以看出,两侧髂静脉分腿的流体以相同的流速汇合后进入下腔静脉,但流体汇合后的主流动方向基本位于下腔静脉的中央,双侧髂静脉汇合后的流场未见其他明显异常。

图2 髂静脉支架植入前端进入下腔静脉的示意图

图3 髂腔静脉连接部管状模型的流速图

图4 髂腔静脉连接部管状模型的流线图
3.植入血管支架后的髂腔静脉流场测试情况:将血管支架植入左髂静脉分腿,前端送入下腔静脉中,并完全覆盖右髂静脉开口。PIV测试流场测试情况见图5、6。从图中可见,支架植入后因受到金属支架的二次折射,示踪粒子的图像在支架部位受到一定程度的影响。双侧髂静脉血流以相同的流速汇入下腔静脉后,流体的主流动方向右侧明显偏移,血管支架的上缘与下腔静脉的左内壁之间的出现部分流速降低区域,但双髂静脉的流速并无变化,也未出现明显的涡流现象。

图5 支架置入后髂腔静脉的流场测试流线图,主流动方向右偏(黄箭头)
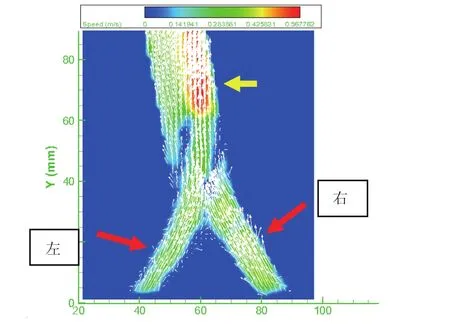
图6 支架置入后髂腔静脉的流场测试流速图,主流动方向右偏(黄箭头)
讨 论
IVCS是血管外科常见病之一,血管支架植入是其常用的治疗方法[4-6]。文献报道非血栓性的IVCS行支架植入术后3~5年通畅率高达90~100%,下肢深静脉血栓治疗后的髂静脉狭窄或闭塞的支架植入术,术后远期通畅率也达到67%~93%[3-4],提示髂静脉支架植入具有良好的远期通畅率。
在植入的髂静脉支架近端的具体定位目前尚有争议,有学者认为如支架进入下腔静脉过少,后期支架容易受压移位,建议支架进入下腔静脉20~30 mm[3-4,7]。Hartung等[3]研究发现:血管支架前段完全进入下腔静脉者,术后发生对侧髂静脉闭塞或深静脉血栓形成的风险在0.9%~1%以下,相反如支架前端仅覆盖髂静脉病变,未完全进入下腔静脉者,则患侧的髂静脉远期再狭窄或闭塞的风险高达40%。但也有研究认为支架头端应尽量较少进入下腔静脉,以避免覆盖对侧髂静脉开口,减少影响血液回流或对侧形成血栓的可能性[8]。因此,髂静脉支架头端是否需进入下腔静脉,覆盖对侧的髂静脉是否影响其血液回流,尚需进一步的研究论证。
PIV技术是目前检测流场最准确的可视化技术,近年发展较快[10-12]。其原理是通过在体外构建流体模型,选择有良好跟随性的示踪粒子,这些粒子在流经特定平面时被脉冲激光连续照亮2次,数字照相技术将粒子图像拍摄记录下来,通过计算机图像软件的后续处理,就可得到示踪粒子在某个特定时间内的位移,计算出流场的相关信息。这样通过PIV技术,我们就可相对准确详尽的得到同一时刻的流场特点。
目前国内外对髂腔静脉的流体动力学方面鲜有研究,在髂静脉狭窄的局部流场变化、支架植入后对流场的影响等方面了解甚少。本研究发现在髂静脉支架植入前,双侧髂静脉分腿的血流汇合后,流体的主流动方向基本位于中轴线。植入左髂静脉支架后,因裸支架网丝遮挡作用,较大角度的左髂静脉血流受到来自右髂静脉血流的冲击力减少,主流动方向在下腔静脉向右侧偏移。另外,在支架的上方与下腔静脉的左内侧壁支架也出现一定区域的低流速区域。但支架植入前后,双侧髂静脉血液回流的流速无变化,也未见明显的涡流区域。
本实验证实支架植入后对髂腔静脉连接部的血液流速的影响并不明显,这与我们原来的设想不同,提示在髂静脉支架植入的早期,还不会对局部的流场造成明显的干扰。在支架和下腔静脉左侧壁之间有一定的流速降低区域,该区域在后期是否容易引起局部大分子物质的沉积、诱发局部血栓形成,或促进血管内膜增生等,今后还需进一步研究。
1 董国祥.应重视髂静脉压迫综合征的诊断和治疗[J].中国血管外科杂志,2012,4(1):1-5.
2 Meng QY, Li XQ, Qian AM, et al. Endovascular treatment of iliac vein compression syndrome[J]. Chin Med J (Engl),2011,124(20):3281-3284.
3 Hartung O.Results of stenting for postthrombotic venous obstructive lesions[J]. Perspect Vasc Surg Endovasc Ther ,2011,23(4):255-260.
4 Neglén P, Hollis KC, Olivier J, et al. Stenting of the venous outfow in chronic venous disease: long-term stent-related outcome, clinical, and hemodynamic result[J]. J Vasc Surg,2007,46(5):979-990.
5 Kibbe MR,Ujiki M,Goodwin AL,et al.Iliac vein compression in all asymptomatic patient population[J].J Vasc Surg,2004,39(5):937-943.
6 Rosales A, Sandbæk G, Jørgensen J.Stenting for chronic postthrombotic vena cava and iliofemoral venous occlusions: mid-term patency and clinical outcome[J].Eur J Vasc Endovasc Surg,2010, 40(2):234-240.
7 Ye K,Lu X,Li w,et al. Long-term outcomes of stent placement for symptomatic nonthrombotic iliac vein compression lesions in chronic venous disease[J].J Vasc Interv Radiol, 2012, 23(4):497-502.
8 Park JY, Ahn JH, Jeon YS,et al.Iliac vein stenting as a durable option for residual stenosis after catheter-directed thrombolysis and angioplasty of iliofemoral deep vein thrombosis secondary to May-Thurner syndrome[J]. Phlebology,2014,29(7):461-470.
9 Barbaro V,Grigioni M,Daniele C,et al.Principal stress analysis in LDA measurement of the fow feld downstream of 19-mm Sorin Bicarbon heart valve[J].Technol Health Care, 1998,6(4):259-270.
10 朱光宇, 袁奇, 陈珍. 狭窄血管内流场的PIV实验研究[J].西安交通大学学报,2010,44(6):120-124.
11 于凤旭,廖斌,石应康,等.体外人颈动脉血管分叉模型的建立[J].四川大学学报(医学版),2007,38(6):1029-1032.
12 于凤旭,石应康,邓万权,等.颈动脉分叉管模型流场分布的PIV测量[J].生物医学工程杂志,2007,24(1):104-108.
The study of particle image velocimetry in measuring the fow felds distribution at the iliocava junction afteriliac venous stent implantation
Zhang xicheng*, Xi Bin, Huang Caian, Chen Zhaolei, Xu Miao,Pan Guangrui, Li Xiaoqiang.*Clinical Medicine College of Yangzhou University, Yangzhou 225001,China
Li Xiaoqiang, Email:fytsg@126.com
Objective To discuss the impact of iliac venous stent implantation upon the contralateral iliac vein detected by particle image velocimetry (PIV). Methods The iliocava junction models were in vitro constructed , The working fuid consists of glycerine and water mixed similar to human blood,and the metal oxide particles were used to be the tracer particles.PIV technology was used to study the flow fields of the iliocava junction models. Results Before the stent implantation, bilateral iliac venous blood fows converged at the inferior vena cava and the main blood fow was located at the middle axes. Then the bare stent was implanted into the left iliac vein,proximal end of the stent completely covered the opening of the right iliac vein and entered into the inferior vena cava.The direction of the main convergence fow of bilateral iliac venous fuid was signifcant shifted to the right side. Neither signifcant reduction in the velocity of bilateral iliac , venous fow nor obvious eddy current was observed. Conclusions After iliac venous stent implantation,and it's proximal end entered into the inferior vena cava, PIV revealed moderate changes in the velocity felds of the iliocava junction before and after stent implantation, suggesting that complete coverage of bare stent on the opening of contralateral iliac vein seldom affects its blood fow after stent implantation.
Iliac vein; Bare stent; Particle image velocimetry
2015-10-20)
(本文编辑:王剑锋)
10.3877/cma.j.issn.2095-5782.2015.04.010
225001,扬州大学临床医学院(张喜成,陈兆雷,徐淼,潘广锐);扬州大学水利学院(奚斌,黄才安);苏州大学附属第二医院血管外科(李晓强)
李晓强,Email:fytsg@126.com
张喜成,奚斌,黄才安,等.髂静脉支架植入后髂腔静脉连接部流场分布的PIV测试[J/OD].中华介入放射学电子杂志, 2015,3(4):211-214.
