未足月双胎胎膜早破的40例临床观察
2015-05-05杨利何春梅古素芬
杨利 何春梅 古素芬
双胎妊娠是指在一次妊娠中,孕妇子宫中同时有两个胎儿,为多胎妊娠中的常见的一种。其虽为一种生理现象,但在妊娠期、分娩期和产后极易出现多种产科并发症和合并症,且发生率显著高于单胎妊娠患者的,因此,临床医师高度重视双胎妊娠患者。双胎妊娠发生率同种族、民族、遗传、营养因素、母亲年龄、胎次和垂体促性腺激素之间具有一定关系。目前,随着促排卵药物和辅助生殖技术的应用,双胎妊娠发生率逐渐上升,但随之而来的双胎妊娠发病率也逐渐上升,其给妇产科医生带来较大的挑战。临床上,双胎妊娠风险显著高于单胎妊娠的,且双胎妊娠患者出现早产和胎膜早破发生率较高[1]。未足月胎膜早破又被称之为足月前胎膜早破或早产胎膜早破,是孕妇妊娠没有达到37周,胎膜在孕妇临床前自发性破裂,其全部妊娠中其发生率为2.0%~3.5%,占早产的30%~40%。未足月双胎胎膜早破发生率为30.77%,其主要因胎儿体重较小,极易出现新生儿窒息、呼吸窘迫综合征、败血症和死亡等现象[2]。通过临床研究证明,孕妇越接近足月时,其胎膜早破发生率越高,且主要出现在34周后,高达81%,34周前的发生率约为19%。为进一步了解未足月双胎胎膜早破的临床特点和妊娠结局进行研究,结果如下。
1 资料与方法
1.1 一般资料 选取本院在2011年6月-2013年2月收治的40例未足月双胎胎膜早破患者设为治疗组和40例未足月单胎胎膜早破患者设为对照组。其中,治疗组患者平均年龄(25.32±3.52)岁,26例为初产,14例为经产;对照组患者平均年龄(26.01±3.21)岁,27例为初产,13例为经产。对本次研究选取患者的一般资料进行比较,差异无统计学意义(P>0.05),具有可比性。
1.2 诊断标准 根据人民卫生出版社《妇产科学》(第7版)胎膜早破诊断标准对本次研究选取患者进行诊断。胎膜早破孕妇具有下列症状,未足月孕妇突感有较多液体从阴道流出,之后少量间断性排出;孕妇做打喷嚏、负重和咳嗽等增加腹压动作时,羊水便从阴道流出,肛诊将胎先露部上推流液量增多,可确诊。辅助检查:石蕊试纸pH值≥6.5;窥阴器检查见羊水从宫颈口流出;吸管吸出宫颈管中液体涂于玻片上,酒精灯加热10 min后变成白色为羊水;阴道液干燥涂片见羊齿状结晶等。
1.3 方法 患者入院后均按照胎膜早破常规护理措施对其进行护理,指引其绝对卧床休息并将臀部抬高,保持外阴清洁。尽可能避免不必要的肛诊和阴道指检。根据患者病史和超声检查对其孕周胎龄进行确定,充分了解胎儿生长状况、剩余羊水量、胎位和胎儿是否大体异常等,同时,对患者体温、心率、阴道流液状况、子宫是否有压痛和血常规白细胞计数等进行仔细观察。对于怀疑有感染患者,应对其进行超敏C-反应蛋白检查。对于胎膜早破不伴感染、羊水池深度≥3 cm且胎儿没有出现窘迫的患者,通过期待疗法进行治疗,同时,肌注塞米松1次/8 h,6 mg/次,共肌注6次,促使胎肺成熟。20周之上的患者用5 g/30 min硫酸镁抑制宫缩,之后按照1.5~2 g/h的剂量进行治疗,直至宫缩被抑制,维持12~24 h,同时口服安宝。通过常规抗生素对患者进行3~7 d的抗感染治疗。对于妊娠周期≥35周、宫颈成熟、短时间内能阴道分娩且胎位正常的患者,可实施引导试产。对于宫颈不成熟、胎位异常、胎肺成熟、胎儿窘迫和合并感染的患者,实施剖宫产。对于孕周<34周的患者,应对患者和胎儿进行密切检查,并给其相应的保胎治疗,对于不能避免早产的患者,应即刻通过肌肉注射的方法给以其10 mg的糖皮质激素地塞米松,在一定程度上促使胎儿肺成熟。对于保胎有效的患者,肌内注射方法给以其地塞米松每12小时1次,6 mg/次,共用药4次。同时,通过静脉滴注的方法给以其30~60 mL/d的25%的硫酸镁或是静脉滴注50~100 mg/d的利托君,便于有效抑制宫缩。对于破膜12 h之上的患者,应通过常规抗生素对其进行治疗,有效预防感染。在对患者进行保胎治疗过程中,对于出现不可避免的宫内感染征象和胎儿窘迫等终止妊娠指征的患者,不管其孕周大小应即刻终止妊娠,降低患者死亡率。
1.4 观察指标 对两组患者并发症发生率、围生期状况、处理方法和妊娠结局进行密切观察。
1.5 统计学处理 采用SPSS 18.0统计学软件进行处理,计量资料以(x-±s)表示,比较采用t检验,计数资料采用 字2检验,以P<0.05为差异有统计学意义。
2 结果
2.1 两组患者并发症发生率的比较 治疗组患者贫血占25.00%(10/40)、妊娠期高血压疾病占22.50%(9/40)、胎儿生长受限占20.00%(8/40)、产后出血占17.50%(7/40)、妊娠糖尿病占5.00%(2/40)、羊膜腔感染发生率为7.50%(3/40);对照组患者分别为12.50%(5/40)、7.50%(3/40)、5.00%(2/40)、5.00%(2/40)、2.50%(1/40)和 5.00%(2/40)。两组患者并发症发生率比较,治疗组患者贫血、妊娠期高血压疾病、胎儿生长受限、产后出血均显著高于对照组患者,两组比较差异有统计学意义(P<0.05);两组患者妊娠糖尿病、羊膜腔感染发生率相比,差异无统计学意义(P>0.05)。
2.2 两组患者围生期状况和处理方法比较 两组患者围生期状况和处理方法比较,差异有统计学意义(P<0.05),见表1。
2.3 两组患者妊娠结局比较 对两组患者妊娠结局进行比较,差异有统计学意义(P<0.05),见表2。
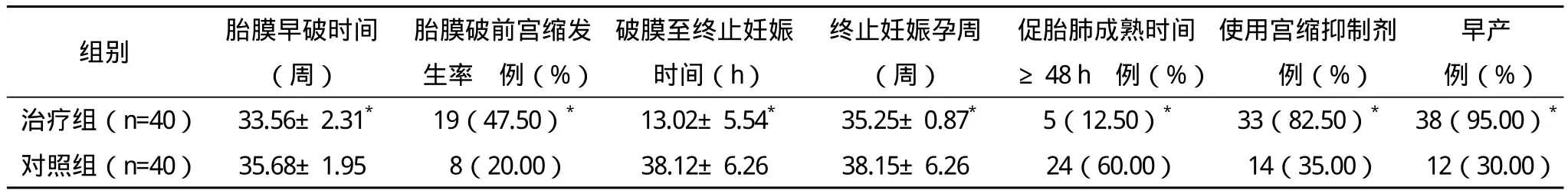
表1 两组患者围生期状况和处理方法的比较

表2 两组患者妊娠结局比较
3 讨论
临床上,未足月孕妇出现胎膜早破中7.7%~9.7%胎膜早破患者的胎膜破口可以自然愈合。基于羊膜腔处于和外界相通的状态,并伴有羊水持续渗漏现象,极易导致孕妇和胎儿出现一系列并发症,威胁母婴健康。其中,孕妇面临的危险为绒毛膜羊膜炎、脐带脱垂、难产、产后出血和胎盘早剥等,胎儿可能出现早产、四肢变形、胎儿窘迫、挛缩、新生儿感染、胎位变化和死亡等现象,给妊娠和分娩带来不利影响,进而在一定程度上提高早产率、宫内感染率、围生儿病死率和产褥病率,为产科严重并发症之一。从上世纪50年代开始,相关人士对未足月胎膜早破病因和发病机制进行研究分析,但到目前依旧没有明确的、确切的发病机制。多数学者认为其由多种因素造成,缺乏根本性的预防措施。因此,未足月胎膜早破处理方法为产科中面临的最具挑战性问题。胎膜早破发生时间越早,其临床处理就越困难。为减少胎膜早破对孕妇和胎儿带来的威胁,相关研究人员表明应通过使用宫缩抑制剂在一定程度上延长孕妇孕周,促使胎儿肺成熟,便于获得可存活的胎儿和提高新生儿生存质量。同时,对孕妇进行保胎治疗时,因延长孕妇保胎时间,羊水持续外漏,在一定程度上增加感染可能性,并加重感染程度。感染严重的和严重羊水过少的会给胎儿和新生儿的发育带来严重影响,病情严重的威胁孕妇和胎儿生命。针对该种现象的出现,是通过期待治疗方法对孕妇进行治疗,还是通过终止妊娠方法对孕妇进行治疗,应从孕妇孕周、有无羊膜腔感染、胎儿成熟度、破膜后引起的母婴并发症、新生儿重症监护水平和早产儿治疗水平等综合因素进行考虑,尽可能降低孕妇、胎儿和新生儿死亡率,改善其预后。未足月双胎胎膜早破发生率在7.11%左右,但未足月单胎胎膜早破发生率仅为2.00%~3.51%。胎膜早破没有明确的病因,目前,通过临床研究证明,单胎妊娠生殖原微生物上行性感染为胎膜早破最常见因素,但国外学者认为感染为妊娠30周后出现双胎胎膜早破的结局,并非其原因[3-6]。通过临床研究证明,多次妊娠、感染等为导致未足月双胎胎膜早破的相关因素,其中,多次妊娠占据重要地位,正常情况下,妊娠中晚期孕妇宫颈内口为关闭状态,其对胎膜完整性具有较高的保护作用。但因为多次妊娠导致引产患者宫颈损伤,进而使得宫颈生理屏障功能遭到破坏,宫颈承受张力的能力下降。伴随着妊娠的发展,宫腔压力增加,胎膜进入扩张的内口中,形成楔形扩展外口,导致胎膜暴露在阴道中,进而感染阴道炎症,因此,应加强对患者进行健康教育,应有计划准备妊娠,减少流产次数,进而在一定程度上减轻对宫颈带来的损伤,最终降低胎膜早破发生率。感染在出现胎膜早破临床上具有一定作用,通过流行病学、临床、组织学、分子生物资料和微生物学提示感染或炎症在一定程度上增加了胎膜早破发生。细菌感染为出现胎膜早破的起始因子,由感染产生的炎症为真正造成患者出现胎膜早破的原因。胎膜早破发生孕周越小,其感染监测率越高。感染可由细菌、沙眼衣原体、病毒、生殖支原体和弓形虫等产生,其通过宫颈口对胎膜产生一定感染,也可能通过血行播散到子宫和胎盘。病原体及其代谢产物刺激局部产生炎症反应,释放蛋白水解酶,导致胎膜组织变脆,极易出现破裂,威胁患者和胎儿健康。此时,医护人员应预防性或是治疗性的用抗生素对其进行治疗,在一定程度上防止下生殖道感染扩散,同时,延长患者妊娠时间,降低新生儿感染发生率。除此之外,还有其他因素导致患者出现胎膜早破,威胁其健康和预后。如妊娠期高血压疾病患者全身小动脉痉挛,导致其肝细胞相对缺氧和肝功能受损,致使患者胎盘胎膜缺血、缺氧和营养不良,出现胎膜发育不良。同时,性交机械刺激会给胎膜带来一定损伤,也会增加感染机会,且精液中的PG也会诱发子宫收缩产生胎膜早破等,因此应给予患者相应健康教育,降低患者和胎儿死亡率,改善其预后。
临床上,相关学者认为双胎妊娠的特点(子宫容量过大、过度膨胀和盆腔血管受压)为导致其出现胎膜早破的主要因素,同时,双胎妊娠患者合并胎位异常、胎膜受力不均等为常见因素,双胎妊娠合并症较多,出现高血压疾病、妊娠期肝内胆汁淤积症、贫血等疾病发生率高于单胎患者的,其均会导致患者出现自发性宫缩,继而出现胎膜早破[7-10]。针对双胎胎膜早破的临床特点和原因,医护人员通过相应的处理措施对其进行处理,妊娠周期短的新生儿,面临体重低、呼吸窘迫率高和窒息率高等风险,因此,应通过长时间的期待治疗方法进行治疗,通过地塞米松促使胎肺成熟,预防感染和抑制宫缩,改善新生儿预后等。本次研究中,82.50%的双胎患者破膜后使用宫缩抑制剂,但是单胎患者破膜后仅有35.00%的使用宫缩抑制剂,究其原因,主要因为双胎妊娠患者并发症较多,且程度较重。胎膜早破后患者宫腔内压在短时间内降低,极易临产,纵使使用宫缩抑制剂也不能延长孕周。胎膜早破后预防性使用抗生素可有效延长妊娠时间,降低患者和围生儿感染率,但是保胎时间过长,极易导致宫腔出现感染,不能继续保胎[11-13]。因此,双胎患者及其家属多数选择剖宫产,本次研究中,双胎患者破膜后剖宫产率高达90.00%,但单胎患者破膜后仅有57.50%。
随着双胎妊娠数量增加,其风险逐渐受到关注。早产为双胎妊娠常见并发症,为新生儿死亡和出现疾病的主要因素。因此,在双胎妊娠中晚期,应加强对其进行产前监护和孕产妇系统管理,对于高危妊娠患者做到早预防、早发现和早处理,预防性的使用宫缩抑制剂便于减轻患者宫腔压力,有效预防、减少胎膜早破和早产[14-15]。胎膜早破后,对其实施积极预防治疗感染和促胎肺成熟,在一定程度上加强胎儿宫内状况检测、患者感染状况检测等,实施保胎期待治疗,并根据胎儿孕周、成熟度、医院抢救水平等,制定相应的处理措施,改善患者和新生儿预后。
[1]黄平,靳卓芳,陈光元.未足月胎膜早破172例临床分析[J].当代医学,2011,17(18):86-87.
[2]汤则男,张欢,孙国强.欣普贝生用于未足月胎膜早破引产临床观察[J].医学信息,2011,24(2):659-660.
[3]林凤琼.未足月胎膜早破158例临床研究[J].中国医学创新,2013,10(11):112-113.
[4]李文媚.未足月胎膜早破112例临床分析[J].海南医学,2011,22(1):63-64.
[5]唐秋英.未足月胎膜早破102例临床分析[J].中国妇幼保健,2011,26(21):3354-3355.
[6]辛辉,周杜娟.未足月胎膜早破90例临床观察与分析[J].安徽医学,2014,35(9):1280-1281.
[7]李嘉,苏利,唐惠容.未足月双胎胎膜早破46例临床分析[J].中国医药导报,2012,9(2):71-73.
[8]陈美霞,方善红,黄月娇.胎膜早破96例妊娠结局临床分析[J].现代生物医学进展,2011,11(S2):5083-5085.
[9]宋美兰,贾艳艳.妊娠晚期未足月胎膜早破208例临床分析[J].华中科技大学学报(医学版),2011,40(4):486-489.
[10]库尔班尼沙·阿不力孜.妊娠晚期未足月胎膜早破40例临床分析[J].中国社区医师(医学专业),2012,14(25):129.
[11]张素琼.273例未足月胎膜早破的临床分析[J].现代医院,2014,14(2):30-32.
[12]赵晓红,王岭梅.135例胎膜早破的临床观察和护理[J].重庆医学,2013,42(19):2261-2262.
[13]黄雪梅.42例未足月双胎胎膜早破的临床分析[J].中国医药指南,2013,11(24):561-562.
[14]李文媚.未足月胎膜早破112例临床分析[J].海南医学,2011,22(1):63-64.
[15]王新春,徐佩风,朱丽红.未足月胎膜早破的临床分析与处理[J].新疆医学,2014,44(1):69-71.
