雷替曲塞联合洛铂治疗晚期消化道肿瘤疗效观察
2015-05-05李伟兵
俞 晨,李伟兵
(江苏省肿瘤医院 中西医结合科,江苏 南京 210000)
雷替曲塞联合洛铂治疗晚期消化道肿瘤疗效观察
俞 晨,李伟兵
(江苏省肿瘤医院 中西医结合科,江苏 南京 210000)
目的:观察雷替曲塞联合洛铂治疗晚期消化道肿瘤的疗效及安全性。方法:19例IV期消化道肿瘤患者使用雷替曲塞联合洛铂的治疗方案进行化疗。雷替曲塞总剂量为2.6mg/m2,第一天使用,洛铂总剂量为30mg/m2,和雷替曲塞同一天或在其后一天使用,均以21d为1个周期,进行2个周期的治疗。治疗2个周期后观察化疗前后病灶大小以及肿瘤指标的变化,评价不良反应。结果:全组共19例,获得部分缓解或疾病稳定10例(52%),无缓解或病情进展9例(48%),有效率52%。患者的血细胞抑制、肌肉关节痛、胃肠道反应、肝功能异常发生率分别为 57%、10%、30%、25%。血清肿瘤标记物CA125、CEA及CA19-9治疗后有效患者呈下降趋势。结论:雷替曲塞联合洛铂治疗晚期消化道肿瘤(胃癌,肠癌)能提高患者的生存率和临床缓解率,且不良反应轻,值得推广。
雷替曲塞; 洛铂; 消化道肿瘤
消化道肿瘤是目前我国常见的恶性肿瘤,化疗依然是消化系统恶性肿瘤的主要治疗方法,目前以含有奥沙利铂或者顺铂的治疗方案最为普遍,但不良反应较重。洛铂为第三代铂类抗癌药,抗瘤谱广,不良反应轻,水溶性好,抗癌活性较强,与其他铂类药物无交叉耐药性,并且消化道反应及肾毒性均小于顺铂[1]。主要用于治疗乳腺癌、小细胞肺癌、慢性粒细胞白血病[2]。但是近年来以洛铂为主的化疗方案已开始用于各种晚期消化道肿瘤的治疗。国内外多项临床研究表明,洛铂除用于适应征已经批准的三种恶性肿瘤外,对淋巴瘤、非小细胞肺癌、食管癌、结直肠癌和胃癌等具有明显的抗癌活性[3-4],常见不良反应为骨髓抑制,特别是血小板减少症的发生率最高。雷替曲塞是一种较强的胸苷酸合成酶抑制剂,主要用于治疗肠癌。但临床试验表明其有更广阔的抗瘤谱,在胃癌[4]、食管癌[5-6]和胸膜间皮瘤[7]均具有明显的抗肿瘤作用。目前国内外关于雷替曲塞联合洛铂治疗消化道肿瘤鲜有报道,本文对19例使用雷替曲塞联合洛铂治疗晚期消化道肿瘤的患者进行回顾性研究,详细如下:
1 临床资料
1.1 一般资料
19例患者为2011年1月至2015年1月期间在江苏省肿瘤医院就诊的晚期消化道肿瘤患者(胃癌,肠癌),病理证实为癌。经CT或MRI检查报告提示为晚期消化道肿瘤患者。已有组织学病理确诊,纳入标准:年龄≤80岁,ECOG≤2分,分期IV期,X线片显示无胃肠穿孔征象,无消化道出血;总胆红素、谷草转氨酶和谷丙转氨酶≤ 2.0×正常值上限;血肌酐≤13.3mmol/L;白细胞≥4.0×109/L,血小板≥100×109/L,血红蛋白≥90g/L;无其它严重的内科疾病。所有患者均无化疗禁忌证,心电图无明显异常;有可测量病灶;化疗有效率分为:完全缓解(CR)、部分缓解(PR)、稳定(SD)、进展(PD);不良反应有:血液学毒性(白细胞、血小板下降)、肌肉或关节痛、胃肠道反应、肝功能损伤等[8]。
排除标准:患者在使用此治疗方案时加用其他化疗药;孕期或哺乳期妇女;某些无法预知的心理或者医疗状况,药物滥用、患者不能完成本试验、患者对治疗成分过敏。
2011年01月至2015年01月之间符合入组条件患者共19例,男性16例,女性3例,年龄为39~79岁,中位年龄56岁。直肠癌9例,结肠9例,胃癌1例。均为肿瘤晚期术后患者辅助化疗。转移部位: 肺11例,淋巴结7例,肝11例,骨3例,腹腔积液、胸腔积液3例,盆腔附件4例,其他部位3例;病理类型均为腺癌。
1.2 治疗方法
化疗方案:雷替曲塞(天津正大天晴药业有限公司,2mg/支,批号:131018,131217 141219)2.6mg/m2,加入生理盐水100ml中静脉滴注,静脉滴注时间大于15min,洛铂(海南长安国际制药有限公司,10mg/支,批号:20140102,20130301,20120304)总剂量为30mg/m2,加入5%葡萄糖水500mL中静脉滴注,与雷替曲塞同一天或其后分次应用。化疗期间常规给予保肝护胃支持治疗同时予以5-羟色胺受体拮抗剂预防性止吐,部分患者给予胃复安或地塞米松加强止吐,一个周期为21d。如果前一周期出现3~4度以上白细胞、粒细胞减少给予粒细胞集落刺激因子治疗,如果出现3~4度血小板减少给予血小板生成素或者白介素-11治疗,出现肌肉痛或肝功能损伤时给予积极对症处理。化疗期间每个治疗周期前复查肝肾功能、血常规,两个治疗周期结束后复查CT或MRI等。
1.3 疗效及不良反应评价
①除浅表可直接测量的病灶外,采用CT或MRI检查测量肿瘤病灶的大小,根据RECIST标准评估疗效[15](表1)。CR+PR等于总有效率(ORR)。CR+PR+SD等于疾病控制率(DCR)。②并按照美国国立癌症研究院(NCI)提出的药物不良反应评价标准(NCI-CTC, V3.0)对不良反应的严重程度进行分级,结果见表2。

表1 RECIST评估标准

表2 NCI-CTC常见毒性分级标准
1.4 血清CA19-9、CA125、CEA水平测定
取肿瘤患者入院后空腹12h 的外周静脉血5ml,3000r/min 离心10min,分离血清后置-80℃保存待用。采用酶联免疫法(ELISA)测定三种肿瘤标志物(CEA、CA19-9、CA125)水平,试剂盒由瑞典CanAg公司提供,严格按试剂盒说明书进行操作。以CEA>5.0μg/L、CA199>30U/ml、CA125>35U/ml为阳性判定标准,患者治疗后较治疗前下降大于等于10%为下降趋势,下降小于10%或上升为上升趋势。
1.5 统计学
2 结果
2.1 近期疗效
全组19例患者,其中近期疗效:CR 0例、PR 4例( 21%)、SD6例( 31%),总有效率ORR(CR+PR)为 21%。疾病控制率DCR(CR+PR+SD)为52%。
2.2 不良反应
全组19例患者,其中骨髓抑制最常见,白细胞下降患者有7例占36%,血小板下降有2例占10%,血红蛋白下降有3例占15%,肌肉或关节痛有2例占10%,胃肠道反应有6例占30%,肝损害有5例占25%,无肾功能异常,未发现过敏反应(表3)。
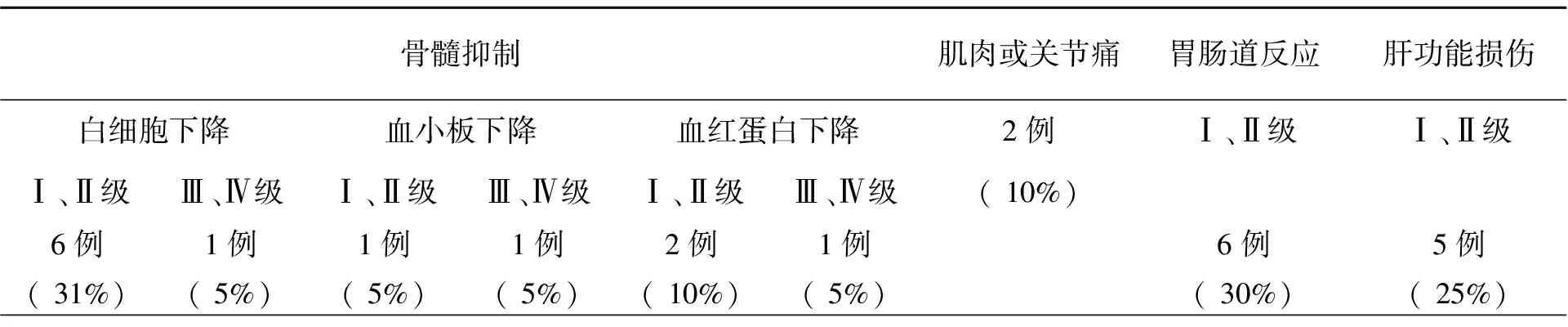
表3 化疗后不良反应
2.3 肿瘤标志物变化趋势与疗效的关系
本组3项标志物变化趋势相符者9例;2例表现为CEA和CA199呈下降趋势而CA125呈上升趋势,2例表现为CA199和CA125呈下降趋势而CEA呈上升趋势,2例表现为CEA呈下降趋势而CA125和CA199呈上升趋势。3例表现CA125呈下降趋势而CEA和CA199呈上升趋势,本组标志物呈下降趋势者13例,呈上升趋势者44例。呈下降趋势者ORR及DCR均明显高于呈上升趋势者,P均<0.05(表4)。
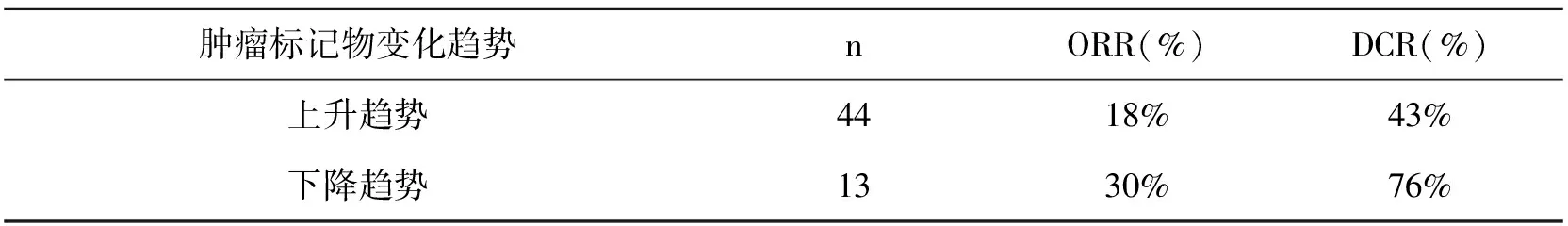
表4 肿瘤标记物变化趋势与疗效的关系
3 讨论
目前对于晚期复发胃肠道肿瘤的主要治疗手段是化疗。与最佳支持治疗相比,化疗能够显著延长患者生存期,改善其生存质量[3]。晚期肠癌患者目前多主张使用氟尿嘧啶或其类似物为基础的化疗方案。由于氟尿嘧啶需持续静脉泵入,使用不方便。多年来不断出现新的氟尿嘧啶类似物,其中雷替曲塞以其独特的作用机制和方便性引起了人们的兴趣。五项大型的二期临床试验和四项大规模三期临床试验[9]均证实,雷替曲塞和氟尿嘧啶/亚叶酸钙的治疗方案疗效相当,使用方便,花费更少,毒性可控,目前该药已经在全球29个国家或地区批准上市。雷替曲塞最初是由RoyalMarsden医院和英国Zeneca公司合作开发的一种喹唑啉叶酸盐类似物,1996年在英国上市,它属于细胞毒类抗肿瘤药,主要通过抑制胸腺嘧啶合成酶起作用;它还可被细胞主动摄取,进入细胞后迅速被叶酸基聚谷氨酸盐合成酶代谢为一类多聚谷氨酸化合物,这类多聚谷氨酸化合物是较强的胸腺嘧啶合成酶抑制剂,能够抑制细胞DNA的合成,促进细胞凋亡,同时它能长时间在细胞内潴留,血浆消除半衰期为50-100小时,从而达到长时间发挥细胞毒作用。所以仅仅需要15分钟静脉滴注即可维持21天化疗周期。多篇报道证实雷替曲塞目前在头颈部肿瘤、结直肠癌、胃癌治疗中有效率高,且不良反应轻,疗效优于氟尿嘧啶,不良反应较氟尿嘧啶低。
目前晚期消化道肿瘤化疗中以铂类联合氟尿嘧啶/亚叶酸钙为主的联合化疗方案临床应用较多,但第一代铂类药物严重的肾耳毒性和消化道反应限制了其在部分患者中的应用,第二代铂类药物消化道反应较第一代轻,但骨髓抑制明显,限制了它的临床应用,同时它与第一代铂类药物表现出显著的交叉耐药性,第一、二代铂类药物在大肠癌中的疗效尚未尽如人意[10]。洛铂是第三代铂类药物,主要作用机制为形成DNA的链内和/或链间交联,阻碍其复制和转录,从而干扰肿瘤细胞周期的正常运行,达到抑制肿瘤细胞生长的目的[11-12]。洛铂的抗肿瘤治疗指数等于或高于卡铂和顺铂,无交叉耐药性[11],是一种广谱、高效低毒的抗癌药物。并且其肾毒性和胃肠道反应轻,国内外多项研究表明,洛铂除适应征批准的三类肿瘤外,对非小细胞肺癌、食管癌、胃癌、淋巴瘤、睾丸肿瘤、结直肠癌等都有抗癌活性[13-14]。
刘思海等[1]观察洛铂、奥沙利铂分别联合替加氟持续泵入治疗晚期胃癌,其中64例晚期胃癌患者,分别给予奥沙利铂 135mg/m2、洛铂 35mg/m2、替加氟 800mg/m2、亚叶酸钙 200mg/m2。每4周重复。结果表明洛铂组的有效率为71.9%, 奥沙利铂组的有效率为65.6%;洛铂联合替加氟优于奥沙利铂联合替加氟,但差异无统计学意义。两组的副反应易于接受。林丽珠等[4]曾报道洛铂联合氟尿嘧啶和亚叶酸钙治疗晚期结直肠癌和胃癌。31例患者中,完全缓解1例, 部分缓解6例, 稳定14例,有效率 22.6%,疾病控制率为67.8%;副反应以乏力最明显,发生率48.4%,血小板减少发生率22.6%。李醒亚等[12]报道应用LLF方案治疗晚期食管癌的Ⅱ期临床研究,给药方式为洛铂50mg,第1天;亚叶酸钙 200mg/m2,第l-3天;氟尿嘧啶 400mg/m2,静脉推注,第1天,600mg/m2,持续静脉滴注22h,第l-3天。其中37例评估疗效,完全缓解l例,部分缓解16例,病情稳定15例,疾病进展5例,有效率45.9%,其中初治患者有效率68.2%,复治患者有效率13.3%。以上3篇文献表明洛铂治疗中晚期消化道肿瘤的疗效与奥沙利铂相近甚至更优,且毒副反应轻。据悉,目前欧美正在进行洛铂治疗胃癌的二期临床研究。
4 结论
本回顾性研究表明洛铂联合雷替曲塞治疗的主要不良反应为骨髓抑制,以白细胞下降为主,发生率为36%,其中Ⅲ、Ⅳ度占5%,多在用药后第3~7天出现,使用粒细胞集落刺激因子后能恢复正常,不影响继续治疗;血小板减少的发生率为10%,其中Ⅲ、Ⅳ度占5%,明显低于文献报道的6%~44%[4-5],获得部分缓解或疾病稳定占52%,明显高于普通化疗30~40%左右的有效率。我们认为,洛铂联合雷替曲塞可用于治疗晚期消化道肿瘤,尤其是用于多次化疗后不能耐受、产生多药耐药以及年老体弱者的多线治疗,可作为一个较好的替代选择。它疗效显著,且不良反应较轻,患者依从性好,生活质量高,值得进一步大规模临床研究加以证实。
[1] 刘思海,冯雯,朱瑞霞,等.洛铂和草酸铂分别联合替加氟及卡培他滨治疗晚期大肠癌的比较研究[J].中华肿瘤防治杂志, 2008, 15(23): 1830-1834.
[2]林丽珠,周岱翰,郑心婷,等.洛铂联合氟尿嘧啶和甲酰四氢叶酸治疗晚期耐药胃癌结直肠癌疗效观察[J].中国肿瘤临床, 2007, 34(5): 286-288.
[3]Glimelius B, Hoffman K, Graf W, et al. Quality of life during chemotherapy in patients with symptomatic advanced colorectal cancer. The Nordic Gastrointestinal Tumor Adjuvant Therapy Group[J]. Cancer, 1994, 73(3):556-562.
[4]Caravatta L, Picardi V, Tambaro R, et al. Neoadjuvant accelerated concomitant boost radiotherapy and multidrug chemotherapy in locally advanced rectal cancer: a dose-escalation study[J]. Am J Clin Oncol, 2012, 35(5):424-431.
[5]Mackay HJ, McInnes A, Paul J, et al. A phase Ⅱ study of epirubicin, cisplatin and raltitrexed combination chemotherapy (ECT) in patients with advanced oesophageal and gastric adenocarcinoma[J]. Ann Oncol, 2001, 12(10):1407-1410.
[6]Shen J, Wang H, Wei J, et al. Thymidylate synthase mRNA levels in plasma and tumor as potential predictive biomarkers for raltitrexed sensitivity in gastric cancer[J]. Int J Cancer, 2012, 131(6):938-945.
[7]Surmont VF, van Meerbeeck JP. Raltitrexed in mesothelioma[J]. Expert Rev Anticancer Ther, 2011, 11(10): 1481-490.
[8]Jamieson ER. Lippard SJ. Structure, recognition, and processing of cisplatin-DNA adducts [J]. Chem Rev, 1999, 99 (9): 2467-2498.
[9]王佳蕾,李进,秦叔逵,等,雷替曲塞或尿嘧啶/亚叶酸钙联合奥沙利铂治疗局部晚期或复发转移性结直肠癌的随机对照多中心Ⅲ期临床试验[J]. 临床肿瘤学杂志,2012,1(17):6-11.
[10]SarisCP, Van VP, RietbroekRC, et al. In vitro formation of DNA adducts by cisplatin, lobaplatin and oxaliplatin in calf thymusDNA in solution and in cultured human cells[J]. Carcinogenesis, 1966, 17(12): 2763-2769.
[11]De GramontA, Figer A, Seymour M, et al. Leucovorin and fluorou-racilwith or without oxaliplatin as first line treatment in advanced colorectal caner[J]. J Clin Onco, 2000, 18(16): 2938-2947.
[12]李醒亚,周芳,中海,等.洛铂联合氟尿嘧啶与亚叶酸钙治疗晚期食管癌的Ⅱ期临床研究[J].中华肿瘤防治杂志,2007,14(1):64-66.
[13]杨柳青,秦叔逵.第3代铂类药物洛铂的研究新进展[J].临床肿瘤学杂志,2009,14(12):1134-1139.
[14]Mc Keage, M J.Lobaplatin: a new antitumor platinum drug[J]. Expert Opin Investing Drugs, 2001, 10(1): 119-128.
[15]Nishino M, Jackman D M, Hatabu H, et al. New response evaluation criteria in solid tumors(RECIST) guidelines for advanced small cell lung cancer: comparison with original RECIST and impact on assessment of tumor response to targeted therapy[J]. Am J Roentgenol, 2010, 195(3) : 221-228.
Observation on the Efficacy of the Combination of the Raltitrexed and Lobaplation Treatment with the Late Digestive Tract Tumor
YU Chen, LI Wei-bing
(Department of Integrated Traditional Chinese and Western Medicine,Jiangsu Cancer Hospital, Nanjing 210000, China)
Objective: To observe the efficacy and safety of the combination of the raltitrexed and lobaplation in the treatment of the advanced digestive tract tumor. Methods: 19 patients with IV stage digestive tract tumor (carcinoma, gastric cancer) were treated by using the combination of the raltitrexed and lobaplation. The dose of raltitrexed was 2.6mg/m2in the first day, and the total dose of lobaplation was 30mg/m2, in the same day or in the subsequent use of the same day, and the treatment of 2-6 cycles was performed by 21d. After 2 cycles, the changes of lesion size and tumor index were observed, and the adverse reactions were evaluated. Results: there were 19 cases in the whole group, 10 cases (52%) with partial remission or stable disease, 9 cases (48%) without remission or disease progress. The incidence of gastrointestinal tract reaction, blood cell inhibition, muscle pain and abnormal liver function were 30%, 57%, 10% and 25% respectively. The serum tumor markers CA125, CEA and CA19-9 were decreased in the treatment of effective patients.Conclusions:The treatment of advanced gastrointestinal tumor with the combination of the raltitrexed and lobaplation has a certain significance to the clinical remission rate and survival rate of the advanced digestive tract tumor, and the adverse reactions are light and worth further promotion.
Raltitrexed ; Lobaplation; Digestive Tract Tumor
2015-05-01
江苏省中医药局科技项目(LZ13061)。
俞晨(1980-),女,江苏省泰兴市人,博士,主治医师,主要从事中西医结合抗肿瘤研究。
R969.3
A
1673-8772(2015)04-0028-05
