基于1,8-萘酰亚胺的荧光探针对乙腈中微量水的检测
2015-04-23钱俊红柏红艳刘姗姗陈兆洋
钱俊红, 柏红艳,刘姗姗,陈兆洋
(上海市功能性材料化学重点实验室,华东理工大学化学与分子工程学院,上海 200237)
引言
有机溶剂中水含量的测定在很多领域都具有重要的意义,如常规化学分析、实验室的无水无氧化学反应、工业生产特别是电子工业和精细化学品领域等。通常测定有机溶剂中水含量的方法有卡尔-费休滴定法、色谱法、电化学方法和光谱法。荧光分析法因实时、准确、灵敏、快速、无损等特点,近年来受到人们越来越多的重视。利用光诱导质子转移或电子转移等机理,通过荧光强度的变化可以测定有机溶剂中的水含量[1,2];利用质子化和极性作用,Suzuki等设计了基于氢键作用的吖啶荧光染料聚合物膜[3],Niu等将10-烯丙基-吖啶橙[4]、4’-N,N-二甲基氨基-4-甲基丙烯酰胺查耳酮[5]、N-烯丙基-4-吗啉基-1,8-萘二甲酰亚胺[6]等荧光染料共价键合到玻璃载体表面制成光学传感聚合物膜用于对有机溶剂中水含量的检测,Chang利用部分花青素染料在非质子溶剂的吸收波长随水含量的增加而显著蓝移的特性测定有机溶剂中的微量水[7];利用染料分子在水溶液中的二聚现象,Chang等以荧光素为荧光团设计合成了检测水含量的比率荧光探针[8,9];Li等利用Pb4Br113–阴离子荧光簇的Stokes位移的变化测定非质子溶剂中的微量水[10]。
1,8-萘酰亚胺荧光团因物理化学稳定性好、激发和发射波长、易于修饰等优点被广泛用于合成各种离子和分子探针[11~15]。本文以1,8-萘酰亚胺为荧光团合成了对质子和极性敏感的探针,并研究了有机溶剂中水含量的变化对探针光谱性质的影响,结果表明乙腈中微量水的存在极大改变了探针的光谱性质,此结果为有机溶剂中微量水的检测提供依据。
1 实验部分
1.1 试剂与仪器
根据文献[16,17]的步骤合成化合物1,甲醇和乙腈(分析纯)使用前经干燥处理,二次蒸馏水。Varian Cary 500 紫外可见分光光度计,Varian Cary Eclipse荧光分析仪,所有实验均在室温下进行。
1.2 光谱测试
配制1.0×10-3mol/L的探针母液,取200 μL上述母液加入到20 mL不同水含量的水-乙腈或水-甲醇溶剂中,检测溶液的吸收和发射光谱。
1.3 荧光量子测定
以硫酸奎宁(ΦF= 0.51)为基准,按公式1计算。

式中Φ(sample)、Φ(standard)分别表示待测样品和标准物的荧光量子产率,A(sample)、A(standard)分别表示待测样品和标准物在激发波长下的吸光度,S(sample)、S(standard)分别表示待测样品和标准物的荧光发射峰面积。
2 结果与讨论
化合物1是基于ICT机理设计的,其中4-位取代氨基是电子供体、1,8-位的羰基和亚胺基是电子受体;其荧光团上的亚胺基易发生质子化从而改变化合物的ICT作用,导致化合物光谱性质的变化;4-位疏水性十二烷基链的引入使得化合物溶解度随水含量的变化而变化,在高含量水介质中探针分子易于发生聚集,从而影响化合物1的光谱性质。
2.1 化合物1在不同溶剂中的光谱特性
图1是化合物1在不同溶剂中的吸收和发射光谱图,由图可知,随着溶剂极性的增加,化合物的吸收和发射光谱均发生红移。化合物1在甲醇、乙腈和二氯乙烷中的吸收峰均是单峰,而在水溶液中其最大吸收波长为467 nm,并在490 nm处有一明显肩峰,可能由于化合物在水溶液中发生了聚集。表1列出了化合物1在不同溶剂中的吸收和发射光谱数据。由表可知,随着溶剂极性的增大,化合物的摩尔吸光系数和荧光量子产率均降低。上述结果表明,含疏水取代基的化合物的光谱性质对溶剂极性非常敏感,可用于检测微环境的极性。

图1化合物1在不同溶剂中的吸收和发射光谱Fig.1The absorption and emission spectra of 1 in different solvents.

表1化合物1在不同溶剂中的光谱性质Table.1Spectral properties of 1 in different solvents
2.2 pH对化合物1光谱特性的影响
图2是酸含量对化合物光谱性质的影响,由图可知,随着对甲基苯磺酸浓度的增加,化合物的紫外吸收光谱由435 nm红移至451 nm,而其荧光发射波长略有蓝移;化合物的吸光度值和荧光强度均随着酸浓度的增加而增大。表明,酸含量的增加使得化合物基态的质子化程度增大,电子推拉作用增强,吸收光谱红移。

图2在乙腈中,对甲基苯磺酸对化合物1吸收和发射光谱得影响Fig.2p-Toluenesulfonic acid effect on the absorption and emission spectra of 1 in MeCN.
2.3 化合物1在MeCN-H2O 体系的光谱变化
图3是化合物1在不同水含量MeCN-H2O体系的吸收光谱。由图3a可知,当水含量从0提高至60%时,溶液的最大吸收波长由435 nm红移至471 nm,其最大吸收波长处的吸光度值增大至原来的两倍;进一步增加水含量,吸光度值急剧降低,吸收峰变宽。当水含量由90%增大到99%时,最大吸收波长略有蓝移,在长波长处有一肩峰,表明随着水含量的增加,化合物1可能发生了聚集。由图3c可知,当水含量从0增加值40%时,化合物的最大吸收波长几乎线性增大;此后,化合物的最大吸收波长几乎不变。
图4显示了化合物1的发射光谱随水含量的变化。由图可知,乙腈中少量水的存在使得化合物的发射波长急剧红移(当水含量从0增至0.1%时,化合物的最大发射波长从504 nm增大至538 nm),其后继续增加水含量至5.0%(547 nm),其发射波长略有增大;当水含量由5%增大至16.7%时,最大发射波长蓝移至512 nm;当水含量由16.7%增至99.0%时,最大发射波长略有红移(由512 nm红移至525 nm)。图4d是化合物的荧光量子产率随水含量的变化曲线,由图可知,随着水含量的增加,化合物的荧光量子产率先近乎线性降低(0~0.1%,图4d插入图),然后稳步增大(5%~50%);荧光量子产率在水含量50~80%时达最大值且几乎保持恒定,此后又急剧降低。由上述结果可知,在水含量小于0.1%时,随着水含量的增加,化合物1的最大吸收波长几乎不变(小于440 nm),发射波长显著红移、荧光量子产率几乎线性降低;因此,化合物1可用于对乙腈中微量水含量(<0.1%)的定量。
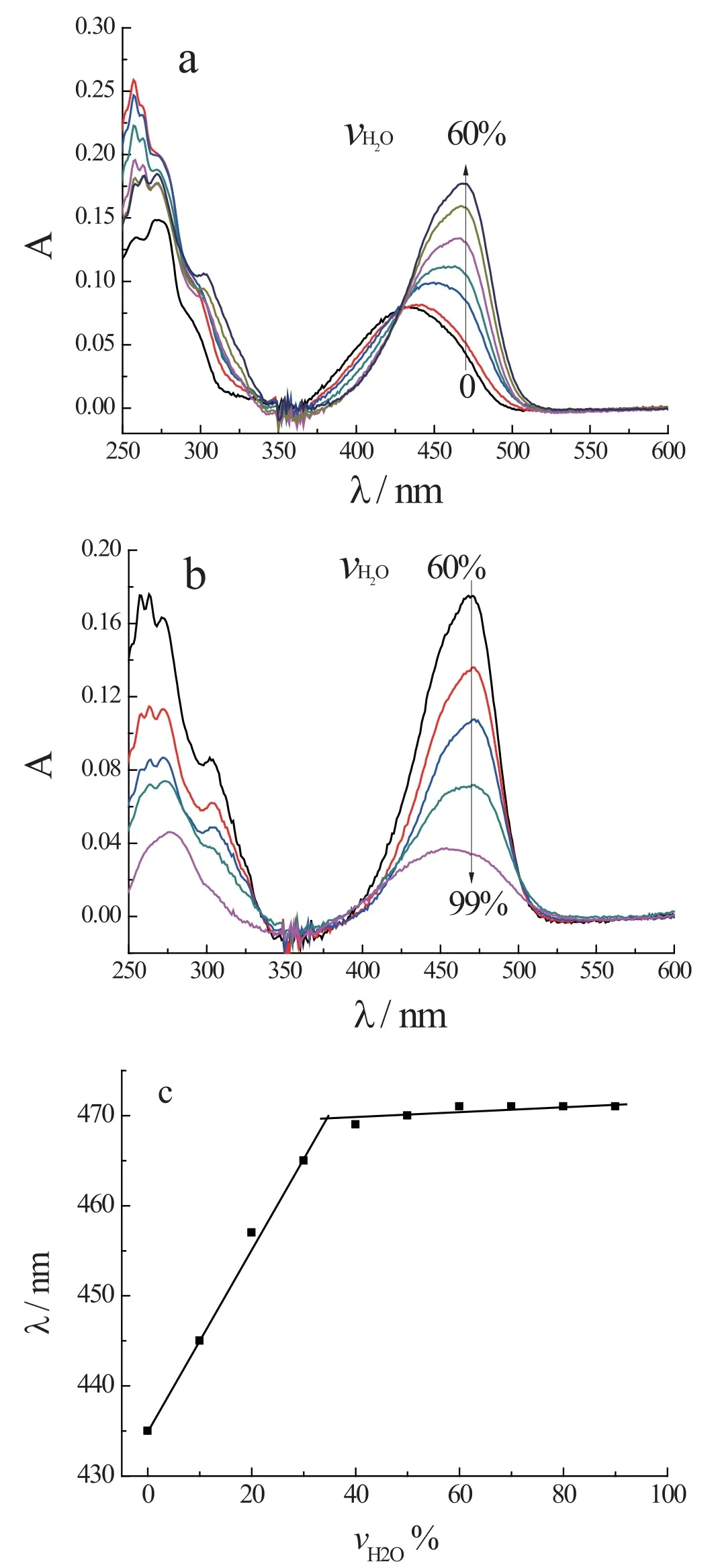
图3乙腈中水含量的变化对化合物1吸收光谱(a,b)及吸收波长(c)的影响Fig.3Water effect on the absorption spectra (a, b) and the absorption maximun (c) of 1 in MeCN-H2O system.

图4乙腈中水含量的变化对化合物1发射光谱(a-c)及荧光量子产率(d)的影响Fig.4Water effect on the emission (a-c) and the fl uorescence quantum yield (d) of 1 in MeCN-H2O system ,λex = 460 nm, λem = 525 nm.
2.4 化合物1在MeOH-H2O体系的光谱变化

图5甲醇中水含量的变化对化合物1吸收光谱(a,b)及吸收波长(c)的影响Fig.5Water effect on the absorption spectra (a, b) and the absorption maximun (c) of 1 in MeOH-H2O system.
图5和6 是化合物1在不同水含量MeOH-H2O体系的吸收和发射光谱。与在MeCN-H2O体系类似,当水含量由0增加到50%时,溶液的最大吸收波长由445 nm红移至471 nm,化合物的吸光度值增至最大值;其荧光发射波长从511 nm红移至525 nm,荧光量子产率在水含量50%时达最大值;此后随着水含量的增加,吸收和发射波长均无明显变化,但吸光度和荧光量子产率均降低。
化合物1分子具有较大的共轭体系,在吸收一定能量的紫外光后发生π→π*跃迁,其激发态的极性比基态强,随着溶剂极性的增大,基态与激发态之间的能级差减小,吸收和发射波长红移[18]。
在乙腈-水体系中,当水含量较低时(0-5%),由于大量乙腈的存在阻隔了水分子与探针分子以及水分子之间氢键的形成,少量水的存在使得溶剂的极性急剧增大,化合物的吸收和发射光谱红移、荧光量子产率降低;当水含量介于5~17%时,水含量的增加使得探针分子中亚胺基上的N原子发生质子化,导致荧光发射波长蓝移、荧光量子产率增大;随着水含量的进一步增大,溶液的极性增大、化合物的荧光发射波长略有红移。当水含量高于60%时,此时溶液以水相为主,由于长链烷基的疏水性作用,化合物的溶解性急剧下降并可能发生聚集,导致吸收峰变宽并在长波长处出现肩峰、荧光量子产率急剧下降。
甲醇和水同为质子溶剂且水的酸性强于甲醇。在甲醇-水体系中,随着水含量的增加,一方面使得探针分子更容易质子化,导致荧光发射波长蓝移、荧光量子产率增大;另一方面,水含量的增加使得溶剂的极性增大,化合物的光谱红移、荧光量子产率降低;同时在较高水含量的甲醇-水体系,化合物的溶解度降低、易于发生聚集,亦使得荧光量子产率急剧下降。在水含量较低时(小于50%),水含量的增加主要使得探针的质子化程度提高,荧光量子产率增加;在水含量较高时,水的加入对溶剂极性以及化合物溶解度的影响占主导作用,因此荧光量子产率降低。
3 结论
水是强极性、质子化溶剂,有机溶剂中微量水的存在导致溶剂的极性和质子化能力变大。化合物1的分子上同时含有质子受体和极性敏感基团,有机溶剂中微量水的存在使得化合物的光谱性质急剧变化。在乙腈溶剂中,微量水(<0.1%)的存在使得1的荧光发射波长显著红移、荧光量子产率线性降低,而其最大吸收波长几乎不变(小于440 nm),因此,利用化合物1的光谱变化可测定乙腈中的微量水。
[1] Kim J S, Choi M G, Huh Y,et al.Determination of water content in aprotic organic solvents using 8-hydroxyquinoline based fl uorescent probe. Bulletin of the Korean Chemical Society, 2006, 27(12): 2058-2060.
[2] Ooyama Y, Sumomogi M, Nagano T,et al.Detection of water in organic solvents by photo-induced electron transfer method. Organic& Biomolecular Chmistry, 2011, 9(5): 1314-1316.
[3] Citterio D, Minamihashi K, Kuniyoshi Y,et al.Optical determination of low-level water concentrations in organic solvents using fluorescent acridinyl dyes and dye-immobilized polymer membranes. Analytical Chemistry, 2001, 73(21): 5339-5345.
[4] Yang X, Niu C G, Shang Z J,et al.Optical-fiber sensor for determining water content in organic solvents. Sensors and Actuators B: Chemical, 2001, 75(1-2): 43-47.
[5] Niu C G, Guan A L, Zeng G M,et al.Fluorescence water sensor based on covalent immobilization of chalcone derivative [J].Analytica Chimica Acta, 2006, 577(2): 264-270.
[6] Niu C G, Qin P Z, Zeng G M,et al.Fluorescence sensor for water in organic solvents prepared from covalent immobilization of 4-morpholinyl-1, 8-naphthalimide. Analytical and Bioanalytical Chemistry, 2007, 387(3): 1067-1074.
[7] Cha S, Choi M G, Jeon H R,et al.Negative solvatochromism of merocyanine dyes: Application as water content probes for organic solvents. Sensors and Actuators B: Chemical, 2011, 157(1): 14-18.
[8] Choi M G, Kim M H, Kim H J,et al.A simple ratiometric probe system for the determination of water content in organic solvents.Bulletin of the Korean Chemical Society, 2007, 28 (10): 1818-1820.
[9] Choi M G, Joo H H, Kim Y H,et al.Ratiometric determination of water content in acetonitrile by a fl uorescein derivative bearing two pyrene subunits. Bulletin of the Korean Chemical Society, 2010,31(10): 2995-2998.
[10] Li S H, Chen F R, Zhou Y F,et al.Pb4Br113- cluster as a fluorescent indicator for micro water content in aprotic organic solvents. Analyst, 2009, 134(3): 443-446.
[11] Yu C W, Chen L X, Zhang J,et al.“Off-On” based fl uorescent chemosensor for Cu2+in aqueous media and living cells. Talanta,2011, 85(3): 1627-1633.
[12] Xie J, Chen Y H, Yang W,et al.Water soluble 1,8-naphthalimide fl uorescent pH probes and their application to bioimagings. Journal of photochemistry and photobiology A-Chemistry, 2011, 223(2-3):111-118.
[13] Wang P, Liu J, Lv X,et al.A naphthalimide-based glyoxal hydrazone for selective fluorescence turn-on sensing of Cys and Hcy. Organic Letters, 2012, 14(2): 520-523.
[14] Wang J F, Jin S, Akay S,et al.Design and synthesis of longwavelength fl uorescent boronic acid reporter compounds. European Journal of Organic Chemistry, 2007, 2007(13): 2091-2099.
[15] Li Z W, Yang Q W, Chang R X,et al.N-Heteroaryl-1,8-naphthalimide fluorescent sensor for water Molecular design,synthesis and properties. Dyes and Pigments, 2011, 88(3): 307-314.
[16] Qian J H, Qian X H, Xu Y F. Selective and sensitive chromo- and fl uorogenic dual detection of anionic surfactants in water based on a pair of “on-off-on” fl uorescent sensors. Chemistry - A European Journal, 2009, 15(1): 319-323.
[17] Qian J H, Qian X H, Xu Y F,et al.Multiple molecular logic functions and molecular calculations facilitated by surfactant’s versatility. Chemical Communications, 2008, 35: 4141-4143.
[18] 邢其毅, 裴伟伟, 徐瑞秋, 等. 基础有机化学(第三版,上册). 北京:高等教育出版社, 2005: 156-168.
