吹扫捕集—气质联用测定天然水体中异戊二烯的研究
2015-04-20张洪海等
张洪海等

摘 要 建立了吹扫捕集气质联用分析天然水体中痕量异戊二烯的方法,确定了最佳实验条件:吹扫流量50 mL/min、吹扫时间15 min、毛细管分离柱类型(RtAlumina BOND/KCl)以及程序升温等。本方法对于测定水体中异戊二烯浓度的相对标准偏差RSD<4%(n=6),回收率为92%~102%,检出限为0.5 pmol/L。实验表明,水样中异戊二烯浓度在60 d以内没有发生明显变化。利用本方法测得青岛胶州湾及附近河流入海口水样中异戊二烯的浓度在60.8~278.7 pmol/L之间,黄河口水样浓度范围为44.7~77.2 pmol/L,与文献报道的其它近岸及河口水体中的浓度相当,表明本方法能够应用于天然水体中异戊二烯浓度的准确分析。
关键词 异戊二烯; 吹扫捕集; 气质联用; 天然水体
1 引 言
生物源和人为源释放的非甲烷烃类物质(Nonmethane hydrocarbons,NMHCs)是大气中的重要组成成分,对于对流层中的O3的浓度和二次有机气溶胶(Second organic aerosol)的形成及气候变化具有重要影响[1~4]。异戊二烯(Isoprene)作为NMHCs中含量最丰富、最重要的一种物质,它不仅参与多种大气化学反应,影响大气氧化平衡,而且对全球碳循环有着巨大贡献[5,6]。众所周知,大气中的异戊二烯主要来源于陆生植物的光合成释放[7],但异戊二烯也普遍存在于天然水体中,主要由浮游植物的光合作用和有机物的光降解产生[8,9]。经估算仅由海洋释放到大气的异戊二烯的年平均释放量可达1 Tg[10,11],可见海洋作为大气异戊二烯的源对全球碳循环及气候变化的影响也是不容忽视的。因此,开展天然水体中异戊二烯的研究对于认识其海气交换通量及环境效应具有重要意义。
由于水体中异戊二烯的浓度很低,一般在10 12~10 11 mol/L之间,最高至10 10 mol/L数量级[12],而且其浓度明显受到光照强度、界面交换和微生物活动等因素的影响,对其分析技术及准确性要求较高。目前,国外测定痕量NMHCs气体的主要方法是使用气相色谱(GC)进行分离,后由氢火焰离子检测器(FID)、电子捕获检测器(ECD)或质谱检测器(MSD)进行检测[6,13]。而国内关于水体中异戊二烯的研究方法尚未见文献报道。因此,本研究利用吹扫捕集前处理技术,建立了气相色谱质谱联用分析天然水体中异戊二烯浓度的方法。与现有方法相比,本方法样品分析体积大大减少,提高了实验分析的效率; 此外,吹扫捕集前处理技术中引入反吹系统,极大地消除了样品的残留干扰,保证了分析结果的准确性。本方法操作简单,精密度好,检出限低,并成功用于胶州湾及附近河流入海口和黄河口水体样品中异戊二烯的含量测定。
2 实验方法
2.1 仪器与试剂
GC7890型气相色谱仪(美国Agilent公司); MSD5975型质谱检测仪(美国Agilent公司),配EI源和四级杆质量分析器; 手动六通阀(美国VICI公司); RtAlumina BOND/KCl毛细管柱(30 m × 0.32 mm × 5 μm,美国RESTEK公司); 气提室: 玻璃圆柱体,底端加有砂芯(4#)滤板; 硬质玻璃管(10 cm×1.5 cm, o.d.)作干燥管,经硅烷化处理,内填无水Mg(ClO4)2; 玻璃管(10 cm×1.5 cm, o.d.)CO2作去除管,经硅烷化处理,内填进口NaOH颗粒; 捕集管: 长1.5 m的1/16进口钝化不锈钢管; 进样注射器: 50 mL(澳大利亚SGE公司)。
异戊二烯标准品(色谱纯,99.9%,美国SigmaAldrich公司); 甲醇(色谱纯,99.8%,德国Merck公司); 液氮(青岛天源配气有限公司); 高纯N2和高纯He(青岛合利气体有限公司)。
2.2 实验装置
对于水体中易挥发的痕量气体而言,无法使用GC直接进样测定,因此提取富集成为准确测定的关键。本研究采用目前国际上通用的痕量气体提取方法—吹扫捕集技术对水体中的异戊二烯进行低温预富集,经热解析后接GC分离,再进入MSD进行检测,实验装置如图1所示。主要分析流程如下: 六通阀在捕集状态下,将适量水样(50~100 mL)用气密性良好的注射器注入气体室,高纯N2鼓泡将水样中的异戊二烯吹出,经过装有无水Mg(ClO4)2的干燥管和装有固体NaOH的玻璃管进行干燥和CO2去除,后进入浸泡在液氮(
178 ℃)的不锈钢捕集管进行富集。富集一定时间后,关闭吹扫N2,将不锈钢捕集管迅速放入沸水(100 ℃)中加热解析,同时将六通阀切换到进样状态,用高纯He将解析出来的气体组分送入GC分离后,最后MSD检测分析。
2.3 GCMSD分析条件
配制一定浓度的异戊二烯溶液,优化测定水体中异戊二烯的GCMSD分析条件如下: 进样口温度: 150 ℃; 程序升温: 设定起始温度为60 ℃, 保持3 min; 以10 ℃/min升温至120 ℃,保持1 min; 再以30 ℃/min升温至160 ℃,保持3 min。 载气(He)流速: 流量为1.5 mL/min,分流比10∶1; 检测器温度: 四级杆温度150 ℃,离子源温度230 ℃,EI工作电压70 eV。
3 结果与讨论
3.1 色谱柱的选择
毛细管色谱分离柱的柱性、长度和管径等参数都是GCMSD分离的重要影响因素,因此,选择适宜的毛细管色谱柱也是本实验的关键。
分别选用DB1(30 m × 0.32 mm × 0.25 μm)、DB624(60 m ×0.25mm × 1.4 μm)、RTX624(60 m × 0.32 mm × 1.8 μm)和RtAlumina BOND/KCl(30 m×0.32 mm×5 μm)4根不同的毛细管分离柱进行柱分离对比实验。实验表明,与其它色谱柱相比,RtAlumina BOND/KCl(30 m × 0.32 mm × 5 μm)毛细管柱不仅可以实现异戊二烯和其它吹扫出的气体组分(其它NMHCs、挥发性卤代烃VHCs等)的有效分离,而且出峰时间较短,无临近峰干扰,峰形好。因此,本研究选用RtAlumina BOND/KCl毛细管柱作为水体中异戊二烯分析的色谱分离柱。
3.2 吹扫捕集条件
吹扫流量的选择不仅影响捕集效率,同时也会影响分析时间。较低流速首先会影响单位时间内的吹扫效率,导致分析时间的延长; 但高流速又会影响样品组分的捕集效率,甚至将大量水分吹出,除影响干燥效果外,还会影响MSD的基线漂移程度。因此,吹扫流量对于该实验的前处理条件的优化至关重要。在一定的吹扫时间内,分别将364 pmol/L水溶液与吹扫速率进行实验,为确保实验的准确性进行了平行实验(n=5),获得了不同吹扫速率与峰面积的对应曲线(图2)。从图2可见,流速小于45 mL/min时,峰面积随吹扫流速的增大而迅速增加,而且增加趋势随流量增大逐渐减缓; 当流速大于50 mL/min时,峰面积几乎不再随流速的增加而发生改变,这说明在此情况下水体中异戊二烯几乎完全被吹出。综合考虑各因素,既保证吹扫效率,又不影响干燥剂的除水效果和MSD灵敏度的情况下,选择50 mL/min为水体中异戊二烯的最佳吹扫流量。
在一定的吹扫流速和吹扫时间内,如果能将水体中较高浓度的异戊二烯吹出,那么较低浓度的样品也就得以保证。因此,实验中配制已知浓度的异戊二烯水样进行吹扫时间的实验。在选定的最佳吹扫流量为50 mL/min条件下,对同一浓度溶液分别吹扫6, 8, 10, 12, 15, 18和20 min,并进行平行实验(n=5),得到峰面积与吹扫时间的对应关系曲线(图3)。从图3可见,6~12 min内,峰面积随着吹扫时间的延长而明显增加; 12 min后,峰面积趋于稳定,可以认为水体中的异戊二烯已经完全被吹出。为了保证水体中的异戊二烯吹出效率和实验操作的准确性,本研究选择15 min作为异戊二烯的最佳吹扫时间。
3.3 标准曲线及线性范围
由于水体中异戊二烯的浓度一般在10 12~10 10 mol/L,配制的标准溶液浓度应包含此范围。实验中,以甲醇为溶剂,准确配制异戊二烯一级母液,用微量注射器依次抽取0.5, 1, 2, 3, 5, 7, 10, 13和16 μL的一级母液并分别注入已吹扫过的50 mL空白海水的注射器中,并直接注入吹扫室进行气提分析。在测定的实验浓度下(3.80~304 pmol/L),峰面积与浓度呈线性关系,工作曲线为y=455.9x+12715(R2=0.999, n=9, p<0.0001)。目前,已报道的或测定的异戊二烯的浓度均在该浓度范围以内,完全可以满足水体中异戊二烯浓度测定的要求。
3.4 精密度、检出限与回收率
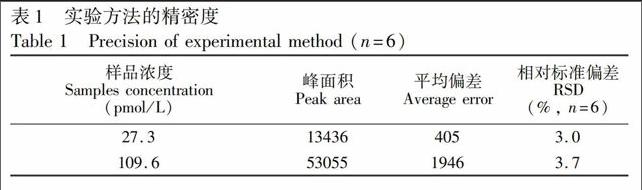
分别配制27.3和109.6 pmol/L标准溶液,在优化实验条件下平行测定6次,以测定方法的精密度,结果见表1。两种不同浓度水样测定结果的精密度分别为3.0%和3.7%,表明本方法精密度良好。
对于异戊二烯的回收实验,通过前处理吹扫捕集进样与GC柱头直接进样的测量结果比对计算方法的回收率。对于已知准确浓度的异戊二烯样品,用柱头和前处理进样两种方式获得的峰面积分别为18647和17747(n=8), 平均回收率为95%。经过计算可知,本方法对异戊二烯回收率在92%~102%之间。采用本方法得水体中异戊二烯的检出限为0.5 pmol/L(检测器产生的响应信号为噪声值3倍时的量为检出限)。
3.5 保存实验
由于GCMSD使用条件和环境的限制,目前还无法达到船载要求,因此水体中异戊二烯的浓度还不能满足海上现场分析,如何保存水样,对于异戊二烯含量的准确测定至关重要。影响水体中异戊二烯含量变化的主要因素是微生物活动和光照[1],因此,避光和限制微生物活动也就成为水样保存成功与否的关键。本实验选用100 mL棕色窄口玻璃瓶进行采样,排空气泡后加入2滴饱和HgCl2溶液,带聚四氟乙烯衬垫的铝盖压盖密封,在4 ℃避光保存。除微生物活动和光照影响外,保存时间对于异戊二烯的准确分析也应予以考虑。在上述保存条件下,取青岛石老人海水浴场海水样品进行实验,分别于0, 1, 2, 3, 5, 7, 10, 15, 20, 30, 40, 50和60 d对采集的平行样品进行分析,结果表明,样品中异戊二烯的含量几乎没有明显变化。因此,在保证实验测定结果准确性的前提下,样品可以加饱和HgCl2、4 ℃避光保存两个月以上。
3.6 天然水体中异戊二烯浓度的测定
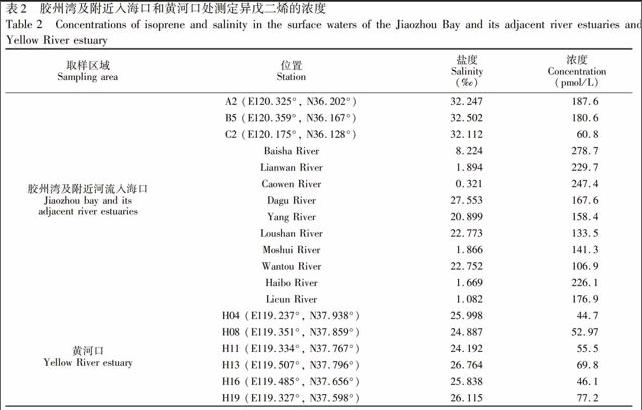
分别对2013年5月份采集的胶州湾以及附近河流入海口处的表层水样(见图4)和2013年10月采集黄河口海域的表层水样,利用本方法对其中的异戊二烯进行了测定,结果见表2。胶州湾及附近河流入海口处水体中异戊二烯的浓度在60.8~278.7 pmol/L之间,平均浓度为176.6 pmol/L,黄河口水体中异戊二烯的浓度范围在44.7~ 77.2 pmol/L,平均浓度为57.7 pmol/L。此结果与文献报道的其它近海海域及河口区中异戊二烯的浓度调查结果相接近[12,14],却明显高于北太平洋海水中平均值为30 pmol/L [10]。这可能是因为水体中异戊二烯主要来自于浮游植物的释放和有机物的光降解[9],而胶州湾海域及附近河流入海口和黄河口海域受人为活动的影响严重,浮游植物生物量明显高于大洋海区; 另外,由调查数据可知,胶州湾附近河流中异戊二烯的浓度(盐度 S<10)明显高于胶州湾及黄河口水样中的浓度,表明陆地植物对于河流水体中异戊二烯的贡献较大,通过河流输入进入近海,可能也是导致调查海域异戊二烯浓度偏高的重要原因。此分析结果也表明,近岸、河口海域虽然只占全球海域的很小一部分,但由于其异戊二烯浓度较高,对全球海洋异戊二烯的贡献较大,进而对全球或区域环境气候变化产生重要影响。
4 结 语
建立了吹扫捕集法结合气质联用技术测定水体中异戊二烯的方法,用于胶州湾及附近河流入海口和黄河口表层水样中异戊二烯的测定。本方法操作简单,进样体积小,灵敏度及准确性高,适用于天然水体中异戊二烯浓度的分析测定。
References
1 Kurihara M, Iseda M, Loriya T, Horimoto N, Kanda J, Ishimaru T, Yamaguchi Y, Hashimoto S. Mar. Chem., 2012, 134135: 71-79
2 Daniel D R, Peter J M, Rod G Z, Willer H P. Mar. Chem., 2000, 71: 177-198
3 Satio T, Yokouchi Y, Kawamura K. Atmos. Environ., 2000, 34: 4373-4381
4 Shaw S L, Chisholm S W, Prinn R G. Mar. Chem., 2003, 80: 227-245
5 Sahu L K, Lal S, Venkataramani S. Atmos. Environ., 2011, 45: 2356-2366
6 Pacifico F, Harrison S P, Jones C D, Sitch S. Atmos. Environ., 2009, 43: 6121-6135
7 Fortunati A, Barta C, Brilli F, Centritto M, Zimmer I, Schnitzler J P, Loreto F. Plant J., 2008, 55: 687-697
8 Pszenny A A P, Prinn R G, Kleiman G L, Shi X. J. Geophys. Res., 1999, 104(17): 21785-21801
9 Bonsang B, Polle C, Lambert G. Geophys. Res. Lett., 1992, 19(11): 1129-1132
10 Matsunaga S, Mochida M, Satio T, Kawamura K. Atmos. Environ., 2002, 36: 6051-6057
11 Milne P J, Riemer D D, Zika R G, Brand L E. Mar. Chem., 1995, 48: 237-244
12 ZHAO Jing, ZHANG GuiLing. J. Zhejiang Ocean Univ. (Natural Sci. Edition), 2009, 2: 453-460
赵 静, 张桂玲. 浙江海洋学院学报(自然科学版), 2009, 2: 453-460
13 Kansal A. J. Hazard. Mater., 2009, 166: 17-26
14 Sharma U K, Kajii Y, Akimoto H. Atmos. Environ., 2000, 34: 4447-4458
Abstract Gas chromatography with mass spectrum detector (GCMSD) coupled with purgeandtrap system was set up to analyze the concentration of isoprene in natural waters. The best experimental conditions were established, including purge gas flow rate (50 mL/min), purge time (15 min), the optimum capillary column (RtAlumina BOND/KCl) and the appropriate condition of temperature programming. When analyzing isoprene in natural waters, the precision was <4% (n=6), the detection limit was 0.5 pmol/L and the recovery was 91%-102%. The preservative experiment showed that there was no obvious variation in sample concentrations of isoprene within 60 days. The concentrations of isoprene measured with the method ranged from 60.8 to 278.7 pmol/L in the Jiaozhou Bay and its adjacent river estuaries and from 44.7 to 77.2 pmol/L in Yellow River estuary, which was in good accord with those results reported in literatures in other coastal waters. In conclusion, the analytical method could meet the requirements of the analysis of concentration of isoprene in natural waters.
Keywords Isoprene; Purge and trap system; Gas chromatographymass spectrometry; Natural water
(Received 3 November 2014; accepted 24 December 2014)
This work was supported by the National Natural Science Foundation of China (Nos. 41306069 and 41030858), the Changjiang Scholars Program, Ministry of Education of China, and the Taishan Scholars Program of Shandong Province, China
