Fe3O4/AuNPs磁性复合粒子的制备与表征
2015-04-19黄丹丹初园园
代 昭,杨 坤,黄丹丹,初园园
(天津工业大学环境与化学工程学院,天津 300387)
Fe3O4/AuNPs磁性复合粒子的制备与表征
代 昭,杨 坤,黄丹丹,初园园
(天津工业大学环境与化学工程学院,天津 300387)
通过溶剂热法合成了较大粒径的磁性Fe3O4纳米粒子,使用3-氨丙基三乙氧基硅烷(APTES)在乙醇/异丙醇体系中将其表面功能化一层氨基,随后将金纳米粒子(AuNPs)自组装于Fe3O4粒子表面,得到了Fe3O4/ AuNPs纳米粒子;采用透射电子显微镜(TEM)、X-射线衍射(XRD)、振动样品磁强计(VSM)和紫外-可见光吸收光谱仪(UV-Vis)对复合粒子的形态、结构及性质进行表征.结果表明:所制备的Fe3O4磁纳米粒子粒径均一,平均粒径约为250 nm,形状几乎都呈球形,磁性Fe3O4/AuNPs复合粒子包覆均匀、具有良好的的分散性和磁化率,同时兼有磁性和金纳米粒子的特性.
Fe3O4;金纳米粒子(AuNPs);磁性纳米粒子;复合粒子
在众多的纳米材料中,金纳米粒子(AuNPs)因其具有独特的物理、化学和生物学性质,被广泛应用于传感器、催化、生物医药、环境监测等领域[1-2].这些应用大都要求AuNPs在多种溶液中具有良好的分散性以及较易进行转运、组装等操作.由于AuNPs的小尺寸(颗粒大小多在1~100 nm)和高比表面能使其很容易团聚与流失,导致AuNPs的应用受到很大的限制.为了解决这一问题,同时为进一步实现材料的可控操作和重复利用,研究者们将AuNPs固定在磁性粒子表面合成了诸如Fe3O4@Au、γ-Fe2O3@Au和Fe3O4/Au等多种磁性金纳米复合结构[3-7].然而研究者们大多选用小粒径的磁核(5~100 nm),合成的复合结构普遍具有磁响应性与分散性较低的缺点.2010年,Wang等[8]用 L-半胱氨酸作连接剂,将AuCl4-吸附于不同粒径Fe3O4磁核(300~500 nm)表面,然后加入抗坏血酸将其还原生成AuNPs,从而制备了Fe3O4/Au复合纳米球,但是所合成的复合纳米球在水中的分散性较差同时磁核的团聚现象也较严重.2013年,Deng等[9]通过在粒径为320 nm左右的Fe3O4磁核上引入中间硅层,然后利用双氨基硅烷偶联剂γ-(乙二胺基)丙基三甲氧基硅烷将硅层修饰上氨基后连接AuNPs,制备得到包覆均匀且具有较好分散性的Fe3O4/Au复合微球.然而硅层的引入使得复合粒子的磁性降低.本文采用溶剂热法制备出大粒径的Fe3O4磁球,在乙醇/异丙醇体系中,由3-氨丙基三乙氧基硅烷(APTES)将其表面修饰一层氨基,并通过静电吸附作用与AuNPs进行连接,从而获得了一种简单有效的制备Fe3O4/Au纳米粒子的方法.
1 实验部分
1.1 实验试剂与仪器
实验试剂包括:三氯化铁(FeCl3·6H2O)、柠檬酸钠、无水乙醇,分析纯,天津市风船化学试剂科技有限公司产品;无水乙酸钠,分析纯,天津市科密欧化学试剂有限公司产品;乙二醇,分析纯,天津市光复精细化工研究所产品;异丙醇、氨水(25%),分析纯,天津市北方天医化学试剂厂产品;3-氨丙基三乙氧基硅烷(APTES),分析纯,美国Alfa-Aesar公司产品;氯金酸(HAuCl4·4H2O),分析纯,云南贵研铂业股份有限公司产品;实验中所用水均为二次水.
实验仪器包括:H-7650型透射电子显微镜,日本日立公司产品;XRD-7000S/L型X-射线衍射仪,日本岛津制作所产品;PPMS-9型振动样品磁强计,美国Quantum Design公司产品;Helios-γ型紫外-可见光吸收光谱仪,美国热电公司产品.
1.2 实验过程
1.2.1 Fe3O4磁纳米粒子的合成
取2.2 g FeCl3·6H2O和3.6 g无水乙酸钠溶于60 mL乙二醇中,超声使其完全溶解,随后加入0.5 g柠檬酸钠,混合液剧烈搅拌(转速约600 r/min)1 h后装入100 mL的聚四氟乙烯内衬的不锈钢反应釜中,并转移至220℃的烘箱中反应12 h,反应完成后取出反应釜冷却至室温,产物用无水乙醇洗涤数次后放入60℃真空干燥箱中干燥至恒重.
1.2.2 Fe3O4磁纳米粒子的表面改性
取40 mg Fe3O4分散于40 mL无水乙醇-异丙醇体系中(体积比为 3∶1),随后加入 2 mL氨水,0.3 mLAPTES,混合液超声10 min后置于60℃水浴锅中,同时机械搅拌(转速约300 r/min)2 h后,所得产物磁分离,用无水乙醇和水各洗涤数次后分散于100 mL水中备用.
1.2.3 AuNPs的制备
首先需分别配制质量分数为1%的氯金酸溶液和质量分数为1%的柠檬酸钠溶液,其配制方法均为取1.0 g溶质充分溶解于99 mL水中,然后置于125 mL棕色瓶中4℃温度下保存备用.
根据经典的Fren′s法[10]合成AuNPs:取200 mL水倒入500 mL烧杯中,随后加入2 mL的HAuCl4·4H2O溶液,放置于磁力恒温搅拌器上,加热,当液体达到亚沸状态(温度大约达到98℃)时,向溶液中迅速加入4 mL柠檬酸钠溶液,继续煮沸,待溶液出现稳定的鲜红色时,降温至50℃左右,保持30 min后取出冷却至室温,10 000 r/min离心,倒掉上清液将下层液体转入棕色瓶中备用.
1.2.4 Fe3O4/Au纳米粒子的合成
将1.2.2步骤中100 mL的改性磁纳米粒子分散液与1.2.3步骤中制备的AuNPs分散液混合,置于250 mL的三口烧瓶中,超声同时缓慢机械搅拌2 h.产物磁分离,用水洗涤数次后放入60℃真空干燥箱中干燥至恒重.
1.3 表征
将干燥后的Fe3O4磁球和Fe3O4/AuNPs复合粒子超声分散于无水乙醇中,用碳支持膜的铜网在悬浮液中捞10~20次,真空干燥后用透射电子显微镜(TEM)观察其粒径和结构并拍摄照片;用干燥后Fe3O4磁球和Fe3O4/AuNPs复合粒子的粉末测X-射线衍射图像和磁饱和强度;通过紫外-可见光吸收光谱仪(UVVis)对Fe3O4/AuNPs复合粒子的光学特性进行检测.
2 结果与讨论
2.1 Fe3O4磁纳米粒子的合成
本文采用改进的溶剂热法合成Fe3O4磁纳米粒子[11],以乙二醇为还原性溶剂,在220℃的高温下将FeCl3还原生成Fe3O4,反应体系中无水乙酸钠作为一种弱碱性钠盐可提高体系的碱度从而促进FeCl3的水解,柠檬酸钠分子中存在的3个羧基与Fe(Ⅲ)离子具有很强的配位亲和力,在形成磁核时其表面配合的柠檬酸根离子可阻止形成较大的单晶磁球,而且生成的Fe3O4磁纳米粒子表面因为结合了大量的柠檬酸根离子而具有良好的分散性.所制备的Fe3O4磁球的透射电子显微镜照片及粒径分布图如图1所示.
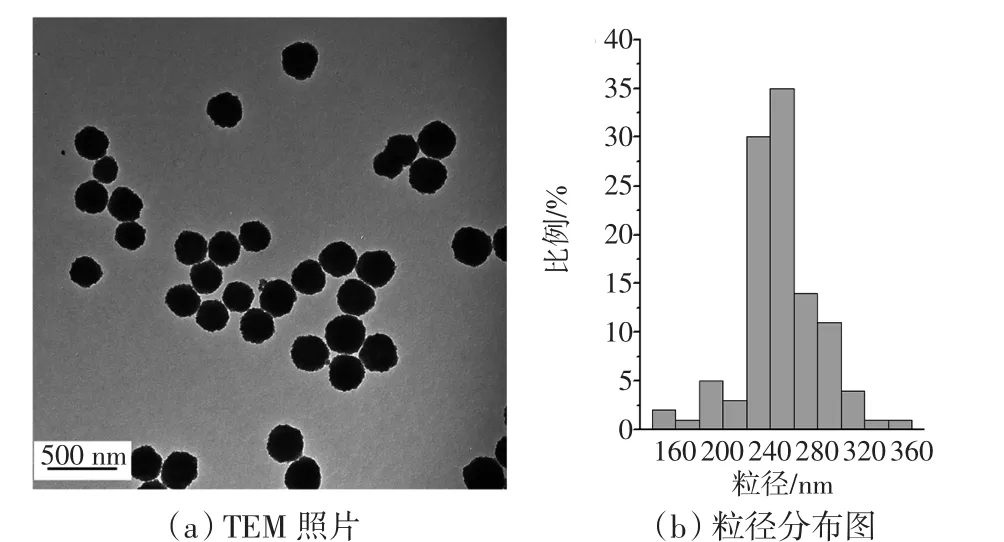
图1 Fe3O4磁性纳米粒子的TEM照片和粒径分布图Fig.1 TEM images of Fe3O4nanoparticles and size distribution
由图1(a)可见,Fe3O4磁性纳米粒子呈规则的球形,粒径均匀分布于200 nm到280 nm之间,通过专业的透射电子显微镜分析软件Gatan DigitalMicrograph,所得结果表明Fe3O4磁性纳米粒子的粒径均值约为250 nm.
图2为所制备的Fe3O4磁性纳米粒子的X-射线衍射谱图(XRD).由图2可见,谱图中各峰形尖锐,根据德拜-谢乐公式对谱图中的最强峰(311)进行计算,得出了Fe3O4磁球是由粒径约为12.8 nm左右的晶核组成的,晶核与晶核之间可能是由无定形基质作为桥架相互连接形成了多晶型的Fe3O4磁球.
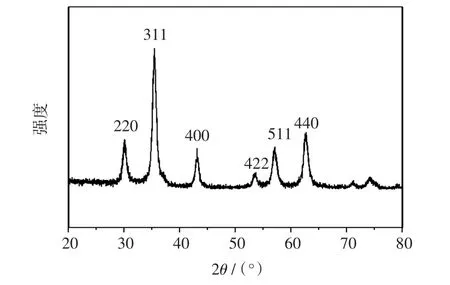
图2 Fe3O4磁球的XRD图Fig.2 XRD pattern of Fe3O4nanoparticles
2.2 Fe3O4纳米粒子的表面改性与AuNPs的自组装
通过溶剂热法制备的Fe3O4磁球表面含有丰富的羟基[12],在氨水的作用下,3-氨丙基三乙氧基硅烷(APTES)先水解生成硅醇,随后与Fe3O4磁球表面的羟基进行脱水键合,从而将Fe3O4磁球表面原来的羟基修饰成氨基,使其具有与金结合的亲和性[13].其反应原理如图3所示.
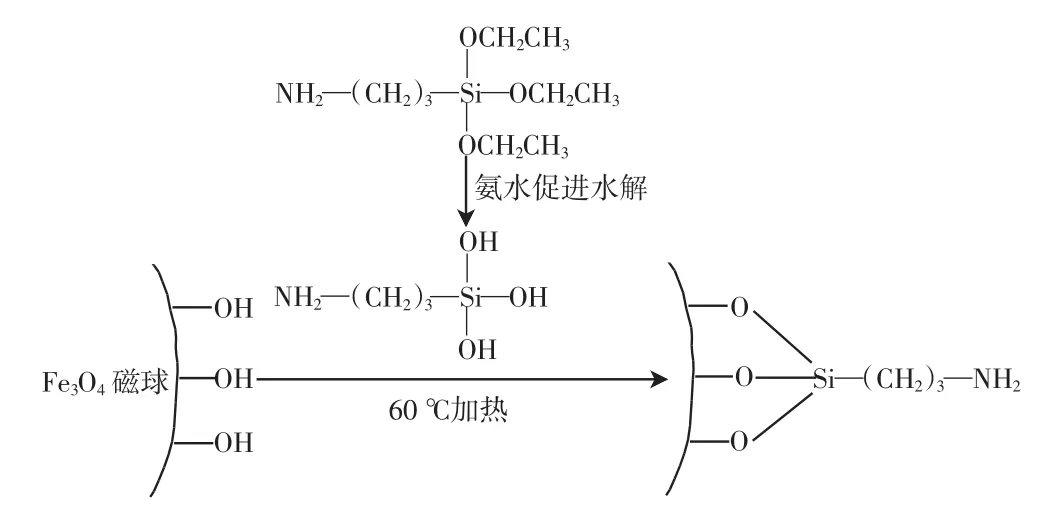
图3 磁球表面改性的原理图Fig.3 Illustration of surface modification of Fe3O4nanoparticles
图4所示为制备的AuNPs与Fe3O4/AuNPs复合纳米粒子.
由图4可见,所得AuNPs的粒径约为20 nm,由于被APTES改性后的Fe3O4表面带有氨基,因此AuNPs可与其表面氨基发生作用并自组装于Fe3O4粒子表面得到Fe3O4/AuNPs复合磁性纳米粒子.AuNPs自组装前后对粒子磁性的影响可用振动样品磁强计(VSM)进行测试,所得结果如图5所示.插图为Fe3O4/ AuNPs复合粒子分散于水中以及磁分离时的情况.

图4 AuNPs与Fe3O4/AuNPs复合纳米粒子的TEM图Fig.4 TEM images of AuNPs and Fe3O4/AuNPs nanoparticles
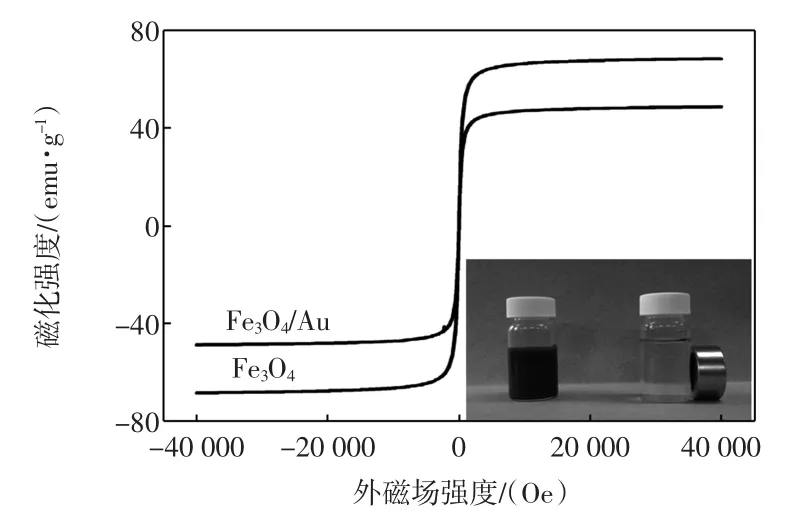
图5 Fe3O4与Fe3O4/AuNPs复合磁性粒子的磁化曲线,Fig.5 Magnetization curves of Fe3O4and Fe3O4/AuNPs composite nanoparticles
由图5可见,Fe3O4粒子与Fe3O4/AuNPs复合磁性纳米粒子的磁饱和强度(MS)分别为69.4 emu/g和49.8 emu/g.图中小插图显示的是合成的Fe3O4/AuNPs纳米复合粒子分散于二次水时的分散和磁分离情况,复合粒子的分散液在1 min之内即可完成分离,撤去磁铁后轻轻震荡复合粒子又可重新均匀分散,说明所制备的Fe3O4/AuNPs复合磁性纳米粒子具有较高的磁响应强度以及良好的分散性,其表面的AuNPs对粒子的磁性影响较小.
图6所示为AuNPs水分散液与Fe3O4/AuNPs复合粒子水分散液的紫外光谱图.
由图6可以看出,合成的粒径为20 nm左右的AuNPs分散于水中,在520 nm有一处强烈的等离子体共振吸收峰,而Fe3O4/AuNPs复合粒子在595 nm出现了一处较宽的吸收峰,说明AuNPs自组装于Fe3O4磁球表面,使得粒子尺寸变大,吸收峰发生约75 nm的红移.
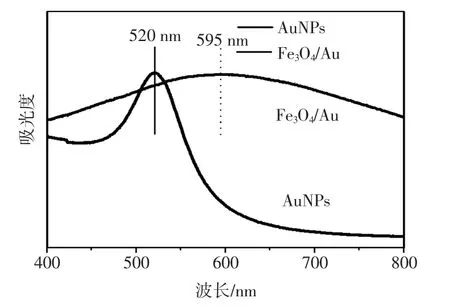
图6 AuNPs水分散液与Fe3O4/AuNPs复合粒子水分散液的紫外光谱图Fig.6 UV-Vis spectra of AuNPs aqueous dispersion and Fe3O4/Au nanoparticles aqueous dispersion
3 结论
本文以改进的溶剂热法制备出粒径均一的球型Fe3O4磁性纳米粒子,然后在乙醇/异丙醇体系中,由3-氨丙基三乙氧基硅烷与其表面的羟基脱水键合生成氨基改性的Fe3O4磁球,在超声条件下连接AuNPs,从而制备了Fe3O4/AuNPs复合磁性纳米粒子.通过TEM、XRD证明了磁球与复合粒子的结构及形貌特征,通过VSM、UV-Vis表征了其磁学特性和光学特性,结果表明AuNPs均匀分散于Fe3O4磁性纳米粒子表面,且所得Fe3O4/AuNPs复合磁性纳米粒子具有良好的磁响应性能.
[1]MAYER K M,HAFNER J H.Localized surface plasmon resonance sensors[J].Chem Rev,2011,111:3828-3857.
[2]JIANG X Q.Gold nanoparticles for biosensor development[D]. New Zealand:Maeesy University,2009.
[3] 庄严,周群,周全法.磁性纳米粒子Fe3O4@Au和Fe3O4@Ag的制备及表征[J].贵金属,2011,32(2):5-8.
[4]HEXL,TANLF,CHEND,etal.Fe3O4-Au@mesoporous SiO2microsphere:An ideal artificial enzymatic cascade system[J]. Chemical Communications,2013,49(41):4643-4645.
[5]KOUASSI G K,IRUDAYARAJ J.Magnetic and gold-coated magnetic nanoparticles as a DNA sensor[J].Anal Chem,2006,78:3234-3241.
[6]CARUNTUD,CUSHINGBL,CARUNTUG,et al.Attachment of gold nanograins onto colloidal magnetite nanocrystals[J]. Chem Mater,2005,17:3398-3402.
[7]葛兆强,刘翠翠,张根义,等.Fe3O4@Au核壳纳米颗粒的制备及表征[J].热加工工艺,2011,40(8):99-101.
[8]WANG Y,SHEN Y H,XIE A J,et al.A Simple method to construct bifunctional Fe3O4/Au hybrid nanostructures and tune their optical properties in the near-infrared region[J].J Phys Chem C,2010,114:4297-4301.
[9]DENG X J,LIN K,CHEN X P,et al.Preparation of magnetic Fe3O4/Au composites for extraction of benzo[a]pyrene from aqueous solution[J].Chemical Engineering Journal,2013,225:656-663.
[10]FRENS G.Controlled nucleation for the regulation of the particle size in monodisperse gold suspensims[J].Phys Sci,1973,241:20-22.
[11]LIU J,SUN Z K,DENG Y H,et al.Highly water-dispersible biocompatible magnetite particles with low cytotoxicity stabilized by citrate groups[J].Angew Chem Int Ed,2009,48:5875-5879.
[12]滕爱兰,米登海.磁性纳米材料在生物医学中的最新研究进展[J].生物医学工程学杂志,2014,31(2):472-476.
[13]DANIEL M C,ASTRUC D.Gold nanoparticles:Assembly,supramolecular chemistry,quantum-size-related properties,and applications toward biology,catalysis,and nanotechnology[J].Chem Rev,2004,104:293-346.
Synthesis and characterization of Fe3O4/AuNPs magnetic composite nanoparticles
DAI Zhao,YANG Kun,HUANG Dan-dan,CHU Yuan-yuan
(School of Environmental and Chemical Engineering,Tianjin Polytechnic University,Tianjin 300387,China)
Fe3O4magnetic nanoparticles with large particle size were synthesized by a solvothermal method,and then modified by (3-aminopropyl)triethoxysilane (APTES)in the system of ethanol and isopropanol,which can functionalized the surface a layer of amino groups.Then,magnetic Fe3O4/Au nanoparticles were prepared by connecting gold nanoparticles under the condition of ultrasound.These composite particles have been characterized by transmission electron microscopy(TEM),X-ray powder diffraction(XRD),vibrating sample magnetometer(VSM)and ultraviolet-visible spectrophotometer(UV-Vis).The result shows that the prepared Fe3O4nanoparticles have a uniform particle size and spherical shape,the average size is 250 nm.Fe3O4/Au composite particles coated evenly,have a good dispersibility and magnetic susceptibility,possess magnetism and characteristics of gold nanoparticles at the same time.
Fe3O4;gold nanoparticles(AuNPs);magnetic nanoparticles;composite particles
TB331
A
1671-024X(2015)03-0028-04
10.3969/j.issn.1671-024x.2015.03.007
2015-03-23
国家自然科学基金资助项目(21172171,21206124).
代 昭(1975—),男,博士,教授,硕士生导师,研究方向为生物与纳米材料.E-mail:daizhao@gmail.com
